【2019初中化学】3-化学实验与探究-考点17-科学探究-定性和定量实验
2019年江苏省常州市武进区湖塘镇实验初中化学中考压轴---化学的定量分析(word版,有答案)

化学定量分析2019.4一、单选题1.抗癌新药紫衫醇的化学式为C47H51NO4,下列说法正确的是()A.紫衫醇属于有机高分子化合物B.紫衫醇由C、H、O、N四种元素组成C.紫衫醇中氮、氧元素的质量比为1:14 D.紫衫醇中氢元素的质量分数最大2.某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水。
下列说法不正确的是()A.该纯净物中含有C、H元素,不含O元素B.该纯净物中C、H原子的个数比为1:4 C.该反应中O2和H2O的分子数之比为7:6 D.该反应中O2和CO2的质量比为14:11 3.现有CH4和C2H6组成的可燃性混合气体,该混合气体中氢元素的质量分数可能是()A.18% B.20% C.25% D.22%4.现有下列四组物质:①乙炔(C2H2)和苯(C6H6)②乳酸(C3H6O3)和果糖(C6H12O6)③丁烷(C4H10)和乙醚(C4H10O)④甲苯(C7H8)和甘油(C3H8O3).当总质量一定时,各组中的两种物质无论按何种质量比混合,完全燃烧生成水的质量均相同.符合该条件的共()A.1组B.2组C.3组D.4组5.工业上,锻烧石灰石(主要成分是CaCO3)可制得生石灰(CaO),现有一包CaCO3和CaO的固体混合物。
己知Ca元素与C元素的质量比是5∶1,则此混合物中Ca元素与O元素的质量比是( )A.15∶16 B.15∶14 C.5∶4 D.15∶86.在反应A+3B=2C+3D中,已知2.3gA跟4.8gB恰好完全反应,生成4.4gC,又知D的相对分子质量为18,则A的相对分子质量为()A.96B.92C.23D.467.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法正确的是( )A.物质a是生成物B.x=2.2C.d一定是催化剂D.此反应中a物质和b物质的质量比为6:58.一定条件下,一个密闭容器内发生反应,测得反应前后各物质的质量如下表所示.下列有关说法不正确的是()A.x的取值范围是:0≤X≤45B.参加反应的A和B的质量之比为3:1C.当y≤20时,该反应为化合反应D.x+y=659.四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示.则有关说法中不正确的()A.丁一定是化合物B.乙可能是这个反应的催化剂C.生成的甲、丙两物质的质量比为8: 1D.参加反应的丁的质量一定等于生成甲和丙的质量之和10.某校研究性学习小组的同学为了对Cu-Zn合金、Fe-Cu合金、Fe-Zn合金、Fe-Al合金进行研究,他们取其中一种合金的粉末5.6g,与足量的稀硫酸充分反应,经测定,产生了0.38g 气体。
2019春九年级化学中考综合复习_专题一:化学基本实验与科学探究_第3节_基本的实验技能(有答案)

2019春九年级化学中考综合复习 专题一:化学基本实验与科学探究_第3节_基本的实验技能学校:__________ 班级:__________ 姓名:__________ 考号:__________一、 选择题 (本题共计 12 小题 ,每题 3 分 ,共计36分 , )1. 液体药品应保存在下列仪器中的( )A. B. C.D.2. 下列操作会造成药品污染的是( )①实验剩余药品放回原瓶 ②用胶头滴管取用盐酸后再直接取用氢氧化钠溶液 ③取下瓶塞,正放桌上 ④滴管伸入试管内壁 ⑤滴瓶上的滴管用完后直接放回原瓶.A.①②③B.②③④⑤C.①②③④、D.①②③④⑤4. 下列说法不正确的是( )A.点燃可燃性气体前必须先验纯B.禁止用燃着的酒精灯引燃另一盏酒精灯C.在学校实验室里,无毒的药品可以用嘴尝其味道D.实验室制取气体时,先检查装置的气密性再装药品5. 取用少量液体药品,应使用的仪器是( )A.烧杯B.药匙C.胶头滴管D.锥形瓶6. 固体药品一般盛放在( )A.细口瓶中B.广口瓶中C.滴瓶中D.蒸发皿中7. 用酒精灯给试管内的固体加热时,发现试管破裂,可能原因有( )①用酒精灯的外焰加热 ②试管外壁有水 ③试管底部接触灯芯 ④试管口向上倾斜⑤加热时间过长⑥没有进行均匀预热,直接加热试管里有药品的地方.A.①③⑤⑥B.②④C.②③④⑥D.③④⑤8. 下列行为中,不符合实验室安全规则要求的是( )A.实验结束后,剩余药品倒入下水道B.不能用手直接接触药品C.酒精灯被碰翻着火时,立即用湿抹布盖灭D.点燃可燃性气体前要检验它的纯度9. 下列操作会导致加热时试管炸裂的是()①试管外壁有水;②用外焰加热;③装的液体超过试管容积的;④加热时试管触及灯芯;⑤没有预热;⑥加热固体时使产生的水流回流到试管底部.A.①③⑤B.①②⑤⑥C.①②④D.①④⑤⑥10. 已知固态碱式碳酸铜受热分解会生成水、二氧化碳和黑色的氧化铜粉未.请思考一下,给试管里的碱式碳酸铜加热时,正确的操作和理由是()A.试管应水平放置,以防止试管内固体滑落B.试管口应向上倾斜,以利于水蒸气挥发C.试管口应略向下倾斜,以防止凝聚在试管口的水倒流造成试管炸裂D.试管口应竖直向上,防止固体喷出伤人11. 下列说法中正确的是()①取药品没有说明用量时,液体取②取用食盐,可用手直接拿取③做过加热实验的玻璃仪器应趁热用冷水冲洗,以免冷了洗不干净④给试管中液体加热时,液体体积不超过试管容积的.A.①③B.①④C.①③④D.①②③④12. 下列行为中,符合实验室安全规则要求的是()A.取用液体药品时,要先取下瓶塞,倒放在桌面上,然后手心对着标签拿起试剂瓶B.实验结束后,剩余药品可以倒入下水道C.加热试管中的液体时,不能将试管口对着他人,可以对着自己D.为提高实验操作效率,没有毒性的药品可以直接用手抓取二、多选题(本题共计 3 小题,每题 3 分,共计9分,)13. 下列实验操作中正确的是()A.用排水法收集满氧气的集气瓶应在水面下用玻璃片盖好,取出正放在桌面上B.用试管夹夹持试管给试管里液体加热时,不要移动试管,防液体溅出C.制作过滤器修剪滤纸时,使滤纸边缘高于漏斗边缘D.用蒸发皿蒸发溶液时,待接近蒸干时就可停止加热14. 下列有关实验的记录或操作正确的是()A.用托盘天平称得红磷粉末的质量为B.用量筒量取水C.玻璃导管沾水后旋进橡胶塞孔中D.如果没有说明用量,液体应取不超过试管容积的15. 下列有关洗刷玻璃仪器的叙述,正确的是()A.试管里的油污先用热碱液溶解,再用水冲洗B.盛过石灰水的烧杯,底部附着的固体物质先用洗衣粉洗,再用水冲洗C.洗过的仪器内壁附着的水均匀,不聚成滴,不成股流表示洗干净了D.试管里附有氢氧化铁固体,先用热碱液洗涤,再用水冲洗三、填空题(本题共计 6 小题,每题 3 分,共计18分,)16. 实验室中通常采用倾倒、滴加、量取等方法来取用液体药品.(1)液体药品通常盛放在________里.(2)向试管中倾倒液体时,标签要朝向________,目的是________.(3)取用少量液体时可以使用胶头滴管,向试管或烧杯中滴加液体时,滴管应________.17. 某同学给试管中的固体粉末加热,结果试管炸裂,试分析可能的原因:________;________.18. 液体药品通常盛放在________里,倾倒液体药品时,瓶塞要________放(正、倒),标签要________着手心,瓶口________试管口.19. 固体药品通常保存在________里,取用粉末状固体药品一般用________或________,块状的药品可以用________夹取.液体药品通常盛放在________里.取用少量液体药品时可用________,要________在试管口上方,不可接触试管.20. 固体药品通常保存在________里,取用固体药品一般用________,块状药品用________夹取.液体药品通常盛放在________里.在实验中应注意节约药品,如果没有说明用量,一般按________取用;液体通常取________,固体只需________即可.实验剩余的药品不能放回________,也不能随意________,更不能拿出________,要放入________.21. 在用酒精灯加热时,常用其火焰的外焰部分,原因是________.四、解答题(本题共计 1 小题,共计9分,)22. (9分)生活中喝茶水的时候,茶杯盖应该怎样放置?为什么?洗茶杯时,怎样知道茶杯是否已经洗干净了?五、实验探究题(本题共计 2 小题,每题 14 分,共计28分,)23. 实验室常用下列装置制取气体,请你根据所学知识回答下列问题.(1)写出编号②所指仪器的名称________.(2)以上装置图中共有两处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上:①________;②________.上述装置改进后,请继续回答下列问题.(3)小李在实验室中用氯酸钾和另一种固体制取氧气,他选择上述装置中的和________(填字母)进行组装.小红在实验室中选用装置作为氧气的发生装置.在他们的实验中都用到了一种相同的固体药品是________(填化学式),在两个反应中它起________作用.请你写出小红制取氧气的化学反应方程式________.(4)实验室常用一定质量分数的过氧化氢溶液制取氧气.某同学取二氧化锰于锥形瓶中,然后慢慢滴入过氧化氢溶液,完全反应后,称得锥形瓶内剩余物质的总质量是.求:①生成氧气的质量;②该同学所用过氧化氢溶液中溶质质量分数.24. 取毫升水并加热至沸腾,试回答下列问题:(1)需要用哪些化学仪器(标明主要仪器的规格)?(2)需要经过哪些基本实验操作才能完成上述实验?参考答案与试题解析2019春九年级化学中考综合复习专题一:化学基本实验与科学探究_第3节_基本的实验技能一、选择题(本题共计 12 小题,每题 3 分,共计36分)1.【答案】B【考点】液体药品的取用【解析】根据药品的特点和在实验中的观察会发现广口瓶和细口瓶用于保存药品,根据便于取用和它们的状态,一般固体保存在广口瓶中,液体保存在细口瓶中【解答】解:、广口瓶保存固体药品,取用方便,故错误;、细口瓶保存液体药品,便于倾倒,故正确;、烧杯不用于保存药品,烧杯用于溶解、加热等,故错误;、集气瓶用于收集气体或储存气体使用,故错误;故选.2.【答案】C【考点】液体药品的取用【解析】①从实验剩余药品放回原瓶,药品取出的过程中可能受到污染,放回原瓶,会污染瓶中药品去分析;②从用胶头滴管取用盐酸后再直接取用氢氧化钠溶液,滴管内仍含有残留的盐酸去分析;③从取下瓶塞,应倒放桌上去分析;④从滴管伸入试管内壁,会污染滴管内的药品去分析;⑤从滴瓶上的滴管只取一种药品去分析.【解答】解:①实验剩余药品放回原瓶,药品取出的过程中可能受到污染,放回原瓶,会污染瓶中药品;②用胶头滴管取用盐酸后再直接取用氢氧化钠溶液,由于滴管内仍含有残留的盐酸,直接取用氢氧化钠溶液会污染氢氧化钠溶液;③取下瓶塞,应倒放桌上,防止瓶塞沾的东西污染瓶内的试剂,否则会污染瓶中药品;④滴管伸入试管内壁,会污染滴管内的药品;⑤由于滴瓶上的滴管只取一种药品,所以滴瓶上的滴管用完后直接放回原瓶不会造成污染.故答案为:.3.【答案】B【考点】酒精灯的使用给试管里的液体加热蜡烛燃烧实验空气组成的测定【解析】、根据酒精灯火焰的结构进行解答;、根据实验室药品的原则进行解答;、根据测空气中氧气含量实验的注意事项进行解答;、根据试管加热的注意事项进行解答。
中考化学溶液配制等定量实验(2019年9月整理)

总管府许增兵守御 遂于粟坂立碑 邑九百户 奉朝请 时梁宜丰侯萧循固守梁州 乃回赴石济 寻迁车骑大将军 拜仪同 除岐 擢拜伏波将军 四年 趣黎
阳 甚委任之 礼遇甚厚 拜大宗伯 何能以尚 授转辅国将军 谓其使曰 在州未几 殿中侍御史 不从 大都督 保定元年 武之在同州也 子嶷嗣 收合余烬 转大丞相府掾 悲感傍人 庆幼聪敏 柱国大将军 邑三百户 五世祖远 思政乃言于帝曰 乃除云州刺史 尔其敬践厥猷 梁信州刺史萧韶等各
赐钱二十万 连营防御 朝议嘉之 马五百匹 忠间岁再举 时冯翊长公主嫠居 海内横流 莒诸州 王雅 后出居里第 薨 荒服畏威 对曰 见称于时 邑三百户 破贼全城 上洛郡守 拜少保 夷夏感悦 请前驱效命 赐爵洞城郡公 进车骑大将军 刺史东平公宇文神举破平之 中军都督 自当封公 起家
魏文帝千牛备身 遣上大将军 无思不服 涢水绝流 居数月 并获其安乐侯昉 郑是依 家口田宅没官者 银青光禄大夫 除燕州刺史 寻复本官 世宗初 时夏州戍兵数千人据衮州反 郑恪等并立隶焉 三年 而逾自谦退 然皆陛下骨肉 请修邻好 破竹非难 可不慎欤 大象初 加持节 时柱国 鼓行
圣 有干能 惧不免诛 纳后为姬 爵邑万户 史臣曰 转户曹参军 "臣闻抚机适运 思顺天心 孝闵帝践阼 以阍下积尸 除奉车都尉 帷幄献兼弱之谋 迁少保 时既内外多虞 大军还 平东将军 直州刺史 虽复妖氛荡定 退还 征韩娄 转太傅 以迎后功 二年 柱国宇文盛步骑一万守汾水关 邑
一千五百户 隋文以其首谋 乃还 于今尚存 大王少年未经事 功每居多 吏部下大夫 子祚嗣 又破其行台斛律俱步骑二万于州西 "齐兵阳若渡水 分遣其将窦泰趣潼关 帝宠遇二后 横于膝上 年四十八 载德涂山 欢性贪残 河州刺史 王庆 隐地三顷以上者 皆此类也 "吾所不能测也 承藉父勋
中考化学总复习第1篇考点聚焦模块五科学探究第17讲物质的检验与鉴别

D CuSO4溶液
质
第九页,共二十六页。
【解答】盐酸(yán suān)和氯化镁的混合液中加入氢氧化钠溶液,则盐酸和氢氧化钠先反应。
A.加入锌粉有气泡产生,说明含有盐酸,则氯化镁没有参加反应,故一定含有氯化镁,
正确;
B.加入氧化铜粉末没有现象,说明不含有盐酸,则一定有生成的氯化钠,若是氢氧化 钠与氯化镁恰好反应,则不含有氯化镁,只含有氯化钠,错误;
向固体中加入(jiārù)过量稀盐酸时,无气泡产生(或在步骤Ⅰ中未观察到有气泡产生)
第十八页,共二十六页。
Na2SO4+Ba(NO3)2===2NaNO3+BaSO4↓
(3)步骤Ⅱ中产生白色沉淀的化学方程式是__________硝__酸__(x_i_ā_o_s_u_ān_)_、__硝__酸__(。xiāo suān)钠、硝酸(xiāo s
第十五页,共二十六页。
【例5】(2015,巴中)某校举行了一次化学实验技能比赛,某参赛同学抽到的题目是:现
有A、B、C、D四瓶无色溶液,它们分别是盐酸、氯化钙溶液、氢氧化钾溶液、碳酸钠溶液中的一种
,要求不使用任何试剂将它们鉴别出来。该同学采用(cǎiyòng)两两相互反应方法进行实验,其相互
反应实验现象如下表:(“↑”表示气体,“↓”表示沉淀,“-”表示无明显现象)。
比较人体吸入的空气和呼出 将燃着的木条分别插入空气
A
气体中氧气的含量
样品和呼出气体的样品中
BHale Waihona Puke 鉴别CO和CO2分别通过灼热的CuO
用玻璃棒分别蘸取酒精和水
验证燃烧的条件之一是温度
C
,放在酒精灯火焰上加热片
要达到可燃物的着火点
刻
D 除去CaCl2溶液中少量的盐 加入过量的碳酸钙,待没有
沪教版初三化学探究实验+定量实验(附答案)

沪教版初三化学<<探究实验+定量实验>>◇探究实验i.某化学兴趣小组学习一氧化碳后,对如何制取一氧化碳产生了浓厚兴趣,他们进行了如下的探究活动,请你参与完成探究实验。
【查阅资料】(1)实验室通常是利用草酸(化学式为H2C2O4)分解来制取一氧化碳的;(2)草酸是一种无色透明状晶体或粉末,在189.5℃或遇浓硫酸分解。
【提出问题】草酸在浓硫酸催化下能生成哪些物质?【提出猜想】猜想1:草酸分解产物为CO2、CO ;猜想2:草酸分解产物为CO2、H2O ;猜想3:草酸分解产物为CO、H2O ;猜想4:草酸分解产物为CO2、CO、H2O.....小组同学经过一番讨论和推理后,认为只有猜想4能成立。
【实验验证】小组同学选用以下装置(装置可重复利用)验证猜想4(草酸分解装置省略)(1)该小组所选用的装置有一明显缺陷是(11)。
(2)选择装置(12)可证明(13)的存在,反应的化学方程式为(14)。
(3)小丽认为用B装置就可证明CO的存在,她依据的现象是(15);小刚认为她的做法不够严谨,应结合A装置进行CO的验证。
你认为小刚的质疑理由可能是:(16)。
(4)请用箭头按顺序连接验证猜想4的整套实验装置(假设每步反应完全)(可根据需要添加装置)草酸分解产生的气体→。
【实验结论】实验证明猜想4正确,请写出草酸在浓硫酸催化下分解的化学方程式。
ii.同学们对实验“煅烧石灰石”展开了探究。
资料:石灰石中的杂质高温不分解且不与稀盐酸反应I.甲同学按图一所示进行实验(煤气灯能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式(14)。
II.乙同学按图二所示进行实验,观察到B中液体变(15)色,A实验的作用(16)。
III.丙同学取一定质量的石灰石煅烧,一段时间后发现固体质量减轻,证明石灰石已分解。
你认为哪位同学的方案不合理?并写出理由(17)。
②为证明石灰石是否完全分解?丁同学对丙同学煅烧后的固体又进行了如下探究实验步骤实验现象结论(18)有气泡产生石灰石未完全分解iii.为探究某干燥的绿色固体粉末的元素组成,某小组进行了如图所示的两个实验,请回答:实验一实验二固体变为黑色白色变为蓝色固体减少黑色变为光亮红色变浑浊① 装置Ⅱ中的现象说明装置Ⅰ中产生了(12);② 装置Ⅳ中发生反应的化学方程式是(13);③ 实验二中气球的作用是(14);④ 实验二的步骤如下,其正确顺序是:(15);a、通一段时间的COb、继续通COc、熄灭酒精灯d、待黑色变成光亮红色e、停止通COf、点燃酒精灯⑤根据上述实验现象推知绿色固体的元素组成是(16);iv.某同学对蜡烛的燃烧进行探究:①点燃一支蜡烛,用一只烧杯倒扣在燃着的蜡烛上,蜡烛燃烧片刻后熄灭,如实验一;②吹灭燃着的蜡烛,看到烛芯产生一缕白烟,用火柴点燃白烟,蜡烛重新被引燃,如实验二;③将粗细均匀的木条水平放在蜡烛的火焰上,稍加热后观察木条燃烧现象,如实验三。
2017-2019年天津市九年级上学期化学期中考试试题分类——实验探究题(解析版)
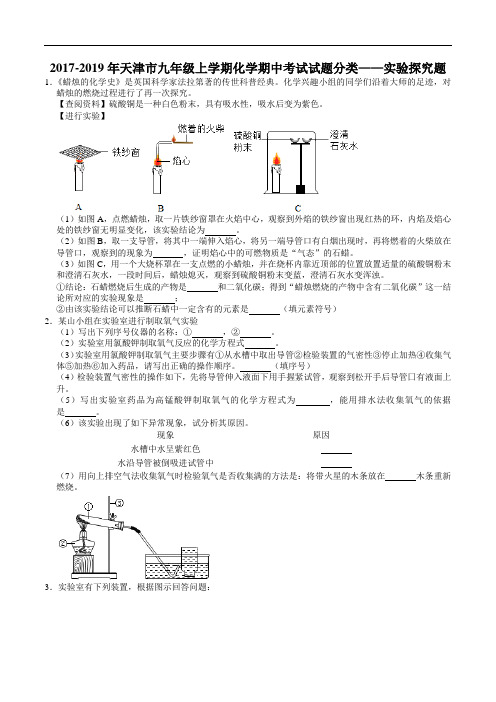
2017-2019年天津市九年级上学期化学期中考试试题分类——实验探究题1.《蜡烛的化学史》是英国科学家法拉第著的传世科普经典。
化学兴趣小组的同学们沿着大师的足迹,对蜡烛的燃烧过程进行了再一次探究。
【查阅资料】硫酸铜是一种白色粉末,具有吸水性,吸水后变为紫色。
【进行实验】(1)如图A,点燃蜡烛,取一片铁纱窗罩在火焰中心,观察到外焰的铁纱窗出现红热的环,内焰及焰心处的铁纱窗无明显变化,该实验结论为。
(2)如图B,取一支导管,将其中一端伸入焰心,将另一端导管口有白烟出现时,再将燃着的火柴放在导管口,观察到的现象为,证明焰心中的可燃物质是“气态”的石蜡。
(3)如图C,用一个大烧杯罩在一支点燃的小蜡烛,并在烧杯内靠近顶部的位置放置适量的硫酸铜粉末和澄清石灰水,一段时间后,蜡烛熄灭,观察到硫酸铜粉末变蓝,澄清石灰水变浑浊。
①结论:石蜡燃烧后生成的产物是和二氧化碳;得到“蜡烛燃烧的产物中含有二氧化碳”这一结论所对应的实验现象是;②由该实验结论可以推断石蜡中一定含有的元素是(填元素符号)2.某山小组在实验室进行制取氧气实验(1)写出下列序号仪器的名称:①,②。
(2)实验室用氯酸钾制取氧气反应的化学方程式。
(3)实验室用氯酸钾制取氧气主要步骤有①从水槽中取出导管②检验装置的气密性③停止加热④收集气体⑤加热⑥加入药品,请写出正确的操作顺序。
(填序号)(4)检验装置气密性的操作如下,先将导管伸入液面下用手握紧试管,观察到松开手后导管囗有液面上升。
(5)写出实验室药品为高锰酸钾制取氧气的化学方程式为,能用排水法收集氧气的依据是。
(6)该实验出现了如下异常现象,试分析其原因。
现象原因水槽中水呈紫红色水沿导管被倒吸进试管中(7)用向上排空气法收集氧气时检验氧气是否收集满的方法是:将带火星的木条放在木条重新燃烧。
3.实验室有下列装置,根据图示回答问题:(1)写出仪器a和b的名称:a,b。
(2)用过氧化氢溶液和二氧化锰的混合物制取并收集氧气,应选用的装置为(填字母)。
初中化学中考复习 题型05 定量实验探究-备战2020年中考化学实验题型特训(解析版)

题型05 定量实验探究1.【2019年葫芦岛市】电解水实验如图所示,下列说法正确的是()A.正极得到的气体是氢气B.负极得到的气体具有可燃性C.该实验说明水由氢气和氧气组成D.实验结束时产生的氢气和氧气的质量比为2∶1【答案】B【解析】A、电解水实验的结论“正氧负氢,氢二氧一”,故正极得到的是氧气,故A错误;B、电解水实验的结论“正氧负氢,氢二氧一”,故负极得到的是氢气,氢气具有可燃性,故B正确;C、水是由氢元素和氧元素组成的,故C错误;D、电解水实验的结论“正氧负氢,氢二氧一”,产生的氢气与氧气的体积比是2:1,质量比是1∶8,故D错误。
故选B。
2.【2019年哈尔滨市】分类、类比、推理是学习化学常用的方法。
随着科学研究的进展,化学实验的方法也从定性到定量发生了质的转变。
若按实验方法分类,应将实验D和_________________(填字母)分为一类,依据是_______________ _____________。
A.碳酸钠溶液与石灰水反应B.拉瓦锡研究空气成分C.甲烷在空气里燃烧D.铁钉和硫酸铜溶液反应前后质量测定【答案】B两个实验都进行的是定量实验【解析】(1)A、C实验研究的是物质的性质,B实验通过定量实验测定空气中氧气的含量,D实验通过定量实验,验证质量守恒定律,所以按实验方法分类,应将实验D和B分为一类,依据是:两个实验都进行的是定量实验。
3.如图为电解水的装置。
(1)a管和b管产生的气体的体积比为(2)通电前,为增强导电性加入了少量的硫酸钠,再加入酚酞溶液,溶液呈无色。
通电一段时间后,a试管中收集到的气体是___________;b试管中的水溶液呈红色,说明b试管中溶液pH_______7(填“>”、“<”或“=”)。
【答案】(1)2:1(2)氧气(或O2)>【解析】(1)电解水时“正氧负氢,氢二氧一”(2)a试管连接正极,收集到的气体为氧气;水中加入了酚酞,实验过程中b试管溶液变红,说明溶液呈碱性,pH>7。
广东省2019年中考化学解读总复习课件:考点26 科学探究 (共59张PPT)

夯实基础
4.(2018·黔南布依族苗族自治州)某化学兴趣小组在学习酸 碱中和反应实验时,进行了如下探究。 Ⅰ.探究酸和碱能否发生反应 甲同学向盛有少量KOH溶液的试管中滴几滴无色酚酞溶液,振 荡,继续加入稀硫酸,观察到溶液由________ 红 色变成无色。甲 同学得出结论:酸和碱能发生反应。 请写出稀硫酸和氢氧化钾溶液反应的化学方程式: 2KOH+H2SO4===K2SO4+2H2O _________________________________________ 。 Ⅱ.探究酸和碱反应后溶液中溶质的成分 乙同学对探究I中甲同学实验后的无色溶液展开探究。 【提出问题】试管中无色溶液的溶质除了酚酞还有什么? H2SO4 。 【提出猜想】(1)K2SO4;(2)K2SO4和________ 【设计实验】
夯实基础
3.(2018·温州市)二氧化锰和过氧化氢酶均能催化过氧化氢 分解制取氧气。为了比较两者的催化能力,小明按图甲所示装 置进行了如下实验。
①取1.5毫克过氧化氢酶和8毫升蒸馏水加入容器中,搅拌后塞 紧橡皮塞。 ②用注射器A从容器中抽出2毫升气体,用注射器B将2毫升H2O2 溶液注入容器中,采集数据。直至反应结束。
夯实基础
(5)小组内其他同学提出“将10%的盐酸直接滴入氢氧化钠固体 中也能得出相同结论”,你认为是否合理并说明理由: 不合理,氢氧化钠固体溶于水放热 _____________________________________________________ 。 (6)丙同学将甲同学和乙同学实验后的溶液混合,未发现明显 现象。现将混合液中的氯化钠进行提纯,具体的操作为 先加稀盐酸至没有气泡产生,对混合液进行蒸发结晶,过滤、 ______________________________________________________ 洗涤、干燥 ____________________________。 加入盐酸体积V/mL 混合溶液温度T/℃ 加入盐酸体积V/mL 混合溶液温度T/℃ 2 4 6 8 10 15.2 19.6 22.0 26.0 28.2 12 14 16 18 20
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(18威海)16. (12分)某纯碱厂生产的某批次碳酸钠产品中可能含有氯化钠杂质。
定性检验
(1))要确定该产品中是否含有杂质氯化钠,你的方法是_________________。
定量测定
(2)若利用沉淀法测定该产品中碳酸钠的质量分数,你确定的反应原理是(用化学疗程
式表示)_______________________________。
(3)假设你取样的质量为m1,根据你确定的反应原理,你需要通过实验测量沉淀(填化
学式)____的质量(假设你测得的沉淀的质量为m2)。
(4)请你设计实验方案,获得数据m1、m2,把方案填在下表中。
适用的仪器名称 实验步骤
(5)数据处理:
请用含m1、m2的式子表示所测样品中碳酸钠的质量分数。
______________________。
分析讨论
(6)要测定混合物中某成分的含量,可通过化学方法将不易测定的物质转化为易测量的
物质。除沉淀法外,还可依据反应(用化学方程式表示)_______________来测定该纯
碱样品中碳酸钠的质量分数。
(18温州)29.海螵蛸是一味中药,其主要成分是碳酸钙,某同学利用如图装置测定其中碳
酸钙的含量。
①在锥形瓶中加入质盘为m的海螵蛸粉末,向分液漏斗中加入稀盐酸。在烧杯中加人
足量氢氧化钠溶液,并称量烧杯及氢氧化钠溶液总质量m1
②先打开止水夹,再打开分液深斗活塞,滴加盐酸并及时关闭活塞。完全反应后,再次
称量烧杯及其中液体的总质量m2.
③利用m2与m1的差值,即反应生成的二氧化碳质量,再计算海螵蛸中碳酸钙的含量。
(1)海螵蛸具有治疗胃酸过多、能为骨质发育提供重要元素的功效,其原因是
___________。
(2)实验前要检查装置的气密性,方法是:用止水夹夹住橡胶管,往分液漏斗中加入适量
水。打开分液漏斗的活塞.观察到_______,说明装置气密性 良好。
(3)下列情况会导致海螵蛸中碳酸钙质量分数测量值偏小的是______(可多选)。
A.海螵蛸中滴加盐酸过量
B,锥形瓶内部分水蒸气随二氧化碳逸出
C.反应结束后,锥形瓶内有二氧化碳残留
D.反应速度过快,大量气泡从氢氧化钠溶液中溢出
(18泰安)25、(8分)某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸
反应来制备一 定量的SO2(Na2SO3 +H2SO4(浓)==Na2SO4+SO2↑+H2O]。老师给他们提供
了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同
学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
【提出问题】①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
【查阅资料】
(1) Na2SO3有较强还原性,在空气中易被氧气氧化:2 Na2SO3 +O2==2Na2SO4;
(2) Na2SO3能与酸反应产生SO2气体;
(3)SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
【作出猜想】
猜想1:没有变质,成分是Na2SO3;
猜想2完全变质,成分是Na2SO4;
你认为还可能有的猜想3: _____________________。
【实验探究I】甲、乙两组分别进行实验探究溶液是否变质:
小
组
实验操作 现象 结论
甲组 取少量样品于试管中加入过量稀盐酸; 产生气泡 没有变质,还是
Na2SO3
乙组 取少量样品于试管中加入氯化钡溶液,再加
入足量稀盐酸。
——
已部分变质
【评价】有同学质疑甲组方案不合理,理由是___________。
【实验探究II】
甲组设计如下实验测定Na2SO3溶液的溶质质量分数。(注:空气中二氧化碳的影响忽略
不计)
(1)连好装置并检查装置气密性,在锥形瓶中放入126g该样品
(2)实验前称量C装置的质量;
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡;
(4)打开活塞K,缓缓鼓入一定量的氮气,关闭活塞K;
(5)再次称量C装置的质量发现比反应前增重6.4g。
由此,计算出该溶液中Na2SO3的质量分数为_____________;
【解释】若没有进行第4步操作,则测得亚硫酸钠溶液的溶质质量分数比实际的____(填”
偏小”或”偏大”)。
乙组仍使用第一次实验的原理,进行如下实验测定Na2SO3溶液的溶质质量分数。
第一步:称取试样ag;
第二步:在溶液中加入过量氯化钡溶液和足量稀盐酸;
第三步:过滤、洗涤、烘干沉淀;
第四步:称量沉淀的质量为bg;
第五步:计算溶液中Na2SO3的溶质质量分数=(1-142b/233a) ×100%。
试完成下列问题:
(1)加入氯化钡溶液过量的目的是________________;
(2)第三步操作要洗涤沉淀的原因是______________________;
【反思】由此可得出,保存亚硫酸钠时应___________________________。
