第八讲 吸附等温方程式(BET吸附)
BET的原理及使用方法

BET的原理及使用方法BET(Brunauer-Emmett-Teller)是一种常用的表征吸附物理性质的方法,它可以用来测量固体表面的比表面积。
本文将介绍BET原理及其使用方法。
BET原理:BET原理是基于吸附等温线为Langmuir等温线的假设,该假设认为吸附在固体表面上的分子是均匀分布的,且各个吸附位点之间没有相互作用。
基于这个假设,BET理论推导出了吸附等温线的表达式。
吸附等温线描述了在固体表面吸附分子的吸附量与相对气相压力的关系。
通常,BET等温线可以近似为一个H型曲线,即在低压下,吸附量随着压力的升高而增加,直至达到一个饱和吸附量,然后吸附量在较高压力下逐渐减小。
根据BET理论,可以通过测量不同相对气相压力下吸附量的变化来确定固体的比表面积。
BET使用方法:BET方法主要包括以下几个步骤:1.准备样品:将待测固体样品研磨成细粉末,然后通过烘干或者其他方法将样品中的水分等挥发性物质去除。
2.选择适当的吸附剂:通常,选择与待测样品相互作用较弱的气体作为吸附剂,例如氮气。
吸附剂的选择应该考虑到其与样品的化学性质以及实验条件。
3.测量吸附等温线:使用气体吸附仪器,例如比表面积分析仪,对样品进行吸附等温线测量。
实验过程中需要控制气体的流速、温度和压力,并进行相应的记录。
4.数据处理:将吸附等温线中的吸附量和相对气相压力的数据转化为BET等式的形式。
5.拟合曲线:根据BET等式,使用非线性拟合技术将实验数据拟合为BET等式,从而得到比表面积的数值。
需要注意的是,BET方法适用于固体样品的比表面积大于10平方米/克的情况。
对于具有较小比表面积的样品,可以考虑使用其他表征方法,如X射线衍射。
BET方法的应用:BET方法广泛应用于材料科学、化学工程、环境科学和生物科学等领域。
其中一些典型的应用包括:1.反应催化剂的性能评价:固体催化剂的催化活性与其表面积密切相关,通过BET方法可以评估催化剂的比表面积从而预测其催化性能。
第八讲 吸附等温方程式(BET吸附)

四、吸附等温方程式
p / p0 根据实验数据用 对 p / p0 做图, V (1 p / p0 )
若得直线,则说明该吸附规律符合BET公式,且通过
直线的斜率和截距便可计算出二常数Vm和C。
若吸附发生在多孔物质上,吸附层数就要受到限制,
设只有n 层,于是:
V Vm
C i xi
i 1
这说明x就是相对压力(即 x = p/p0)。将 x = p/p0代入,得到
V
Vm Cp ( p0 p )[1 (C 1) p / p0 ]
这就是著名的BET二常数公式。 Vm——表面盖满一个单分子层时的饱和吸附量,mL/g; C——常数。
四、吸附等温方程式
a1b2 Q1 QL C a b exp RT 2 1
(2)第二层及以后各层的吸附热都一样,而且等于液化热QL。
以S0、S1,S2…Si分别表示被0,1,2…i层分子所覆盖
的面积,如下图所示:
多分子层吸附示意图
则,S0=3个位置 S1=3个,S2=2个,S3=1个,S4=0个,S5=1个。
四、吸附等温方程式
达到平衡时,各种分子层覆盖的面积保持一定。例如,从空白 面积S0来看,吸附到S0上的速度要和S1层脱附的速度相等,在这种
p 2VL cos ln p0 rRT
pr,p0 ——与弯月液面、平液面平衡的蒸气压;VL ——液体的摩尔体积;
——液体的表面张力;
——润湿角(接触角)。
五、毛细凝聚现象
但是不管是否发生毛细凝聚,固体表面与蒸气共存时,
表面总会因吸附蒸气而形成吸附膜,在毛细孔壁上也一样,
也就是说,毛细凝聚是发生在吸附膜这个基础上的,据此 上式应修正为:
(完整版)BET吸附-脱附曲线分析及含义
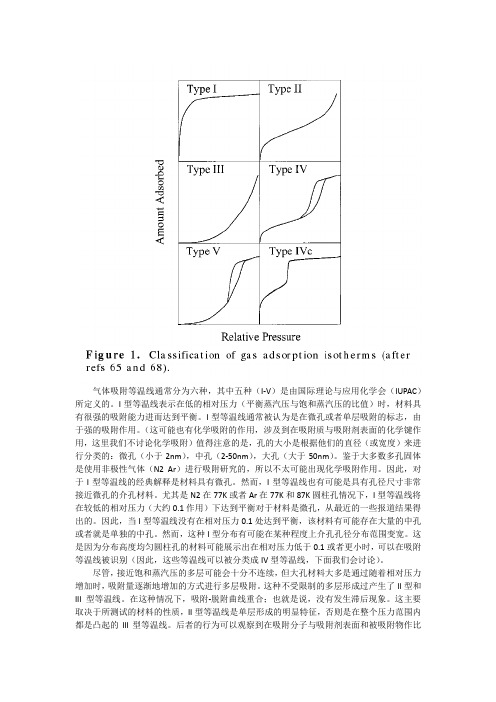
气体吸附等温线通常分为六种,其中五种(I-V)是由国际理论与应用化学会(IUPAC)所定义的。
I型等温线表示在低的相对压力(平衡蒸汽压与饱和蒸汽压的比值)时,材料具有很强的吸附能力进而达到平衡。
I型等温线通常被认为是在微孔或者单层吸附的标志,由于强的吸附作用。
(这可能也有化学吸附的作用,涉及到在吸附质与吸附剂表面的化学键作用,这里我们不讨论化学吸附)值得注意的是,孔的大小是根据他们的直径(或宽度)来进行分类的:微孔(小于2nm),中孔(2-50nm),大孔(大于50nm)。
鉴于大多数多孔固体是使用非极性气体(N2 Ar)进行吸附研究的,所以不太可能出现化学吸附作用。
因此,对于I型等温线的经典解释是材料具有微孔。
然而,I型等温线也有可能是具有孔径尺寸非常接近微孔的介孔材料。
尤其是N2在77K或者Ar在77K和87K圆柱孔情况下,I型等温线将在较低的相对压力(大约0.1作用)下达到平衡对于材料是微孔,从最近的一些报道结果得出的。
因此,当I型等温线没有在相对压力0.1处达到平衡,该材料有可能存在大量的中孔或者就是单独的中孔。
然而,这种I型分布有可能在某种程度上介孔孔径分布范围变宽。
这是因为分布高度均匀圆柱孔的材料可能展示出在相对压力低于0.1或者更小时,可以在吸附等温线被识别(因此,这些等温线可以被分类成IV型等温线,下面我们会讨论)。
尽管,接近饱和蒸汽压的多层可能会十分不连续,但大孔材料大多是通过随着相对压力增加时,吸附量逐渐地增加的方式进行多层吸附。
这种不受限制的多层形成过产生了II型和III型等温线。
在这种情况下,吸附-脱附曲线重合;也就是说,没有发生滞后现象。
这主要取决于所测试的材料的性质,II型等温线是单层形成的明显特征,否则是在整个压力范围内都是凸起的III型等温线。
后者的行为可以观察到在吸附分子与吸附剂表面和被吸附物作比较时,吸附分子之间的作用是强相互作用。
在介孔材料多层吸附过程中,常常伴随有毛细管冷凝现象发生(IV和V型等温线)。
bet多层等温吸附公式缺点

bet多层等温ห้องสมุดไป่ตู้附公式缺点
2. 温度依赖性:BET模型假设吸附过程是等温的,即吸附等温线在整个温度范围内保持不 变。然而,在实际情况下,吸附过程的温度依赖性可能存在,吸附等温线可能随温度变化而 变化。因此,BET模型在描述温度变化下的吸附行为时可能不准确。
3. 单一吸附层假设:BET模型假设只存在一层吸附层,而实际情况下可能存在多个吸附层 。这些额外的吸附层可能会对吸附行为产生重要影响,但BET模型无法准确描述这些多层吸 附行为。
bet多层等温吸附公式缺点
4. 不考虑表面异质性:BET模型假设吸附位点完全相同且相互独立,而实际情况下固体表 面可能存在异质性,即吸附位点的性质和能量可能不同。BET模型无法考虑这种表面异质性 对吸附行为的影响。
综上所述,BET模型在描述气体吸附行为时存在一些缺点,特别是在实际情况下假设条件 不成立的情况下。因此,在使用BET模型时需要考虑这些缺点,并在适用范围内进行合理的 应用。
bet多层等温吸附公式缺点
多层等温吸附模型(BET模型)是一种常用的描述气体吸附在固体表面的模型。它基于以 下假设:吸附层之间没有相互作用,吸附位点完全相同且相互独立,吸附分子在吸附层内的 分布是均匀的。
尽管BET模型在许多情况下能够提供准确的结果,但它也存在一些缺点:
1. 假设限制:BET模型的假设条件可能在实际情况下不成立。例如,吸附层之间可能存在 相互作用,吸附位点的分布可能不均匀,吸附分子在吸附层内的分布可能不是均匀的。这些 假设限制可能导致模型的适用性受到限制。
langmuir吸附等温式与bet吸附等温式的异同

Langmuir吸附等温式和BET吸附等温式都是描述气体或液体分子在固体表面上吸附的模型,但它们之间存在着一些明显的异同。
下面,我将从深度和广度的角度来探讨这两种吸附等温式的异同,并根据你的要求,以序号标注的方式呈现。
1. 定义和原理Langmuir吸附等温式是由Irving Langmuir提出的吸附理论,它假设吸附分子只能吸附在固体表面上的特定位置,且吸附分子之间不存在相互作用。
这种模型适用于单分子层吸附,通常用于描述表面活性剂和气体在固体表面上的吸附过程。
而BET吸附等温式则由Brunauer、Emmett和Teller共同提出,适用于多层吸附的情况。
相比Langmuir模型,BET模型考虑了多层吸附和吸附分子之间相互作用的影响,更贴近实际吸附过程的情况。
2. 参数和公式Langmuir吸附等温式的公式为:\[ \frac{q_{e}}{C_{e}} =\frac{{q_{\text{max}}K_{\text{L}}C_{e}}}{{1+K_{\text{L}}C_{e}}} \]其中,qe表示单位质量吸附剂上吸附的物质量,Ce表示在平衡时的吸附剂上物质的浓度,qmax为最大吸附量,KL为Langmuir常数。
而BET吸附等温式的公式则为:\[ \frac{1}{q_e(1-C_e)} = \frac{1}{q_m(1-C_e)} - \frac{C_e}{q_mB_0} \]其中,qe表示单位质量吸附剂上吸附的物质量,Ce表示在平衡时的吸附剂上物质的浓度,qm为吸附量最大值,B0为BET常数。
可以看出,Langmuir和BET模型的公式形式和参数设定有一定的区别,分别适用于单分子层吸附和多层吸附的情况。
3. 实验数据拟合在实际应用中,Langmuir和BET模型常常用于拟合吸附实验数据,以获得吸附等温线和吸附量等相关参数。
针对单分子层吸附的情况,Langmuir模型通常能够较好地拟合实验数据,给出较为准确的吸附量预测。
bet等温式属于五种吸附等温线中的类型

在研究物理化学领域时,我们经常会遇到各种吸附等温线类型的分类。
其中,bet等温式作为五种吸附等温线中的一种类型,具有其独特的特点和应用。
本文将深入探讨bet等温式的定义、特性和应用,并从不同角度进行全面评估,以便更好地理解这一主题。
一、bet等温式的定义bet等温式是由布鲁诺·保罗·贝特在1938年提出的吸附等温线类型之一。
它描述的是气体或液体在固体表面上的吸附情况,通常用来研究大面积吸附体系。
bet等温式的基本假设是固体表面上存在两种吸附位点,即吸附作用较弱的类型Ⅰ位点和吸附作用较强的类型Ⅱ位点。
根据这一假设,bet等温式能够较好地描述气体或液体在固体表面上的吸附行为。
二、bet等温式的特性1. 双层吸附:bet等温式假设固体表面上存在两种吸附位点,这导致了双层吸附的现象。
在低覆盖度下,气体或液体分子首先吸附在类型Ⅰ位点,形成单层吸附层;随着覆盖度的增加,分子继续吸附在类型Ⅱ位点,形成第二层吸附层。
这种双层吸附的特性是bet等温式的重要特点之一。
2. 吸附热:bet等温式可以通过吸附热来描述吸附过程中的能量变化。
根据bet等温式的理论,吸附热随着覆盖度的增加而减小,这与吸附类型Ⅰ位点和Ⅱ位点的吸附能力有关。
这种特性在实际应用中具有一定的意义,可以帮助我们更好地理解和控制吸附过程。
3. 吸附平衡:bet等温式还可以描述气体或液体在固体表面上的吸附平衡状态。
通过研究吸附等温线,我们可以了解吸附系统在不同温度、压力下的平衡状态,从而为工业生产和环境保护提供重要的参考依据。
三、bet等温式的应用1. 气体吸附分离:利用bet等温式的双层吸附特性,可以设计并优化气体吸附分离过程。
在石油化工行业中,通过合理选择吸附剂和操作条件,可以实现二氧化碳和甲烷等气体的有效分离和提纯。
2. 表面积测定:bet等温式广泛应用于固体材料的比表面积测定。
通过建立吸附等温线模型,可以准确地计算固体材料的比表面积,为材料表征和性能评价提供重要依据。
BET的原理与应用

BET的原理与应用一、BET的定义BET是指Brunauer-Emmett-Teller模型,是一种常用的物理吸附等温线理论模型。
它描述了气体分子在固体表面上的吸附行为,能够定量地表征固体材料的比表面积和孔隙结构。
二、BET的原理BET模型基于以下假设: 1. 固体表面是吸附分子与固体之间相互作用的场所。
2. 吸附分子吸附在固体表面形成一个单分子层。
3. 吸附分子在吸附过程中不会发生任何化学反应。
根据以上假设,BET模型推导出了以下公式: BET equation其中,P表示吸附物分子的压力,P0表示饱和蒸汽压力,V表示单位质量的吸附物分子对应的摩尔体积,C表示吸附物分子在单层上的分子个数,C_0表示单位表面积上的分子个数,V_m表示单分子层的摩尔体积。
三、BET等温线的测定方法BET等温线的测定通常需要使用气体吸附仪器,按照以下步骤进行: 1. 准备样品:样品必须是粉末或多孔颗粒状的材料。
2. 真空处理:将样品置于高真空中,除去吸附在样品表面的杂质和空气。
3. 吸附测量:通过将气体以不同的压力逐渐加入吸附仪器中,测量吸附到样品表面上的气体量。
4. 计算分析:根据BET模型的公式,将测定结果进行数据处理,得到比表面积和孔隙结构参数。
四、BET的应用领域BET广泛应用于各个领域,包括但不限于以下几个方面:1. 材料科学BET被用来评估材料的比表面积,对催化剂、吸附材料等的研究有重要意义。
通过测定材料的比表面积,可以了解其与周围环境的接触程度,进而优化材料的设计与性能。
2. 孔隙结构研究BET可以揭示材料的孔隙结构,包括孔径、孔体积等。
这对于吸附、分离等过程的研究有着重要意义,也在材料的制备和改良过程中起到指导作用。
3. 药物研发在药物研发过程中,BET可用于评估药物固体的溶解度、稳定性等关键性质。
同时,通过研究药物与载体的吸附行为,可以优化药物制剂的效果和质量。
4. 环境保护BET可用于研究和评估环境材料的吸附性能,如水处理材料、废气净化材料等。
吸附等温线解读

发生蒸发时的蒸汽压力不同
Vad
p / ps
1.0
p / ps
1.0
Langmuir 吸附等温式 Langmuir 基本假设 • 气体在固体表面上的吸附是单分子层的
• 被吸附的分子间无相互作用力
• 吸附剂表面是均匀的
• 吸附平衡是动态平衡
Langmuir 吸附等温式 Langmuir 公式推导 • 表面覆盖度 θ = V/Vm • 空白表面为 1 - θ
1 /n
V:吸附量 k,n:与温度、系统有关的常数,n一般大于1
1 lgV lg k lg p n
以lgV和lgp作图的适用范围比Langmuir公式要宽,适用 于物理吸附、化学吸附和溶液吸附。
BET 吸附等温式 BET基本假设 • 吸附可以是多分子层的 • 固体表面是均匀的 • 除第一层以外,其余各层的吸附热等于吸附质的 液化热
q f (T , p)
(1)T =常数,q = f (p),称为吸附等温式 (2)p =常数,q = f (T),称为吸附等压式
(3)q =常数,p = f (T),称为吸附等量式
吸附等温线类型
类型 I
• 单分子层吸附、L型 Vad • p远低于ps时,固体表 面就几乎被完全覆盖, 达到饱和
举例
Langmuir 吸附等温式
ka p(1 ) kd
ka 令: a kd
ka p kd ka p
ap 1 ap
这公式称为 Langmuir 吸附等温式,式中a 称为 吸附平衡常数(或吸附系数),它的大小代表了固
体表面吸附气体能力的强弱程度。
Langmuir 吸附等温式
举例
水或乙醇在硅胶上的吸附
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
p 2VL cos ln p0 rRT
pr,p0 ——与弯月液面、平液面平衡的蒸气压;VL ——液体的摩尔体积;
——液体的表面张力;
——润湿角(接触角)。
五、毛细凝聚现象
但是不管是否发生毛细凝聚,固体表面与蒸气共存时,
表面总会因吸附蒸气而形成吸附膜,在毛细孔壁上也一样,
也就是说,毛细凝聚是发生在吸附膜这个基础上的,据此 上式应修正为:
Q1 QL C exp( ) RT
是等温线为Ⅱ类,即S型;反之,若C <1,即Q1 < QL,则吸附质
与吸附剂分子间的吸引力小于吸附质为液体时分子之间的引力,
这时低压下曲线是凹的,这就是第Ⅲ类曲线。Jones的细致分析表
明,正确的临界点不是在C =1处,而是在C =2处。
四、吸附等温方程式
n
1 C xi
i 1
n
四、吸附等温方程式
x(1 x n ) 因为 x i 1 x i 1
n
d n i d x(1 x n ) ixi x x x dx i 1 dx 1 x i 1
n
VmCx 1 (n 1) x n nxn 1 所以V (1 x) 1 (C 1) x Cxn 1
§2
气相吸附
1 2
固体的表面积和孔
表征多孔性物质结构的物理量
3
4 5
吸附等温线的类型
吸附等温方程式
毛细凝聚现象
五、毛细凝聚现象
BET公式不能说明等温线的第Ⅳ、Ⅴ种类型,因为 这两类属于有毛细管凝聚作用的吸附。
所谓毛细凝聚现象是指液体蒸气在小于其饱和蒸气
压时而在固体毛细中发生液化而吸附的现象。前面讲过 kelvin公式,对于一端开口的半径为 r 的筒形毛细孔:
第八讲
吸附
四、吸附等温方程式
3. BET吸附等温式——多分子层吸附理论
这个理论是由Brunauer. Emmett和Teller在1938年将langmuire 单分子层吸附理论加以发展而建立起来的,而且迄今仍是规模 最大,影响最深、应用最广(特别是在固体比表面的测定上) 的一个吸附理论,虽然它在定量的方面并不很成功,但却能半 定量或至少定性地描述物理吸附的五类等温线,使我们对物理 吸附图像有了一个初步的正确认识。
从a,b的性质来看, a1b2 a2b1 ,所以
Q1 QL C exp RT
为便于验证,将BET公式改写成下列直线形式,
p 1 C 1 p V ( p0 p) Vm C Vm C p0 p 1 C 1 p 或 V (1 p / p0 ) Vm C Vm C p0
P 2VL cos ln P0 (r t ) RT
t ——吸附膜的厚度。
上式说明,当θ< 90°,即液体对毛细孔是润湿的,则pr < p0,即 液体在毛细孔中凝聚的压力小于正常(即平液面)的饱和蒸气压,
即在毛细管内发生凝聚所需的蒸气压低于所需正常的蒸气压,且 r
越小,pr 越低。
五、毛细凝聚现象
四、吸附等温方程式
BET理论最大的用处是测定固体的比表面。现时通用的 标准方法是N2吸附,温度是液氮的沸点。测定比表面时通常 只要在p/p0= 0.05~0.35的范围内测定4~5个点,然后将实验 数据用BET二常数公式的直线式处理,求出Vm(标准状态,
0℃,1atm)后计算总表面积。
吸附氮的优点
应当指出,kelvin公式是自热力学导出的,因此严格而言,只适合
于r 远大于吸附分子的孔中的凝聚,即r >>t,这时液体的 和弯月面 都有平常的热力学意义。倘若孔和液体分子的大小相近,例如一个孔只
能容纳几个分子,则 和曲率半径的物理意义就不明确了。由于这个理
由,kelvin公式可能不适用于微孔,至少定量上有问题,可惜这一点往 往被忽视了。另一方面,对于大孔,由于 r 大, pr 与 p0十分接近,实验 很困难,因此kelvin公式只在处理中孔的凝聚作用时才最有用。 若液体完全润湿孔壁,即θ=0°,cosθ=1,写成:
因为原假设在固体表面上的吸附层可以无限多,所以吸附量
不受限制。只有当压力等于凝结液的饱和蒸气压(即p = p0)时,才
能V→∞使。从上式可知,只有x = 1,V→∞。因为
p x ( ) exp(QL / RT ) g
四、吸附等温方程式
所以将上述关系代入x得
p0 1 ( ) exp(QL / RT )或p0 g exp(QL / RT ) g
(2)第二层及以后各层的吸附热都一样,而且等于液化热QL。
以S0、S1,S2…Si分别表示被0,1,2…i层分子所覆盖
的面积,如下图所示:
多分子层吸附示意图
则,S0=3个位置 S1=3个,S2=2个,S3=1个,S4=0个,S5=1个。
四、吸附等温方程式
达到平衡时,各种分子层覆盖的面积保持一定。例如,从空白 面积S0来看,吸附到S0上的速度要和S1层脱附的速度相等,在这种
四、吸附等温方程式
p / p0 根据实验数据用 对 p / p0 做图, V (1 p / p0 )
若得直线,则说明该吸附规律符合BET公式,且通过
直线的斜率和截距便可计算出二常数Vm和C。
若吸附发生在多孔物质上,吸附层数就要受到限制,
设只有n 层,于是:
V Vm
C i xi
i 1
p 2VL ln p0 rRT
和
p 2V ln p0 (r t ) RT
五、毛细凝聚现象
设孔都是一端开口半径为r的圆筒,r 的大小在中孔范围。因此,可以 应用kelvin公式,这样所得的吸附等温式如图所示:
存在毛细管凝聚时的等温线情形
因孔的大小是一样的,故在p处等温线沿BC垂直上升;在C处 通常认为在AB区固体的微孔(如果有的话)将被吸附分子填满。当压力达 图中CD段包括孔中由a经b至变平时所增加的凝聚液体,以及 毛细孔都被填满到图中的弯月面a处。因θ=0°,故a处的曲率半径 到p’时,发生了毛细凝聚现象,这时与p与r的关系按kelvin公式处理。 为(r-t)。压力继续升高,弯月面的曲率将降低(图中虚线所示),pr = 正常情况全部外表压力因由p’增加至p0而引起的吸附量的增量。 p0时,弯月面的曲率为0,即平面。
式中
y a1 Q1 QL C ( ) g exp( ) x b1 RT
S S i S 0 S1 S i S 0 S i
于是:
i 0
i 1
S 0 Cxi S 0 S 0 (1 C x i )
i 1 i 1
a2pS1 = b2S2exp(-QL/RT)
四、吸附等温方程式
第i层为:ai p Si-1 = bi Si exp(-QL/RT)
吸附剂的总面积:
S S 0 S1 S 2 Si Si
i 0
相应地,被吸附气体的总体积V为
V V0 (1S1 2S 2 iSi ) V0 iSi '
此时θ可以大于1。 又令b2/a2=b3/a3=…=bi/ai=g,g为常数,而认定第二层以上 的吸附、脱附性质和液态吸附质的蒸发、凝聚是一样的,换言
之,就是将第二层以上的吸附看作液体。由
a1 pS0 S1 b1 exp( Q1 / RT )
四、吸附等温方程式
令 则 又因 所以
a1 y ( ) p exp( Q1 / RT ) b1 S1 yS0 a2 pS1 b2 S 2 exp( Q2 / RT ) a2 pS1 S2 b2 exp( Q2 / RT )
上式中有三个常数,因此称为BET三常数公式,当
n =1时,BET演变为Langmuir单分子吸附方程式。
(C / p0 ) p VmCx bp V Vm Vm (1 Cx) 1 (C / p0 ) p 1 bp
四、吸附等温方程式
当n =1时,BET可以解释第Ⅰ类等温线,即
Langmuir等温线,而当n >1时,BET公式可以用
四、吸附等温方程式
BET理论认为,固体对气体的物理吸附是Vander waals
引力造成的后果。因为分子之间也有Vander wanls力,所以
分子撞在已被吸附的分子上时也有被吸附的可能,也就是
说,吸附可以形成多分子层。
四、吸附等温方程式
为了导出应用结果,他们作了两个重要假设:
(1)第一层的吸附热Q1是常数。
第Ⅱ类等温线的例子十分普通,例如许多固体在低温下
吸附N2、Ar、O2、CO等气体。第Ⅲ类等温线现象不常遇到,
最常见的水在炭黑上的吸附,这是因为水分子之间能形成比
较强烈的氢键,故表面一旦吸附了水分子,第二、三…层就 很易形成,较大的非极性有机蒸气分子在极性吸附剂上也常 得第Ⅲ类等温线,这可能与有机分子存在较大的Vander waals 引力有关。 BET公式虽然考虑到毛细孔空间对吸附层数n 的限制,但 并未涉及毛细凝结现象,因此不能解释第Ⅳ和Ⅴ类等温线。
令
a2 p x ( ) p exp(Q2 / RT ) ( ) exp(QL / RT ) b2 g
则
S 2 xS1
四、吸附等温方程式
S 3 xS2 x 2 S1
同理
S i x i 1S1
又因
S1 yS0 ,代入上式得: Si yxi 1 S0 Cxi S0
① 在-195.8℃这样的低温下,一般可避免化学吸附的干扰。
② 得到的等温线总是Ⅱ型的,这样可以得到准确的Vm。 ③ 应用最广,与其它结果相符较好,并已被定为比表面测定 的标准方法。
