基础化学电子教案习题解答(第十章)
基础化学 人卫第 版 课后习题参考答案

习题
3、(1) 5 位; (2) 3 位; (3) 2 位; (4) 1 位; (5) 2 位.
4、 RE X T 0.1023 0.1024 0.001 0.1%
T
0.1024
5
、
mol L1 J K 1 mol 1 K J L1 kg m2 s 2 L1 1000kg m1 s 2 1000Pa kPa
MB
mB Kb Tb m A
2.80g 512K g mol 1 0.51K 100g
28g mol 1
方法一:
T f
K f bB
Kf
mB M BmA
1.86
103
K
g
mol
1
28
g
2.80g mol 1 100
g
=1.9K
方法二:
T f
K f bB
Kf
Tb Kb
1.86
K
kg
mol
溶液中水的质量为: 500mL 1.00kg L1 25.0g 475g ,则葡萄糖的摩尔分
数为:
m(C6 H12O6 )
x(C6 H12O6 )
n(C6 H12O6 ) n(C6 H12O6 ) n(H 2O)
M (C6 H12O6 ) m(C6 H12O6 ) m(H 2O)
M (C6 H12O6 ) M (H 2O)
2 ,分子式为: C10 H14 N2 。
5.
Tb
K b bB
Kb
mB M BmA
MB
mB Kb Tb m A
3.24g 5120K g mol 1 1.62K 40.0g
256g mol 1
《基础化学》课后习题参考答案(有机部分)
均为 Na + , K + , Br , Cl 离子各 1mol 。
第十章开链烃1、扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答:2、NaCl 相同?如将 CH 4 及 CCl 4 各 1mol 混在一起,与 CHCl 3 及 CH 3Cl 各 1mol 的混合物是否相同? 为什么?答: NaCl 与 KBr 各 1mol 与 NaBr 及 KCl 各 1mol 溶于水中所得溶液相同。
因为两者溶液中 - -由于 CH 4 与 CCl 4 及 CHCl 3 与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合 物。
3、用系统命名法命名下列化合物:⑴2-甲基丙烷⑵2,4,4-三甲基-5-丁基壬烷⑶己烷⑷3-乙基戊烷⑸3-甲基-5-异丙基辛烷⑹2-甲基-5-乙基庚烷4、写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
H 3CCH 3 ⑴3,3-二甲基丁烷 H 3CH 2CH 3H 3C错,2,2-二甲基丁烷CH 2CH 3 ⑵2,3-二甲基-2-乙基丁烷 H 3C HC C3错,2,3,3-三甲基戊烷CH 3CH 3⑶2-叔丁基-4,5-二甲基己烷H 3CC CH 3CH 33错,2,2,3,5,6-五甲基庚烷H 3CC H 2CH 3CH 3H 3CCH⑷2,3-二甲基-4-丙基庚烷H 3H CH 2 CC H 2CH 3CH 2CH 2CH 3H 3CH 3CCH 2CH 3H 2⑸2,4,5,5-四甲基-4-乙基庚烷H 3CHC H 2 CH 3CC C 3 32 CH32CH2 3CH 2 3CH 3 3CH 3 2CH 3⑹2,2,3-三甲基戊烷H3CH3CCCH3CH2CH35、写出分子式为C6H14的烷烃的各种异构体,用系统命名法命名,丙标出伯、仲、叔、季碳原子。
1oCH 32oCH 2 2 o22 oCH2 oCH 21 o己烷1oCH 3oCH 21 o CH32 o CHo1 oCH32-甲基戊烷1 o CH31oCH 32ooCH2 oCH2 1 oCH3 3-甲基戊烷1oCHo3 oCH1 o3 2,3-二甲基丁烷1 o CH31 o1 o CH31oCH2o4 oCCH32,2-二甲基丁烷H3C 1 o 1 o CH36、⑶>⑵>⑸>⑴>⑷7、写出2,2,4-三甲基戊烷进行氯代反应可能得到的一氯代产物的结构式。
人民卫生出版社第7版《基础化学》习题第十章

共价键与分子间力首页难题解析学生自测题学生自测答案章后习题解答难题解析[TOP]例10-1试用杂化轨道理论说明乙烯分子的形成及其构型。
分析根据杂化轨道理论,形成乙烯分子时,C原子的价层电子要杂化。
共价键形成时,σ键在成键两原子间能单独存在,且只存在一个; 键在成键两原子间不能单独存在,但可存在多个。
乙烯分子中C原子的4个价电子分别与其它原子形成三个σ键,C、C原子间的双键中有一个是π键。
三个σ键决定分子构型,因此C原子有三个原子轨道参与杂化,形成三个等性杂化轨道。
解乙烯分子C2H4中有2个C原子和4个H原子,每个基态C原子的价层电子组态为2s2 2p2,在形成乙烯分子的过程中,1个2s电子被激发到2p空轨道上,然后1个2s轨道和2个2p轨道杂化形成3个等同的sp2杂化轨道,彼此间夹角为120º。
每个C原子的2个sp2杂化轨道各与1个H原子的1s轨道重叠形成2个C—H σ键;2个C原子间各以1个sp2杂化轨道互相重叠,形成1个σ键。
由于2个C 原子的这6个sp2杂化轨道处于同一平面,未参与杂化的2p z轨道则垂直于该平面,“肩并肩” 重叠形成1个π键,构成C=C双键。
乙烯分子中6个原子在一个平面上,分子呈平面构型。
例10-2 利用价层电子对互斥理论预测-I的空间构型。
3分析先确定中心原子的价电子对数,中心原子提供7个电子,配位提供1个电子,加上负离子的电荷数,得价层电子数的总和再除以2。
然后根据价层电子对构型和孤对电子决定-I的空间构型。
3解-I中有3个I原子,我们可将其中1个I作为中心原子,其余2个作为配位体。
中心原子I有73个价电子,2个配位I原子各提供1个电子,-I离子的负电荷数为1,所以中心原子的价电子对数为3(7+2+1)/2=5 。
价层电子对构型为三角双锥,因配位原子数为2,说明价层电子对中有2对成键电子对和3对孤对电子,以3对孤对电子处在三角双锥的三角形平面上排斥能最小,所以-I为直线型。
基础化学电子教案习题解答(第八章)

习题解答(第八章)一、选择题1. 下列反应中,属于氧化还原反应的是( C )A.硫酸与氢氧化钡溶液的反应B.石灰石与稀盐酸的反应C.二氧化锰与浓盐酸在加热条件下反应D.醋酸钠的水解反应2. 单质A和单质B化合成AB(其中A显正价),下列说法正确的是( C )A. B被氧化B. A是氧化剂C. A发生氧化反应D. B具有还原性3. 对于原电池的电极名称,叙述中有错误的是( B )A.电子流入的一极为正极B.发生氧化反应的一极是正极C.电子流出的一极为负极D.比较不活泼的金属构成的一极为正极4. 根据下列反应:2FeCl3+Cu→2FeCl2+CuCl22Fe3++Fe→3Fe2+2KMnO4+10FeSO4+8H2SO4→2MnSO4+5Fe2(SO4)3+K2SO4+8H2O 判断电极电势最大的电对为( C )A.Fe3+/Fe2+B.Cu2+/CuC.MnO4-/Mn2+D.Fe2+/Feϕ5. 在含有Cl-,Br-,I-离子的混合溶液中,欲使I-氧化成I2,而Br-,Cl-不被氧化,根据φ值大小,应选择下列氧化剂中的( B )A.KMnO4B.K2Cr2O7C.(NH4)2S2O8D.FeCl36. 在酸性溶液中和标准状态下,下列各组离子可以共存的是( D )A.MnO4- 和Cl-B.Fe3+ 和Sn2+C.NO3- 和Fe2+D.I- 和Sn4+7. 利用标准电极电势表判断氧化反应进行的方向,正确的说法是( B )A.氧化态物质与还原态物质起反应;ϕ较大电对的氧化态物质与φϕ较小电对的还原态物质起反应;B. φC.氧化性强的物质与氧化性弱的物质起反应;D.还原性强的物质屯还原性弱的物质起反应。
二、是非题(下列叙述中对的打“√”,错的打“×”)1. MnO4-离子中,Mn和O的化合价分别为+8和-2。
( ×)2. 根据标准电极电势判定SnCl2 + HgCl2 =SnCl4 + Hg反应能自发向右进行。
2024届高考一轮复习化学教案(人教版)第十章有机化学基础热点强化24多官能团有机物的结构与性质
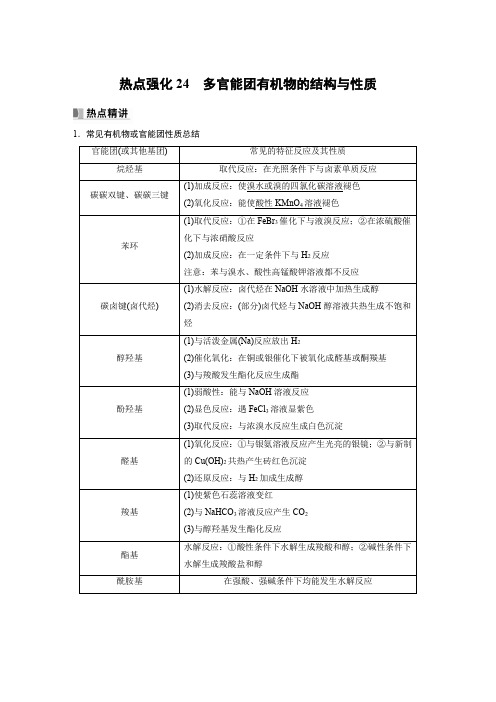
热点强化24多官能团有机物的结构与性质1.常见有机物或官能团性质总结官能团(或其他基团)常见的特征反应及其性质烷烃基取代反应:在光照条件下与卤素单质反应碳碳双键、碳碳三键(1)加成反应:使溴水或溴的四氯化碳溶液褪色(2)氧化反应:能使酸性KMnO4溶液褪色苯环(1)取代反应:①在FeBr3催化下与液溴反应;②在浓硫酸催化下与浓硝酸反应(2)加成反应:在一定条件下与H2反应注意:苯与溴水、酸性高锰酸钾溶液都不反应碳卤键(卤代烃)(1)水解反应:卤代烃在NaOH水溶液中加热生成醇(2)消去反应:(部分)卤代烃与NaOH醇溶液共热生成不饱和烃醇羟基(1)与活泼金属(Na)反应放出H2(2)催化氧化:在铜或银催化下被氧化成醛基或酮羰基(3)与羧酸发生酯化反应生成酯酚羟基(1)弱酸性:能与NaOH溶液反应(2)显色反应:遇FeCl3溶液显紫色(3)取代反应:与浓溴水反应生成白色沉淀醛基(1)氧化反应:①与银氨溶液反应产生光亮的银镜;②与新制的Cu(OH)2共热产生砖红色沉淀(2)还原反应:与H2加成生成醇羧基(1)使紫色石蕊溶液变红(2)与NaHCO3溶液反应产生CO2(3)与醇羟基发生酯化反应酯基水解反应:①酸性条件下水解生成羧酸和醇;②碱性条件下水解生成羧酸盐和醇酰胺基在强酸、强碱条件下均能发生水解反应2.有机反应中的几个定量关系(1)1 mol加成需要1 mol H2或1 mol Br2。
(2)1 mol苯完全加成需要3 mol H2。
(3)1 mol —COOH与NaHCO3反应生成1 mol CO2气体。
(4)1 mol —COOH与Na反应生成mol H2;1 mol —OH与Na反应生成mol H2。
(5)与NaOH反应,1 mol —COOH消耗1 mol NaOH;1 mol (R、R′为烃基)消耗1 mol NaOH。
1.4-溴甲基-1-环己烯的一种合成路线如下:下列说法正确的是()A.化合物W、X、Y、Z中均有一个手性碳原子B.①②③的反应类型依次为加成反应、还原反应和消去反应C.由化合物Z一步制备化合物Y的转化条件是NaOH的水溶液,加热D.化合物Y先经酸性高锰酸钾溶液氧化,再与乙醇在浓硫酸催化下酯化可制得化合物X 答案C解析A项,化合物X、Y、Z连接支链的碳原子为手性碳原子,化合物W中没有手性碳原子;B项,1,3-丁二烯与丙烯酸乙酯加成生成X,X发生还原反应生成Y,Y发生取代反应生成Z;D项,Y中含有碳碳双键,可被酸性高锰酸钾溶液氧化。
《基础化学》习题答案第3版

《基础化学》习题答案(第3版)第一章 习题答案1.答:能量单位J 、质量单位μg 、长度单位nm 、温度单位℃、属于SI 单位;其他不是。
2.答:SI 基本单位:m 、kg 、s 、A 、K 、mol 、cd 。
3.答:一切属于国际单位制的单位都是我国的法定计量单位。
根据我国的实际情况,在法定计量单位中还明确规定采用了若干可与国际单位制并用的非国际单位制单位。
第二章习题答案1. 解: 根据)()O H ()O H ()O H (222蔗糖n n n x +=0292mol .0mol 342g g0.10)( mol 56.5mol 18.0g g 100)O H (1-1-2=⋅==⋅=蔗糖n n995.00.0292molmol 56.5mol56.5)O H (2=+=xkPa33.20.995kPa 34.2)O H ()O H (2*2=⨯==x p p2.解:)B ()O H ()()O H (999.00.1molmol 08mol08)O H ()O H ()O H ()O H (899.00.1molmol 04mol04)O H ()O H ()O H ()(999.00.1molmol 80mol80)()()()O H (999.00.1mol mol 80mol80)O H ()O H ()O H (*2**2*22*22*2*22*23***2*2*22*21答案为苯苯苯苯苯∴>=+⋅===+⋅===+⋅===+⋅==p p p p x p p p p x p p p p x p p p p x p p3.解:与人体血浆等渗。
11os f 11os f B f B f f 11-1-1-os L mmol 310L mol 31.0C58.0K58.0L mol 31.0mol kg K 86.1L mol 31.0L00.1mol 147g g33.03mol 74.6g g 30.02mol 58.5g g 50.82-----⋅=⋅=︒-==⋅⨯⋅⋅=≈≈=∆⋅=⋅⨯+⋅⨯+⋅⨯=c T c K c iK b iK T c4.解:K 85.1molkg K 512.00.510Kmol kg K 86.1mol g 1.28mol kg 0281.00.510K 250g g 00.7mol kg K 512.011b b f B f f 111b A B b B =⋅⋅⋅⋅⋅=∆⋅=⋅=∆⋅=⋅=⨯⨯⋅⋅=∆⋅⋅=-----K T K b K T T m m K MT f = -1.85℃ 5. 解:压略高于人体眼液的渗透kPa869K 310K mol L kPa 314.8L mol 337.0L mmol 337L mol 337.0mL10001.000LmL 1000mol 61.8g g 00.17mol 161.5g g 00.52111-os 1-1-1-1-os =⨯⋅⋅⋅⨯⋅==⋅=⋅=⨯⋅+⋅⨯=--RT c Πc6. 解:11A fB f B 11A b B b B mol kg 61.1100g0.220K g0.19mol kg K 86.1mol kg 62.1100g 0.0600K g 0.19mol kg .512K 0----⋅=⨯⨯⋅⋅=∆=⋅=⨯⨯⋅⋅=∆=m T m K M m T m K M用两种方法计算该物质的相对分子质量基本相同。
基础化学电子教案习题解答(第二章)

习题解答(第二章)1.选择题(1)25℃时,0.01mol/kg的糖水的渗透压为π1,而0.01 mol/kg的尿素水溶液的渗透压为π2,则____②____。
①π1<π2②π1 =π2③π1>π2④无法确定(2)应用克-克方程回答问题:当物质由固相变为气相时,平衡压力随温度降低而__③_____。
①不变②升高③降低④视不同物质升高或降低(3)通常称为表面活性剂的物质,是指当其加入少量后就能____③_____的物质。
①增加溶液的表面张力②改变溶液的导电能力③显著降低溶液的表面张力④使溶液表面发生负吸附(4)兰格缪尔(Langmuir)等温吸附理论中最重要的基本假设是_④___。
①气体为理想气体②多分子层吸附③固体表面各吸附位置上的吸附能力是不同的④单分子吸附(5)溶胶的基本特征之一是____④____。
④①热力学上和动力学上皆稳定的系统②热力学上和动力学上皆不稳定的系统③热力学上稳定而动力学上不稳定的系统④热力学上不稳定而动力学上稳定的系统(6)下列各性质中,属于溶胶的动力学性质的是___①_____。
①布朗运动②电泳③丁达尔现象④流动电势(7)引起溶胶聚沉的诸因素中,最重要的是___④______。
①温度的变化②溶胶浓度的变化③非电解质的影响④电解质的影响(8)用KBr加入浓的AgNO3溶液中,制备得AgBr溶胶,再向其中加入下列不同的电解质,能使它在一定时间内完全聚沉所需电解质最少的是__③______。
①Na2SO4②NaNO3 ③K3[Fe(CN)6] ④KCl(9)等体积0.10mol/dm3 KI和0.12mol/dm3的AgNO3溶液混合制成的AgI溶胶,下列电解质中,聚沉能力最强的是___④_______。
①Na 2SO 4 ②MgSO 4 ③K 3[Fe(CN)6] ④FeCl 32. 简答题(1) 理想气体存在吗?真实气体的pVT 行为在何种条件下可用pV=nRT 来描述?答:事实上,理想气体不存在。
2024届高考一轮复习化学教案(鲁科版)第10章化学实验基础知识及实验热点第64讲物质的分离与提纯

第64讲物质的分离与提纯[复习目标] 1.掌握常见物质分离和提纯的方法。
2.能综合运用物质的不同性质对常见的物质进行分离和提纯。
考点一物质分离、提纯的常用物理方法及装置(一)物质分离与提纯的区别分离将混合物的各组分分开,获得几种纯净物的过程提纯将混合物中的杂质除去而得到纯净物的过程,又叫物质的净化或除杂(二)辨认下列五个装置的作用及使用注意事项1.固液分离(1)图1为过滤装置,适用于不溶性固体与液体的分离。
操作注意:一贴、二低、三靠。
(2)图2为蒸发装置,溶解度随温度变化不大的易溶性固体溶质,采用蒸发结晶;溶解度受温度变化较大的易溶性固体溶质,采用蒸发浓缩、降温结晶的方法。
注意在蒸发结晶操作中:①玻璃棒的作用:搅拌,防止液体局部过热而飞溅;②当有大量晶体析出时,停止加热,利用余热蒸干而不能直接蒸干。
2.液液分离(1)图3为分液装置,分离两种互不相溶且易分层的液体。
注意下层液体从下口放出,上层液体由上口倒出。
(2)图4为蒸馏装置,分离沸点相差较大且互溶的液体混合物。
注意①温度计的水银球在蒸馏烧瓶的支管口处;②蒸馏烧瓶中要加沸石或碎瓷片,目的是防止暴沸;③冷凝管水流方向为下口进,上口出。
3.固固分离图5为升华装置,适应于某种组分易升华的混合物的分离。
1.过滤时,为加快过滤速度,应用玻璃棒不断搅拌漏斗中的液体()2.根据食用油和汽油的密度不同,可选用分液的方法分离()3.用乙醇萃取出溴水中的溴,再用蒸馏的方法分离溴与乙醇()4.在蒸馏过程中,若发现忘加沸石,应停止加热立即补加()5.利用加热的方法分离NH4Cl和I2的固体混合物()6.制取无水乙醇可向乙醇中加入CaO之后过滤()答案 1.× 2.× 3.× 4.× 5.× 6.×1.利用物质的溶解度对物质进行分离、提纯图甲、图乙所示为一些物质的溶解度随温度变化的曲线。
(1)A点KNO3溶液是__________(填“饱和溶液”或“不饱和溶液”)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
思考与习题
一、选择题
1.分子组成符合CnH2n-2通式的化合物可能是 B
A 环烷烃
B 环烯烃
C 环状共轭二烯烃
D 单环芳烃
2.能使溴水溶液颜色褪去的物质可能是 B
A 环戊烷
B 甲基环丙烷
C 苯
D 乙基环己烷
3.不能发生傅-克反应的物质是 B
A 甲苯
B 硝基苯
C 氯苯
D 叔丁基苯
4.不能使酸性高锰酸钾溶液褪色的物质是 B
A 环己烯
B 环己烷
C 甲苯
D 1,3-丁二烯
5.能够活化苯环的第一类定位基是 C
A -Cl
B -CHO
C –NHCOCH3
D -SO3H
二、判断正误。
正确的划“√”,错误的划“ⅹ”。
1.环己烷分子内碳原子间的键角为正常键角109.5°,不存在环张力,分子很稳定,体现
同饱和脂肪烃一样性质。
(√)
2.芳香烃和卤素在催化剂的作用下发生反应,苯环上的氢原子被卤素取代,生成卤代芳烃。
(√)
3.—NHCOR,—OCOR,—CONH2都是邻对位定位基。
(×)
4.吡啶环碳原子的电子云密度相对于苯环小,是缺电子的芳杂环。
(√)
5.五元芳杂环是富电子的芳杂环。
噻吩与硫酸亲电取代反应易于苯,在室温条件下即可
发生反应。
(√)
三、填空题
1.把下列化合物的结构式填在横线上面。
呋喃O, 1,1,2-三甲基环戊烷,
2
Cl
,
,噻吩O,吡啶N,8-羟
基喹啉
N
OH,2,4-二甲基环己烯
CH3
CH3。
2.硝基是间位定位基;烷氧基是邻、对位定位基3.完成下列反应方程式:
+
HBr
(1)
CH 2H C
C
CH 3
CH 3
3H
CH 2CH 3
24
KMnO4
(2)
HOOC CH 2CH 2CH 2CH 2CH 3
COOH
CH
CH 2CH 3
24
2Fe
H 2O
(3)
CH 2CH 3
3H
CH 2CH 3
SO 3H
Cl
CH 2CH 3
Cl
(4)
C 12H 25
24
40~50℃
NaOH
C 12H 25
SO 3H
C 12H 25
SO 3Na
(5)
CH 3
+CH 3
C
O
O
C
O CH 3
无水AlCl 3
CH 3
C O CH 3
(6)
浓H
SO
∆
SO 3H
Cl
N
浓HNO 324
(7)
N
NO 2
S
室温
S
SO 3H
+
H 2O
(8)
N HNO 3
(9)
N COOH COOH
(10)
N
CH 3
HNO 3N
COOH
四、简答题
1.什么是角张力?
解答:偏离正常键角而产生的张力。
2.什么是芳香性?
解答:以苯为代表的一类高度不饱和的烃易取代而不易加成的性质。
3.如何用简单的化学方法区别下列各组化合物。
(1)环己烷、环己烯和1-己炔
解答:
环己烷环己烯1-
己炔
有沉淀生成的是1-己炔
无明显现象的是
环己烷环己烯
(2)丙烷、环丙烷和丙烯
解答:
丙烷环丙烷丙烯
KMnO 4
KMnO 4颜色褪去的是丙烯无明显现象的是
环丙烷
丙烷
无明显现象的是丙烷
(3)环己烯、苯和甲苯
解答:
甲苯苯环己烯
溴水褪色的是
无明显现象的是
甲苯
苯
+
KMnO 4
(4)乙苯、苯乙烯和苯乙炔
解答:
乙苯苯乙烯
苯乙炔
不能使溴水褪色的是乙苯
溴水颜色褪去的是
苯乙烯
苯乙炔
4.如何除去下列化合物中的少量杂质。
(1)将甲苯中混有少量的吡啶除去。
解答:在其中加入适量的H2SO4,充分混合振荡,吡啶的碱性与酸化合进入酸层,静置分层分离出H2SO4即可。
(2)苯中混有少量的噻吩。
解答:在其中加入适量的浓H2SO4,室温下噻吩与浓H2SO4发生磺化反应,产生溶于H2SO4层,静置分层分离出浓硫酸层即可。
5.简述邻对位定位基、间位定位基的特点。
解答:邻对位定位基在结构上与芳环直接相连的碳原子以单键与其它原子相连接,有些与芳环直接相连的原子带有负电荷或有未共用的孤电子对;多为活化苯环的基团。
间位定位基在结构上与芳环直接相连的原子多以重键与其它原子相连接,有些与芳环直接相连的原子带正电荷;全为钝化苯环的基团。
五、综合题
1.某芳烃的分子式为C8H10,用高锰酸钾和浓硫酸氧化后,可得一种二元酸。
将原来的芳烃进行硝化,所得一元硝基化合物只有一种。
写出此芳烃的结构式,并写出有关反应式。
解:依题意推知该芳烃的结构式为:
CH3
3
CH3
CH3
或
推导过程为:
CH 3
CH 3CH 3
CH 3
KMnO 424
COOH
H 2SO 43
COOH
COOH
NO 2
[O ]
COOH
COOH
HNO 3
24
COOH
COOH
NO 2
2.某化合物其分子式为C 6H 6OS ,它不发生银镜反应,但能与羟胺作用生成肟,与次氯酸钠作用生成α—噻吩甲酸钠。
写出该化合物的结构式,并写出有关反应式。
解:依题意推知该化合物的结构为:
S
CH 3
O
推导过程为:
S
CH 3
O
NH 2-OH
S
CH 3
N
OH
+
H 2O
S
COONa
H +
S
COOH。
