《工程化学》教学日历
《工程化学》授课计划

2题
讲授
19
3.5.5电极电势的应用(二)
(拓展到电解的应用)
2
2题
讲授
20
实验三原电池、配合物
4
实验报告
实验
21
阶段二考核
2
试卷
习题课
22
5有机化合物与高聚物(自编内容)
5.1有机化合物的概述
5.2有机化合物的命名(一)---烷烃、卤代烷烃
2
2题
讲授
23
5.2有机化合物的命名(二)---炔烃、烯烃及其他
配合物的应用
2
2题
讲授
15
实验二化学反应平衡
3
实验报告
实验
16
3.5氧化还原平衡及电化学基础
3.5.1氧化还原反应
3.5.2原电池和电极电势(一)
2
2题
讲授
17
3.5.2原电池和电极电势(二)
3.5.3原电池的电动势与摩尔反应吉布斯函数变化的关系
2
2题
讲授
18
3.5.4影响电极电势的因素
3.5.5电极电势的应用(一)
水的解离平衡
2
2题
讲授
缓冲溶液的解离平衡
2
2题
讲授
11
3.3沉淀—溶解平衡(一)
沉淀—溶解平衡的建立
溶度积与溶解度
溶度积规则
2
2题
讲授
12
3.3沉淀—溶解平衡(二)
溶度积的应用实例
2
2题
讲授
13
3.4配位平衡(一)
配合物的组成和命名
配位平衡及稳定常数
2
2题
讲授
14
3.4配位平衡(二)
化工原理及实验 教学日历
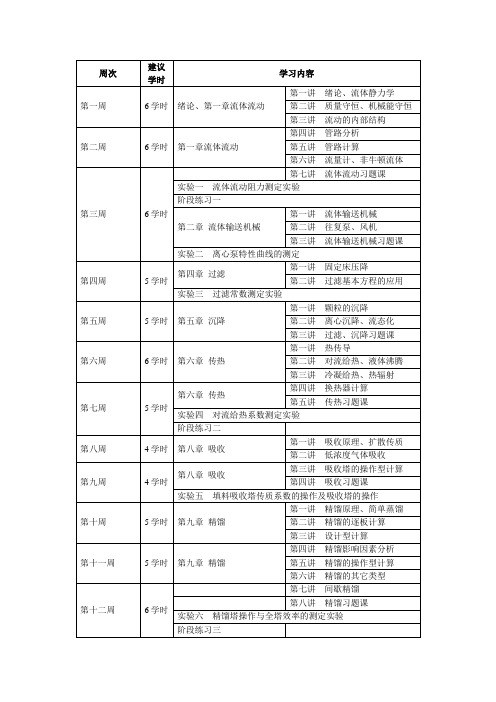
5学时
第九章精馏
第一讲精馏原理、简单蒸馏
第二讲精馏的逐板计算
第三讲设计型计算
第十一周
5学时
第九章精馏
第四讲精馏影响因素分析
第五讲 精馏的操作型计算
第六讲 精馏的其它类型
第十二周
6学时
第七讲 间歇精馏
第八讲 精馏习题课
实验六 精馏塔操作与全塔效率的测定实验
阶段练习三
第十章气液传质设备
第一讲 板式塔,填料塔
第二讲往复泵、风机
第三讲 流体输送机械习题课
实验二 离心泵特性曲线的测定
第四周
5学时
第四章过滤
第一讲 固定床压降
第二讲 过滤基本方程的应用
实验三 过滤常数测定实验
第五周
5学时
第五章沉降
第一讲 颗粒的沉降
第二讲 离心沉降、流态化
第三讲 过滤、沉降习题课
第六周
6学时
第六章传热
第一讲 热传导
第二讲 对流给热、液体沸腾
实验八 干燥速率曲线测定实验
阶段练习四
第三讲 冷凝给热、热辐射
第七周
5学时
第六章传热
第四讲换热器计算
第五讲 传热习题课
实验四 对流给热系数测定实验
阶段练习二
第八周
4学时
第八章吸收
第一讲 吸收原理、扩散传质
第二讲 低浓度气体吸收
第九周
4学时
第八章吸收
第三讲 吸收塔的操作型计算
第四讲 吸收习题课
实验五 填料吸收塔传质系数的操作及吸收塔的操作
第十三周
4学时
第十一章萃取
第一讲 液液萃取
实验七 液萃取塔的操作及萃取传质单元高度的测定实验
《工程化学》教案

《工程化学》教案总纲一、课程性质及教学目的:《工程化学》是全校非化学化工专业理工科本科生校级必修课。
是素质教育的重要课程之一。
工程化学是从物质的化学组成、化学结构和化学反应出发,密切联系现代工程技术中遇到的如材料的选择和寿命、环境的污染与保护、能源的开辟与利用、信息传递、生命科学发展等有关化学问题,深入浅出地介绍有现实应用价值和有潜在应用价值的基础理论和基本知识 ,使学生在今后的实际工作中能故意识的运用化学观点去思量、认识和解决问题。
该课程的任务是激发学生学习化学的兴趣,将化学的思维方法和能力传授给学生,通过介绍化学理论在工程实际中的应用,把化学对人类进步的影响逐渐渗透到学生的脑海中,从而提高学生的化学素质。
二、课程内容:工程化学课程内容包含绪论、物质的化学组成和会萃状态、化学反应原理、水溶液中的化学反应和水体保护、电化学基础、物质结构基础等六部份。
纵观工程化学所含内容可知,该课程内容较为庞杂。
具有三多的特点;即所谓内容头绪多、原理规律多(涉及原理、规律几十个)、概念定义多,由于该课程具有上述特点,加之微观结构看不见、摸不到。
因此,教师感到难教,学生感到难学。
三、教学对象:非化学化工类理工科本科新生。
四、教学时间:第一学期或者第二学期五、教学指导思想:1. 从工程实际和生活实际的角度出发讲授《工程化学》,体现21 世纪教学理念、教学改革精神和世界工程教育思想。
2. 严格按《工程化学》教学大纲及《工程化学实验大纲》进行教学,注意课程内容的准确定位和整体优化,注重课程的趣味性和实用性。
3. 开设的实验及课堂讨论应有利于激发学生的学习兴趣、有利于培养学生分析问题、解决问题及知识创新的能力。
六、教学重点:1. 系统与环境、反应进度、化学计量数;2. 气体分压定律,大气相对湿度,等离子体;3. 稀溶液的依数性;3. 晶体及其性质;4. 热力学第一定律;5. 焓与焓变,熵与熵变,吉布斯函数变;6. 盖斯定律;7. 化学反应等温式;8. 浓度(压力)、温度等因素对化学平衡的影响;9. 浓度、温度、催化剂等因素对化学反应速率的影响;10. 酸碱质子理论;11. 酸碱解离平衡常数;12. 缓冲溶液及有关pH 计算;13. 溶度积及溶度积规则的应用;14. 难溶电解质稳定平衡常数;;15.四个量子数的意义、符号及电子组态表示的意义;16.杂化轨道理论;17.周期系元素原子的核外电子分布的普通规律;18.份子间作用力。
大学化学课程 教学日历

(3)太阳能、风能、生物质能
1
15课堂报告2 Nhomakorabea第17周
第10章材料与化学
10.1重要金属及合金材料
10.2新型无机材料
新材料VCD,纳米材料VCD
2
课堂报告
2
第17周
10.3有机高分子材料
10.5建筑用胶凝材料
2
6
2
第18周
专题学习
(1)稀土元素与光电技术
(2)神奇的纳米材料
(3)形形色色的化学建材
2
2
第4周
一级反应积分式,
T与v的关系,
催化作用,
2.4几种类型的反应
2
6
2
第5周
第3章化学平衡
3.1平衡常数
3.1.1分压定律
3.1.2平衡常数
3.1.3标准平衡常数与吉布斯自由能的关系
2
2
第5周
3.1.3标准平衡常数与温度的关系
3.2弱电解质电离平衡
3.2.1一元弱酸,弱碱的电离平衡
3.2.2多元弱酸的电离平衡
3.2.3缓冲溶液
2
2
第6周
3.3沉淀-溶解平衡
3.3.1溶度积
3.3.2溶度积规则
3.4配离子离解平衡
2
8
2
第7周
课堂讨论:
从化学热力学和动力学角度,结合生产实际谈谈合成氨的条件
4.1原电池
4.1.1原电池
1
1
2
第7周
4.1.2电极类型
4.2电极电势
4.2.1电极电势的产生
4.2.2电极电势的测量
5.1.4电子运动状态的完全描述与四个量子数
2
工程化学课程教学大纲

工程化学课程教学大纲英文名称:Engineering Chemistry 课程编码:10110010学时:32/6 学分:2课程性质:公共必修课课程类别:理论课先修课程:开课学期:第一学期适用专业:机械工程学院、电气工程学院、信息工程学院、理学院、建工学院等一、课程的性质与任务工程化学是机械学院、电气学院、信息学院、理学院、车辆学院、建工学院等学院学生必修基础课程,工程化学从物质的化学组成、化学结构和化学反应出发,密切联系现代工程技术中遇到的如材料的选择和寿命、环境的污染与保护、能源的开发与利用、信息传递、生命科学发展等有关化学问题,深入浅出地介绍有现实应用价值和有潜在应用价值的基础理论和基本知识,使学生在今后的实际工作中能有意识地运用化学观点去思考、认识和解决问题。
二、教学目标与要求工程化学课程内容共分六章,第一章物质的聚集状态;第二章化学反应原理;第三章水溶液中的离子平衡;第四章电化学基础;第五章物质结构基础;第六章化学与人类的进步。
通过本课程的学习,使机械学院、电气学院、信息学院、理学院、车辆学院、建工学院等学院学生掌握化学基础知识,为进一步提高专业素质训练奠定基础。
三、课程的基本内容与教学要求第一章物质的聚集状态[教学目的与要求]:理解系统、环境概念;掌握“物质的量”的符号、单位及有关计算;理解反应进度的概念,掌握化学计量数正、负值的确定。
理解各类晶体名称、晶格结点上粒子及其作用力、熔点、硬度、延展性、导电性,掌握溶液的蒸汽压下降、凝固点下降、沸点上升和产生渗透压的原因;了解等离子态的形成和组成,了解大气湿度概念和相对湿度的计算,掌握酸雨的pH值范围,理解温室气体和温室效应,理解臭氧层出现空洞原因、危害和预防措施。
[本章主要内容]:1.1化学基本概念1.2气体、等离子体1.3液体和水污染1.4固体、固体废弃物污染及治理[本章重点]:1.分子、原子、元素、系统、环境、相、气体、等离子体等基本概念2.稀溶液的通性3. 晶体类型[本章难点]:1.稀溶液的通性2.过渡型晶体第二章化学反应原理[教学目的与要求]:明确焓变和内能的变化是不同过程中系统变化时总能量的改变,理解Qp,Qv,ΔrH,Δf H m(H2O),ΔrHθm等各符号的名称、意义,了解ΔG在化学反应中的意义,理解其作为反应自发性判据,理解ΔrHθm(T)≈ΔrHθm(298.15),ΔrSθm(T)≈ΔrSθm(298.15),掌握ΔrGθm(T), ΔrG(298.15), ΔrGm的计算方法。
《工程化学》教学日历
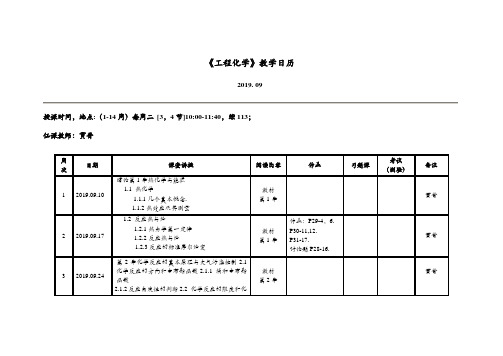
教材
第4章
P156-9, 13, 14
P157-15, 23,24
黄晋
8Hale Waihona Puke 2019.10.29第5章物质结构基础5.1原子结构的近代概念5.1.1波函数5.1.2电子云5.2多电子原子的电子分布方式和周期系5.2.1多电子原子轨道的能级5.2.2核外电子分布原理和核外电子分布方式
5.4晶体结构5.4.1晶体的基本类型
教材
第5章
P156-9, 13, 14
P157-15, 23,24
黄晋
10
2019.11.12
第7章高分子化合物7.1高分子化合物概述
7.1.1高分子化合物的定义7.1.2高分子的一般结构特点7.1.3高分子的分类7.1.4高分子的命名7.2高分子的合成7.2.1高分子聚合反应的分类7.2.2几种重要的聚合反应7.2.3可控聚合反应7.3高分子的结构和性能7.3.1高分子的结构7.3.2高分子的分子热运动与玻璃化转变
第9章分析化学基础(主要教材中无此章节,采用自编PPT材料)
自编材料
第9章
黄晋
教学14周,授课14周完成;
授课14次,每次90分钟(连续);
实验(项目)2次;测验(考查)1次。
2.1.2反应自发性的判断2.2化学反应的限度和化学平衡2.2.1反应限度和平衡常数
2.2.2化学平衡的有关计算
教材
第2章
黄晋
4
2019.10.1
2.2.3化学平衡的移动及温度对平衡常数的影响
2.3化学反应速率2.3.1化学反应速率和速率方程2.3.2温度对反应速率的影响(自学)2.3.3反应的活化能和催化剂(自学)2.3.4链反应和光化反应(自学)
《工程化学基础》课程教学大纲
《工程化学基础》课程教学大纲第一篇:《工程化学基础》课程教学大纲《工程化学基础》课程教学大纲授课专业:机械自动化学时数: 36 学分:2 •课程的性质和目的《工程化学基础》是非化工类各专业培养现代工程技术和管理人才的必修基础课,是工科非化工类各专业(本科)化学类课程的终结课程,将为工科非化工类各专业的专业课程学习提供必要的化学理论知识基础。
本课程从物质的化学组成、化学结构和化学反应出发,结合工程材料、环境污染、能源开发、信息传递、生命科学等当今五大领域的有关化学问题进行讨论,帮助学生建立物质变化的观点和能量变化的观点,提高学生的基本素质和创新能力。
•课程教学内容第一章绪论(2学时)要求一般理解与掌握的内容:系统、相、物质的量及反应进度的概念。
重点;相的概念。
难点:反应进度的概念和表达式的导出。
第二章物质的化学组成和聚集状态(6学时)要求一般理解和掌握的内容有:具有复杂化学组成的物质、高分子化合物、配位化合物、生物大分子、晶体与非晶体、固体吸附剂、固体废弃物、石油、表面活性剂、大气相对湿度、酸雨、温室效应和臭氧层空洞、气溶胶、等离子体等概念。
水的性质及其应用。
稀溶液的依数性。
理想气体状态方程式。
重点:稀溶液的依数性;理想气体状态方程式的应用条件和相关计算。
难点:稀溶液依数性的相关计算及应用。
第三章物质的结构和材料的性质(6学时)要求一般理解和掌握的内容有:电子运动的特征。
原子轨道和电子云。
四个量子数。
多电子原子的核外电子排布。
金属元素和金属材料。
能级跃迁和光谱分析。
化学键。
分子间力和氢键。
分子能级跃迁和分子吸收光谱。
高分子的结构和高分子材料。
晶体缺陷。
能带理论。
陶瓷的结构和性能。
复合材料。
重点:离子键理论和共价键理论;四个量子数表征的意义和可取数值。
难点:核外电子运动的特征;原子轨道和电子云的涵义。
第四章化学反应与能源(8学时)要求一般理解和掌握的内容有:热力学能、热效应和焓变、等容过程的热和等压过程的热、标准摩尔焓变、热力学能变和焓变的关系;化学反应的自发性、熵、吉布斯自由能、自由能判据;化学反应速率、影响化学反应速率的因素;化学反应的可逆性、化学平衡和平衡常数、化学平衡的移动;原电池、电极电势的产生、标准电极电势、能斯特方程、电极电势的应用;化学电源、新能源。
工程化学课程教学大纲
课
程
内
容
及
学
时
分
配
课
程
内
容
及
学
时
分
配பைடு நூலகம்
第一章:物质结构(9学时)
1.原子结构
2.分子结构
3.分子间力和氢键
4.固态物质的结构
了解微观粒子的波粒二象性。了解波函数和原子轨道、几率密度和电子云。理解四个量子数。了解原子轨道和电子云的角度分布图。了解多电子原子的能级。掌握核外电子排布的规律。掌握原子的电子层结构和元素周期系。了解原子结构与元素性质的关系(重点是电离能和电负性)。
《工程化学》课程教学大纲
课程
编号
01064001
课程
名称
(中文)工程化学
(英文)Engineering Chemistry
课
程
基
本
情
况
1.学分:3学时:30(课内学时:30实验学时:)
2.课程性质:公共基础课
3.适用专业:理学、工学、文学、经济学、教育学、管理学
适用对象:本科
4.先修课程:
5.首选教材:《工程化学》上大工程化学编写组上海大学出版社1999.08
理解氢键的形成及其对物质性质的影响。掌握离子晶体、共价晶体、分子晶体、金属晶体四种晶体的内部结构及性质特征。
掌握一元弱酸、碱的电离平衡和电离度的概念,并能进行有关计算。掌握缓冲溶液pH值的计算。
掌握离子-电子法配平电极反应式。
掌握电极电位的概念、能斯特方程及其有关计算。
掌握金属的腐蚀及电化学腐蚀的原理及影响金属腐蚀的因素。
掌握金属的腐蚀及电化学腐蚀(析氢腐蚀,吸氧腐蚀,差异充气腐蚀)的原理及影响金属腐蚀的因素。
学年第一学期教学日历及教学环节表
2019 -2020 学年第一学期教学日历及教学环节表(一)2019.9.2更新备注:1. 老生2019年8月31日~9月1日报到、领取教材,9月2日正式上课,9月21、22日补考18-19-2学期不及格课程。
2. 2019级新生9月7~8日报到,9月9日-12日入学教育、体检,9月11日上午开学典礼,9月16日~9月29日军训,10月8日上课。
3.“中秋节”放假:9月13~15日(三天);“国庆节”放假:10月1日~10月7日(七天),9月29日调上10月4日的课,10月12日调上10月7日的课;2020年“元旦”放假按照国家规定的法定假日执行。
4. 2019年10月24、25日校运动会;第十周为期中考试周,各二级学院安排期中考试。
5. 2019年11月16日为职业技能鉴定全省统一鉴定日;2019年12月14日为大学英语四、六级考试日;2019年12月15日为大学英语A、B级考试日。
6. 本学期学生上课结束时间为2020年1月3日,期末考试时间为1月4~5日。
学生寒假时间为2020年1月6日~2月14日。
7. 19材料631、19材料661合班上课,19环境631、19精化331合班上课,19自动661、19光伏331合班上课,19电子631、19无人机631合班上课。
2019 -2020学年第一学期教学日历及教学环节表(二)备注:1. 老生2019年8月31日~9月1日报到、领取教材,9月2日正式上课,9月21、22日补考18-19-2学期不及格课程。
2. 2019级新生9月7~8日报到,9月9日-12日入学教育、体检,9月11日上午开学典礼,9月16日~9月29日军训,10月8日上课。
3.“中秋节”放假:9月13~15日(三天);“国庆节”放假:10月1日~10月7日(七天),9月29日调上10月4日的课,10月12日调上10月7日的课;2020年“元旦”放假按照国家规定的法定假日执行。
4. 2019年10月24、25日校运动会;第十周为期中考试周,各二级学院安排期中考试。
昆明理工大学教学进度日历表(下学期)
4
肉桂酸合成
5
七
4
乙酰水杨酸合成
6
八
6
黄连素提取
7
九
4
醛、酮、糖的性质
学院名称:化学工程学院
院长审批(签字):填表日期:
教研室名称:化学教研室教研室主任审批(签字):填表日期:
烷烃的结构、命名、性质
P39、习题
2
4
第三章烯烃(3)
第四章炔烃二烯烃(4)
烯烃的结构、命名及性质
炔烃、二烯烃的结构、命名、
P63、习题
3
4
第四章(二)
第五章脂环烃(2)
炔烃、二烯烃性质、共轭基本概念
脂环烃结构、命名、
P94习题
4
4
第五章(二)
第六章芳烃(5)
性质、构象
芳烃的结构、命名、苯的性质、
P109习题
杂环化合物的分类、结构、命名、性质(一)
单糖的结构、命名
P405习题
15
4
第十四章碳水化合物(二)
第三单元习题课(2)
单糖的性质
二糖、多糖的结构及性质
P429、P449习题
16
4
复习
实验安排:(3~10周)
序号
周
学时
实验项目
1
三
4
有机化合物沸点、熔点测定
2
四
4
乙酸正丁酯合成
3
五
6
从槐花米中提取芦丁
4
醇的结构、命名、性质
酚的结构、命名、性质
P244、P269习题
9
4
第九章醇酚醚(二)
第十章醛、酮(4)
酚的性质
醚的结构、命名、性质
醛、酮的结构、命名、制法、
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2019.09
授课时间,地点:(1-14周)每周四[3,4节]10:00-11:40,综508;
任课教师:唐昊
周次
日期
课堂讲授
阅读内容
作业
习题课
考试
(测验)
备注
1
2019.09.12
绪论第1章热化学与能源
1.1热化学
1.1.1几个基本概念.
1.1.2热效应及其测量
教材
第1章
2
2019.09.19
7.3.3高分子的一些物理性能
教材
第7章
12
2019.12.05
7.4高分子的改性和加工7.4.1高分子的改性
7.4.2高分子的加工7.5高分子的应用7.5.1塑料7.5.2橡胶7.5.3纤维7.5.4感光高分子材料7.5.5复合材料7.6未来的材料及材料的分子设计7.6.1未来的材料7.6.2材料的分子设计
8.3糖类8.3.1单糖8.3.2单糖的聚合物(低聚糖和多糖)
教材
第8章
P320复习思考题:1,5,13
习题:2(1)(3),5,6(1)(3)(5)(6),7.
14
2019.12.02
第9章分析化学基础(主要教材中无此章节,采用自编PPT材料)
自编材料
第9章
期末考试
考试周:时间另行通知
教学14周,授课14周完成;
1.2反应热与焓
1.2.1热力学第一定律
1.2.2反应热与焓
1.2.3反应的标准摩尔焓变
教材
第1章
作业:P29-4,6. P30-11,12.
P31-17.
讨论题P28-16.
3
2019.09.26
第2章化学反应的基本原理与大气污染控制2.1化学反应的方向和吉布斯函数2.1.1熵和吉布斯函数
2.1.2反应自发性的判断2.2化学反应的限度和化学平衡2.2.1反应限度和平衡常数
第2章
P75 6,8,12 P76 15,18 P77 22
6
2019.10.17
第3章水溶液化学3.1溶液的通性
3.1.1非电介质稀溶液的通性3.1.2电解质溶液的通性3.2酸碱解离平衡3.2.1酸碱的概念
3.2.2酸和碱的解离平衡3.2.3缓冲溶液和pH控制
教材
第3章
7
2019.10.24
3.3难溶电解质的多相离子平衡3.3.1多相离子平衡和溶度积3.3.2溶度积规则及其应用
教材
第5章
P156-9, 13, 14
P157-15, 23,24
期中考试
时间另行通知
11
2019.11.28
第7章高分子化合物7.1高分子化合物概述
7.1.1高分子化合物的定义7.1.2高分子的一般结构特点7.1.3高分子的分类7.1.4高分子的命名7.2高分子的合成7.2.1高分子聚合反应的分类7.2.2几种重要的聚合反应7.2.3可控聚合反应7.3高分子的结构和性能7.3.1高分子的结构7.3.2高分子的分子热运动与玻璃化转变
第4章电化学与金属腐蚀4.1原电池
4.1.1原电池的化学反应4.1.2原电池的热力学
教材
第3章
P117-9,10,12
P118-19,21,22
8
2019.11.07
4.2电极电势4.2.1标准电极电势
4.2.2电极电势的能斯特方程4.3电动势与电极电势在化学上的应用4.3.1氧化剂和还原剂相对强弱的比较4.3.2反应方向的判断4.3.3反应进行程度的衡量
授课14次,每次90分钟(连续);
实验(项目)2次;测验(考查)1次。
教材
第7章
作业P293:1(1,3, 5,6,8),2(1,3,4,6, 7),3(5),4(2,3),5(3,6),8,9(2),11(2)讨论P292:4,6,9,11,14
13
2019.12.12
第8章生物大分子基础
8.1氨基酸多肽和蛋白质8.1.1氨基酸8.1.2多肽8.1.3蛋白质
8.2核苷酸、DNA、RNA和基因工程8.2.1核苷酸8.2.2核酸8.2.3基因和基因工程
2.2.2化学平衡的有关计算
教材
第2章
4
2019.10.03
国庆假期
5
2019.10.10
2.2.3化学平衡的移动及温度对平衡常数的影响
2.3化学反应速率2.3.1化学反应速率和速率方程2.3.2温度对反应速率的影响(自学)2.3.3反应的活化能和催化剂(自学)2.3.4链反应和光化反应(自学)
教材
教材
第4章
P156-9, 13, 14
P157-15, 23,24
9
2019.11.14
第5章物质结构基础5.1原子结构的近代概念5.1.1波函数5.1.2电子云5.2多电子原子的电子分布方式和周期系5.2.1多电子原子轨道的能级5.2.2核外电子分布原理和核外电子分布方式
教材
第5章
复习思考题P205-2,4,1Fra bibliotek;P206-14习题P206-2;P207-3
10
2019.11.21
5.2.3原子的结构与性质的周期性规律5.2.4电子跃迁(自学)5.3化学键和分子间相互作用力
5.3.1化学键5.3.2分子的极性和分子的空间构型(部分自学)5.3.3分子间相互作用力5.3.4超分子化学(自学)
5.4晶体结构5.4.1晶体的基本类型
