高中化学有机合成及推断
高中化学讲义《有机物的合成与推断(一)》
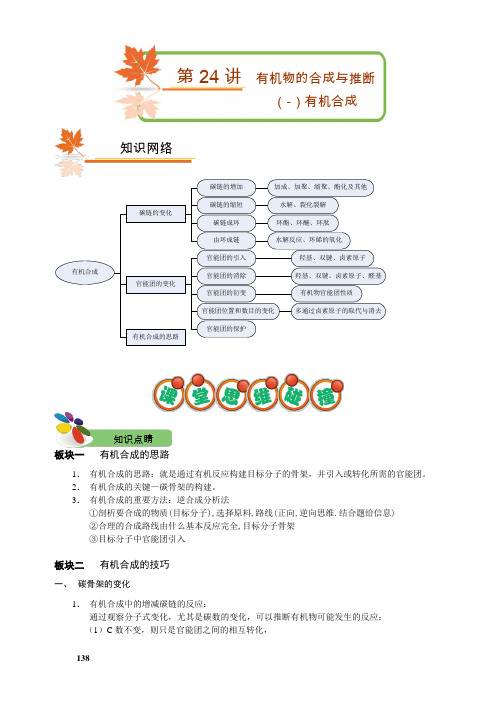
138有机合成碳链的变化官能团的变化有机合成的思路碳链的增加碳链的缩短碳链成环由环成链加成、加聚、缩聚、酯化及其他水解、裂化裂解环酯、环醚、环肽水解反应、环烯的氧化官能团的引入官能团的消除官能团位置和数目的变化官能团的保护官能团的衍变羟基、双键、卤素原子羟基、双键、卤素原子、醛基有机物官能团性质多通过卤素原子的取代与消去板块一 有机合成的思路1. 有机合成的思路:就是通过有机反应构建目标分子的骨架,并引入或转化所需的官能团。
2. 有机合成的关键—碳骨架的构建。
3. 有机合成的重要方法:逆合成分析法①剖析要合成的物质(目标分子),选择原料,路线(正向,逆向思维.结合题给信息) ②合理的合成路线由什么基本反应完全,目标分子骨架 ③目标分子中官能团引入板块二 有机合成的技巧一、 碳骨架的变化1. 有机合成中的增减碳链的反应:通过观察分子式变化,尤其是碳数的变化,可以推断有机物可能发生的反应: (1)C 数不变,则只是官能团之间的相互转化, 知识点睛 知识网络第24讲有机物的合成与推断(-)有机合成如:CH2=CH2→CH3CH2OH →CH3CHO→CH3COOH(2)增长碳链的反应:①酯化反应②加聚反应③缩聚反应(3)减短碳链的反应:①水解反应:酯的水解,糖类、蛋白质的水解;②裂化和裂解反应;2.链状变环状:不饱和有机物之间的加成,同一分子中或不同分子中两个官能团互相反应结合成环状结构。
有机合成中的成环反应:3.环状变链状:酯及多肽的水解、环烯的氧化等。
二、官能团的变化1.官能团的引入:在有机化学中,卤代烃可谓烃及烃的衍生物的桥梁,只要能得到卤代烃,就可能得到诸如含有羟基、醛基、羧基、酯基等官能团的物质。
此外,由于卤代烃可以和醇类相互转化,因此在有机合成中,如果能引入羟基,也和引入卤原子的效果一样,其他有机物都可以信手拈来。
同时引入羟基和引入双键往往是改变碳原子骨架的捷径,因此官能团的引入着重总结羟基、卤原子、双键的引入。
高一化学有机合成与推断试题答案及解析

高一化学有机合成与推断试题答案及解析1.(7分)来自石油的有机化工原料A,其产量已作为衡量一个国家石油化工发展水平的标志,A 可以发生如下转化:已知:E是具有果香味的有机物,其分子式为C4H8O2,F是一种高分子化合物。
(1)A的分子式是,C的名称是。
(2)D分子中的官能团名称是,证明该官能团具有酸性的方法是。
(3)反应③的化学方程式是;反应④的类型是反应。
【答案】(1)C2H4(1分)乙醛(1分)(2)羧基(1分);向D中滴加碳酸氢钠溶液,若有无色无味的气体产生,则证明羧基具有酸性(1分)(3)CH3COOH+C2H5OH CH3COOC2H5+H2O (2分)加聚(1分)【解析】A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平,所以A是H2C=CH2,E是具有果香味的有机物,E是酯,酸和醇反应生成酯,则B和D一种是酸一种是醇,B能被氧化生成C,A反应生成B,碳原子个数不变,所以B是乙醇,D是乙酸,铜作催化剂、加热条件下,乙醇被氧气氧化生成C,所以C是乙醛,A反应生成F,F是一种高聚物,可制成多种包装材料,所以F是聚乙烯,则(1)通过以上分析知,A的分子式为:C2H4,C的名称为乙醛;(2)D分子中的官能团名称是羧基,检验羧基具有酸性的方法是:向D中滴加碳酸氢钠溶液,若有无色无味的气体产生,则证明羧基具有酸性;(3)反应③是酯化反应,方程式为CH3COOH+C2H5OH CH3COOC2H5+H2O。
反应④一定条件下,乙烯发生加聚反应生成聚乙烯,该反应属于加聚反应。
【考点】考查有机物的推断2.一种高分子化合物(VI)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):回答下列问题:(1)化合物III中所含官能团的名称是、。
(2)化合物III生成化合物IV的副产物为。
(提示:原子利用率100%,即原子全部都转化成产物)(3)CH2=CH2与溴水反应方程式:。
有机合成及推断
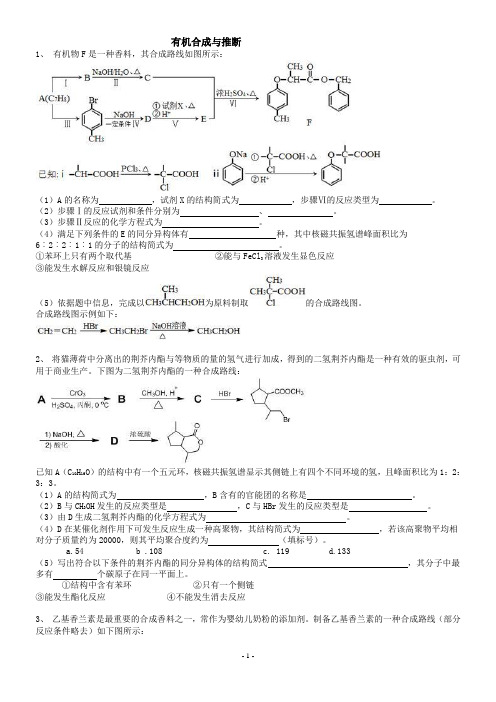
有机合成与推断1、有机物F是一种香料,其合成路线如图所示:(1)A的名称为,试剂X的结构简式为,步骤Ⅵ的反应类型为。
(2)步骤Ⅰ的反应试剂和条件分别为、。
(3)步骤Ⅱ反应的化学方程式为。
(4)满足下列条件的E的同分异构体有种,其中核磁共振氢谱峰面积比为6︰2︰2︰1︰1的分子的结构简式为。
①苯环上只有两个取代基②能与FeCl3溶液发生显色反应③能发生水解反应和银镜反应(5)依据题中信息,完成以为原料制取的合成路线图。
合成路线图示例如下:2、将猫薄荷中分离出的荆芥内酯与等物质的量的氢气进行加成,得到的二氢荆芥内酯是一种有效的驱虫剂,可用于商业生产。
下图为二氢荆芥内酯的一种合成路线:已知A(C10H16O)的结构中有一个五元环,核磁共振氢谱显示其侧链上有四个不同环境的氢,且峰面积比为1:2:3:3。
(1)A的结构简式为,B含有的官能团的名称是。
(2)B与CH3OH发生的反应类型是,C与HBr发生的反应类型是。
(3)由D生成二氢荆芥内酯的化学方程式为。
(4)D在某催化剂作用下可发生反应生成一种高聚物,其结构简式为,若该高聚物平均相对分子质量约为20000,则其平均聚合度约为(填标号)。
a.54 b .108 c. 119 d.133(5)写出符合以下条件的荆芥内酯的同分异构体的结构简式,其分子中最多有个碳原子在同一平面上。
①结构中含有苯环②只有一个侧链③能发生酯化反应④不能发生消去反应3、乙基香兰素是最重要的合成香料之一,常作为婴幼儿奶粉的添加剂。
制备乙基香兰素的一种合成路线(部分反应条件略去)如下图所示:已知:①R—ONa + R’—Br —→R—O—R’+ NaBr②Ⅲ中生成的Cu2O经氧化后可以循环利用(1)A的核磁共振氢谱有3组峰。
A的结构简式为。
(2)Ⅰ中可能生成的一种烃是(填名称);催化剂PEG可看作乙二醇脱水缩聚的产物,PEG的结构简式为。
若PEG的平均相对分子质量为17618,则其平均聚合度约为。
新高考化学有机合成与推断专项训练之知识梳理与训练及答案
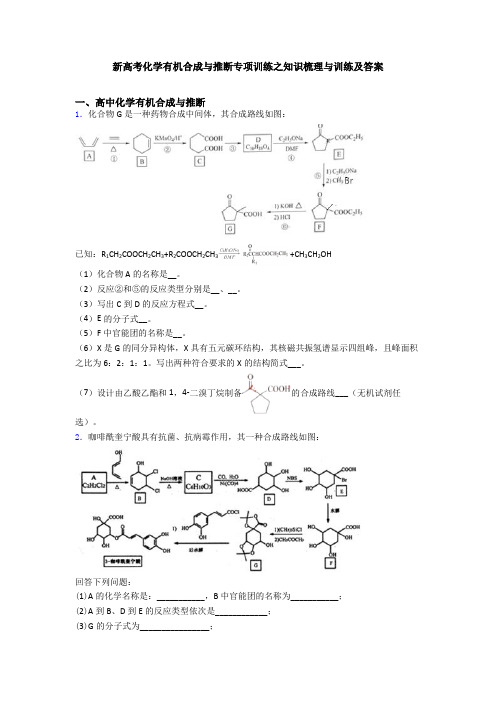
新高考化学有机合成与推断专项训练之知识梳理与训练及答案一、高中化学有机合成与推断1.化合物G是一种药物合成中间体,其合成路线如图:已知:R1CH2COOCH2CH3+R2COOCH2CH3+CH3CH2OH(1)化合物A的名称是__。
(2)反应②和⑤的反应类型分别是__、__。
(3)写出C到D的反应方程式__。
(4)E的分子式__。
(5)F中官能团的名称是__。
(6)X是G的同分异构体,X具有五元碳环结构,其核磁共振氢谱显示四组峰,且峰面积之比为6:2:1:1。
写出两种符合要求的X的结构简式___。
(7)设计由乙酸乙酯和1,4-二溴丁烷制备的合成路线___(无机试剂任选)。
2.咖啡酰奎宁酸具有抗菌、抗病霉作用,其一种合成路线如图:回答下列问题:(1)A的化学名称是:___________,B中官能团的名称为___________;(2)A到B、D到E的反应类型依次是____________;(3)G的分子式为________________;(4)B 生成C 的化学方程式为__________;(5)X 是C 的同分异构体,其能发生银镜反应和水解反应,核磁共振氢谱有2组峰,且峰面积比为9:1,写出符合题意的X 的一种结构简式:____________;(6)设计以1,3-丁二烯和氯乙烯为起始原料制备的合成路线:_________(无机试剂任用)。
3.“达芦那韦”是抗击新型冠状病毒潜在用药,化合物M 是它的合成中间体,其合成路线如下:已知:R 1CHO 22R NH −−−→回答下列问题:(1)有机物A 的名称是______________;反应②反应类型是__________。
(2)物质B 的结构简式是____________;E 的分子式为_____________。
(3)G 中含氧官能团的名称是________;F 中有________个手性碳原子。
(4)请写出反应⑤的化学反应方程式_____________。
高中化学之有机合成与推断(三) ——药物合成

有机合成与推断专题训练(三)——药物合成1、水芹烯是一种具有祛痰、抗菌、杀虫作用的添加剂,由水芹烯合成聚合物H的路线如图所示。
已知:回答下列问题:(1)B的结构简式为_______________,C的化学名称是_________________(2)③的反应试剂和反应条件分别是_____________,该反应的反应类型是____________(3)⑥的化学方程式为_____________,⑥中浓H2SO4的作用是_______________(4)H的分子式为_________________(5)M是G的同分异构体,M能与NaHCO3溶液反应生成CO2,则M可能的结构有___________种(6)乙酸—2—丙酯()是重要的有机化工中间体,写出以2-甲基-2-丁烯()为原料(其他试剂任选)制备乙酸-2-丙酯的路线:____________2、阿司匹林是一种解毒镇痛药。
烃A是一种有机化工原料,下图是以它为初始原料设计合成阿司匹林关系图:已知:①②烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:③(苯胺,易被氧化)请根据本题所给信息与所学知识回答下列问题:(1)C的结构简式为__________________________(2)反应④的反应类型________,在③之前设计②这一步的目的是_____________(3)F中含氧官能团的名称__________________________(4)G(阿司匹林)与足量NaOH溶液反应的化学方程式为_____________________(5)符合下列条件的E的同分异构体有________种,写出核磁共振氢谱中有四组峰,峰面积之比为3:2:2:1的结构简式:________________(只写一种)a.苯环上有两个取代基b.遇氯化铁溶液显紫色c.能发生水解反应(6)利用甲苯为原料,结合以上合成路线和信息合成功能高分子材料(,无机试剂任选)____ 3、伪麻黄碱(D)是新康泰克的成分之一,能够缓解感冒时带来的鼻塞、流鼻涕和打喷嚏等症状,其中一种合成路线如下:回答下列问题:(1)伪麻黄碱(D)的分子式为_________________;B中含有的官能团有_______________________(写名称)(2)写出B→C反应的化学方程式:_____________________C→D的反应类型为________________(3)B的消去反应产物可以用于合成高分子化合物E,请写出E的结构简式:_____________(4)满足下列要求的A的同分异构体有_____种①能发生银镜反应②苯环上的一氯代物有两种结构其中核磁共振氢谱为4组峰,且峰面积之比为6:2:1:1的为______________(写出其中一种结构简式即可) (5)已知:。
高中化学专题14 有机物合成与推断(解析版)

专题14 有机合成与推断1.[化学——选修5:有机化学基础](15分)扎来普隆是一种短期治疗失眠症的药物,其合成路线如下:回答下列问题:(1)A 中的官能团名称是________________。
(2)A B →所需的试剂和条件分别为______________________________。
(3)B C →、E F →的反应类型依次为_______________、_______________。
(4)扎来普隆的分子式为_______________________。
(5)C D →的化学方程式为______________________________________。
(6)属于芳香化合物,且含有硝基,并能发生银镜反应的B 的同分异构体有________种(不考虑立体异构),其中核磁共振氢谱有4组峰的结构简式有________________。
(7)已知:2NH -有碱性且易被氧化。
设计由和乙醇制备的合成路线(无机试剂任选)。
________【答案】(1)羰基(或酮基) (1分) (2)浓HNO 3,浓H 2SO 4/Δ (1分)(3)还原反应(1分) 取代反应(1分) (4)17155C H ON (1分)(5) (2分)(6)17(3分) 、(2分)(7)(3分)【解析】(1)A 的结构简式为,含有的官能团名称是羰基;(2)A 的结构简式为,B 的结构简式为,则A B →发生取代反应,所需的试剂和条件分别为浓3HNO ,浓24H SO /∆;(3)由B 的结构简式为、C 的结构简式为、E 的结构简式为、F 的结构简式为可知,B C →是-NO 2转化为-NH 2,发生了还原反应,而E F →的反应类型为取代反应;(4)扎来普隆的结构简式为,其分子式为17155C H ON ;(5)C 的结构简式为、D 的结构简式为,则C D →发生取代反应的化学方程式为;(6)B 的结构简式为,其属于芳香化合物,且含有硝基,并能发生银镜反应的同分异构体满足:①含有苯环和硝基;②含有-CH 2CHO 或一个甲基和一个-CHO ;若为-NO 2和-CH 2CHO ,则有4种结构,其中有一种为苯环上连接-CH(NO 2)CHO ;若为-NO 2、-CH 3和-CHO ,则有4+4+2=10种,另外还有-CH 2NO 2和-CHO 共有3种,共有4+10+3=17种,其中核磁共振氢谱有4组峰的结构简式有、;(7)因2NH -有碱性且易被氧化,则由和乙醇制备时,应先将-CH 3氧化为-COOH ,再与乙醇发生酯化反应,最后再将-NO 2还原为-NH 2,具体合成路线为。
2022年高考化学高考化学压轴题 有机合成与推断专项训练分类精编及解析

2022年高考化学高考化学压轴题有机合成与推断专项训练分类精编及解析一、高中化学有机合成与推断1.化合物H是一种药物合成中间体,其合成路线如下:(1)A→B的反应的类型是____反应。
(2)化合物H中所含官能团的名称是______。
(3)化合物C的结构简式为____。
B→C反应时会生成一种与C互为同分异构体的副产物,该副产物的结构简式为____。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:____。
①能发生水解反应,所得两种水解产物均含有3种化学环境不同的氢;②分子中含有六元环,能使溴的四氯化碳溶液褪色。
(5)已知:HClCH2ClCH2OH。
写出以环氧乙烷()、、乙醇和乙醇钠为原料制备的合成路线流程图____。
(无机试剂任用,合成路线流程图示例见本题题干)2.科学家研究发现药物肉桂硫胺(M)可能对2019-nCoV有效,是抗击新型冠状病毒潜在用药,以芳香烃A为原料,合成肉桂硫胺路线如图:已知:回答下列问题:(1)A的名称为___。
B→C的试剂和条件为__。
(2)C中含有的官能团名称为__。
(3)有机物D与新制的Cu(OH)2悬浊液加热煮沸产生砖红色沉淀的化学方程式是__。
(4)E反式结构简式为__,F最多有__个原子共平面。
(5)G→H的化学方程式为__,G→H的反应类型为__。
(6)J是E的同分异构体,满足下列条件的J的结构有___种;①J能与溴水发生加成反应②J水解产物遇到FeCl3溶液显紫色其中苯环上有两种化学环境的氢的结构简式为__。
3.某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式是____。
(2)A中的碳原子是否都处于同一平面_____?(填“是”或“不是”)。
(3)在图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
I.C的化学名称是_____;II.反应⑤的化学方程式为_____;III.D2的结构简式是____;④、⑥的反应类型依次是____、_____。
高中化学有机合成与推断

【考点透视】 考点透视】
考点一:烃及烃的衍生物的重要化学性质 烷烃、烯烃、炔烃、苯及其同系 考点一 物、卤代烃、醇、醛、酚、羧酸、酯、糖类、油脂、蛋白质、有机高分子构成高中有机化 学部分,熟悉和掌握重要有机物(如烯烃、卤代烃、醇、醛、酚、羧酸、酯)的化学性质 ,是解决有机问题的基础。复习时可列表对比学习,这里不再赘述。 考点二:重要的反应类型 反应类型是有机化学的重要考查内容,它是描述和书写有机 化学方程式的一般规律,考有机内容必定考反应类型的判断和识别。 1.取代反应---等价替换式 有机分子里某一原子或原子团与另一物质里同价 态的原子或原子团相互交换位置后就生成两种新分子,这种分子结构变化形式可概括为等 价替换式. 2.加成反应—开键加合式 有机分子中含有碳碳双键,碳氧双键(羰基)或碳碳叁键,当打 开其中一个键或两个键后,就可与其他原子或原子团直接加合生成一种新分子,这可概括为 开键加合式 3.消去反应---脱水/卤化氢重键式 有机分子(醇/卤代烃)相邻两碳原子上脱去水/卤代氢 分子后,两个碳原子均有多余价电子而形成新的共价键,可概括为脱水/卤化氢重键式. 4.氧化反应----脱氢重键式/氧原子插入式 醛的氧化是在醛基的C---H键两个原子间插入 O原子;醇分子脱出氢原子和连着羟基的碳原子上的氢原子后,原羟基氧原子和该碳原子有 多余价电子而再形成新共价键,这可概括为脱氢重键式/氧原子插入式. 5.缩聚反应—缩水结链式 许多个相邻小分子通过羧基和氨基,或羧基和羟基,或醛基和酚 中苯环上的氢原子---的相互作用,彼此间脱去水分子后留下的残基顺序连接成长链高分子, 这可称为缩水结链式.
【例题解析】 例题解析】
年全国理综卷 某有机化合物X( 例1[07年全国理综卷Ⅱ] 某有机化合物 (C7H8O)与另一有机化合物 发生反应 年全国理综 )与另一有机化合物Y发生反应 生成化合物Z( 生成化合物 (C11H14O2): X+Y + Z+H2O + (填
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
表述——准确的化学语言
知识精讲
【考点】有机反应常用数据
【知识贮备五】 有机反应中的常用数据信息 n烃 1 烃分子中含有n个H =
n(Cl2) n (当烃与Cl2光照) ★OH~3Br2
C=C ~1H2 C≡C ~2H2
~3H2
n烃
n(Br2)
【知识贮备四】 有机合成常见题眼
1.根据有机物的性质推断官能团
羧基(—COOH) 酚羟基(不产生CO2) 羧基(产生CO2) —CHO,-COOH(中和,无现象)
醛,甲酸及其盐,甲酸酯,葡萄糖
—CHO,-COOH(常温溶解)
C=C,C≡C, 醇羟基、酚羟基、 -CHO、苯同系物(侧首C含H)
C=C、C≡C、-CHO C=C、C≡C、-CHO 苯同系物(侧首C有H) 苯同系物(侧首C有H) 酚(酚羟基) 醇羟基、酚羟基、羧基
苯乙烯 【交流*研讨2】 含有C、H、N三种元素的有机物,C个 数为x,N个数为y,则H原子最多为 2x+2+y
知识贮备(二) 有机物的重要转化关系:
C2H5ONa C2H5—O—C2H5
BrБайду номын сангаас
…
Br
主要代表物之间的转化关系
Br NaOH OH OH O2,Cu,△ O O Ag(NH3)2OH,△ O O CH2 CH2 CH2 CH2 H ,催化剂 HC CH或Cu(OH)2,△ HOC COH 2 Br
光,热,紫外线,超声波 强酸,强碱,重金属盐 某些有机物(醇,醛,酮,酚等)
3.根据有机物的知识网络推断
R-CH2OH→R-CHO→R-COOH (伯醇)
RCOOR'→RCOOH+R'OH
-R'表示脂肪烃基,也可以表示芳香烃基
一卤代烃
NaOH/醇
烯烃
X2
二卤代烃 NaOH/醇 炔烃
NaOH/H2O
知识贮备(一)
有机物通式
烃 CnH2n+2
-2H
含H最大值
烷烃 烯烃 环烷烃 炔烃 二烯烃 苯 苯的同糸物
CnH2n+2
CnH2n
-2H
CnH2n-2
-4H
CnH2n-6
【交流*研讨1】推测C8H8可能结构
(1)不能使溴水或酸性KMnO4溶液褪色:
立方烷
(2) 能使溴水或酸性KMnO4溶液褪色:
《考试说明》解读
●掌握各类有机物官能团的特征反应,根据 物质性质推断分析其结构和类别。 ●关注外界条件对有机反应的影响。 ●掌握重要有机物间的相互转变关系。
推理分析的主要依据(知识储备)
1.各类有机化合物官能团的性质 2.各类烃及其含氧衍生物的分子通式 3.重要的有机反应及类型及反应条件 4.有机物的同分异构现象和同分异构体 5.一些典型有机反应发生时的各种定量 的关系
=
1
n
n=1 n=2
含1个C=C 含2个C=C或1个C≡C
(当烃与Br2/H2O或Br2/CCl4)
知识精讲
【考点】有机反应常用数据
☆有反应常用数据 RCOORˊ~1NaOH RX~1NaOH
“策略” 先水解 后中和
☆ RCOO~2NaOH
☆ X~2NaOH HCHO~4Ag
RCHO~2Ag
RCHO~Cu2O↓
酯、二糖、肽及蛋白质水解
烃基或苯环侧链上的烃基取代 苯环上的取代
醇的催化氧化成醛或酮 加成(碳碳双键、叁键、 醛基、羰基、苯环) [ 醛、甲酸类(包括甲酸、甲酸盐、 甲酸酯)、单糖、麦芽糖、其他含 醛基的物质] 羧酸、多元醇(常温) CHO (△ )等]
酚的取代反应 银镜;苯硝化、磺化;酯、糖类水解
★醇羟基、酚羟基、羧基与钠、氢氧化钠、 碳酸钠、碳酸氢钠反应的比较:
★酸性:
-COOH>H2CO3>C6H5OH>HCO3->ROH
2.特征反应条件
①羧酸②酚③卤代烃的水解 ④酯的水解⑤肽及蛋白质 卤代烃消去
醇消去(170℃)、醇成醚(170℃),硝化(50— 60 ℃)、磺化、酯化(△),多糖水解
Ni
C H 3C H 2O H
C 2H 5O H + H X C 2 H 5 C l + H 2 O
NaOH 溶液
( 3 ) 酯 水 解 法 : R C O O R ’ + H 2O → R C O O H + R ’ O H ( 4 ) 烯 烃 水 化 法 : C H 2= C H 2+ H O H → C 2H 5O H (5)葡 萄 糖 发 酵 法
酚,羧酸;酯卤代烃(△)
C=C,C≡C,—CHO,酮基,苯环
C=C,C≡C 羧基、酯基、肽键
醇或卤代烃(β有H)
酯,卤代烃,二多糖,酰胺键
知识存盘
【考点】化学性质与官能团
酯、糖类、酰胺的水解等 醇消去,成醚,酯化,硝化等 醇催化氧化(α有H) A
氧化
B
氧化
C
C=C,C≡C
多羟基 A:-CH2OH或乙烯 淀粉 蛋白质
醇RCH2OH
加氢还原
去氢氧化
醛RCHO
加氧氧化
RCOOH
醇(RCH(OH)R’)
加氢还原 去氢氧化 酮(R
O C
R’ )
羧酸 + 醇
稀H2SO4 浓H2SO4
酯 + H2O
NaOH
羧酸盐 + 醇
4.根据新信息、新情景推断 阅读和理解——信息的内容
信息与问题间的关系
分析—— 挖掘信息中的隐含条件
处理信息要充分、细微
CH2=CH2
H2 O 催化剂 浓H2SO4 170℃ O2,Cu,△
CH3CH2Br
NaOH
CH3CH2OH
H2,催化剂
CH3CHO
Ag(NH3)2OH,△
或Cu(OH)2,△
CH3COOH
稀H2SO4, △
浓H2SO4, △
CH3COOC2H5
【知识贮备三】示例:引入羟基的五种方法
( 1 ) 醛 还 原 法 : C H 3C H O + H 2 (2)卤 代 烃 水 解 法 :
HCHO~ 2Cu2O↓
知识精讲
【考点】有机反应常用数据
☆有机反应常用数据 2-OH~1H2 -COOH~1NaOH OH~1NaOH OH~1Na2CO3 -COOH~1/2Na2CO3
-COOH~1NaHCO3
【考点】有机推断*化学式
【知识贮备六】 常见有机化合物的通式
1、常见有机化合物的通式:(重视常见) ① CnH2n(n≥3),单烯烃与环烷烃 ② CnH2n-2(n≥3),单炔烃、二烯烃、环单烯烃 ③ CnH2n-6(n≥6),苯及其同系物与多烯 ④ CnH2n+2O(n≥2),饱和一元醇和醚 ⑤ CnH2nO(n≥3),饱和一元醛、酮和烯醇 ⑥ CnH2nO2(n≥2),饱和一元羧酸、酯、羟基醛 ⑦ CnH2n-6O(n>6),一元酚、芳香醇、芳香醚 ⑧ CnH2n+1NO2,氨基酸和一硝基化合物 ⑨ C6H12O6,葡萄糖和果糖, ⑩C12H22O11,蔗糖和麦芽糖 2、重视化学式的缺H数:猜测可能官能团(还需验证)
