影响酶活力的因素的曲线分析
例析酶曲线图的变化

例析酶曲线图的变化作者:吴浩来源:《理科考试研究·高中》2013年第04期影响酶活性的因素很多,如温度、pH.影响酶促反应的因素除影响酶活性的因素外,还涉及酶浓度和底物浓度等。
在研究酶问题时涉及很多类型的曲线,通过改变曲线中某一因素会引起曲线中相关“点”或曲线走势的变化.1.曲线中相关“点”的变化例1下图甲是H2O2酶活性受pH影响的曲线,图乙表示在最适温度下,pH=b时H2O2分解产生的O2量随时间的变化曲线.若该酶促反应过程中改变某一初始条件,以下改变正确的是A.pH=a时,e点下移,d点左移B.pH=c时,e点为0C.温度降低时,e点不移动,d点右移D.H2O2量增加时,e点不移动,d点左移解析O2的最大释放量只与H2O2的量有关,与酶的活性无关,与pH=b时相比,pH=a时酶的活性下降,e点不变,d点右移;H2O2不稳定,在H2O2酶失活时,H2O2仍能分解;温度降低时酶的活性降低,e点不变,但H2O2完全分解所用的时间延长,d点右移;增加H2O2量,e点上移,d点右移.答案:C2.曲线走势的改变例2将新鲜萝卜磨碎、过滤得到提取液.在温度为30℃的条件下,取等量提取液分别加到四个盛有图1pH分别为3、5、7、9的100 mL体积分数为3%的过氧化氢溶液的烧杯中,结果每一个烧杯都产生气体,然后,将加入四个烧杯中提取液的量减半,重复上述实验.在相同时间内,分别测得两次实验中过氧化氢的含量变化并绘制成图1所示曲线,请回答:(1)该实验的目的是.(2)该实验中的自变量是,因变量是.(3)曲线A和B中,过氧化氢含量的最低点位于横坐标同一位置的原因是.(4)曲线A是第次实验的结果,原因最可能是.(5)图2表示萝卜的过氧化氢酶在体外的最适条件下,底物浓度对酶所催化反应的速率的影响.请在图上画出:①如果在A点时,将温度提高5℃时的曲线变化;②如果在B点时,向反应混合物中加入少量同种酶的曲线变化;③如果在C点时加入大量pH为1.8的HCl的曲线变化.解析要确定实验的目的,可围绕自变量和因变量进行分析.本实验中因变量是过氧化氢含量的多少,自变量包括4个烧杯中不同的pH和加入4个烧杯中的提取液的量的多少,据此可以确定实验的目的是探究过氧化氢在不同pH条件及不同量的提取液条件下分解图2图3的快慢或探究等量的提取液在不同pH条件下对过氧化氢分解的影响及同种不同量提取液在相同pH条件下对过氧化氢分解的影响.曲线A和B中过氧化氢含量的最低点对应的pH为最适pH,过氧化氢分解的速度最快,这说明同一种酶在相同条件下的最适pH相同.曲线A与B对照,说明在相同条件下过氧化氢分解的速度较慢,应该是酶的数量的影响,因此,曲线A的实验结果由第二次实验得出.由于图2曲线本身是在最适条件下形成的,如果在A点升高温度,则酶活性会减弱,反应速率会处于较低水平;如果在B点,往反应混合物中加入少量同种酶,反应速率会进一步升高;如果在C点加入大量pH为1.8的HCl,则酶可能变性失活,反应速率会迅速下降,直至反应停止.答案:(1)探究过氧化氢在不同pH条件及不同量的提取液条件下分解的快慢(或探究等量的提取液在不同pH条件下对过氧化氢分解的影响及同种不同量提取液在相同pH条件下对过氧化氢分解的影响)(2)pH的大小和提取液的量单位时间产生气泡的多少(或单位时间内过氧化氢的减少量)(3)同一种酶的最适pH不变(4)二A中所含酶的量较少,相同时间分解的过氧化氢量较少(5)见上图:例3动物脑组织中含有丰富的谷氨酸脱羧酶,能专一催化1 mol谷氨酸分解为1 mol氨基丁酸和1 mol CO2.某科研小组从小鼠的脑中得到该酶后,在谷氨酸起始浓度为10mmol/L,最适温度、最适pH值的条件下,对该酶的催化反应过程进行研究,结果见图38-1和图38-2.图38-1产物CO:浓度随时间变化曲线图(注:酶浓度固定)38-2酶催化反应速率随酶浓度变化曲线(注:反应物浓度过量)请根据以上实验结果,回答下列问题:(1)在图38-1画出反应过程中谷氨酸浓度随时间变化的曲线(请用“1”标注).(2)当一开始时,将混合物中谷氨酸脱羧酶的浓度增加50%或降低反应温度10℃,请在图38-1中分别画出理想条件下CO2浓度随时间变化的曲线(请用“2”标注酶浓度增加后的变化曲线,用“3”标注温度降低后的变化曲线),并分别说明原因.(3)重金属离子能与谷氨酸脱羧酶按比例牢固结合,不可解离,迅速使酶失活.在反应物浓度过量的条件下,向反应混合物中加入一定量的重金属离子后,请在图38-2中画出酶催化反应速率随酶浓度变化的曲线(请用“4”标注),并说明其原因.解析本题考查酶的作用以及影响酶活性的因素等相关知识.①根据题干知谷氨酸脱羧酶发生催化作用时,每分解1 mmol谷氨酸会产生1 mmol CO2,即反应过程中谷氨酸的减少量(溶液中谷氨酸剩余量等于谷氨酸起始量减去减少量)与CO2的生成量相等,因此,根据曲线中CO2浓度随时间的变化,可得到严格的谷氨酸浓度随时间变化变化减少的数量曲线.②在一定范围内,增加酶浓度加速化学反应速率,但由于反应物总量不变,因此,最终反应生成物总量不变,增加酶浓度仅是使化学反应提前达到平衡.③当反应处于最适温度下,再降低或升高反应温度时,酶催化的活性将会下降,化学反应速度减慢,使反应达到平衡的时间延长.④重金属离子与酶结合,使酶失活,当加入的金属离子都与酶结合完全后,再加入的酶就呈游离状态,具有催化活性.根据图2中曲线,可知在酶浓度较低时,随着酶浓度的变化,催化反应速率与酶浓度呈正比变化.答案:(1)见曲线1(2)当谷氨酸脱羧酶的浓度增加50%时,见曲线2,其原因:酶量增加50%,酶催化反应速率相应提高,反应完成所需时间减少. 当温度降低10℃时,见曲线3,其原因:温度降低,酶催化反应速率下降,但酶并不失活,反应完成所需时间增加.(3)见曲线4(注:曲线4为一条不经过原点的平行直线,平移距离不限).原因:一定量的重金属离子使一定量的酶失活,当加入的酶量使重金属离子完全与酶结合后,继续加入的酶开始表现酶活力,此时酶的催化反应速率与酶浓度变化的直线关系不变.。
冲刺2020高考生物实验突破专题:影响酶活性的条件(附答案及解析)

影响酶活性的条件1.实验原理(1)探究温度对酶活性的影响 ①反应原理②鉴定原理:温度影响酶的活性,从而影响淀粉的水解,滴加碘液,根据是否出现蓝色及蓝色的深浅来判断酶的活性。
(2)探究pH 对酶活性的影响①反应原理(用反应式表示):2H 2O 2――――→过氧化氢酶2H 2O +O 2。
②鉴定原理:pH 影响酶的活性,从而影响氧气的生成速率,可用带火星的卫生香燃烧的情况来检验O 2的生成速率。
2.实验步骤和结果 (1)探究温度对酶活性的影响(2)探究pH对酶活性的影响考点一:“梯度法”探究酶的最适pH(1)设计思路(2)设计方案例一、为了探究某种淀粉酶的最适温度,某同学进行了如图所示的实验操作。
实验步骤如下:步骤①:取10支试管,分为五组。
每组两支试管中分别加入1 mL某种淀粉酶溶液和2 mL 质量分数为5%的淀粉溶液。
步骤②:将每组淀粉酶溶液和淀粉溶液混合并摇匀。
步骤③:将装有混合溶液的五支试管(编号1、2、3、4、5)分别置于15 ℃、25 ℃、35 ℃、45 ℃、55 ℃水浴中。
反应过程中每隔1分钟从各支试管中取出一滴反应液,滴在比色板上,加1滴碘液显色。
回答下列问题:(1)实验原理:淀粉在淀粉酶的催化作用下分解成还原糖;淀粉酶的活性受温度影响;用碘液可检测淀粉,因为淀粉遇碘液变蓝,根据蓝色深浅来推断淀粉酶的活性。
(2)该实验的设计存在一个明显的错误,即步骤②前应__________________________________________________________________________________________________。
(3)在本实验中,各组溶液的pH要保证______________,该实验能否选用斐林试剂检测实验结果?__________,理由是________________________________________________________________________________________________________________________。
影响酶活力的因素的曲线分析

对于温度和pH的影响,可以采用更精细的温度和pH梯度进行实验, 以获得更准确的酶活力变化曲线。
03
在研究抑制剂和激活剂的影响时,可以尝试更多的抑制剂和激活剂种 类,以更全面地了解它们对酶活力的影响。
04
在实验结束后,应对实验数据进行详细的分析和解释,确保结论的准 确性和可靠性。
对未来研究的展望
不同酶的最适pH值不同,大多 数酶的最适pH值在6.5-8.0之间。
pH对酶活性的影响主要与酶的 解离状态有关。过酸或过碱的环 境会使酶的解离状态发生变化, 从而影响其活性。
抑制剂对酶活力的影响
抑制剂对酶活力的影响也呈曲线变化。抑制剂可以降低酶的活性,且不同抑制剂对酶活性的影响程度 不同。
抑制剂可以分为不可逆抑制剂和可逆抑制剂两类。不可逆抑制剂与酶结合后,会导致酶永久失活;可逆 抑制剂与酶结合后,可以通过其他物质的作用使酶恢复活性。
温度对酶活性的影响主要与酶的稳定 性有关。高温会使酶的结构变得不稳 定,导致酶失活。
不同酶的最适温度不同,有些酶的最 适温度在30-40℃,而有些酶的最适 温度可能高达70-80℃。
pH对酶活力的影响
01
02
03
pH对酶活力的影响也呈曲线变化。 在一定pH范围内,酶的活性随着 pH的升高而增强,但超过一定范 围后,酶的活性会迅速降低。
pH对酶活力的曲线分析
总结词
pH对酶活力具有显著影响,随着pH的改变,酶活力呈现先升高后降低的趋势。
详细描述
酶的活性受溶液的酸碱度影响。在一定的pH范围内,酶的活性随着pH的升高而增强。这是因为合适的pH能够维 持酶的活性中心结构和功能,使酶与底物更好地结合。但当pH过高或过低时,酶的结构可能发生变化,导致酶 失活。
影响酶活性的因素实验设计解析

酶具高度的特异性。所谓特异性是指一种 酶能对一种化合物或一类化合物起催化作 用,而不能对别的物质发生催化反应。
本实验以唾液淀粉酶为例,此酶只能催化 淀粉的水解,最终产物为麦芽糖和少量的 葡萄糖 。
淀粉水解程度不同,遇碘呈色反应不同。因 此,可以通过呈色反应,了解淀粉水解的程 度,从而间接判断唾液淀粉酶活力的大小。 淀粉水解如下:
影响酶活性的因素
生化实验第五组 组员:林诗雯、伍晨楠、 段宇鑫、王雪翎、张艺
一、目的
1、了解pH对酶活性的影响。 2、了解淀粉的水解过程,与各个过程遇碘
的呈色现象。
二、原理
酶的活性受环境pH的影响极为显著。通常, 各种酶只有在一定的pH范围内才表现它的 活性。一种酶表现其活性最高时的pH值, 称为该酶的最适pH。低于或高于最适pH 时,酶的活性逐渐降低。
五、观察并记录实验现象
实验现象
解释结果
淀粉水解:淀粉 紫色糊精 红色糊精 麦芽糖及 少量葡萄糖
遇碘呈色: 蓝色 紫色 红色 无色
三、试剂与仪器
(一)试剂
蒸馏水 0.2%淀粉液 0.1mol/L柠檬酸 0.2mol/LNa2HPO4 pH8.0缓冲液 pH6.8缓冲液 pH5.0缓冲液 碘液
(二)仪器
控温水浴锅 白瓷板 试管、滴管、移液管(1-2ml)、锥形瓶
0.1mol/L柠檬酸 (mL) 9.70
4.55
0.55
取试管3支,编号,按下表进行操作
项目
试管编号
1
2
3
pH5.0的缓冲溶液(mL)
2
—
—
pH6.8的缓冲溶液(mL)
—
2
—
pH8.0的缓冲溶液(mL)
2020届高考生物实验突破 专题06 影响酶活性的条件(解析版)
2020届高考生物实验突破 专题06 影响酶活性的条件1.实验原理(1)探究温度对酶活性的影响 ①反应原理②鉴定原理:温度影响酶的活性,从而影响淀粉的水解,滴加碘液,根据是否出现蓝色及蓝色的深浅来判断酶的活性。
(2)探究pH 对酶活性的影响①反应原理(用反应式表示):2H 2O 2――――→过氧化氢酶2H 2O +O 2。
②鉴定原理:pH 影响酶的活性,从而影响氧气的生成速率,可用带火星的卫生香燃烧的情况来检验O 2的生成速率。
2.实验步骤和结果 (1)探究温度对酶活性的影响(2)探究pH对酶活性的影响考点一:“梯度法”探究酶的最适pH(1)设计思路(2)设计方案例一、为了探究某种淀粉酶的最适温度,某同学进行了如图所示的实验操作。
实验步骤如下:步骤①:取10支试管,分为五组。
每组两支试管中分别加入1 mL某种淀粉酶溶液和2 mL 质量分数为5%的淀粉溶液。
步骤②:将每组淀粉酶溶液和淀粉溶液混合并摇匀。
步骤③:将装有混合溶液的五支试管(编号1、2、3、4、5)分别置于15 ℃、25 ℃、35 ℃、45 ℃、55 ℃水浴中。
反应过程中每隔1分钟从各支试管中取出一滴反应液,滴在比色板上,加1滴碘液显色。
回答下列问题:(1)实验原理:淀粉在淀粉酶的催化作用下分解成还原糖;淀粉酶的活性受温度影响;用碘液可检测淀粉,因为淀粉遇碘液变蓝,根据蓝色深浅来推断淀粉酶的活性。
(2)该实验的设计存在一个明显的错误,即步骤②前应__________________________________________________________________________________________________。
(3)在本实验中,各组溶液的pH要保证______________,该实验能否选用斐林试剂检测实验结果?__________,理由是________________________________________________________________________________________________________________________。
探究影响酶活性的因素

2.实验步骤和结果 (1)探究温度对酶活性的影响
序号
实验操作内容
试管1
试管2
试管3
1 加入等量的可溶性淀粉溶液
2 mL
2 mL
2 mL
60 ℃热水(5分钟
2
控制不同的温度条件
沸水(5分钟) 冰块(5分钟)
)
1 mL(5分钟 3 加入等量的新鲜淀粉酶溶液 1 mL(5分钟) 1 mL(5分钟)
)
4
产物总量也不会1 2增3加4 5
解析
答案
(4)生物体内酶的化学本质是__蛋__白__质__或__R__N_A, 其特性有__高__效__性__、__专__一__性_(答出两点即可)。
12345
解析
答案
(排除温度干扰),且将酶溶液的pH调至 预设 pH后再 滴入,
不宜在未达到预设pH前,让反应物与酶接触。
过氧 化氢
过
过酶
氧
氧
化
化
氢
氢
酶
酶
关键点拨
1.实验材料选择时的注意事项 (1)在探究温度对酶活性的影响的实验中,不宜选择过氧化氢 (H2O2)和过氧化氢酶作为实验材料,因为过氧化氢(H2O2)在常 温常压时就能分解,加热的条件下分解会加快,从而影响实 验结果。 (2)在探究pH对酶活性的影响实验中,不宜选用淀粉和淀粉酶 作为实验材料,因为在酸性条件下淀粉本身分解也会加快, 从而影响实验结果。
长句应命题探究 答突破简答 题
如图为不同条件下,某酶促反应生成物的浓度随时间的变化曲线,请分析:
1.若表示的是不同催化剂条件下的反应,③是不加催化剂, ②是加无机催化剂,①是加酶,这体现了酶的高效性, 酶具有该特性的原理是同无机催化剂相比,酶能显著降低化 学反应的活化能。
影响酶活力的因素的曲线

3.底物浓度——反应速度
反 应 速 率
B · · A
· C
底物浓度 描述曲线特征: (当酶浓度、温度和pH恒定时)在底物浓度很低的范围 内,反应速度与底物浓度成正比;继续增加底物浓度, 反应速度增加转慢;达到最大后保持不变。
O
解释:酶数量一定时,底物浓度越大,形成的酶—底物 复合物越多;达到一定程度后,有限的酶全部与底物 结合而达到饱和。 BC段有限的不影响酶的活性。 8
比较:酶与无机催化剂
2
影响酶促反应速度的主要因素
反应速率: 单位时间内生成物的增加量,或底物的消耗量 = 酶活力 = 酶的催化效率
底物浓度 酶浓度 酶 酶活性
温度
pH 抑制剂或激活剂等 竞争性抑制
可逆 (降低酶活性,但不使酶变性) 抑制剂作用机制 (形成氢键) 非竞争性抑制 不可逆 使酶永久性失活 (抑制剂与酶共价连接)
1.催化剂加快反应速度的本质原因:降低反应活化能
[活化分子] 过渡态(活化态)
催化后活化能的减少值 非催化过程的活化能
自由能
无机催化剂
酶催化过程的活化能
(酶使活化能更低)
初态 反应物S 平均能量水平较低 终态 产物P 反应过程
反应前后自由能之差
★反应活化能:反应物进入活化状态所需的能量。 (类似于跨栏时栏的高度)(只调节能够反应的反应速度) 催化剂能降低反应活化能,提高活化分子百分数,因此加快了反应速度。 即:在催化反应中,只需较少的能量就可使反应物进入活化态。 ★某反应在不同情况下的反应速度不同,本质原因是反应活化能的不同。 ★酶与无机催化剂相比,活化能水平被降得更低,显示出高效性。 1
思考:
①限制OA段的因素 是底物浓度; 限制BC段的因素是 酶浓度。
影响酶活力的因素
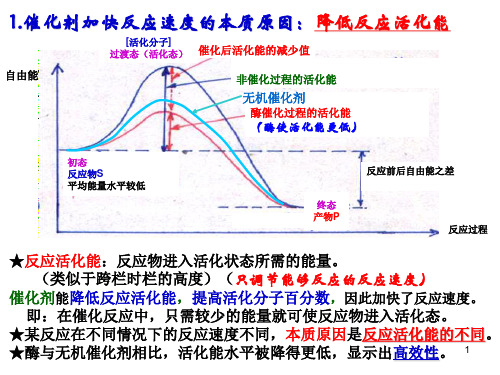
抑制剂——能与酶结合并降低酶活性的分子
▲某些抑制剂能可逆地与酶 结合 和分离。可逆抑制剂可分为 竞争性抑制剂 竞争性抑制剂 和 非竞争性抑制剂。
①竞争性抑制剂与底物结构相似,都结合在
酶活性部位上,从而阻止酶与底物的结合。
★可通过增加底物浓度而解除抑制。
V
无抑制剂
●使v下降的原因: Vmax 酶(E)与抑制剂(I)结合,使部分酶 被抑制剂占据而不能再同时与底物结合, 加竞争性抑制剂 但EI不能生成产物。 ●增加底物浓度,使反应液中的底物分 子%增大,进而使v接近vmax。 底物浓度 竞争性抑制剂的效应取决于 【E总】=【E游离】+【ES】+【EI】 抑制剂与底物的相对浓度。 ●例如:喝酒能治疗甲醇中毒。因为 12 甲醇与乙醇竞争性结合酶的活性部位。 改变S/I的比值可证明之。
曲线在最适温度两侧不对称,因为酶对高温很敏感。21
酶活性
●
嗜冷微生物, 如加酶洗衣粉 中的酶
嗜热微生物如: TaqDNA聚合 酶
酶活性
●
●
温度 温度
耗氧量/ 产热量/ 代谢强度
人离体细胞的呼吸作用酶活 性与环境温度的关系 人体内细胞的呼吸作用酶 活性与环境温度的关系
20 30
40 温度(℃) 22
④温度降低10℃,分子运动速度减慢,与酶结合的底 20 物减少,v减慢。
5.温度——酶活性
温度影响分子运动。温度高,则反应物自由能提高,与酶的接触 机会多。但温度过高,酶变性失活。(超过60℃,大多数失活)
思考:酶的最适温度是个体生长的最适温度吗? 不一定。不同的酶对生长所起的作用可能不同,有的甚至起抑制 或破坏作用。 人体温的相对恒定有何意义? 体温的相对恒定对于维持内环境稳定,保证新陈代谢等生命活动 正常进行的必要条件。 解释①:较低温度范围内,温度 越高,分子运动速度越快,与酶 酶活性 结合的底物越多,v越大。温度 过高,酶逐渐失活。 曲线终点则为0,因为高温使酶变 温度 性失活;但曲线起点不为0,因为 低温下酶活性弱但不变性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
★某反应在不同情况下的反应速度不同,本质原因是反应活化能的不同。 ★酶与无机催化剂相比,活化能水平. 被降得更低,显示出高效性。 1
比较:酶与无机催化剂
相同点: ①改变反应速度,但本身的质、量不变;
在解读坐标图题型时,要注意以下要点: ●看坐标轴含义——了解两个变量的关系 ●看曲线走势——掌握变量的增减快慢特征与
意义 ●看特殊点——理解特殊点的意义
(起止点、拐点、交叉点) ●看不同曲线的异同——理解曲线之间的内在
联系与区别
.
4
反应速度的测定:
▲测定反应速度时,可以测定 产物增加量 或 底物减少量。 ▲如果底物过量,则测定底物减少量不容易精确,
4.酶浓度——反应速度。
再增加:①底物浓度增加一倍;
②温度降低10℃;
③反应开始时加入一定量的不可逆抑制剂。
5.温度——酶活性。
再增加:①嗜冷微生物、嗜热微生物的酶
【加酶洗境温度;
6.pH——唾液淀粉酶活性。
再增加:①胃蛋白酶; ②肠肽酶. 。
6
2.开始时的反应物浓度、酶浓度均不变。 时间——产物浓度;时间——反应物浓度。
●在①的基础上,反应物浓度增加一倍的曲线【 ③】
☆4条竖线提示:斜率、拐点的变. 化。
7
3.底物浓度——反应速度
反
应 速
·B
率 ·A
· C
描述曲线特征: O
底物浓度
(当酶浓度、温度和pH恒定时)在底物浓度很低的范围 内,反应速度与底物浓度成正比;继续增加底物浓度, 反应速度增加转慢;达到最大后保持不变。
.
11
抑制剂——能与酶结合并降低酶活性的分子
▲某些抑制剂能可逆地与酶 结合 和分离。可逆抑制剂可分为
竞争性抑制剂 和 非竞争性抑制剂。
竞争性抑制剂
①竞争性抑制剂与底物结构相似,都结合在
酶活性部位上,从而阻止酶与底物的结合。
★可通过增加底物浓度而解除抑制。
V 无抑制剂
●使v下降的原因:
Vmax
酶(E)与抑制剂(I)结合,使部分酶
.
5
时间
关于酶的常见曲线图【关注坐标轴的含义】
1.催化剂加快反应速度的本质原因:降低反应活化能。
2.开始时的反应物总量、酶浓度均不变。
时间——产物浓度;时间——反应物浓度。
每图再增加:①酶浓度增加一倍;②反应物浓度增加一倍。
3.底物浓度——反应速度。
再增加:①酶浓度增加一倍;
②加入竞争性抑制剂;
③非竞争性抑制剂
被抑制剂占据而不能再同时与底物结合,
反应 速度
酶浓度增加一倍;【红线, 注意斜率和拐点变化】
底物浓度
.
底物浓度
10
3.底物浓度——反应速度(酶浓度不变) 再增加:加入竞争性 / 非竞争性抑制剂
反应速率
①
②
③
O
底物浓度
曲线③属于非竞争性抑 制剂作用情形,类似于 不可逆抑制剂霸占酶。 因此,存在非竞争性抑 制剂相当于降低了酶的 浓度,曲线斜率变小, 很快达到最大。
●竞争性抑制剂与底物竞争性地与 酶的活性部位结合。它既与酶结合, 又与酶分离,即酶与竞争性抑制剂 的结合是可逆的。竞争性抑制剂的 效应取决于抑制剂与底物的相对浓 度。增加底物浓度,使反应液中的 底物分子%增大,进而使v不断接近 vmax,即竞争性抑制剂可以通过增加 底物浓度来降低抑制剂与酶结合的 概率,以缓解抑制。因此②表示竞 争性抑制剂加入后的情形,随底物 浓度的增加抑制作用逐渐减弱并接 近正常的最大反应速度。
每图再增加:①酶浓度增加一倍;②反应物浓度增加一倍。
产物 浓度
②①
③ 改变纵坐标含义 反应物 浓度
●比较 ①与 ② ●比较 ①与 ③
③ ①
②
时间
时间
●描述曲线 ①的特征(分段、准确);
解释曲线变化的原因(底物浓度降低,产物浓度增加,可能pH
或温度发生变化等)
●在①的基础上,酶浓度增加一倍的曲线【 ② 】
解释:酶数量一定时,底物浓度越大,形成的酶—底物 复合物越多;达到一定程度后,有限的酶全部与底物 结合而达到饱和。
BC段有限的酶被饱和,反应速度达到最大,再增加
底物浓度,底物浓度并不.影响酶的活性。
8
思考:
①限制OA段的因素 是底物浓度; 限制BC段的因素是 酶浓度。
反
应 速
· B
率
·A
O
· C
底物浓度
②酶浓度增加1倍,曲线发生怎样的变化?
如图的红色曲线。
【理解走势、斜率、拐点等特征性变化】
相同底物浓度下,酶浓度越高,形成的酶—底物复 合物越多,v越大;酶浓度越高,使酶饱和需要的底 物浓度越大。说出曲线几段的限制因素。
③请举出两种能够影响这一曲线形状的因素。
酶浓度、温度和pH等
.
9
反应 速度
温度或PH改变;【红线, 注意斜率和拐点变化】
而产物从无到有,便于测定,只要方法灵敏。
产物
最
浓度
初
阶
段
?
反应 速度
最 初 阶 段
据图分析回答:
▲如何计算反应速度(v)?
△浓度
V=
=斜率
t
▲描述反应速度变化的特征:
时间
v只是在最初一段时间保持恒定,
随着时间延长,v逐渐下降直到0。
▲反应速度下降的原因是什么?
底物浓度的降低,产物浓度的增加,
pH或温度的变化等。
【但是,所有酶都必须参与反应过程!】 ②只能催化热力学允许进行的反应; ③加快v,缩短达到平衡的时间,但不改变平衡点; ④降低活化能,使v加快。
不同点:
①高效性;
②专一性(酶对底物);
③多样性;
④易变性;
⑤反应条件的温和性;
⑥酶活性受到调节、控制;
⑦有些酶的活性需要辅助因子。.
2
影响酶促反应速度的主要因素
反应速率: 单位时间内生成物的增加量,或底物的消耗量 = 酶活力 = 酶的催化效率
底物浓度
酶浓度
酶 酶活性
温度 pH 抑制剂或激活剂等
竞争性抑制
可逆
(降低酶活性,但不使酶变性)
抑制剂作用机制 (形成氢键) 非竞争性抑制
不可逆
使酶永久性失活
(抑制剂与酶共. 价连接)
3
酶作用曲线
酶活性易受多种因素制约,常用坐标图来表示.
1.催化剂加快反应速度的本质原因:降低反应活化能
[活化分子] 过渡态(活化态)
催化后活化能的减少值
自由能
非催化过程的活化能
无机催化剂
酶催化过程的活化能
(酶使活化能更低)
初态 反应物S 平均能量水平较低
反应前后自由能之差
终态 产物P
反应过程
★反应活化能:反应物进入活化状态所需的能量。 (类似于跨栏时栏的高度)(只调节能够反应的反应速度)
