化工原理答案
化工原理答案

蒸馏5、在连续精馏塔中分离由二硫化碳和四氯化碳所组成的混合液。
已知原料液流量为4000kg/h ,组成为0.3(二硫化碳质量分数),要求釜液组成不大于0.05,馏出液回收率为88%。
试求馏出液的流量和组成,分别以摩尔质量和摩尔分数表示。
解:全塔物料衡算(质量分数表示)WD F Wx Dx Fx W D F +=+= 由题意得:F=4000,x F =0.3,x W =0.5,88.0%100=⨯=FD D Fx Dx η代入上式得 故 943.011203.0400088.0/112028804000/288005.03.0400012.0=⨯⨯===-===⨯⨯D Fx x hkg D hkg W WF D D η 下面用摩尔分数表示h kmol x D /36.14760.9741120D 974.0154/057.076/943.076/943.0=⨯==+=18 6 在常压操作的连续精馏塔中分离甲醇0.4与水0.6(均为摩尔分数)溶液,试求以下各种进料状况下的q 值。
(1)进料温度为40℃(2)泡点进料(3)饱和蒸汽进料(1) 查得甲醇汽化潜热1150kJ/kg ,水的汽化热为2300 kJ/kg ,故平均汽化热为:kg /kJ 27.1676186.0324.01823006.0186.0324.03211504.0r =⨯+⨯⨯⨯+⨯+⨯⨯⨯= 由题中数据可得x=0.4时,溶液泡点温度为75.3℃,则平均温度为: 65.572403.75=+=m t ℃ 查平均温度下甲醇比热为65kJ/kg·K溶液平均比热为K kg kJ ∙=⨯+⨯⨯⨯+⨯+⨯⨯⨯=/35.3186.0324.01818.46.0186.0324.03265.24.0cp 最后由热状态参数q 定义得:07.127.167627.1676)403.75(35.3=+-⨯=+∆=r rt c q p(2) 泡点进料q=1(3) 饱和蒸汽进料q=07 对于习题6中的溶液,若原料液流量为100kmol/h ,馏出液组成为0.95,釜液组成为0.04(摩尔分数),回流比为2.5,试求产品流量,精馏段下降液体流量和提馏段上升蒸气流量。
化工原理课后答案

3.在大气压力为的地区,一操作中的吸收塔内表压为130 kPa 。
若在大气压力为75 kPa 的高原地区操作吸收塔,仍使该塔塔顶在相同的绝压下操作,则此时表压的读数应为多少解:KPa.1563753.231KPa 3.2311303.101=-=-==+=+=a a p p p p p p 绝表表绝1-6 为测得某容器内的压力,采用如图所示的U 形压差计,指示液为水银。
已知该液体密度为900kg/m 3,h=,R=。
试计算容器中液面上方的表压。
解:kPaPa gmρgR ρp ghρgh ρp 53529742.70632.600378.081.990045.081.9106.13300==-=⨯⨯-⨯⨯⨯=-==+1-10.硫酸流经由大小管组成的串联管路,其尺寸分别为φ76×4mm 和φ57×。
已知硫酸的密度为1831 kg/m 3,体积流量为9m 3/h,试分别计算硫酸在大管和小管中的(1)质量流量;(2)平均流速;(3)质量流速。
解: (1) 大管: mm 476⨯φ (2) 小管: mm 5.357⨯φ质量流量不变 h kg m s /164792= 或: s m d d u u /27.1)5068(69.0)(222112=== 1-11. 如附图所示,用虹吸管从高位槽向反应器加料,高位槽与反应器均与大气相通,且高位槽中液面恒定。
现要求料液以1m/s 的流速在管内流动,设料液在管内流动时的能量损失为20J/kg (不包括出口),试确定高位槽中的液面应比虹吸管的出口高出的距离。
解: 以高位槽液面为1-1’面,管出口内侧为2-2’面,在1-1’~2-2’间列柏努力方程:简化: g W u H f /)21(22∑+=1-14.附图所示的是丙烯精馏塔的回流系统,丙烯由贮槽回流至塔顶。
丙烯贮槽液面恒定,其液面上方的压力为(表压),精馏塔内操作压力为(表压)。
塔内丙烯管出口处高出贮槽内液面30m ,管内径为140mm ,丙烯密度为600kg/m 3。
化工原理课后习题(参考答案)

解
x
1 / 17 0.0105 1 / 17 100 / 18
p* 798 E= 76 kPa x 0.0105 1 / 17 c 0.584 kmol / m3 (100 1) / 998 .2
0.584 H c / p 0.73kmol /(m3 kPa) 0.798 y * 798 / 100 10 3 7.98 10 3
1 1 m K Y k Y kY
1 m 比较 与 kY kX
(2)
N A KY Y Y *
5-15Байду номын сангаас在一吸收塔中,用清水在总压为0.1MPa、温度20oC条件下吸收混合 气体中的CO2,将其组成从2%降至0.1%(摩尔分数)。20oC时CO2水溶 液的亨利系数为E=144MPa。吸收剂用量为最小用量的1.2倍。试求(1) 液-气比L/G及溶液出口组成X1;(2)总压改为1MPa时的L/G及溶液出口 组成X1 解:(1)
qm qm1 qm 2 20 10 30t / h 30000 kg / h
qv qm / 30000 / 998 .2 30.05m3 / h 流速为 v 1.0m / s
d
4qv 4 30.05 0.103 m 103 mm v 3600 1.0
G(Y1 Y2 ) L( X 1 X 2 )
Y1 Y2 L G min X 1,max X 2
通过
算出最小液气比:(L/G)min
(2)解题过程类似于(1)小题
0.01 1.8 10 4 解 x1 0.01 1 997 / 18
p1 1.662 10 5 1.8 10 4 29.92 kPa
化工原理——带答案

第一章流体力学1.表压与大气压、绝对压的正确关系是(A )。
A.表压=绝对压-大气压B.表压=大气压-绝对压C.表压=绝对压+真空度2.压力表上显示的压力,即为被测流体的(B )。
A.绝对压B.表压C.真空度D.大气压3.压强表上的读数表示被测流体的绝对压强比大气压强高出的数值,称为(B )。
A.真空度B.表压强C.绝对压强D.附加压强4.设备内的真空度愈高,即说明设备内的绝对压强(B )。
A.愈大B.愈小C.愈接近大气压D.无法确定5.一密闭容器内的真空度为80kPa,则表压为(B )kPa。
A. 80B. - 80C. 21.3D.181.36.某设备进、出口测压仪表中的读数分别为p1(表压)=1200mmHg和p2(真空度)=700mmHg,当地大气压为750mmHg,则两处的绝对压强差为(D )mmHg。
A.500B.1250C.1150D.19007.当水面压强为一个工程大气压,水深20m处的绝对压强为(B )。
A. 1个工程大气压B. 2个工程大气压C. 3个工程大气压 D. 4个工程大气压8.某塔高30m,进行水压试验时,离塔底10m高处的压力表的读数为500kpa,(塔外大气压强为100kpa)。
那么塔顶处水的压强(A)。
A. 403 . 8kpaB. 698. 1kpaC. 600kpaD. 100kpa9.在静止的连续的同一液体中,处于同一水平面上各点的压强(A )A.均相等B.不相等C.不一定相等10.液体的液封高度的确定是根据(C ).A.连续性方程B.物料衡算式C.静力学方程D.牛顿黏性定律11.为使U形压差计的灵敏度较高,选择指示液时,应使指示液和被测流体的密度差(P指-P)的值(B )。
A.偏大B.偏小C.越大越好12.稳定流动是指流体在流动系统中,任一截面上流体的流速、压强、密度等与流动有关的物理量(A )。
A.仅随位置变,不随时间变B.仅随时间变,不随位置变C.既不随时间变,也不随位置变D.既随时间变,也随位置变13.流体在稳定连续流动系统中,单位时间通过任一截面的(B )流量都相等。
化工原理习题答案.
第一章 流体流动1.某设备上真空表的读数为 13.3×10 3Pa ,试计算设备内的绝对压强与表压强。
已知该地区大气压强为 98.7×10 4Pa 。
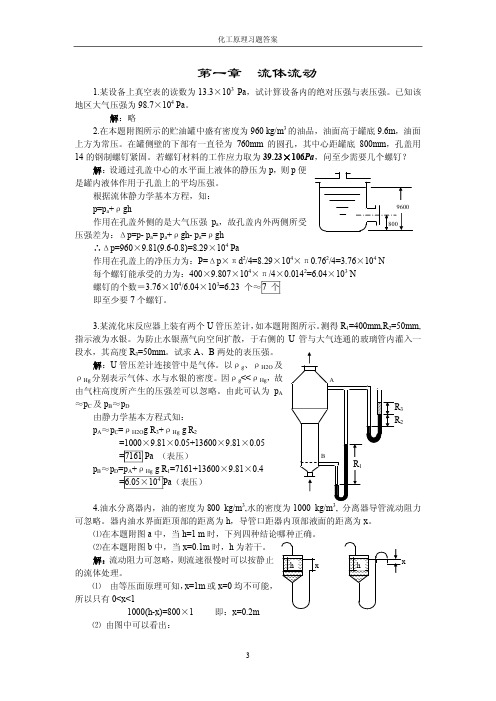
解:略2.在本题附图所示的贮油罐中盛有密度为 960 kg/m 3的油品,油面高于罐底 9.6m ,油面 上方为常压。
在罐侧壁的下部有一直径为 760mm 的圆孔,其中心距罐底 800mm ,孔盖用 14 的钢制螺钉紧固。
若螺钉材料的工作应力取为 39.23×106Pa ,问至少需要几个螺钉?解:设通过孔盖中心的水平面上液体的静压为 p ,则p 便 是罐内液体作用于孔盖上的平均压强。
根据流体静力学基本方程,知:p=p a +ρgh作用在孔盖外侧的是大气压强 p a ,故孔盖内外两侧所受 压强差为:Δp=p p a = p a +ρgh p a =ρgh∴Δp=960×9.81(9.60.8)=8.29×10 4Pa作用在孔盖上的净压力为:P=Δp ×πd 2 /4=8.29×10 4 ×π0.76 2 /4=3.76×10 4N每个螺钉能承受的力为:400×9.807×10 4 ×π/4×0.014 2 =6.04×10 3N螺钉的个数=3.76×10 4 /6.04×10 3=6.23 个≈7 个 即至少要 7个螺钉。
3.某流化床反应器上装有两个 U 管压差计, 如本题附图所示。
测得 R 1=400mm,R 2=50mm, 指示液为水银。
为防止水银蒸气向空间扩散,于右侧的 U 管与大气连通的玻璃管内灌入一 段水,其高度 R 3=50mm 。
试求 A 、B 两处的表压强。
解:U 管压差计连接管中是气体。
以ρg 、ρH2O 及 ρHg 分别表示气体、水与水银的密度。
化工原理课后习题答案

化工原理课后习题答案1. 请计算下列物质的摩尔质量,(1) H2O (2) CO2 (3) NaCl。
(1) H2O的摩尔质量 = 21 + 16 = 18 g/mol。
(2) CO2的摩尔质量 = 12 + 216 = 44 g/mol。
(3) NaCl的摩尔质量 = 23 + 35.5 = 58.5 g/mol。
2. 一种化合物的分子式为C6H12O6,其摩尔质量为180 g/mol,请问这种化合物的分子量是多少?这种化合物的分子量就是其摩尔质量,即180 g/mol。
3. 在一次化学反应中,反应物A和B按化学方程式2A + 3B → C + D 反应,如果A的摩尔质量为20 g/mol,B的摩尔质量为30 g/mol,C的摩尔质量为40 g/mol,D的摩尔质量为50 g/mol。
请问,如果A和B分别以40 g和90 g的质量参与反应,求反应后C和D的质量各是多少?根据化学方程式2A + 3B → C + D,A和B的物质的摩尔比为2:3,因此A和B的摩尔数分别为40 g / 20 g/mol = 2 mol和90 g / 30 g/mol = 3 mol。
根据摩尔数的比例,C和D的摩尔数分别为21 = 2 mol和31 = 3 mol,所以C和D的质量分别为240 g/mol = 80 g和350 g/mol = 150 g。
4. 请问在下列反应中,哪些是氧化还原反应?(1) 2Mg + O2 → 2MgO。
(2) 2Na + Cl2 → 2NaCl。
(3) Zn + 2HCl → ZnCl2 + H2。
(4) Cu + 2AgNO3 → Cu(NO3)2 + 2Ag。
(3) 和(4)是氧化还原反应。
在(3)中,Zn被HCl氧化生成ZnCl2,同时HCl被还原生成H2。
在(4)中,Cu被AgNO3氧化生成Cu(NO3)2,同时AgNO3被还原生成Ag。
5. 请问下列哪些是双原子分子?H2、Cl2、O2、N2、HCl、CO2。
化工原理习题答案

化工原理习题答案问题一:质量守恒及干燥问题问题描述:一种含有30%水分的湿煤经过加热后,其水分含量降低到15%。
问:为了使1000kg湿煤的水分含量降到15%,需要排除多少千克水分?解答:根据质量守恒原则,该问题可以通过计算质量的变化来求解。
设湿煤的初始质量为m1,水分含量为w1,加热后的质量为m2,水分含量为w2。
根据题意可得到以下关系:m1 = m2 + m水分 w1 = (m水分 / m1) × 100% w2 = (m水分 / m2) × 100%根据题意可得到以下关系: w2 = 15% = 0.15 w1 = 30% = 0.30将以上关系代入计算,可得到: 0.15 = (m水分 / m2) × 100% 0.30 = (m水分 / m1) × 100%解得:m水分 = 0.15 × m2 = 0.30 × m1代入具体数值进行计算: m水分 = 0.15 × 1000kg = 150kg因此,需要排除150千克水分。
问题二:能量守恒问题问题描述:一个装有100升水的水箱,水温为20°C。
向该水箱中加热10000千卡的热量,水温升高到40°C。
问:热容量为1千卡/升·°C的水箱的温度升高了多少度?解答:根据能量守恒原理,可以通过计算热量的变化来求解。
热量的变化可表示为:Q = mcΔT其中,Q为热量的变化量,m为物体的质量,c为物体的比热容,ΔT为温度的变化。
根据题意可得到以下关系: Q = 10000千卡 = 10000 × 1000卡 m = 100升 = 100升 × 1千克/升 = 100 × 1千克 c = 1千卡/升·°C 代入公式计算温度的变化ΔT:10000 × 1000 = (100 × 1) × (ΔT) ΔT = (10000 × 1000) / (100 × 1) = 1000000 / 100 = 10000°C 因此,热容量为1千卡/升·°C的水箱的温度升高了10000度。
化工原理课后答案

化工原理课后答案
1. 甲烷的氧化反应方程式为:CH4 + 2O2 → CO2 + 2H2O。
2. 水的沸腾是因为液态水的分子具有一定的热运动能量,在特定的温度和压力下,水中的分子能克服水的表面张力,从而从液相转变为气相。
3. 化学反应速率可以通过测量反应物浓度的变化来确定。
一般情况下,反应速率与反应物浓度之间存在正比关系,即反应速率随着反应物浓度的增加而增加。
4. 标准气体体积的计量单位是摩尔,即每个摩尔的气体占据的体积为标准状况下的体积。
5. 配比是指化学反应中不同反应物之间的摩尔比例关系。
化学方程式中的系数即为反应物的配比关系。
6. 溶液的浓度可以通过溶质的质量或体积与溶液总质量或总体积的比例来计算得到。
常见的浓度单位包括摩尔浓度、质量浓度和体积浓度等。
7. 反应的热力学变化可以通过反应物和产物之间的化学键的形成和断裂来解释。
在化学反应中,反应物中的化学键断裂需要吸收能量,而产物中的化学键形成释放能量。
8. 氧化还原反应是指化学反应中电子的转移。
氧化剂接收电子,被还原;还原剂失去电子,被氧化。
9. 反应热是指在恒定压力下,化学反应发生时放出或吸收的能量。
反应热可通过测量反应物和产物的焓变来确定。
10. 反应平衡是指在特定的温度和压力下,反应物和产物之间的浓度或压力保持不变。
在平衡态下,反应物和产物之间的反应速率相等,且不再出现净反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
6. 在并流换热器中,用水冷却油。
水的进出口温度分别为15℃,40℃,油的进出口温度分别为150℃和100℃。
现生产任务要求油的出口温度降至80℃℃,假设油和水的流量,进出口温度及物性不变,若换热器的管长为1m,试求此换热器的管长增至若干米才能满足要求。
设换热器的热损失可忽略。
解:根据题意列出关系式:热流体(油):T1=150℃→ T2=100℃冷流体(水):t1=15℃→ t2=40℃现在要求:热流体(油):T1=150℃→T2=80℃冷流体(水):t1=15℃→ t2=开始: Q= W h C ph(T1 - T2)=50 W h C ph =W c C pc(t2-t1)=25W c C pc=K0S0ΔtmΔt m=(Δt1-Δt2)/ln(Δt1/Δt2)=(135-60)/ln(135/60)=改变后: Q,=W h C ph(T1 - T2)=700 W h C ph=W c C pc(t2,-t1)=(t2,-15)W c C pc=K0S0,Δtm,∴25/(t2,-15)=50/70 ∴t2,=50℃Δt m, =(Δt1-Δt2,)/ln(Δt1/Δt2,)=∴Q/Q*= K0SΔtm / K0S,Δtm,= LΔtm / L,Δtm,=50/70∴ L,==7.重油和原由在单程套换热器中呈并流流动,粮站油的初温分别为243℃和128℃;终温分别为167℃和157 ℃。
若维持两种油的流量和初温不变,而将两流体改为逆流,试求此时流体的平均温度差及他们的终温。
假设在两种流动情况下,流体的无性和总传热系数均不变,换热器的热损失可以忽略。
解:由题意得:并流时:热流体(重油):T1=243℃→T2=167℃冷流体(原油):t1=128℃→t2=157℃∴ Q =W h C ph(T1 - T2)=76 W h C ph =W c C pc(t2-t1)=29W c C pc=K0S0ΔtmΔt m =(Δt1-Δt2)/ln (Δt1/Δt2)=43改为逆流后:热流体(重油):T1=243℃→ T2,=冷流体(原油):t2,= ←t1=128℃同理:Q ,=W h C ph(T1 - T2,)=(243- T2,)W h C ph=W c C pc(t2,-t1)=(t2,-128)W c C pc=K0S0,Δtm,∴29/(t2,-128)=76/(243- T2,)∴T2,= t2, --------(1)Δtm,=[(243- t2,)-(T2,-128)]/ln[(243- t2,)/(T2,-128)] -------(2)又 Q/Q*= Δtm / Δtm,=29/(t2,-128) ---------(3)由(1)(2)(3)解得 t2,=℃ T2,=℃Δtm,=℃8.在下列各种管式换热器中,某溶液在管内流动并由20℃加热到50℃。
加热介质在壳方流动,其进出口温度分别为100℃和60℃,试求下面各种情况下的平均温度差。
(1)壳方和管方均为单程的换热器。
设两流体为逆流流动。
(2)壳方和管方分别为单程和四程的换热器。
(3)壳方和管方分别为二程和四程的换热器。
解:(1)热流体:T1=243℃→ T2=60℃冷流体:t2=50℃← t1=128℃Δt1=50℃Δt2=40℃∴Δt m=(Δt1-Δt2)/ln(Δt1/Δt2)=℃(2)壳方和管方分别为单程和四程,则需计算平均温度差校正系数ψΔt,由已知条件计算得ψΔt=∴Δtm,=ψΔtΔtm=×=℃(3)查图得,ψΔt=∴Δtm,=ψΔtΔtm=×=℃9.在逆流换热器中,用初温为20℃的水将s的液体(比热容为kg•℃,密度为850kg/m),由80℃冷却到30℃。
换热器的列管直径为ф,水走管方。
水侧和液体侧的对流传热系数分别为 W/(m2•℃)和 W/(m2•℃)。
污垢热阻忽略。
若水的出口温度不能高于50℃,试求换热器的传热面积。
解:热流体:T1=80℃→ T2=30℃冷流体:t2=50℃← t1=20℃Δt1=30℃Δt2=100℃∴Δt m=(Δt1-Δt2)/ln(Δt1/Δt2)=℃Q =W h C ph(T1 - T2)=×10³××50=又Q= K0S0Δtm,其中 1/ K0= d0/αi d i+1/α0 解得K0=×10³m2•℃/W∴×10³× S0=×10³∴S0=³10.在列管式换热器中用冷水冷却油。
水在直径为ф192mm的列管内流动。
已知管内水侧对流传热系数为3490 W/(m2•℃),管外油侧对流传热系数为258 W/(m2•℃)。
换热器用一段时间后,管壁两侧均有污垢形成,水侧污垢热阻为•℃/W,油侧污垢热阻•℃/W。
管壁导热系数λ为45 W/(m•℃),试求:(1)基于管外表面的总传热系数;(2)产生污垢后热阻增加的百分比。
解:(1)1/K0 =d0/αi d i+1/α0+R sid0/d i+R s0+bd0/λd m=19/(3490×15)+×19/15++(×19)/(45×)+1/258∴K0 =208 m2•℃/W(2)产生污垢后增加的总热阻:d0/αi d i+ R s0=19/(3490×15)+=产生污垢前的总热阻:d0/αi d i+1/α0+ bd0/λd m=19/(3490×15)+(×19)/(45×)+1/258 =∴增加的百分比为:=%11.在一传热面积为50m2的单程列管式换热器中,用水冷却某种溶液。
两流体呈逆流流动。
冷水的流量为33000kg/h,温度由20℃升至38℃。
溶液的温度由110℃降至60℃。
若换热器清洗后,在两流体的流量和进出口温度不变的情况下,冷水出口温度增至45℃。
试估算换热器清洗前后传热面两侧的总污垢热阻。
假设(1)两种情况下,流体物性可视为不变,水的比热容可取(kg•℃);(2)可按平壁处理,两种工况下αi和α0分别相同;(3)忽略管壁热阻和热损失。
解:换洗前:热流体:T1=110℃→ T2=60℃冷流体:t2=38℃←t1=20℃Δt1=72℃Δt2=40℃∴Δt m =(Δt1-Δt2)/ln (Δt1/Δt2)=℃Q= W h C ph(T1 - T2)=50W h C ph =W c C pc(t2-t1)=18W c C pc=K0S0Δtm =代入数据计算得K0=254 W/(m2•℃)换洗后::热流体:T1=110℃→T2=60℃冷流体:t2=38℃←t1=20℃Δt1=72℃Δt2=40℃∴Δt m =(Δt1-Δt2)/ln(Δt1/Δt2)=℃Q= W h C ph(T1 - T2)=(100-T2)W h C ph=W c C pc(t2-t1)=25W c C pc=K0,S0Δtm,∴50/(100-T2)=18/25 →T2=℃∴Δt m, =(Δt1,-Δt2,)/ln(Δt1,/Δt2,)=35℃Q= =W c C pc(t2-t1)= K0,S0Δtm,代入数据计算得K0,= W/(m2•℃)∴总污垢热阻为:1/ K0-1/ K0,=1/245-1/=×10-3 m2•℃/W 12.在一单程列管换热器中,用饱和蒸汽加热原料油。
温度为160℃饱和蒸汽在壳程冷凝(排出时为饱和液体),原料油在管程流动,并由20℃加热到106℃,列管换热器尺寸为:列管直径为ф19×2mm,管长为4m ,共25根管子。
若换热器的传热量为125Kw,蒸汽冷凝传热系数为7000 W/(m2•℃),油侧污垢热阻可去为 m2•℃/W,管壁热阻和蒸汽侧垢层热阻可忽略,试求管内油侧对流传热系数。
又若有的流速增加一倍,此时若换热器的总传热系数为原来的倍,试求油的出口温度。
假设油的物性不变。
解:1/K0 =d0/αi d i+1/αi+R si d0/d i,又K0=Q/S0Δtm其中S=25××19×10³×4=Δt m=(Δt1-Δt2)/ln(Δt1/Δt2)=℃∴K0=125×10³/(×)= W/(m2•℃)可以解得αi = W/(m2•℃)改变流速后:K0,= = W/(m2•℃)Q*=2Q(t2,-t1)/(t2-t1)=125×10³(t2,-20)/86又Δt m, =[(T-t1)-(T-t2,)]/ln[(T-t1)/(T-t2,)]=Q,/K0S可以解得 t2,=℃℃的正丁醇在逆流换热器中被冷却到50℃。
换热器的传热面积为6m2,总传热系数为230 W/(m2•℃)。
若正丁醇的流量为1930kg/h,冷却介质为18℃的水。
试求:(1)冷却水的出口温度;(2)冷却水的消耗量,以m³/h表示。
解:由传热方程式Q=K0SΔt m= W h C ph(T1 - T2)查表得70℃的正丁醇的比热为×10³J/(kg•℃)∴Q=1930/3600××10³×(90-50)=×10³J/sΔt m =Q/K0S=×10³/(230×6)=℃Δt m =(Δt1-Δt2)/lnΔt1/Δt2=[(90- t2)-(50-18)]/ln[(90- t2)/(50-18)]试差得t2=℃假定无热阻损失即冷水吸收热量和正丁醇放出热量相等Q =W c C pc(t1-t2),C pc=(kg•℃)×10³=×10³W c()W c=s ∴V=12m。
