(完整word版)人胰岛素的工业制备
人胰岛素的制备

⼈胰岛素的制备⼈胰岛素得制备⼀、获得⽬得基因从供体细胞中提取mRNA,以其为模板,在反转录酶得作⽤下,反转录合成胰岛素mRNA互补DNA,再以cDNA第⼀链为模板,在反转录酶或DNA聚合酶I得作⽤在,最终合成编码它得双链DNA序列。
即得到了⽬得基因。
反转录-聚合酶链反应法(⼀)从⼈体细胞内提取胰岛素基因转录得mRNA1, 细胞总RNA得提取 :取胰岛B细胞,⽤PBS洗后,加⼊TRIZOL试将细胞破裂,后⽤DEPC处理,多次离⼼后,取RNA⽩⾊沉淀,测OD值,电泳。
2 ,从总RNA中分离mRNA:取上述提取得总RNA若⼲,加⼊Buffer OBB ,Oligotex Suspension ,打匀。
70℃⽔浴(裂解RNA得⼆级结构), 20-30℃条件下,静置(让Oligotex与mRNA结合)。
将Oligotex/mRNA复合物得沉淀加到EP管SPIN柱上⾼速离⼼,加Buffer 将其她RNA洗脱,最后⽤琼脂糖凝胶电泳纯化mRNA。
(⼆)mRNA转录合成cDNA第⼀链cone 第⼀链得合成加⼊上步获得得mRNA与适当引物于EP管中,加⼊RNase-free water,混匀后,70℃反应10分钟,反应完成后,⽴刻将反应体系置于冰上5min;稍微离⼼⼀下,顺序加⼊缓冲液、 RNA酶抑制剂、反转录酶、 dNTP(加⼊放射性同位素利于检验), 混匀,稍微离⼼反应物之后,42℃放置2分钟。
取出置于冰上。
电泳分析,同位素活性测定。
(三)PCR法扩增,特异合成⽬得cDNA链通过胰岛素得特异引物,⽤PCR法进⾏扩增,特异得合成胰岛素得cDNA 链。
PCR法得操作步骤:预变性引物退⽕引物延伸循环25-35次最后延伸前端引物:5’-ggt tcc gga tct ggt tct ggt tct ctg gtc ccc cgc ggt agt cac caccac cac cac cac cgt ttt gtg aac caa cac ctg tgc ggc-3’后端引物:5’-agt gtc gac tta gtt gca gta gtt ctc cag ctg gta-3’⼆、组建重组质粒采⽤pQE--30质粒作为载体,⽤双酶切法进⾏基因重组。
胰岛素工艺流程

胰岛素工艺流程
《胰岛素工艺流程》
胰岛素是一种重要的荷尔蒙,被用于治疗糖尿病患者。
胰岛素工艺流程是指将动物源或重组DNA技术获得的前体胰岛素经过一系列的生物化学反应和分离纯化过程,最终得到纯净的胰岛素的制备流程。
首先,采用动物源或者重组DNA技术获得前体胰岛素,然后通过一系列的生物化学反应和分离纯化过程,如酶解反应、蛋白质纯化、过滤、结晶、浓缩等步骤,将其提取并获得纯净的胰岛素产品。
在这个流程中,每一步都需要严格控制温度、PH值、反应时间等因素,避免影响反应产率和产品的纯度。
同时,要确保生化反应的条件和反应物的质量都符合生产要求,以确保最终产品的质量和效果。
这个工艺流程中需要使用各种生物化学技术和设备,如酶解反应釜、离心机、膜分离设备、结晶设备等。
同时,还需要进行严格的质量控制和产品检测,以确保产品符合相关标准和法规要求。
胰岛素工艺流程的成功应用,使得胰岛素的生产得以规模化和工业化,为糖尿病患者提供了重要的药物治疗手段,也促进了制药工业的发展和进步。
重组人胰岛素制备工艺

重组人胰岛素制备工艺引言胰岛素是一种由胰腺β细胞分泌的激素,它参与调节葡萄糖代谢,维持血糖水平稳定。
然而,对于许多糖尿病患者,体内胰岛素分泌不足或胰岛素抵抗使得血糖控制成为难题。
为了解决这一问题,重组人胰岛素制备工艺应运而生。
本文将详细介绍重组人胰岛素的制备工艺,以及如何通过优化制备工艺提高其产量和质量。
关键词介绍1、重组人胰岛素:是指利用基因工程技术,通过细胞培养或微生物发酵生产的胰岛素。
它具有与天然人胰岛素相同的结构和功能,因此在临床上有广泛的应用。
2、制备:是指通过一系列工艺步骤,从原料中提取或制造出所需物质的过程。
在重组人胰岛素制备中,主要包括基因工程操作、细胞培养、发酵、分离和精制等步骤。
3、工艺:是指实现制备过程的一系列具体方法和操作规程。
工艺的选择和优化直接影响到产品的产量和质量。
重组人胰岛素制备工艺1、酵母菌的筛选:选用适合生产重组人胰岛素的酵母菌种,对其进行筛选和改良,以提高发酵过程中的产量。
2、基因工程操作:将人胰岛素基因插入到酵母菌的染色体或质粒中,确保基因正确表达。
3、发酵:在适宜的营养条件下,利用筛选得到的酵母菌进行发酵生产。
4、分离和精制:通过一系列物理、化学和生物学方法,将重组人胰岛素从发酵液中分离出来,并进行精制和纯化,以得到高纯度的产品。
制备工艺优化1、通过现代实验设计方法和技术,如响应面法和均匀设计法,筛选最佳工艺条件,以提高重组人胰岛素的产量和质量。
2、通过基因工程技术改良酵母菌,增强其生产重组人胰岛素的能力,提高产量。
3、采用先进的分离和精制技术,如高效液相色谱和超滤膜过滤等,进一步提纯产品,提高产品质量。
4、结合计算机模拟技术和实验验证,模拟工艺过程,指导实际生产,优化制备工艺。
重组人胰岛素制备工艺在糖尿病治疗中具有重要意义,本文详细介绍了其制备过程及优化方法。
通过合理选择工艺条件和基因工程改良,可以有效提高重组人胰岛素的产量和质量。
随着科学技术的发展,相信未来制备工艺将进一步优化,为糖尿病患者提供更好的治疗选择。
胰岛素工艺流程说明

胰岛素工艺流程说明-标准化文件发布号:(9456-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII
重组人胰岛素产品生产工艺流程
时转入发酵罐培养
分两阶段进行控制,第一阶段主要通过控制溶氧和补加
体达到富集的目的,第二阶段通过补加甲醇使菌体进行高密度表
达目的产物,HPLC检测目的产物含量
目的产物存在于发酵液上清中,此步骤主要控制目的产物收率
通过两步柱层析,分别去除发酵上清液中的色素和杂蛋白
利用紫外检测仪控制目的产物收率,主要试剂为乙醇与异丙醇
调节PH值,使P1沉淀,再经离心干燥,得中间体I 固体
2
3
控温进行转肽反应,主要试剂为DMSO 与1,4-丁二
醇
再通过柱层析进行提纯,主要试剂为异丙醇
调节PH 值,使P2沉淀,再经离心干燥,得中间体
II 固体
通过控制湿度与温度进行脱帽反应,得到终产物胰岛素
主要试剂为丙酮,产品为半固体
经过两步柱层析对胰岛素进行提纯,试剂为Tris-HCl 和异丙醇
通过超滤对提纯后的胰岛素进行浓缩,通过管道传递
到下工序
通过制备色谱对胰岛素粗品进行精制,主要试剂为色谱乙腈
然后经两步结晶后通过管道过滤除菌到百级区
对胰岛素成品进行一次结晶和水洗
对水洗后的胰岛素进行过滤除菌后冻干,即得胰岛素成品
4
重组人胰岛素生产工艺流程功能间分布
5。
人胰岛素的工业制备

人工胰岛素制备工艺的研究及其进展摘要:据WHO 统计,全世界糖尿病患者已接近1.2亿,而我国目前糖尿病患者的总数已达到3000万人,跃居世界第二位,其中数百万患者长期使用胰岛素治疗。
如今我国经济发展迅速,同时也带来了巨大生活的压力和健康问题,并且带有一定的遗传因素,数百万患者需要长期使用胰岛素治疗。
胰岛素是由胰岛β细胞受内源性或外源性物质如葡萄糖、乳糖、核糖、精氨酸等的刺激而分泌的一种蛋白质激素。
而目前临床使用的胰岛素有三种来源:1、动物胰岛素(从猪和牛的胰腺中提取,两者药效相同,但与人胰岛素相比,猪胰岛素中有1个氨基酸不同,牛胰岛素中有3个氨基酸不同,因而易产生抗体)。
2、半合成胰岛素(将猪胰岛素第30位丙氨酸,置换成与人胰岛素相同的苏氨酸,即为半合成人胰岛素)。
3、重组人工胰岛素(利用生物工程技术,获得的高纯度的生物合成人胰岛素,其氨基酸排列顺序及生物活性与人体本身的胰岛素完全相同)。
可见第三种方法是目前最好的副作用最小,而且简单安全的方法。
所以针对重组人工胰岛素的制备做了以下研究。
关键词:重组人工胰岛素;大肠杆菌;(His)6一Arg—Arg一人胰岛素原;在当今世界范围内,诺和诺德、辉瑞、万安特以及我们国内的通化东宝、深圳科兴等生物技术公司在胰岛素的生产技术上已经都是很先进的水平了,也就是重组人工胰岛素的制备方法。
这种方法是自从动物中提取胰岛素和人工合成胰岛素的方法以来,最简便而且是最有效最安全的制备胰岛素的方法。
它是发酵工程技术和基因工程技术结合的产物,也是造福人类的新一代药物生产方法。
不仅在治疗糖尿病方面的作用突出,同时对治疗癌症等严重影响人类健康的疾病的治疗开创了思路。
所以,作为本科生的生物技术专业制药方向的大学生来说,这种利用基因工程,发酵工程等方法工业制备胰岛素的原理和流程的工艺,和这种开拓创新的思维是我们必须要了解和学习得。
1重组人工胰岛素的生产原理通过基因工程酵母菌发酵生产hPI,经后加工形成hI。
人胰岛素的制备
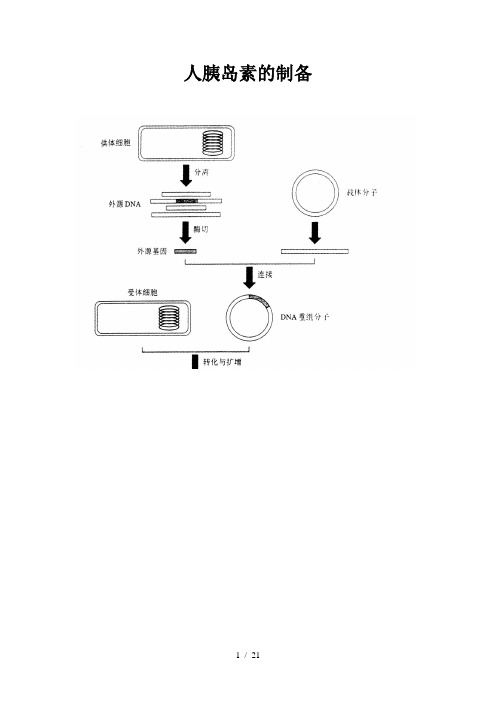
人胰岛素的制备一、获得目的基因从供体细胞中提取mRNA,以其为模板,在反转录酶的作用下,反转录合成胰岛素mRNA互补DNA,再以cDNA第一链为模板,在反转录酶或DNA聚合酶I的作用在,最终合成编码它的双链DNA序列。
即得到了目的基因。
反转录-聚合酶链反应法(一)从人体细胞内提取胰岛素基因转录的mRNA1, 细胞总RNA的提取:取胰岛B细胞,用PBS洗后,加入TRIZOL试将细胞破裂,后用DEPC处理,多次离心后,取RNA白色沉淀,测OD值,电泳。
2 ,从总RNA中分离mRNA:取上述提取的总RNA若干,加入Buffer OBB ,Oligotex Suspension ,打匀。
70℃水浴(裂解RNA的二级结构),20-30℃条件下,静置(让Oligotex与mRNA结合)。
将Oligotex/mRNA复合物的沉淀加到EP管SPIN柱上高速离心,加Buffer将其他RNA洗脱,最后用琼脂糖凝胶电泳纯化mRNA。
(二)mRNA转录合成cDNA第一链cone 第一链的合成加入上步获得的mRNA和适当引物于EP管中,加入RNase-free water,混匀后,70℃反应10分钟,反应完成后,立刻将反应体系置于冰上5min;稍微离心一下,顺序加入缓冲液、RNA酶抑制剂、反转录酶、dNTP (加入放射性同位素利于检验),混匀,稍微离心反应物之后,42℃放置2分钟。
取出置于冰上。
电泳分析,同位素活性测定。
(三)PCR法扩增,特异合成目的cDNA链通过胰岛素的特异引物,用PCR法进行扩增,特异的合成胰岛素的cDNA链。
PCR法的操作步骤:预变性引物退火引物延伸循环25-35次最后延伸前端引物:✧5’-ggt tcc gga tct ggt tct ggt tct ctg gtc ccc cgc ggt agt caccac cac cac cac cac cgt ttt gtg aac caa cac ctg tgc ggc-3’✧后端引物:✧5’-agt gtc gac tta gtt gca gta gtt ctc cag ctg gta-3’二、组建重组质粒采用pQE--30质粒作为载体,用双酶切法进行基因重组。
胰岛素工艺流程说明

胰岛素工艺流程说明胰岛素是一种由胰腺分泌的激素,主要功能是调节血糖水平。
当血糖水平升高时,胰岛素促使身体细胞摄取和利用血糖,从而使血糖水平恢复正常。
胰岛素的工艺流程包括胰岛素的提取、纯化、结晶和制剂的制备。
接下来是胰岛素的纯化。
胰岛素提取液中一般含有其他蛋白质、酶和杂质等,需要经过纯化步骤去除这些杂质。
纯化的方法可以使用超滤、透析、离子交换和凝胶层析等技术,将胰岛素与其他组分分离开来。
在纯化过程中,要保持一定的温度和小生物活性分子获得高纯度的胰岛素。
然后是胰岛素的结晶。
结晶是将纯化后的胰岛素溶液通过降温或添加结晶剂,使胰岛素分子结合在一起形成晶体。
结晶过程中,需要调节温度、pH值和添加剂的浓度等参数,以优化结晶的效果。
结晶后的胰岛素晶体需要通过离心、洗涤和干燥等步骤,获取纯净的胰岛素固体。
最后是胰岛素制剂的制备。
制剂是将胰岛素转化为适合人体使用的药物形式,以便于患者的使用和储存。
常见的胰岛素制剂形式包括注射剂、胶囊和鼻喷剂等。
在制剂制备过程中,需要在胰岛素固体中添加适当的辅料,如稳定剂、调节剂和缓冲剂等,以确保胰岛素的稳定性和药效。
1.温度的控制:胰岛素是一种蛋白质,对于温度的变化非常敏感,过高的温度会导致蛋白质变性失活。
因此,在提取、纯化和结晶过程中,需要确保温度的适宜。
2.pH值的控制:胰岛素的活性受到pH值的影响,过高或过低的pH值都会对胰岛素的活性产生不良影响。
在工艺流程中,需要根据胰岛素的特性,调节溶液的pH值,以保持胰岛素的活性。
3.杂质的去除:胰岛素的提取液中可能存在着其他组分和杂质,如酶、蛋白质和盐等。
这些杂质会影响胰岛素的纯度和活性,需要通过适当的纯化步骤将其去除。
4.结晶剂的选择:结晶是提高胰岛素纯度的关键步骤,合适的结晶剂的选择可以促进胰岛素晶体的生成和增长,从而得到高纯度的胰岛素。
综上所述,胰岛素的工艺流程包括提取、纯化、结晶和制剂制备。
在整个流程中,需要注意温度、pH值、结晶剂的控制以及杂质的去除,以获得高质量的胰岛素制剂。
人胰岛素的制备

人胰岛素的制备一、获得目的基因从供体细胞中提取mRNA,以其为模板,在反转录酶的作用下,反转录合成胰岛素mRNA互补DNA,再以cDNA第一链为模板,在反转录酶或DNA聚合酶I的作用在,最终合成编码它的双链DNA序列。
即得到了目的基因。
反转录-聚合酶链反应法(一)从人体细胞内提取胰岛素基因转录的mRNA1, 细胞总RNA的提取:取胰岛B细胞,用PBS洗后,加入TRIZOL试将细胞破裂,后用DEPC处理,多次离心后,取RNA白色沉淀,测OD值,电泳。
2 ,从总RNA中分离mRNA:取上述提取的总RNA若干,加入Buffer OBB ,Oligotex Suspension ,打匀。
70℃水浴(裂解RNA的二级结构),20-30℃条件下,静置(让Oligotex与mRNA结合)。
将Oligotex/mRNA复合物的沉淀加到EP管SPIN柱上高速离心,加Buffer将其他RNA洗脱,最后用琼脂糖凝胶电泳纯化mRNA。
(二)mRNA转录合成cDNA第一链cone 第一链的合成加入上步获得的mRNA和适当引物于EP管中,加入RNase-free water,混匀后,70℃反应10分钟,反应完成后,立刻将反应体系置于冰上5min;稍微离心一下,顺序加入缓冲液、RNA酶抑制剂、反转录酶、dNTP(加入放射性同位素利于检验),混匀,稍微离心反应物之后,42℃放置2分钟。
取出置于冰上。
电泳分析,同位素活性测定。
(三)PCR法扩增,特异合成目的cDNA链通过胰岛素的特异引物,用PCR法进行扩增,特异的合成胰岛素的cDNA 链。
PCR法的操作步骤:预变性引物退火引物延伸循环25-35次最后延伸✧前端引物:✧5’-ggt tcc gga tct ggt tct ggt tct ctg gtc ccc cgc ggt agt cac cac cac cac cac cac cgtttt gtg aac caa cac ctg tgc ggc-3’✧后端引物:✧5’-agt gtc gac tta gtt gca gta gtt ctc cag ctg gta-3’二、组建重组质粒采用pQE--30质粒作为载体,用双酶切法进行基因重组。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
人工胰岛素制备工艺的研究及其进展摘要:据WHO 统计,全世界糖尿病患者已接近1.2亿,而我国目前糖尿病患者的总数已达到3000万人,跃居世界第二位,其中数百万患者长期使用胰岛素治疗。
如今我国经济发展迅速,同时也带来了巨大生活的压力和健康问题,并且带有一定的遗传因素,数百万患者需要长期使用胰岛素治疗。
胰岛素是由胰岛β细胞受内源性或外源性物质如葡萄糖、乳糖、核糖、精氨酸等的刺激而分泌的一种蛋白质激素。
而目前临床使用的胰岛素有三种来源:1、动物胰岛素(从猪和牛的胰腺中提取,两者药效相同,但与人胰岛素相比,猪胰岛素中有1个氨基酸不同,牛胰岛素中有3个氨基酸不同,因而易产生抗体)。
2、半合成胰岛素(将猪胰岛素第30位丙氨酸,置换成与人胰岛素相同的苏氨酸,即为半合成人胰岛素)。
3、重组人工胰岛素(利用生物工程技术,获得的高纯度的生物合成人胰岛素,其氨基酸排列顺序及生物活性与人体本身的胰岛素完全相同)。
可见第三种方法是目前最好的副作用最小,而且简单安全的方法。
所以针对重组人工胰岛素的制备做了以下研究。
关键词:重组人工胰岛素;大肠杆菌;(His)6一Arg—Arg一人胰岛素原;在当今世界范围内,诺和诺德、辉瑞、万安特以及我们国内的通化东宝、深圳科兴等生物技术公司在胰岛素的生产技术上已经都是很先进的水平了,也就是重组人工胰岛素的制备方法。
这种方法是自从动物中提取胰岛素和人工合成胰岛素的方法以来,最简便而且是最有效最安全的制备胰岛素的方法。
它是发酵工程技术和基因工程技术结合的产物,也是造福人类的新一代药物生产方法。
不仅在治疗糖尿病方面的作用突出,同时对治疗癌症等严重影响人类健康的疾病的治疗开创了思路。
所以,作为本科生的生物技术专业制药方向的大学生来说,这种利用基因工程,发酵工程等方法工业制备胰岛素的原理和流程的工艺,和这种开拓创新的思维是我们必须要了解和学习得。
1重组人工胰岛素的生产原理通过基因工程酵母菌发酵生产hPI,经后加工形成hI。
酵母系统下游后加工比细菌表达系统简单,但缺点是生产慢,生产周期长,且重组蛋白分泌量少(1~50 mg/L),产量低。
因此,虽然rhI投放市场已久,但人们一直在努力寻求和探索更加有效的表达系统和高效的表达策略I2 J,尤其是对E.CO一尻表达系统的研究更是越来越深入,用E.coli系统表达hPI的策略也越来越多。
另一方面,在胰岛素的基因工程生产中,下游处理非常复杂,复杂的下游处理极大地降低了胰岛素的最终收率。
本研究围绕着提高重组目的蛋白表达量,简化下游处理过程等方面进行探索,建立了一套经过优化的高效完整的基因工程E.coli发酵表达(His)6一Arg—Arg一人胰岛素原[(His)6一Arg—Arg—human proinsulin,PPh—PI],后加工成hI的制备工艺。
2重组人工胰岛素的生产工艺流程2.1菌种的制备2.1.1目的基因的提取既从人的DNA中提取胰岛素基因,可使用限制性内切酶将目的基因从原DNA中分离。
主要有如下4种方法:(1)鸟枪法:用一大堆限制性核酸内切酶对附近基因进行剪切,再提取所需要的。
至于如何筛选,用DNA分子杂交,即DNA探针(2)人工合成法:根据转录蛋白或者mRNA推导出基因序列,然后人工合成,没有内含子。
(3)从基因文库中提取:也就是事先已经提取完毕的拿来用(4)PCR扩增技术:用于大量生产该段基因片段,用于商业化运作。
2.1.2提取质粒使用细胞工程,培养大肠杆菌,从大肠杆菌的细胞质中提取质粒质粒为环状。
碱裂解法:此方法适用于小量质粒DNA的提取,提取的质粒DNA可直接用于酶切、PCR扩增、银染序列分析。
2.1.3基因重组将取出目的基因与质粒,先利用同种限制性内切酶将质粒切开,再使用DNA连接酶将目的基因与质粒“缝合”,形成一个能表达出胰岛素的DNA质粒。
2.1.4将质粒送回大肠杆菌再大肠杆菌的培养液中加入含有Ca+的物质,如CaCl2,这使细胞会吸收外源基因,此时将重组的质粒也放入培养液中,大肠杆菌便会将重组质粒吸收。
将大肠杆菌用氯化钙处理,以增大大肠杆菌细胞壁的通透性,使含有目的基因的重组质粒能够进入受体细胞,此时的细胞处于感受态(理化方法诱导细胞,使其处于最适摄取和容纳外来DNA的生理状态)。
2.2胰岛素的产生和精制(即菌种的发酵培养)重组人工胰岛素的工业生产制备和深加工技术在如今已经是炉火纯青。
有近百年的发酵工程为基础,结合现在的基因工程技术的产物,在菌种制备后的发酵培养过程更是可靠和安全的。
发酵培养流程见下图表:对从菌种库中取出的菌种进行活化及初步扩大培养时转入发酵罐培养分两阶段进行控制,第一阶段主要通过控制溶氧和补加甘油使菌体达到富集的目的,第二阶段通过补加甲醇使菌体进行高密度表达目的产物,HPLC检测目的产物含量目的产物存在于发酵液上清中,此步骤主要控制目的产物收率通过两步柱层析,分别去除发酵上清液中的色素和杂蛋白利用紫外检测仪控制目的产物收率,主要试剂为乙醇与异丙醇调节PH值,使P1沉淀,再经离心干燥,得中间体I固体控温进行转肽反应,主要试剂为DMSO与1,4-丁二醇再通过柱层析进行提纯,主要试剂为异丙醇调节PH值,使P2沉淀,再经离心干燥,得中间体II固体通过控制湿度与温度进行脱帽反应,得到终产物胰岛素主要试剂为丙酮,产品为半固体经过两步柱层析对胰岛素进行提纯,试剂为Tris-HCl和异丙醇通过超滤对提纯后的胰岛素进行浓缩,通过管道传递到下工序通过制备色谱对胰岛素粗品进行精制,主要试剂为色谱乙腈然后经两步结晶后通过管道过滤除菌到百级区对胰岛素成品进行一次结晶和水洗对水洗后的胰岛素进行过滤除菌后冻干,即得胰岛素成品制得的胰岛素经过深加工,可以得到片剂,注射剂和肺部吸入制剂等。
3药物检测这种重组人工胰岛素的检测重点应该是①测定生物活性②效价测定③控制产品中杂质潜在有害物质④保证产品安全性和有效性胰岛素的生物效应包括许多方面, 它是体内唯一能降低血糖的激素。
也是唯一时促进糖原、脂肪、蛋白质合成的激素。
胰岛素的主要靶器官为肝脏、肌肉及脂肪组织, 它控制着三大营养物质糖、蛋白质、脂肪的代谢和贮存。
最明显的作用是影响糖的代谢, 降低血糖,即促进肝脏及肌肉组织中葡萄糖的利用, 激活糖原合成酶和丙酮酸脱氢酶等的活性, 促进糖原的合成并抑制糖原的分解。
此外, 对肝脏来说还有抑制蛋白质分解的作用;在肌肉组织中促进+K从细胞外向细胞内的转运;在脂肪组织中促进氨基酸由细胞外向细胞内转运,促进脂肪的合成,抑制脂肪的分解等作用。
这些在细胞水平上对代谢系统的作用是基于胰岛素与其受体的结合得以实现的。
关于效价的测定《中华人民共和国药典》指出供试品制成盐酸溶液,进入高效液相色谱仪进行色谱分离,用紫外吸收检测器,于波长214nm处检测重组人胰岛素的吸收值,计算出其含量。
无数临床试验证明,到目前为止,重组人工胰岛素是稳定糖尿病最好的选择,其没有潜在的危险,并且安全可靠。
4问题与展望胰岛素在糖尿病治疗中具有无可替代的作用和地位,但因注射给药让许多患者产生畏惧心理,使其作用发挥受到限制。
为了减少不便和疼痛,医药界正在全力以赴投入研究,开发更新的胰岛素剂型及给药方式。
目前有关新式胰岛素产品的研究方向,可归纳为3类:1.新的给药方式,例如:口服、吸入;2.改变药物代谢机制;3.改进注射手段,让使用者无痛;这是国际国内胰岛素类药物研究发展的前沿和趋势。
4.1非注射型胰岛素让胰岛素和其他药物一样成为非注射型药品,通过口服、鼻吸等途径进入人体而免除注射,需要研究解决制剂吸收的问题。
由于胰岛素本身的疗效和安全性已经非常确定,而改变的是给药途径,因此吸收程度和速度是需要解决的首要问题。
4.2口服胰岛素胰岛素本身为蛋白质,口服后会被胃肠道降解破坏,所以常规胰岛素不能口服。
口服给药受到胃酸、蛋白分解酶、大分子吸收、肝脏首过效应等影响,因此,口服胰岛素的研究方向主要在以下几方面:1.选用惰性材料如高分子纤维素,制成了微小包裹球。
这种小球在胃中不溶,保护胰岛素不被破坏。
现阶段的研究成果可保持其生物有效性达到皮下注射给药的一半。
2.加入酶抑制剂,将蛋白酶抑制剂与胰岛素一起包裹在小球中,可有助于提高胰岛素的吸收。
3.加入吸收促进剂,将胰岛素与吸收促进剂同时给药,能进一步促进口服胰岛素吸收,其中的螯合剂能与肠粘膜上活性离子结合,造成膜通道通透性增加而促进药物在肠道吸收。
国内外有关口服胰岛素研究报道虽然很多,但至今未见到实际应用于临床。
其主要原因是口服生物利用度低、制剂的稳定性、质量标准等问题尚未解决。
口服胰岛素的成功与否在于如何解决其在胃肠道的活性和稳定性,一旦成功将是胰岛素研究的重大突破。
4.3经肺吸入胰岛素胰岛素经肺吸入给药,是替代注射最有希望的途径之一。
肺部特殊的生理构造是具有极大的肺泡表面积。
此点优势具有决定性,使胰岛素这样的大分子药物吸收成为可能;药物可迅速到达;不必经过肝脏首过效应;提高了药物的生物利用度。
另外重要的一点,胰岛素在肺部吸收的速度快,符合内源性胰岛素的释放特征和人体的需要,并且可以在进餐的同时应用,而使用药更加方便。
最新的进展是采用干粉剂型,其优于早先的液体气雾剂。
干粉的稳定性好,保质期可达两年;干粉的载药量高,仅需吸1~3次即可满足剂量要求,而如果用喷雾则需深吸几十次。
胰岛素吸入制剂在国外已进入第二、三期临床试验,一些制药公司的专家相信在不久的将来就会投入使用。
此项技术已经引起了广泛的关注,但其面临尚待解决的问题是:药物吸收的稳定性、成本高以及对肺功能的影响等,通过临床试验和上市的时间尚属未知。
吸入胰岛素相对于传统的注射方式的优越性不言而喻,且理论上颇具可行性,我们的医生和患者都在热切盼望中。
4.4其他非注射给药方式正在研究中的其他非注射胰岛素给药途径包括:口腔喷雾、鼻腔给药、直肠栓剂给药、滴眼剂、透皮或口腔粘膜给药。
这些非注射给药途径都有一些难以克服的问题,如吸收缓慢、药峰浓度低、生物利用度低等,均不能达到注射剂的效果,目前尚无法适合糖尿病临床治疗的需要。
胰岛素非注射给药是医药界的重大和热门研究课题,其结果对糖尿病治疗产生深远影响。
国内外的专家学者正致力于相关的研究开发。
参考文献:[1] 李晓红,朱慧玲,余荣,李红霞.重组人工胰岛素制备工艺[M].四川大学学报,2007,39卷第4期.[2] 王琼庆,冯佑民.胰岛素蛋白质研究进展.生物化学与生物物理进展,1996,23(5):402.[3] 张晓刚,李志华.发酵工程制药。
北京工业出版社,2004[4] 陈来同,孙宇.B19-Gly-B20人胰岛素的分离纯化及性质研究[J].中国生化药物杂志,2001,22(5):234[5]张友尚.胰岛素生产的回顾与展望[J].食品与药,2008,10卷第01期[6] 李湛君,杨昭鹏,徐康森.重组人胰岛素效价测定中生物测定与理化测定的相关性验证.药物分析杂志,1998,18(4):241。
