第十一章配位化合物
第十一章:配位化合物介绍

配合物中直接与中心原子结合成键的配位原子的总数目。 单齿配体 配位数等于 配体数 如[Fe(CN)6]3多齿配体 配位数不等于配体数 如[Pt(en)2]2+ 表11-1 常见金属离子的配位数 配 位 数 2 4 离 子 Ag+,Cu+,Au+ Zn2+,Cu2+,Hg2+,Ni2+,Co2+,Pd2+, Si4+,Ba2+ Fe2+,Fe3+,Co2+,Co3+,Cr3+,Pt4+, Pd4+,Al3+,Si4+,Ca2+,Ir3+
26Fe 3+ 2+ +
例如:
[Ar] 3d54s04p0 [Ar] 3d84s24p0 [Ar] 4d105s05p0 [Ar] 3d84s24p0
26Si
4+
[SiF6]2-
27Co 47Ag 28Ni
2 配位体 ( ligand ): 在中心原子周围以一定的空间 构型排列的阴离子或 分子(以配位键结合),它 们能给出孤对电子或电子
[Ni(CO)4]
配合物 [Cu(NH3)4]SO4
内层
[ Cu ( NH 3 ) 4 ] 2+ 中 心 原 子 配配 配 配 位位 位 离 原体 数 子 子 电 荷
外层
S O4 2 外 界 离 子
1 中心原子(central atom )
位于配离子中心的离子或原子 具有空的价电子轨道(通常指(n-1)d,ns,np,nd轨 道)能接受孤对电子 一般是金属离子,大多是过度金属,Ⅷ及其附近副族 元素,少数高氧化值的主族元素离子
配位化学

dz2 dx2-y2
eg
3 5
Δo
=6Dq
2 5
Δo
Δo =10Dq
= 4Dq t2g
dxy dxz dyz
八面体场中d轨道能级分裂
24
25
分裂能o
电子成对能(P):两 个电子进入同一轨道 时需要消耗的能量 排布原则:①能量最低原理 ②Hund规则 ③Pauli不相容原理
配位体的电子到底按哪种形式排布决定于分裂能与电子成 对能的大小。电子成对能小些,则电子尽可能排在能量低 的轨道,属于低自旋型,磁矩小,稳定;分裂能小则电子 排在高能量轨道上,属于高自旋型,磁矩大,也不稳定。
[Ni(CN)4]2-的μ = 0,其空间构型为平面正方形
3d
4s 4p
Ni2+
[Ni(CN)4]2-
dsp2杂化 CN- CN- CN-CN-
[NiCl4]2-的μ = 2.83 B.M,空间构型为四面体。
3d
4s
4p
[NiCl4]2-
sp3杂化
Cl- Cl- Cl- Cl17
以Fe(CN)63-为例说明中心离子的杂化轨道 形成配离子 和配合物的配位键形成示意图表示如下:
21
• 形成高自旋配合物的配体有F-、H2O等,其配位原子是电负性 较大的卤素原子和氧原子,不容易给出孤对电子,对中心离子的影 响小,因而不会使中心离子的电子层结构发生改变。 • 反之,如果配位原子电负性小,则容易给出孤对电子,这些 孤对电子影响了中心离子的电子层结构,使(n-1)d轨道上的成单 电子被强行配对,腾出内层能量较低的轨道接受孤对电子,从而形 成低自旋配合物。这类配体主要是CN-(C为配位原子)、-NO2。 • (由CN-形成的配合物一般很稳定,而由F-、H2O 形成的配合物 稳定性差些就是这个原因)
第十一章配合物图片2003-12-8 AND12-11

配位化合物
祖母绿(翡翠)
3BeO·Al2O3 ·6SiO2 + Cr3+ in Al3+ sites
绿宝石
CuAl6(PO4)4(OH)8⋅4H2O
配位化合物的基本概念
CuSO4 + 4NH3 === [Cu(NH3)4]SO4 AgCl + 2NH3 === [Ag(NH3)2]Cl PtCl4 + 2KCl === K2[PtCl6] 3NaF + AlF3 === Na3[AlF6]
MX5Y MX4Y2 MX3Y3 MX4YZ MX3Y2Z
MX2Y2Z2
1 2 2 2 3 5
[PtCl(NH3)5]Cl3,K[PtCl5(NH3)] [PtCl2(NH3)4]Cl2,[PtCl4(NH3)2] [PtCl3(NH3)3]Cl [PtCl(NO2)(NH3)4]Cl2 [PtCl3(OH)(NH3)2] [PtCl2(OH)2(NH3)2]
配位化合物 —— 由简单化合物之间进一步反应形成的含有 复杂离子的分子间化合物。不同于“复盐”,但并无绝对的界限,在它
之间存在大量的处于中间状态的复杂化合物。
配离子 —— 配位化合物的复杂离子称为配离子。是一种较 为稳定的结构单元,既可存在于晶体中,也可存在于溶液中。 可以是阳离子、阴离子或中性分子。通常用[ ]标出。 内界和外界 —— 内界由中心离子和配位体构成,如 [Ag(NH3)2],放在[ ]内。[ ]以外部分称为外界,如 [Ag(NH3)2]Cl中的Cl-。 中心离子或中心原子 —— 亦称为配合物的形成体,位于配 离子(或分子)的中心。绝大多数是带正电的金属离子。许 多过渡金属离子是较强的配合物形成体。如[Ag(NH3)2]-中 Ag+离子,Ni(CO)4中的中性原子Ni,SiF62-中的高氧化态非金 属元素Si(IV)等。
第十一章配位化合物

第十一章配位化合物首页第十一章配位化合物基本要求重点难点讲授学时内容提要1 基本要求 [TOP] 1.1 掌握配合物的命名原则,学会由名称写出化学式。
1.2 掌握配位平衡的基本计算。
1.3 熟悉配合物的价键理论,能够用以解释或推测一些配合物的磁矩和相对稳定性。
1.4 熟悉酸碱反应、沉淀反应和氧化还原反应对配位平衡的影响。
1.5 了解晶体场理论。
1.6 了1.6 了解生物体内的配合物。
1.7 掌握配合物的离解平衡 1.8 了解螯合物的结构特点螯合剂氨羧螯合剂 EDTA 及其二钠盐金属氨羧配合物的稳定性 1.9 配合物与医学的关系,对生命现象的重要作用2 重点难点 [TOP] 2.1 重点 2.1.1 配合物的命名原则。
2.1.2 配位平衡的基本计算。
2.1.3 配合物的价键理论。
2.2 难点晶体场理论。
3 讲授学时 [TOP] 建议4 学时4 内容提要 [TOP] 第一节第二节第三节第四节14.1 第一节配位化合物的基本概念 4.1.1 配位化合物的定义配合物是以具有接受电子对的离子或原子(统称中心原子)为中心,与一组可以给出电子对的离子或分子(统称配体),以一定的空间排列方式在中心原子周围所组成的质点(配离子或配分子)为特征的化合物。
玻尔假定:电子沿着固定轨道绕核旋转;当电子在这些轨道上跃迁时就吸收或辐射一定能量的光子。
轨道能量为4.1.2 配合物的组成大多数配合物由配离子与带有相反电荷的离子组成。
配离子由中心原子与配体组成。
配体中提供孤电子对的原子称配位原子。
常见的配位原子是电负性较大的非金属的原子N、O、C、S、F、Cl、Br、I 等。
只含有一个配位原子的配体称为单齿配体。
含有两个或两个以上配位原子的配体称多齿配体。
4.1.3 配合物的命名配位化合物的命名与一般无机化合物的命名原则相同。
1.配合物的命名是阴离子在前、阳离子在后,像一般无机化合物中的二元化合物、酸、碱、盐一样命名为“某化某”、“某酸”、“氢氧化某”和“某酸某”。
有机化学课件:第11章 配位化合物
如: 乙二胺 H2NCH2CH2NH2
(en)
二基配体
乙二胺四乙酸
(HOOCCH2)2 NCH2CH2N (CH2COOH)2 (EDTA)
六基配体
多基配体和螯合物 单基配体:只有一个配位原子的配体(NH3,H2O); 双基配体:含有二个配位原子的配体 (C2O42- ,en)等; 多基配体:含有多个配位原子的配体 (EDTA)。
配体的命名顺序为:
罗马数字
先无机配体,后有机配体;先阴离子,后中性分子。
若配体均为阴离子或中性分子时,可按配位原 子元素符号英文字母顺序排列。
如: en 、H2O NH3、H2O
先 H2O 后 en 先 NH3 后 H2O
[CoCl2(NH3)2(H2O)2]Cl 氯化二氯·二氨·二水合钴(Ⅲ) 复杂配体均加括号
胺
H2C H2N
NH2 CH2 2
Cu
H2C H2N
NH2 CH2
由中心原子与多齿配 体形成的环状配合物 称为螯合物
形成的环 以5元环 和 6元环稳定
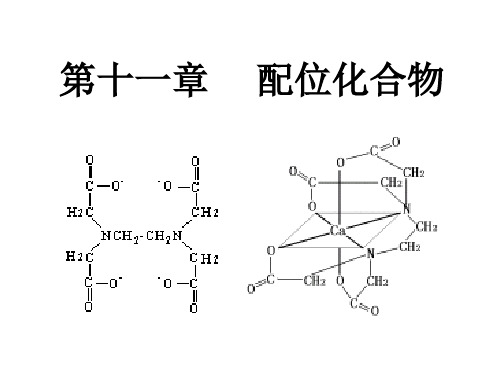
常见的多齿配体:乙二胺四乙酸(EDTA)
HOOCH2C
CH2COOH
NCH2-CH2N
HOOCH2C
CH2COOH
[Ca(edta)]2
5个 5元环
几何异构 光学异构
电离异构
[CoSO4(NH3)5]Br [CoBr(NH3)5]SO4
水合异构
[Cr(H2O)6]Cl3 [CrCl(H2O)5]Cl2·H2O [CrCl2(H2O)4]Cl·2H2O [CrCl3(H2O)3]·3H2O
配位异构
[Co(NH3) 6][Cr(C2O4)3] Cr (NH3) 6][Co (C2O4)3]
高中化学竞赛课程 无机化学第十一章 配位化合物和配位平衡

Chapter 11 Coordination Compounds and Coordication Equilibrium
一、 配合物的基本概念
实验: 1. CuSO4(aq)
+ BaCl2 + NaOH
BaSO4 Cu(OH)2
有SO42有Cu2+
2. CuSO4(aq) + NH3.H2O 深蓝色aq + 乙醇 深兰色晶体
[Co(en)3][Cr(ox)3]和[Cr(en)3][Co(ox)3] [PtII(NH3)4][PtIVCl6]和[PtIV(NH3)4Cl2][PtIICl4]
配位体的种类、数目可以任意组合,中心离子、氧化态可以 相同,也可以不同。
d. 键合异构 组合相同,但配位原子不同的配体,如-NO2-和-ONO[CoNO2(NH3)5]Cl2 (黄褐色) [CoONO(NH3)5]Cl2 (红褐色)
[Co(en)3]2+ > [Co(NH3)6]2+
2. 化学式的书写原则
(1) 配合物中,阳离子在前,阴离子在后。 (2) 配离子中,按如下顺序:
形成体
阴离子配体
中性配体
例如: [Co(NO2)(NH3)5]SO4
3. 配位化合物的命名原则
遵循无机化合物的命名原则,不同点是配离子部分。
NaCl [Co(NH3)6]Cl3
d1~d3构型: 无高低自旋之分,无论强场还是弱场, 均形成内轨型配合物.
d8~d10构型: 无高低自旋之分,无论强场还是弱场, 均形成外轨型配合物.
稳定性:内轨型配合物 > 外轨型配合物
例: [Fe(CN)6]3-中CN-很难被置换,而[FeF6]3-中F-很容易被置换。
医学课件第11章配位化合物-01

离子键 配位键
[Cu┆(NH3)4]2+┆SO4 2-
内界
外界
K4+┆[Fe┆(CN) 6] 外界 内界
[Cu(NH3)4]SO4 [Cu(NH3)4]2++S K2SO4·Al2(SO4)3·24H2O 2K++2Al3++4SO42-+24H2O
(复盐)
配合物的类型
(1) 简单配位化合物([Cu(NH3)4]SO4)
❖ 配体的电荷越多,使配位数越少。 如:[Zn(NH3)6]2+和[Zn(CN)4]2-
13
2. 配体的浓度
在形成配离子时,配体的浓度增大有利于 形成高配位数的配合物(如Fe3+与SCN-的配合 物) 。
3. 温度
反应时温度低,有利于形成高配位的配合物 (热振动加剧时,中心原子与配体的振幅加大)。
(2) 螯合物(内配合物)
H2C—H2N Cu NH2—CH2
H2C—H2N
NH2—CH2
(3)多核配合物 [(H3N)2Pt Cl Pt(NH3)2]Cl2
Cl
(4) 配分子(HC≡CHAg 、Fe (CO)5)
3.配位数
直接与中心原子配合的配位原子数目 2、4、6 对于单齿配 中心原子的配位数=配体数
问题:
为什么血红细胞可以传送氧气? 为什么人会煤气中毒?
1
2
§11.1 配位化合物概述
CuSO4 + 4NH3 → [Cu(NH3)4]SO4 1693年 6KCN + FeSO4 → K4[Fe(CN)6 ] + K2SO4 Ni+CO 325K 1atm Ni(CO)4 (无色液体) SiO2+6HF → H2[SiF6] (无色气体)+2H2O 1、化合物组成不符合经典化合价规律 2、复杂结构单元有特殊稳定性
厦门大学无机化学第11章配位化合物

第十一章配位化合物11.1 基本概念 (1)11.2 化学键理论 (6)11.3 晶体场理论 (11)11.4 螯合物 (18)11.5 配位平衡 (19)11.1 基本概念11.1.1 配位化合物的基本概念前言配位化合物是一类由中心金属原子(离子)和配位体组成的化合物。
第一个配合物是1704年普鲁士人在染料作坊中为寻找蓝色染料,而将兽皮、兽血同碳酸钠在铁锅中强烈煮沸而得到的,即KFe[Fe(CN)6]。
配合物的形成对元素和配位体都产生很大的影响,以及配合物的独特性质,使人们对配位化学的研究更深入、广泛,它不仅是现代无机化学学科的中心课题,而且对分析化学、生物化学、催化动力学、电化学、量子化学等方面的研究都有重要的意义。
1.配位化合物的定义配合物是由中心原子(或离子)和配位体(阴离子或分子)以配位键的形式结合而成的复杂离子或分子,通常称这种复杂离子或分子为配位单元。
凡是含有配位单元的化合物都称配合物。
如:[Co(NH3)6]3+、[HgI4]2-、Ni(CO)4等复杂离子或分子,其中都含配位键,所以它们都是配位单元。
由它们组成的相应化合物则为配合物。
如:[Co(NH3)6]Cl3、k2[HgI4]、Ni(CO)411.1.2 组成2.配位化合物的组成图11-01表11-01 常见的配体表11.1.3 命名3.配位化合物的命名对于整个配合物的命名,与一般无机化合物的命名原则相同,如配合物外界酸根为简单离子,命名为某化某;如配合物外界酸根为复杂阴离子,命名为某酸某;如配合物外界为OH-,则命名为氢氧化某。
但配合物因为存在较为复杂的内界,其命名要比一般无机化合物复杂。
内界的命名顺序为:例如:11.1.4 配合物的类型4.配位化合物的类型(1).简单配位化合物简单配位化合物是指由单基配位体与中心离子配位而成的配合物。
这类配合物通常配位体较多,在溶液中逐级离解成一系列配位数不同的配离子。
例如:这种现象叫逐级离解现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(A)一定要有d轨道参与杂化; (B)一定要激发成对电子成单后杂 化; (C)一定要有空轨道参与杂化; (D)一定要未成对电子偶合后让出空 轨道杂化。 解:C
9、命名下列配合物和配离子 (1)(NH4)3[SbCl6]; (2)[Co(en)3]Cl3; (3)(Co(NO2)6)3-; (4)[Cr(H2O)4Br2]Br·2 H2O; (5)[Cr(Py)2(H2O)Cl3]; (6)NH4[Cr(SCN)4(NH3)2].
解:C
7、价键理论认为,决定配合物空间构 型主要是( ) (A)配体对中心离子的影响与作用; (B)中心离子对配体的影响与作用; (C)中心离子(或原子)的原子轨道杂 化; (D)配体中配位原子对中心原子的作 用。 解:C
8、配位化合物形成时中心离子(或原子)轨道 杂化成键,与简单二元化合物形成时中心原子轨 道杂化成键的主要不同之处是:配位化合物形成 时中心原子的轨道杂化( )
(1)六氯合锑(Ⅲ)酸铵; (2)三氯化三(乙二胺)合钴(Ⅲ); (3)六硝基合钴(Ⅲ)配阴离子; (4)二水合溴化二溴·四水合铬(Ⅲ); (5)三氯·水·二吡啶合铬(Ⅲ); (6)四硫氰根·三氨合铬(Ⅲ)酸铵。
10、根据下列配合物和配离子的名称写出其化学式 (1)四氯合肥铂(Ⅱ)酸六氨合铂(Ⅱ); (2)四氢合铝(Ⅲ)酸锂; (3)氯化二氯·四水合钴 (4)羟基·水·草酸根·乙二胺合铬(Ⅲ) (5)氯·硝基·四氨合钴(Ⅲ)配阳离子; (6)二氨·草酸根合镍(Ⅱ)
(1)[Pt(NH3)6][PtCl4]; (2)Li[AlH4]; (3)[Co(H2O)4Cl2]Cl; (4)[Cr(OH)(H2O)(C2O4)(en)]; (5)[Co(NH3)4(NO2)Cl+]; (6)[Ni(NH3)2(C2O4)]。
11、预测下列各对配离子稳定性相对高 低,并简要说明原因。 (1)Co(NH3)3+与Co(NH3)2+; (2)Zn(EDTA)2-与Ca(EDTA)2-; (3)Cu(NH2CH2COO)2与 Cu(NH2CH2CH2NH2).
解:sp;直线形。
4、价键理论认为,配合物具有不 同的空间构型是由于中心离子(或 原子)采用不同杂化轨道与配体成 键的结果。( )
解:对
5、同一元素带有不同电荷的离子作为 中心离子,与相同配体形成配合物时, 中心离子的电荷越多,其配位数一般 也越大。( )
解:对
6、配合物的磁矩主要取决于形成体的 ( ) (A)原子序数; (B)电荷数; (C)成单电子数; (D)成对电子数。
(1)稳定性Co(NH3)3+>Co(NH3)2+,因 前者中心的正电荷高、离子半径小, 对配体的引力大; (2)稳定性Zn(EDTA)2->Ca(EDTA)2-, 因的Ca2+极化能力和Zn2+变形性都比大;
(3)稳定性 Cu(NH2CH2CH2NH2)>Cu(NH2CH2COO)2,前者 配体中配位原子都是N,后者配体中配位 原子为N和O,N的配位能力比O强。
第十一章
配位化合物
1、价键理论认为,所有中心离子(或 原子)都既能形成内轨型配合物,又能 形成外轨型配合物。( )
解:错
2、不论配合物的中心离子采取d2sp3 或是sp3d2杂化轨道成键,其空间构型 均为八面体形+配离子中,Ag+采用 ________杂化轨道成键,该配离子的几 何构型为________________。
