hadwsw微生物限度检验系统(薄膜过滤器)
微生物限度-薄膜过滤法

微生物限度(薄膜过滤法)
1、用到的设备和仪器:
微生物限度仪,一次性过滤杯,无菌滤膜(0.45um,Φ50mm)酒精灯,电子打火消毒喷枪,不锈钢镊子、无菌均质袋(无菌锥形瓶)、不锈钢剪刀、电子天平
2、环境要求:C+A检验前先开紫外灯和空调净化系统半小时。
3、样品外包装在准备室用75%乙醇或0.1%的新洁尔灭溶液浸泡10秒钟,然后通过传递窗传到检测室超净工作台内
4、供试液制备:在超净工作台内,用无菌剪刀打开外包装,根据样品稀释要求,称取适量供试品,加入稀释液。
(一般称取10g样品,加入90ml胰酪大豆胨液体培养基中)
5、过滤:先用消毒枪对过滤头消毒,然后用无菌镊子把无菌滤膜贴这绿色面朝上贴在过滤头上,在把一次性滤杯放在上面,先用稀释液20ml润湿滤膜,取样品1ml 过滤,用适量冲洗液冲洗滤膜。
取下一次性滤杯,用无菌镊子小心取下滤膜,菌面朝上贴在放有胰酪大豆胨琼脂培养基和沙氏葡萄糖琼脂培养基上。
6、培养:培养皿倒置于培养箱内,胰酪大豆胨琼脂培养基,33℃培养5天。
沙氏葡萄糖琼脂培养基,23℃培养7天。
注:1、操作过程中一定要有无菌意识,防止对样品和环境造成污染。
2、此操作没有具体到品种,如果要具体到品种,冲洗量要在符合药典和法规要求的同时通过方法验证来得到。
3、稀释倍数根据样品污染程度进行,次稀释倍数也要经过验证来得到。
06微生物限度检查记录(薄膜过滤法)
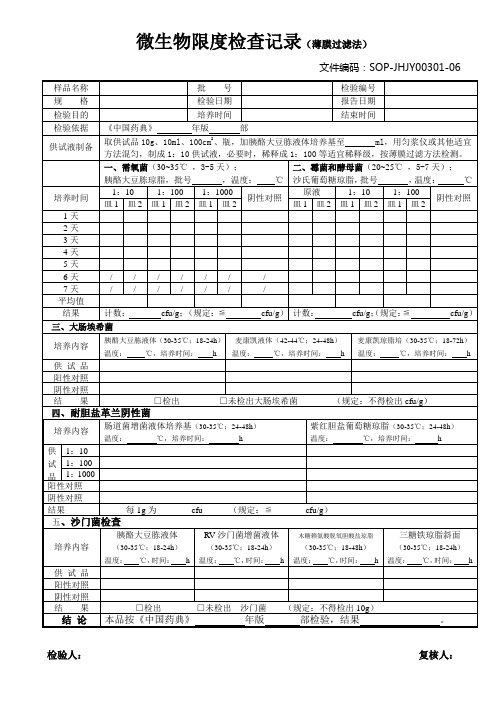
微生物限度检查记录(薄膜过滤法)文件编码:SOP-JHJY00301-06样品名称批号检验编号规格检验日期报告日期检验目的培养时间结束时间检验依据《中国药典》年版部供试液制备取供试品10g、10ml、100cm2、瓶,加胰酪大豆胨液体培养基至 ml,用匀浆仪或其他适宜方法混匀,制成1:10供试液,必要时,稀释成1:100等适宜稀释级,按薄膜过滤方法检测。
一、需氧菌(30~35℃,3-5天);胰酪大豆胨琼脂,批号,温度:℃二、霉菌和酵母菌(20~25℃,5-7天);沙氏葡萄糖琼脂,批号,温度:℃培养时间1:10 1:100 1:1000阴性对照原液1:10 1:100阴性对照皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿21天2天3天4天5天6天/ / / / / / /7天/ / / / / / /平均值结果计数: cfu/g;(规定:≦cfu/g)计数: cfu/g;(规定:≦cfu/g)三、大肠埃希菌培养内容胰酪大豆胨液体(30-35℃;18-24h)温度:℃,培养时间:h麦康凯液体(42-44℃;24-48h)温度:℃,培养时间:h麦康凯琼脂培(30-35℃;18-72h)温度:℃,培养时间:h供试品阳性对照阴性对照结果□检出□未检出大肠埃希菌(规定:不得检出cfu/g)四、耐胆盐革兰阴性菌培养内容肠道菌增菌液体培养基(30-35℃;24-48h)温度:℃,培养时间:h紫红胆盐葡萄糖琼脂(30-35℃;24-48h)温度:℃,培养时间:h供试品1:10 1:100 1:1000阳性对照阴性对照结果每1g为cfu (规定:≦ cfu/g)五、沙门菌检查培养内容胰酪大豆胨液体(30-35℃;18-24h)温度:℃,时间:hRV沙门菌增菌液体(30-35℃;18-24h)温度:℃,时间:h木糖赖氨酸脱氧胆酸盐琼脂(30-35℃;18-48h)温度:℃,时间:h三糖铁琼脂斜面(30-35℃;18-24h)温度:℃,时间:h供试品阳性对照阴性对照结果□检出□未检出沙门菌(规定:不得检出10g)结论本品按《中国药典》年版部检验,结果。
微生物限度检查方法薄膜过滤法验证方案

微生物限度检查方法薄膜过滤法验证方案 Document number【SA80SAB-SAA9SYT-SAATC-SA6UT-SA18】微生物限度检查方法(薄膜过滤法)验证方案微生物限度检查方法(薄膜过滤法) 验证方案编码:表一、验证方案的起草与批准1.验证方案起草起草人:起草时期:年月日2.验证小组成员:3.验证方案审核4.验证方案批准批准人:批准日期:二、验证方案1.验证目的和原理验证目的为确认所采用的方法适合于该药品的细菌、霉菌、酵母菌数的测定,特制定本方案。
验证过程应严格按照本方案规定的内容进行,若因特殊原因确需要变更时,应报验证委员会批准。
原理通过比较试验4组中试验菌的恢复生长结果来评价整个检验方法的准确性、有效性和重现性。
2.验证方法步骤验证前的准备:进行微生物限度检查方法(薄膜过滤法)验证前,所有的平皿和稀释剂都应该严格按照相关的灭菌程序消毒,以确保其对试验的结果没有影响。
试验菌应包括G—、G+、酵母菌和霉菌类微生物以基本覆盖样品中可能存在的微生物。
验证试验的操作计划:用3个不同批号产品微生物限度检测方法进行平行试验,通过计算回收率来判断限度检查方法是否对产品有影响。
试验结果可接受标准:用标准菌株评价方法“”的微生物限度检查对检品中微生物的抑制性,试验结果应显示3次独立的平行试验中,稀释剂对照组的菌回收率应不小于70%,试验组回收率也不低于70%。
3.试验实施试验前的准备3.1.1主要仪器设备:恒温培养箱、生化培养箱、电子天平、高压蒸汽灭菌器、净化工作台。
3.1.2操作环境:操作间应该安装空气除菌过滤层装置。
环境洁净度不应低于10000级,局部洁净度为100级(或放置同等级净化工作台)。
操作间或净化工作台的洁净空气应该保持对环境形成正压,不低于。
3.1.3试验样品:批号:批号:批号:3.1.4培养基:3.1.5稀释液:无菌氯化钠-蛋白胨缓冲液以上经115℃高压蒸汽灭菌30min。
3.1.6验证用微生物名称及其编号实验菌株的来源:编号由菌名首字母—传代代数—制备日期组成。
微生物限度检查方法(薄膜过滤法)验证方案

微生物限度检查方法(薄膜过滤法)验证方案微生物限度检查方法(薄膜过滤法) 验证方案编码:表一、验证方案的起草与批准1.验证方案起草起草人:起草时期:年月日2.验证小组成员:3.验证方案审核4.验证方案批准批准人:批准日期:二、验证方案1.验证目的和原理验证目的为确认所采用的方法适合于该药品的细菌、霉菌、酵母菌数的测定,特制定本方案。
验证过程应严格按照本方案规定的内容进行,若因特殊原因确需要变更时,应报验证委员会批准。
原理通过比较试验4组中试验菌的恢复生长结果来评价整个检验方法的准确性、有效性和重现性。
2.验证方法步骤验证前的准备:进行微生物限度检查方法(薄膜过滤法)验证前,所有的平皿和稀释剂都应该严格按照相关的灭菌程序消毒,以确保其对试验的结果没有影响。
试验菌应包括G—、G+、酵母菌和霉菌类微生物以基本覆盖样品中可能存在的微生物。
验证试验的操作计划:用3个不同批号产品微生物限度检测方法进行平行试验,通过计算回收率来判断限度检查方法是否对产品有影响。
试验结果可接受标准:用标准菌株评价方法“”的微生物限度检查对检品中微生物的抑制性,试验结果应显示3次独立的平行试验中,稀释剂对照组的菌回收率应不小于70%,试验组回收率也不低于70%。
3.试验实施试验前的准备3.1.1主要仪器设备:恒温培养箱、生化培养箱、电子天平、高压蒸汽灭菌器、净化工作台。
3.1.2操作环境:操作间应该安装空气除菌过滤层装置。
环境洁净度不应低于10000级,局部洁净度为100级(或放置同等级净化工作台)。
操作间或净化工作台的洁净空气应该保持对环境形成正压,不低于。
3.1.3试验样品:批号:批号:批号:3.1.4培养基:3.1.5稀释液:无菌氯化钠-蛋白胨缓冲液以上经115℃高压蒸汽灭菌30min。
3.1.6验证用微生物名称及其编号实验菌株的来源:编号由菌名首字母—传代代数—制备日期组成。
3.1.7器具:无菌薄膜过滤器:(孔径直径50mm)、无菌移液管(5ml)4.验证方法菌液的制备将大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌接种至10ml的无菌营养肉汤中在30~35℃下培养18~24小时,将白色念珠菌接种至改良马丁液体培养基中,在23~28℃下培养24~48小时。
微生物限度检查方法(薄膜过滤法)验证方案

微生物限度检查方法(薄膜过滤法)验证方案微生物限度检查方法(薄膜过滤法) 验证方案编码:表一、验证方案的起草与批准1.验证方案起草起草人:起草时期:年月日2.验证小组成员:3.验证方案审核4.验证方案批准批准人:批准日期:二、验证方案1.验证目的和原理1.1验证目的为确认所采用的方法适合于该药品的细菌、霉菌、酵母菌数的测定,特制定本方案。
验证过程应严格按照本方案规定的容进行,若因特殊原因确需要变更时,应报验证委员会批准。
1.2原理通过比较试验4组中试验菌的恢复生长结果来评价整个检验方法的准确性、有效性和重现性。
2.验证方法步骤2.1验证前的准备:进行微生物限度检查方法(薄膜过滤法)验证前,所有的平皿和稀释剂都应该严格按照相关的灭菌程序消毒,以确保其对试验的结果没有影响。
试验菌应包括G—、G+、酵母菌和霉菌类微生物以基本覆盖样品中可能存在的微生物。
2.2验证试验的操作计划:用3个不同批号产品微生物限度检测方法进行平行试验,通过计算回收率来判断限度检查方法是否对产品有影响。
2.3试验结果可接受标准:用标准菌株评价方法“”的微生物限度检查对检品中微生物的抑制性,试验结果应显示3次独立的平行试验中,稀释剂对照组的菌回收率应不小于70%,试验组回收率也不低于70%。
3.试验实施3.1试验前的准备3.1.1主要仪器设备:恒温培养箱、生化培养箱、电子天平、高压蒸汽灭菌器、净化工作台。
3.1.2操作环境:操作间应该安装空气除菌过滤层装置。
环境洁净度不应低于10000级,局部洁净度为100级(或放置同等级净化工作台)。
操作间或净化工作台的洁净空气应该保持对环境形成正压,不低于4.9pa。
3.1.3试验样品:批号:批号:批号:3.1.4培养基:3.1.5稀释液:PH7.0无菌氯化钠-蛋白胨缓冲液以上经115℃高压蒸汽灭菌30min。
3.1.6验证用微生物名称及其编号实验菌株的来源:编号由菌名首字母—传代代数—制备日期组成。
微生物限度过滤系统

微生物限度过滤系统微生物限度过滤系统又叫微生物限度检测装置、微生物限度薄膜过滤器。
一般由1台抽滤泵连接1台由金属制作的过滤支架,支架上可以放入多个抽滤漏斗,支架和抽滤泵中间连接1个真空废液抽吸瓶,整套系统形成真空后,大气压推动滤液通过滤膜。
微生物限度过滤系统对于诸如悬浮固形物检测、微生物检查的用户来说,由于每天或一次需要检测的样品数量多,一次过滤多组样品加强了工作效率。
微生物限度过滤系统将供试品注入微生物限度培养器内,通过检验仪自带内置真空泵负压抽滤,将供试品中微生物截留在滤膜上,用取膜器取出滤膜,转移至配置好的固体培养基上,菌面朝上,平贴。
盖上盖子形成封闭的培养盒,置相应的恒温培养处内培养并计数。
微生物用检验系统,微生物限度过滤系统开放式支架,采用薄膜过滤方法,以负压抽滤的方式,达到细菌截留的目的。
并配有50mm的微孔滤膜与开放式过滤器(3B),降低检验成本,提检验速度。
适用范围:江、河、湖、海、水样食品:纯净水、矿泉水、饮料制药:纯化水、注射用水、原料药、胶囊、生物制品、片剂、口服制剂化工:各种需测试微生物水样化妆品:各种用水及产品微生物限度检查仪适用于纯化水和注射用水的微生物限度检测,也可以用于其他样品的微生物负载检测。
作为微生物限度检测的设备,操作该仪器除了正确的方法以外,还应该注意下列的相关要点:1、添加供试液时的液体高度不能超过滤杯大刻度。
2、随时注意抽滤瓶情况,液体不能淹没进气口。
可以根据实际情况选择抽滤瓶的容积。
3、若无菌室采用化学剂消毒时,将仪器置密封罩内,或搬出无菌室,以免损坏电子部件腐蚀金属部件。
4、环境温度控制在10℃~30℃。
相对湿度≤80%RH无水珠凝结现象。
5、当供试品中含有不溶性的颗粒,悬浮物时,可能导致滤膜堵塞影响过滤,应将供试液进行预处理,出去颗粒或悬浮物。
微生物限度检查薄膜过滤法供试液预处理方法探讨

St dy n u o Di e e Pr t e t n M e ho s f f r nt e r a me t t d o Te tn Li i us d o M e si g qu d e f r mbr ne a Fit r le Pr c - o e du e n r i M i r bi l c o a Li t t c i n mis De e to
t e o c n rt n c a g s o h o to n x e me tl a tr l s l t n e oe a d at r f t t n Re u t c o dn o t e e ut ,h h c n e tai h n e f t e c n rl d e p r n a o a i b ce a o ui s b fr n f l ai . s l A c r i g t h rs l te i o e i r o s s
te h me mbrne—fle r c d e o te ee to o mir b a l t ehod To a i tr p o e ur fr h d tc in f c o il i .M t mi s deem i t ef c o fle me i m o ts by o ai g tr ne he fe t f i tr du n e t c mp rn
A s a t Obe t e T of m w eh r t l a o rt a e t t te t t g l ud c na i a y islbe i p ris i si b n b t c : jc v o c n r h te h ft t n pe e t n o h e i i i o ti n m n nou l m u t s ut l i r i i ei ri r m sn q n g ie ae
微生物限度检测薄膜过滤器的工作原理 薄膜过滤器如何操作

微生物限度检测薄膜过滤器的工作原理薄膜过滤器如何操作微生物限度检查仪(微生物限度过滤系统)接受隔膜泵,不需要抽滤瓶,液体直接通过隔膜泵排出,削减了抽滤瓶使用上的繁琐,避开了连接不好造成抽滤速度慢,不占用操作空间。
微生物限度检查仪是杭州美卓依据药典相关规定设计制造的微生物限度检测专用设备,该产品体积小巧,使用便捷,内置高性能隔膜泵,直接排液,无需抽滤瓶,形成完整的薄膜过滤装置。
检测时将供试液通过薄膜过滤,将供试液内的微生物截留在滤膜上,然后培育形成肉眼可见的菌落并进行计数,以检测供试品内的含菌量。
微生物限度检测仪特别适用于纯化水和注射用水的微生物限度检测,也可以用于其他样品的微生物负载检测。
工作原理接受隔膜液泵负压抽滤原理,在滤杯内的微孔滤膜(使用前灭菌)上下面产生一个压差,滤杯内的受试品由于压差作用通过微孔滤膜。
微孔滤膜具有多而杂的蜂孔结构,即使0.45m以下的微生物亦可被拦截,从而高效地回收微生物,将受试品中可能存在的微生物截留在滤膜上。
0.45m滤膜的孔径利于微生物恢复,且培育基易透过滤膜,利于细菌培育。
微生物限度检验仪的用途不锈钢过滤系统是广泛应用于讨论单位、检验检疫机构、质量监控机构、天然矿泉水行业、饮用水行业、制药行业、制药行业、饮料行业等部门的滤膜法微生物检测、悬浮固形物检测、样品纯化的抽滤设备。
产品特点:内置进口隔膜液泵,效率更高;小巧的机身,削减对操作台面积的占用;过滤杯接受独特的唇形密封设?计,不使用夹钳和O型圈,确保无泄漏操作和均匀的微生物回收率;滤膜预先灭菌,即拆即用,可降低紧要污染物源,提高检测牢靠性;直接抽滤排液,无需抽滤瓶,安装使用便利;不锈钢防水按钮,掌控泵的工作状态,按钮带指示灯,泵开关状态一目了然;过滤头可快速拆装,能单独湿热灭菌;过滤头可以火焰快速灭菌,便利连续试验操作。
??快捷的安装方式、非螺纹结构、非弹簧柱塞结构、无卫生死角薄膜过滤器依照中国药典2023年版之无菌检查法试验要求,参加国际通用标准设计而成,适用于除菌过滤,菌落检查及液体中微粒的测定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
使
用
说
明
书
北京恒奥德仪器仪表有限公司
电话:
网址
【主要特点】
一体化超小型设计,减小了对实验操作空间的占用。
二合一功能,不但是可做微生物限度检查使用,还可当独立真空泵使用,大大节省成本。
可同时抽滤张滤膜,抽滤速度快,工作效率高。
滤杯采用卫生级以上镜面不锈钢制作,经久耐用,耐酸碱,耐高温,易消毒。可重复使用,节省成本,操作方便。
套
附件单元
不锈钢滤网
片
集液瓶
个
产品合格证
份
资料
使用说明书
份
其他:装箱单
以上共计项,是否齐全(是,否)。请验收人签字:。
生产单位:北京恒奥德仪器仪表有限公司
将样品放入微生物限度滤杯内,通过检验仪自带内置真空泵负压抽滤,将样品中微生物截留在滤膜上,用取膜器取出滤膜,转移至配置好的固体培养基上,菌面朝上,平贴。盖上盖子形成封闭的培养盒,置于相应的恒温培养箱内培养并计数。使用时,将带滤头杀菌消毒后直接拧在不锈钢阀门上,将滤膜放在滤头之上,放上密封垫及烧结滤网,将消毒后不锈钢滤杯拧在滤头上,打开不锈钢碟阀,把不锈钢气嘴与集液室及真空动力通过连接管串联。将溶液倒入不锈钢滤杯,打开真空动力,溶剂通过滤头上的滤膜在动力作用下溶液迅速通过过滤支架流入集液室,待滤杯中溶液全部流入集液室,要分析的物质将留在水系滤膜上,只须取下水系滤膜即可。使用后如需消毒杀菌只需将滤杯及滤头一起从阀门上拧下放入高压灭菌器中即可。(用户可选购本单位生产的专用灭菌筒,可直接把滤杯及滤头一起放入灭菌筒内,再把灭菌筒放入高压灭菌器内,避免滤杯及滤头的二次污染。)【使用范围】
每个滤杯都划有刻度,每个刻度,滤杯容量小于
每个滤头采用独立的阀门控制,并且设计为插拔式安装方式,方便操作人员灵活使用。也方便实验人员做消毒杀菌。矚慫润厲钐瘗睞枥庑赖賃軔。
配负压接近,过滤速度极快。
全不锈钢设计,表面镜面处理,方便清洁和杀菌消毒。
【工作原理】
制药:纯化水、注射用水、眼用制剂、原料药、胶囊、生物制品、片剂、口服制剂
化工:各种需测试微生物水样食品:纯净水、矿泉水、饮料,环境监测,卫生防疫,自来水等行业。聞創沟燴鐺險爱氇谴净祸測。
注意:仪器右侧上嘴与集液瓶塞上嘴相连,仪器右侧下嘴与集液瓶塞下嘴相连。
名称
单位
数量
备注
过滤器主机
台
主机单元
滤杯及滤头
