制氢三剂性能及种类
5制氢催化剂的使用

第五章制氢催化剂的性质和使用制氢过程使用的催化剂有如下几种:(1)钴——钼加氢转化脱硫催化剂;(2)脱氯催化剂;(3)氧化锌脱硫剂;(4)烃类——水蒸汽转化催化剂;(5)中温变换催化剂;(6)低温变换催化剂;(7)甲烷化催化剂;(8)吸附剂。
这些催化剂的使用条件非常苛刻,为了使装置实现安稳长满优生产,确保经济、合理、高效的生产目的,必须严格控制原料杂质的浓度,以避免杂质对催化剂的损害。
制氢所使用的原料一般都是轻油,近年一些装置掺用部份炼厂干气制氢,这些制氢原料中通常含有的对制氢催化剂有影响的杂质是硫、氯、有机金属化合物。
硫对含镍的转化催化剂和甲烷化催化剂,对含铜的低温变换催化剂都会造成毒害,一般转化炉入口原料中硫含量要求小于0.5ppm。
硫中毒会使转化炉管产生“热带”,也会促使出口气体甲烷含量增高。
氯离子具有很高的迁移性,可随工艺气流迁移,对下游催化剂及设备造成威胁。
许多合金钢受氯侵蚀后产生应力腐蚀,氯的侵蚀导致许多换热器破裂。
氯会导致转化催化剂失活,对铜系低温变换催化剂的影响更大,氯与铜形成的新物质的熔点很低,易升华又易熔于水,在低变工艺条件下,这些氯化合物可以穿透整个床层。
一般要求原料中含氯应低于5 ppb。
有机金属化合物会沉积在加氢脱硫及转化催化剂表面,导致催化剂活性的永久性衰退,一般要求原料中重金属含量应低于5ppb。
5.1加氢转化催化剂制氢原料中含有不同数量的有机硫和无机硫,这些硫化物的存在,会增加原料气体对设备的腐蚀,尤其重要的是制氢过程所使用的含镍、含铜的催化剂极容易被硫中毒,失去活性,严重影响生产的顺利进行。
但是,有机硫化物性能稳定,不容易被脱除,只有在加氢催化剂的作用下,与氢气反应将有机硫转化生成硫化氢,才能被脱除。
传统加氢转化催剂的主要成份是υ-Al2O3担载的C O O和M O O3,即钴——钼加氢转化催化剂,近年来北京海顺德催化剂有限公司生产的加氢催化剂的载体改用钛的氧化物,这种催化剂也取得一定的实用业绩。
制氢催化剂

制氢催化剂是一种用于促进氢气生成反应的催化剂,它可以提高氢气生成反应的速率和效率。
以下是一些常见的制氢催化剂:
1.铂族金属催化剂:铂族金属催化剂,如铂、钯和铑等,是最常用的制氢催化剂。
它们具有良好的催化活性和稳定性,能够在相对较低的温度下促进氢气生成反应。
2.过渡金属催化剂:一些过渡金属,如镍、钼和钛等,也被广泛应用于制氢催化剂中。
这些过渡金属催化剂在某些反应条件下具有较高的催化活性,同时相对较低的成本。
3.合金催化剂:合金催化剂是由两种或多种金属组成的催化剂,它们通常具有更高的催化活性和稳定性。
常用的合金催化剂包括镍铂合金、铝镍合金等。
4.有机催化剂:有机物催化剂也可以用于制氢反应,例如氨基酸盐、有机聚合物等。
这些有机催化剂通常比无机催化剂更具有选择性和活性。
制氢催化剂的选择取决于制氢反应的条件和要求,如温度、压力、反应物种类和浓度等。
不同的制氢技术和应用领域可能需要不同类型的催化剂。
在实际应用中,需要通过实验和测试来确定最适合的制氢催化剂。
加氢催化剂的分类、功能及选用

其他类型催化剂
金属有机框架(MOF)催化剂
具有多孔性、大比表面积和可调的孔径等特点,为加氢反应提供了更多的可能 性。
碳基催化剂
以碳材料为载体,通过引入活性组分制备的催化剂,在加氢反应中表现出良好 的活性和稳定性。
03 加氢催化剂功能
加速氢气活化与解离
降低氢气活化能
加氢催化剂能够降低氢气分子的活化能,使其更容易解离为氢原子,从而参与加 氢反应。
提高反应速率和选择性
提高反应速率
催化剂能够降低反应的活化能,从而 加快反应速率,提高生产效率。
提高反应选择性
通过选择合适的催化剂,可以使得目 标产物在反应中的选择性得到提高, 减少副产物的生成。
降低反应温度和压力
降低反应温度
催化剂可以降低反应的活化能,从而使得反应在较低的温度下就能进行,有利于节能和 减少副反应。
降低反应压力
某些加氢催化剂能够在较低的压力下促进加氢反应的进行,从而减少设备投资和操作成 本。
04 加氢催化剂选用原则
适应性原则
01
催化剂应与反应物和产物相容, 避免产生副反应或毒化催化剂。
02
催化剂应适应反应条件,如温度 、压力、氢气流速等,以确保催 化活性和选择性。
经济性原则
催化剂应具有较低的成本和较高的活 性,以降低加氢反应的成本。
作用
加氢催化剂在石油化工、有机合 成、精细化工等领域具有广泛的 应用,能够提高产品的收率和质 量,降低生产成本和能源消耗。
发展历程及现状
发展历程
自20世纪初发现加氢催化剂以来,随着科学技术的不断进步和工业生产的不断发展,加氢催化剂的种类和性能得 到了极大的丰富和提升。从最初的简单金属催化剂到后来的复合催化剂、分子筛催化剂等,加氢催化剂的研究和 应用不断取得新的突破。
制氢三剂性能及种类

制氢三剂性能及种类制氢三剂性能及种类制氢过程使用的催化剂有:钴-钼加氢脱硫催化剂、脱氯催化剂、氧化锌脱硫剂、烃类-水蒸汽转化催化剂、中温变换催化剂、低温变换催化剂。
还有PSA吸附剂及磷酸三钠化学助剂。
1.1 钴-钼加氢转化催化剂1.1.1 作用制氢原料中含有不同数量的有机硫和无机硫,这些硫化物的存在,会增加原料气体对设备的腐蚀,尤其重要的是制氢过程所使用的含镍、含铜的催化剂极容易被硫中毒,失去活性,严重影响生产的顺利进行。
但是,有机硫化物性能稳定,不容易被脱除,只有在钴-钼催化剂的作用下,与氢气快速反应生成硫化氢,才能被脱除。
1.1.2 特点钴-钼加氢转化催化剂必须在有氢气存在的条件下,才能将有机硫转化无机硫,否则,将无法起作用。
1.1.3 物理化学特性(T205)外观:灰蓝色条状物几何尺寸:Φ3~3.5×3~10mm堆密度:0.65~0.8kg/L比表面:180~220m2/g1.1.4 化学组成C O O:2~4%M O O3:10~13%载体:TiO2、AL2O31.2 氧化锌脱硫剂(T306)1.2.1 作用氧化锌与硫化氢作用生成难于解离的硫化锌,以此脱除制氢原料气中的硫化氢,一般用于精脱硫过程。
1.2.2 特点氧化锌脱硫剂能脱除无机硫和一些简单的有机硫,硫容较高,能使原料中的硫含量降至0.2~0.02×10-6。
反应温度范围较宽(180~400℃),是一种比较理想的脱硫剂,在较高温度(350~400℃)条件下使用效果更好。
1.2.3 物理化学特性外观:白色条状几何尺寸:Φ5mm×5~10堆密度: 1.16kg/L比表面:45.88m2/g总孔容积:0.28ml/g穿透硫容:>10%1.2.4 化学组成ZnO:≥ 85%1.3 烃类-水蒸汽转化催化剂(Z402、Z405)1.3.1 作用在高温的条件下,烃类和水蒸汽在转化催化剂的作用下,烃类发生裂解,生成甲烷、氢气、一氧化碳和二氧化碳。
制氢技术比较及分析

制氢技术综述&制氢技术路线选择一、工业制氢技术综述1. 工业制氢方案工业制氢方案很多,主要有以下几类:(1)化石燃料制氢:天然气制氢、煤炭制氢等。
(2)富氢气体制氢:合成氨生产尾气制氢、炼油厂回收富氢气体制氢、氯碱厂回收副产氢制氢、焦炉煤气中氢的回收利用等。
(3)甲醇制氢:甲醇分解制氢、甲醇水蒸汽重整制氢、甲醇部分氧化制氢、甲醇转化制氢。
(4)水解制氢:电解水、碱性电解、聚合电解质薄膜电解?、高温电解、光电解、生物光解、热化学水解。
(5)生物质制氢。
(6)生物制氢。
2. 工业制氢方案对比选择(1)煤炭制氢制取过程比天然气制氢复杂,得到的氢气成本也高。
(2)由于生物制氢、生物质制氢和富氢气体制氢等方法制取的氢气杂质含量高、纯度较低,不能达到GT等技术提供商的氢气纯度要求。
(3)国内多晶硅绝大多数都采用的是水电解制氢,只有中能用的是天然气制氢,而国外应用的更多是甲醇制氢,因此,我们重点选择以下三类方案进行对比:(A)天然气制氢(B)甲醇制氢(C)水电解制氢3.(1) 天然气部分氧化制氢因需要大量纯氧增加了昂贵的空分装置投资和制氧成本。
(2) 天然气自热重整制氢由于自热重整反应器中强放热反应和强吸热反应分步进行,因此反应器仍需耐高温的不修锈钢管做反应器,这就使得天然气自热重整反应过程具有装置投资高,生产能力低的特点。
(3) 天然气绝热转化制氢大部分原料反应本质为部分氧化反应。
(4) 天然气高温裂解制氢其关键问题是,所产生的碳能够具有特定的重要用途和广阔的市场前景。
否则,若大量氢所副产的碳不能得到很好应用,必将限制其规模的扩大。
(5)天然气水蒸汽重整制氢,该工艺连续运行,设备紧凑,单系列能力较大,原料费用较低。
因此选用天然气水蒸汽重整制氢进行方案对比。
4. 甲醇制氢(1)甲醇分解制氢,该反应是合成气制甲醇的逆反应,在低温时会产生少量的二甲醚。
(2)甲醇水蒸汽重整制氢,是甲醇制氢法中氢含量最高的反应这种装置已经广泛使用于航空航天、精细化工、制药、小型石化、特种玻璃、特种钢铁等行业。
加氢精制原理及催化剂性能简介

3加氢精制生产装置简介 目前,克拉玛依市石化公司炼油生产单元中,共 有四个联合车间,其中炼油第二联合车间共有生 产装置8套,涵盖了烃类水蒸气制氢、柴油加氢裂 化、汽柴油加氢精制(脱硫)、汽油加氢精制 (脱硫)、润滑油加氢裂化、润滑油临氢降凝 (催化脱蜡)、润滑油加氢精制(脱硫)等八套 主体装置。
硫化升温曲线
350 320 300 250 230 230 290 320 280
温度
℃
200 150 100 50 0 0 3 6 14 22 时间 h 27 30 36 39 150 150
40
4.5 钝化 由于硫化后的催化剂具有很高的活性,直接接 触新鲜原料会造成剧烈反应,严重时引发超温事 故,影响催化剂活性。 钝化方式: 根据装置催化剂的不同一班采用直馏油、加氢 油或注氨钝化。
金属化合物的形式存在,它们在加氢过程中分解后会沉积
在催化剂表面,堵塞催化剂的微孔;As、Pb、Na等与催 化剂活性中心反应,导致催化剂载体结构破坏。另外,石 墨、氧化铝、硫酸铝、硅凝胶等灰分物质,它们堵塞催化 剂孔口、覆盖活性中心,并且当再生温度过高时会与载体
发生固相反应,这些都属于永久性失活。
金属聚集及晶体大小和形态的变化
2 加氢精制催化剂上发生的反应 2.1 加氢精制过程中,主要反应: 加氢脱硫 加氢脱氮 加氢脱氧 加氢脱金属 (包括Ni、V、Fe、Na、Ca、As、Pb、Hg、
Cu等)
烃类加氢饱和 少量烃类分子异构化 少量开环、大分子裂化
2.2 主要反应 2.2.1 加氢脱硫反应 硫化物的存在使油品在燃烧过程中生成二氧化 硫从而造成环境污染。 含硫化合物的加氢反应,在加氢精制条件下石 油馏分中的含硫化合物进行氢解,转化成相应的 烃和H2S,从而硫杂原子被脱掉。几种含硫化合 物的加氢精制反应如下:
制氢材料的研究与开发

制氢材料的研究与开发随着人们对环境污染和气候变化日益关注,发展可再生能源已成为不容忽视的任务。
其中,氢能作为一种清洁能源,因其燃烧产生的唯一排放物是水而备受瞩目。
而实现氢能的产业化需要制备高性能、稳定、经济的制氢材料,这就需要对制氢材料进行深入研究与开发。
一、制氢材料的分类制氢材料主要有金属催化剂、氧化物催化剂以及非催化剂三种类型。
其中,金属催化剂包括铂系、镍系和钯系等;氧化物催化剂主要有过渡金属氧化物、稀土氧化物和贵金属氧化物等;非催化剂则是结构上为膜状或纳米级的材料。
目前,金属催化剂是最常用的制氢材料之一,其性能稳定性高、反应速度快、原料来源广泛。
金属催化剂不仅能催化可再生能源的制氢反应,还可应用于化工、制药、生物学、食品加工等领域。
二、金属催化剂的研究与开发金属催化剂的种类繁多,其中铂系催化剂已被广泛研究,尤其是铂基合金和氧化铂,对其进行改性,可得到更高性能的催化剂。
比如,将铂基合金与金纳米粒子复合,可以有效提高催化剂对甲烷转化为氢气的催化活性和稳定性。
此外,钯系催化剂作为铂系催化剂的替代品也已成为研究热点之一。
钯系催化剂不仅具有与铂系催化剂相似的催化性能,而且显著降低了制氢成本。
例如,钯基合金在不同的工作条件下都表现出良好的催化稳定性和高产氢活性,为其在制氢领域中的广泛应用提供了有力的支持。
三、非催化剂的研究与开发非催化剂由于其稳定性高、废物处理简单等特点,在制氢领域中也越来越受到研究的重视。
例如,通过挑选合适的前驱物和优化制备条件,可制备出具有高活性、高选择性和长时间的烷基碳氢化合物直接脱氢制氢的非催化剂。
近年来,还探索出了多种新型制氢材料,例如边缘化合物和过渡金属铁氮酰化合物等,具有催化活性高、稳定性优、选择性高等特点,已成为未来制氢领域的重要方向。
四、发展前景制氢材料的研究和开发在能源转型、实现绿色能源的机遇和挑战中具有极为重要的意义。
未来的研究方向将不仅注重提高制氢催化剂和非催化剂的制氢效率和稳定性,还要注重研究新型制氢材料及其制备方法。
制氢催化剂
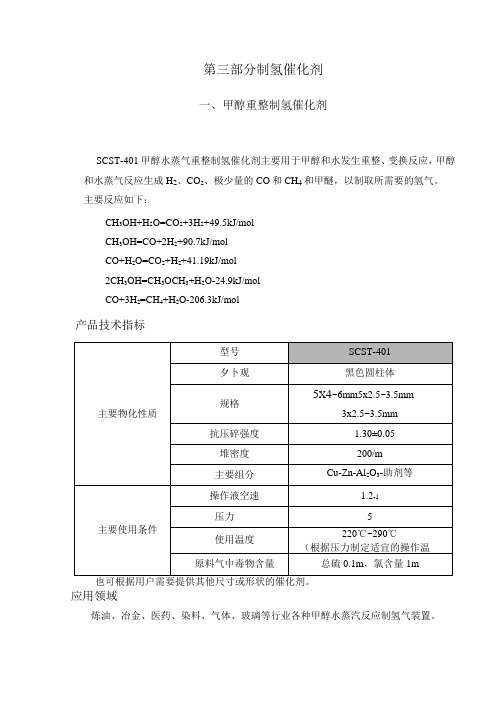
第三部分制氢催化剂一、甲醇重整制氢催化剂SCST-401甲醇水蒸气重整制氢催化剂主要用于甲醇和水发生重整、变换反应,甲醇和水蒸气反应生成H2、CO2、极少量的CO和CH4和甲醚,以制取所需要的氢气。
主要反应如下:CH3OH+H2O=CO2+3H2+49.5kJ/molCH3OH=CO+2H2+90.7kJ/molCO+H2O=CO2+H2+41.19kJ/mol2CH3OH=CH3OCH3+H2O-24.9kJ/molCO+3H2=CH4+H2O-206.3kJ/mol产品技术指标也可根据用户需要提供其他尺寸或形状的催化剂。
应用领域炼油、冶金、医药、染料、气体、玻璃等行业各种甲醇水蒸汽反应制氢气装置。
催化剂特性单程转化率高,水洗塔浓度初期为0,末期小于5%;反应温度低,节约能耗,节约导热油的热量和延长导热油寿命;副反应少,不易结蜡,出口气中甲烷、甲醚、一氧化碳含量更低;强度高,抗水性能好,不易粉化,运行阻力低;较高的活性组分,逐步替代高于山东某公司生产的催化剂。
包装储运催化剂成品用内衬塑料袋的塑料桶或铁桶包装,在运输、储存过程中必须防潮、防火、防倒立和严禁化学污染,搬运时严禁滚动或撞击;露天存放时,底部垫枕木,上面加盖帆布防雨;也可根据用户需要用吨袋包装。
部分使用业绩出口:南亚、中东、欧洲、美洲二、甲醇裂解制氢催化剂SCST-402重整制氢催化剂主要用于甲醇发生裂解或者添加少量水进行重整变换反应,转化为H2、CO2、CO和少量CH4和甲醚,以制取所需要的H2和CO。
主要反应如下:CH3OH+H2O=CO2+3H2+49.5kJ/molCH3OH=CO+2H2+90.7kJ/molCO+H2O=CO2+H2+41.19kJ/mol2CH3OH=CH3OCH3+H2O-24.9kJ/molCO+3H2=CH4+H2O -206.3kJ/mol主要物化性质型号SCST-402r夕卜观黑色圆柱体规格54〜652.5〜3.5mm 抗压碎强度200/m 堆密度 1.30±0.05主要组分Cu-Zn-Al2O3-助剂等主要使用条件操作液空速 1.0-1压力5使用温度220℃~290℃(根据压力制定适宜的操作温度)原料气中毒物含量总硫0.1m,氯含量1m产品技术指标应用领域甲醇直接裂解制氢气、一氧化碳装置;甲醇加部分水蒸汽制氢气、一氧化碳装置。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
制氢三剂性能及种类
制氢过程使用的催化剂有:钴-钼加氢脱硫催化剂、脱氯催化剂、氧化锌脱硫剂、烃类-水蒸汽转化催化剂、中温变换催化剂、低温变换催化剂。
还有PSA吸附剂及磷酸三钠化学助剂。
1.1 钴-钼加氢转化催化剂
1.1.1 作用
制氢原料中含有不同数量的有机硫和无机硫,这些硫化物的存在,会增加原料气体对设备的腐蚀,尤其重要的是制氢过程所使用的含镍、含铜的催化剂极容易被硫中毒,失去活性,严重影响生产的顺利进行。
但是,有机硫化物性能稳定,不容易被脱除,只有在钴-钼催化剂的作用下,与氢气快速反应生成硫化氢,才能被脱除。
1.1.2 特点
钴-钼加氢转化催化剂必须在有氢气存在的条件下,才能将有机硫转化无机硫,否则,将无法起作用。
1.1.3 物理化学特性(T205)
外观:灰蓝色条状物
几何尺寸:Φ3~3.5×3~10mm
堆密度:0.65~0.8kg/L
比表面:180~220m2/g
1.1.4 化学组成
C O O:2~4%
M O O3:10~13%
载体:TiO2、AL2O3
1.2 氧化锌脱硫剂(T306)
1.2.1 作用
氧化锌与硫化氢作用生成难于解离的硫化锌,以此脱除制氢原料气中的硫化氢,一般用于精脱硫过程。
1.2.2 特点
氧化锌脱硫剂能脱除无机硫和一些简单的有机硫,硫容较高,能使原料中的硫含量降至0.2~0.02×10-6。
反应温度范围较宽(180~400℃),是一种比较理想的脱硫剂,在较高温度(350~400℃)条件下使用效果更好。
1.2.3 物理化学特性
外观:白色条状
几何尺寸:Φ5mm×5~10
堆密度: 1.16kg/L
比表面:45.88m2/g
总孔容积:0.28ml/g
穿透硫容:>10%
1.2.4 化学组成
ZnO:≥ 85%
1.3 烃类-水蒸汽转化催化剂(Z402、Z405)
1.3.1 作用
在高温的条件下,烃类和水蒸汽在转化催化剂的作用下,烃类发生裂解,生成甲烷、氢气、一氧化碳和二氧化碳。
1.3.2 特点
Z402催化剂中含有一种带稳定剂的硅酸钾复盐,使催化剂中抗积碳组分钾碱缓慢释放,保证了催化剂较好的抗积碳性和稳定的再生性能。
所以一般Z402催化剂都用于积碳倾向很大的炉管床层上部。
Z405催化剂是一种以镍的活性组分、以铝酸钙为主相的预烧结载体浸渍型催化剂,具有很高的机械强度,热稳定性和活性良好,一般装在炉管的下部。
1.3.3 物理化学特性
(1)Z402的物理性质
外观:瓦灰色环状
几何尺寸:Φ16×6×Φ6
堆密度:0.95~1.20Kg/L
径向破碎强度:25kg/颗
(2)Z402的主要化学组成
NiO:19~23%
K2O:6%
载体:硅铝酸钾复盐
(3)Z405的物理性质
外观:浅灰色环状
几何尺寸:Φ16×16×Φ6
堆密度:0.95~1.05kg/L
径向破碎强度:>45kg/颗
(4)Z405的主要化学组成
NiO:10~12%
K2O:7%
载体:CAX
1.4 中温变换催化剂(B113)
1.4.1 作用
在变换催化剂的作用下,转化气中的一氧化碳与水蒸汽反应,生成二氧化碳和氢气,从而降低转化气中一氧化碳的浓度,达到脱除一氧化碳的目的。
1.4.2 特点
B113型催化剂的突出特点是具有良好的抗沸水和抗蒸汽冷凝性能,在事故状态下,用工艺气干燥处理后,催化剂的强度不减,床层阻力不增加,能保持良好活性。
1.4.3 物理性质
外观:黑褐色圆柱体、碟面圆柱体
几何尺寸:Φ9×5~7mm
径向强度:≥250N/cm
堆密度: 1.35~1.45kg/L
比表面:80~100m2/g
1.4.4 化学组成
Fe2O3:81±2%
Cr2O3:9±2%
S:≤0.02%
Cl:≤0.01%
1.5 低温变换催化剂(B202)
1.5.1 作用
经中变催化剂处理后的转化气,再经过低变催化剂的处理,转化气中的一氧化碳浓度可降至0.2%以下。
1.5.2 特点
(1)B205具有低温活性好,活性区温宽、变换率高、含硫量低及使用强度高等点。
(2)在低温下(小于200℃),有水蒸汽存在时,会使催化剂的强度和活性下降,因此,操作温度必须高于系统气体的露点。
(3)在还原中,耗H2量小,热效应显著,容易使催化剂床层超温,烧坏催化剂。
(4)对硫含量要求甚严,一般要求<1×10-6,为了防止硫中毒,一般要在催化剂床层上部装一些氧化锌脱硫剂。
1.5.3 物理性质
外观:黑色圆柱体、碟面圆柱体
几何尺寸:Φ6×4~6mm
堆密度: 1.05×1.15%
径向强度:≥250N/cm
比表面:60~80m2/g
1.5.4 化学组成
CuO:32~35%
ZnO:45~48%
AL2O3:7~8%
1.6 脱氯催化剂(T402)
1.6.1 作用
氯化物对转化及低温变换催化剂是一种毒物,对低温变换这类铜基催化剂尤其敏感,其易与活性相金属铜相结合形成低熔点化合物而导致活性相熔结,100~300PPm的氯化物可使低温变换催化剂活性在400小时内下降20~40%。
为了减少原料对转化及低变催化剂的毒害,保护转化及低变催化剂,减少下游设备氯离子应力腐蚀的可能。
利用脱氯剂吸收原料经过加氢生成的HCl,从而达到脱氯的目的。
1.6.2 物理化学特性(T402)
外观:白色球状
几何尺寸:Φ3~4mm
堆密度:0.9~1.0kg/L
比表面:40m2/g。
