2015版药典检测方法分类
2015版中国药典四部微生物限度

2015版中国药典四部微生物限度中国药典是我国医药行业的重要规范,其中微生物限度是其中一个关键内容。
微生物限度是指药品中允许存在的微生物数量的上限。
它对药品的质量和安全性提出了严格要求。
2015版中国药典中明确了药品微生物限度的标准和方法,以保障药品的质量和使用的安全性。
一、微生物限度的定义和意义微生物限度是指在药品中存在的微生物数量的上限。
它是衡量药品质量和安全性的重要指标之一。
由于微生物对人体健康有潜在的危害,药品中过多的微生物污染可能导致药品的变质和降解,甚至引起严重的药品安全问题。
因此,微生物限度的控制是确保药品质量和安全性的关键步骤之一。
二、微生物的限度标准和分类微生物限度的标准和分类在2015版中国药典中得到了详细说明。
根据药品的特性和用途不同,微生物限度标准和分类也有所差异。
常见的微生物限度分类包括细菌总数、大肠菌群、霉菌和酵母菌等。
各类微生物的限度标准和方法在药典中都有详细描述,以确保药品的质量和安全性。
三、微生物限度的检测方法为了准确检测微生物限度,2015版中国药典提供了一系列的微生物检测方法。
常见的方法包括菌落总数的测定、大肠菌群的测定、霉菌和酵母菌的测定等。
这些方法要求检测人员具备专业的技术和操作能力,确保检测结果的准确性和可靠性。
四、微生物限度的控制措施为了保证药品的质量和安全性,生产企业需要采取一系列的控制措施来控制微生物限度。
这些措施包括原料和辅料的检验、生产环境的控制、生产工艺的严格执行和产品的质量控制等。
通过全面有效的控制措施,企业可以确保药品的微生物限度在合理的范围内,从而保证药品的质量和安全性。
五、微生物限度的意义和前景微生物限度的控制是保障药品质量和安全性的重要手段,它直接影响着人们的生命健康。
随着人们对药品质量和安全性的要求越来越高,对微生物限度的控制也越来越严格。
中国药典不断完善微生物限度标准和方法,为药品生产和使用提供了规范和指导。
未来,微生物限度的研究和控制将成为药品质量控制的重要方向。
药典三部(2015版)-通则-0832水分测定法

0832 水分测定法第一法(费休氏法)1. 容量滴定法本法是根据碘和二氧化硫在吡啶和甲醇溶液中与水定量反应的原理来测定水分。
所用仪器应干燥,并能避免空气中水分的侵入;测定应在干燥处进行。
费休氏试液的制备与标定(1)制备称取碘(置硫酸干燥器内48小时以上)110g,置干燥的具塞锥形瓶(或烧瓶)中,加无水吡啶160ml,注意冷却,振摇至碘全部溶解,加无水甲醇300ml,称定重量,将锥形瓶(或烧瓶)置冰浴中冷却,在避免空气中水分侵入的条件下,通入干燥的二氧化硫至重量增加72g,再加无水甲醇使成1000ml,密塞,摇匀,在暗处放置24小时。
也可以使用稳定的市售费休氏试液。
市售的费休氏试液可以是不含吡啶的其他碱化试剂,或不含甲醇的其他伯醇类等制成;也可以是单一的溶液或由两种溶液临用前混合而成。
本试液应遮光,密封,阴凉干燥处保存。
临用前应标定滴定度。
(2)标定精密称取纯化水10~30mg,用水分测定仪直接标定;或精密称取纯化水10~30mg,置干燥的具塞锥形瓶中,除另有规定外,加无水甲醇适量,在避免空气中水分侵入的条件下,用费休氏试液滴定至溶液由浅黄色变为红棕色,或用电化学方法[如永停滴定法(通则0701)等]指示终点;另做空白试验,按下式计算:F=WA−B式中F为每1ml费休氏试液相当于水的重量,mg;W为称取纯化水的重量,mg;A为滴定所消耗费休氏试液的容积,ml;B为空白所消耗费休氏试液的容积,ml。
测定法精密称取供试品适量(约消耗费休氏试液1~5ml),除另有规定外,溶剂为无水甲醇,用水分测定仪直接测定。
或精密称取供试品适量,置干燥的具塞锥形瓶中,加溶剂适量,在不断振摇(或搅拌)下用费休氏试液滴定至溶液由浅黄色变为红棕色,或用永停滴定法(通则0701)指示终点;另做空白试验,按下式计算:×100%供试品中水分含量(%)=(A−B)FW式中A为供试品所消耗费休氏试液的体积,ml;B为空白所消耗费休氏试液的体积,ml;F为每1ml费休氏试液相当于水的重量,mg;W为供试品的重量,mg。
药典三部(2015版)-通则-外源病毒因子检查法

3302 外源病毒因子检查法病毒类制品在毒种选育和生产过程中,经常使用动物或细胞基质培养,因此,有可能造成外源因子的污染。
为了保证制品质量,需要对毒种和对照细胞进行外源病毒因子的检测。
对病毒主种子批或工作种子批,应抽取足够检测试验需要量的供试品进行外源病毒因子检测。
根据病毒的特性,有些检测需要在试验前中和病毒。
病毒中和时尽可能不稀释,但当中和抗体不能有效中和病毒而需要进行稀释病毒时,应选择可被中和的最大病毒量,但至少不得超过生产接种时毒种的稀释倍数。
进行病毒中和时,应采用非人源和非猴源(特殊情况除外)的特异性抗体中和本病毒,为降低样品中外源病毒被中和的可能性,最好采用单克隆抗体,中和过程不应干扰外源病毒的检测。
制备抗血清(或单克隆抗体)所用的免疫原应采用与生产疫苗(或制品)不同种而且无外源因子污染的细胞(或动物)制备。
如果病毒曾在禽类组织或细胞中繁殖过,则抗体不能用禽类来制备。
若用鸡胚,应来自SPF 鸡群。
病毒种子批外源因子检查⒈动物试验法⑴小鼠试验法取15~20g小鼠至少10只,取病毒种子批或经抗血清中和后的病毒悬液,每只脑内接种0.03ml,同时腹腔接种0.5ml,至少观察21天。
解剖每只在试验24小时后死亡或有患病体征的小鼠,直接肉眼观察其病理改变,并将有病变的相应的组织制成悬液通过脑内和腹腔接种另外至少5只小鼠,并观察21天。
接种24小时内小鼠死亡超过20%,试验无效。
在观察期内最初接种的乳鼠以及每个盲传组的小鼠至少有80%健存,且小鼠未出现与待测毒种无关的可传播性因子或其他病毒感染,为符合要求。
⑵乳鼠试验法取出生24小时内的乳鼠至少10只,取病毒种子批或经抗血清中和后的病毒悬液,脑内接种0.01ml,同时腹腔接种至少0.1ml。
每天观察至少14天。
解剖每只在试验24小时后死亡或有患病体征的乳鼠,直接肉眼观察其病理改变,并取有病变的相应的组织和脑、脾制备成悬液通过脑内和腹腔接种另外至少5只乳鼠,并每天观察至接种后14天。
15版药典含量均匀度检查法
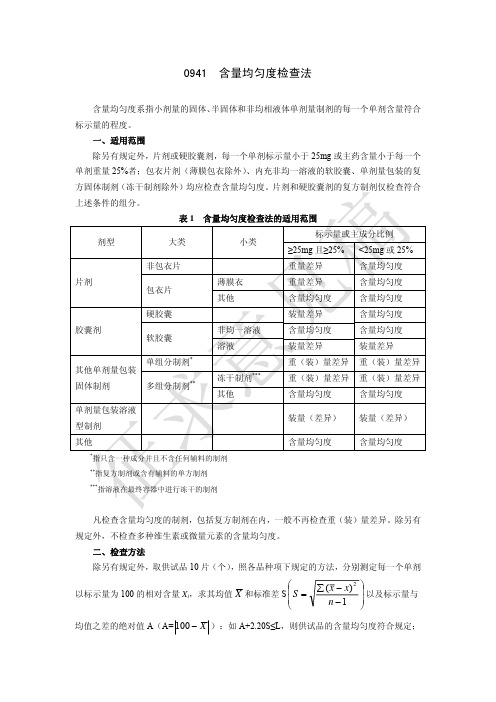
0941含量均匀度检查法含量均匀度系指小剂量的固体、 半固体和非均相液体单剂量制剂的每一个单剂含量符合 标示量的程度。
一、适用范围 除另有规定外,片剂或硬胶囊剂,每一个单剂标示量小于 25mg 或主药含量小于每一个 单剂重量 25%者;包衣片剂(薄膜包衣除外) 、内充非均一溶液的软胶囊、单剂量包装的复 方固体制剂(冻干制剂除外)均应检查含量均匀度。
片剂和硬胶囊剂的复方制剂仅检查符合 上述条件的组分。
表1 剂型 大类 非包衣片 片剂 包衣片 硬胶囊 胶囊剂 软胶囊 单组分制剂* 多组分制剂** 冻干制剂*** 其他 非均一溶液 溶液 薄膜衣 其他 含量均匀度检查法的适用范围 小类 标示量或主成分比例 ≥25mg 且≥25% 重量差异 重量差异 含量均匀度 装量差异 含量均匀度 装量差异 重(装)量差异 重(装)量差异 含量均匀度 装量(差异) 含量均匀度指只含一种成分并且不含任何辅料的制剂 指复方制剂或含有辅料的单方制剂 指溶液在最终容器中进行冻干的制剂<25mg 或 25% 含量均匀度 含量均匀度 含量均匀度 含量均匀度 含量均匀度 装量差异 重(装)量差异 重(装)量差异 含量均匀度 装量(差异) 含量均匀度其他单剂量包装 固体制剂 单剂量包装溶液 型制剂 其他******凡检查含量均匀度的制剂,包括复方制剂在内,一般不再检查重(装)量差异。
除另有 规定外,不检查多种维生素或微量元素的含量均匀度。
二、检查方法 除另有规定外,取供试品 10 片(个) ,照各品种项下规定的方法,分别测定每一个单剂⎛ 以标示量为 100 的相对含量 Xi,求其均值 X 和标准差 S ⎜ S = ⎜ ⎝∑ ( x − x) n −12⎞ ⎟ 以及标示量与 ⎟ ⎠均值之差的绝对值 A(A= 100 − X ):如 A+2.20S≤L,则供试品的含量均匀度符合规定;若 A+S>L,则不符合规定;若 A+2.20S>L,且 A+S≤L,则应另取 20 片(个)复试。
通则2321 铅镉砷汞铜测定法 中华人民共和国药典2015年版四部

2321 铅、镉、砷、汞、铜测定法一、原子吸收分光光度法本法系采用原子吸收分光光度法测定中药中的铅、镉、砷、汞、铜,所用仪器应符合使用要求(通则0406)。
除另有规定外,按下列方法测定。
1.铅的测定(石墨炉法)测定条件参考条件:波长283. 3nm,干燥温度100~120 ℃,持续20秒;灰化温度400~750℃,持续20~25秒;原子化温度1700~2100℃,持续4~5秒。
银标准贮备液的制备精密量取铅单元素标准溶液适量,用2%硝酸溶液稀释,制成每lml含铅(Pb)lug 的溶液,即得(0~5℃贮存)。
标准曲线的制备分别精密量取铅标准贮备液适量,用2%硝酸溶液制成每lml分别含铅0ng、5ng、20ng、40ng、60ng、80ng的溶液。
分别精密量取lml,精密加含1%磷酸二氢铵和0.2%硝酸镁的溶液0 .5 ml,混匀,精密吸取20ul注人石墨炉原子化器,测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准曲线。
供试品溶液的制备A法取供试品粗粉0.5g,精密称定,置聚四氯乙烯消解罐内,加硝酸3~5ml,混匀,浸泡过夜,盖好内盖,旋紧外套,置适宜的微波消解炉内,进行消解(按仪器规定的消解程序操作)。
消解完余后,取消解内罐置电热板上缓缓加热至红棕色蒸气挥尽,并继续缓缓浓缩至2~3ml,放冷,用水转入25ml量瓶中,并稀释至刻度,摇勻,即得。
同法同时制备试剂空白溶液。
B法取供试品粗粉1g , 精密称定,置凯氏烧瓶中,加硝酸-高氣酸(4:1 )混合溶液5~10ml,混勻,瓶口加一小漏斗,浸泡过夜。
置电热板上加热消解,保持微沸,若变棕黑色,再加硝酸-髙氣酸(4:1)混合溶液适量,持续加热至溶液澄明后升高温度,继续加热至冒浓烟,直至白烟散尽,消解液呈无色透明或略带黄色,放冷,转入50ml量瓶中,用2%硝酸溶液洗涤容器,洗液合并于量瓶中,并稀释至刻度,摇匀,即得。
同法同时制备试剂空白溶液。
C法取供试品粗粉0 .5g,精密称定,置瓷坩埚中,于电热板上先低温炭化至无烟,移人高温炉中,于500℃灰化5~6小时(若个别灰化不完全,加硝酸适童,于电热板上低温加热,反复多次直至灰化完全),取出冷却,加10%硝酸溶液5ml使溶解,转人25ml量瓶中,用水洗涤容器,洗液合并于量瓶中,并稀释至刻度,摇匀,即得。
2015版中国药典微生物限度

1.4.2供试品检查
• 供试液制备
– ⑵ 水不溶性非油脂类供试品
• 取供试品, 用 pH7.0 无菌氯化钠-蛋白胨 缓冲液,或 pH7.2 磷酸盐缓冲液,或胰酪 大豆胨液体培养基制备成 1:10 供试液。 分散力较差的供试品,可在稀释液中加入 表面活性剂如 0.1%的聚山梨酯 80,使供 试品分散均匀。若需要,调节供试液 pH 值至 6~8。必要时,用同一稀释液将供 试液进一步 10倍系列稀释。
1.3.3计数方法适用性试验
1. 供试液制备 2. 接种和稀释 3. 抗菌活性的去除与灭活 4. 供试品中微生物的回收
– 平皿法 – 薄膜过滤法 – 最可能数法(MPN 法)
5. 结果判断
1.4 供试品检查
• 1.4.1检验量
– 检验量即一次试验所用的供试品量(g、ml
或cm²)。
– 除另有规定外,一般供试品的检验量为10g 或
• 需氧菌总数是指胰酪大豆胨琼脂培养基上生长的 总菌落数(包括真菌菌落数);
• 霉菌和酵母菌总数是指沙氏葡萄糖琼脂培养基上 生长的总菌落数(包括细菌菌落数)。
• 若因沙氏葡萄糖琼脂培养基上生长的细菌使霉菌 和酵母菌的计数结果不符合微生物限度要求,可 使用含抗生素(如氯霉素、庆大霉素)的沙氏葡 萄糖琼脂培养基或其他选择性培养基(如玫瑰红 钠琼脂培养基)进行霉菌和酵母菌总数测定。
1.4.2供试品检查
• 供试液制备
– ⑷需用特殊方法制备供试液的供试品
• 膜剂供试品 • 肠溶及结肠溶制剂供试品 • 气雾剂、喷雾剂供试品 • 贴膏剂供试品
1.4.2供试品检查
1. 平皿法
– 平皿法包括倾注法和涂布法。 – 除另有规定外,取规定量供试品,按方法适用性
试验确认的方法进行供试液制备和菌数测定,每 稀释级每种培养基至少制备2个平皿。 – 培养和计数 除另有规定外,胰酪大豆胨琼脂培养 基平板在30~35℃培养3~5天,沙氏葡萄糖琼脂 培养基平板在20~25℃培养5 ~7天, 观察菌落 生长情况,点计平板上生长的所有菌落数,必要时 可适当延长培养时间至7 天进行菌落计数并报告 。菌落蔓延生长成片的平皿不宜计数。点计菌落 数后,计算各稀释级供试液的平均菌落数,按菌 数报告规则报告菌数。 – 若同稀释级两个平皿的菌落数平均值不小于15, 则两个平皿的菌落数不能相差1 倍或以上。
药典三部(2015版)-通则-细菌内毒素检查法

1143 细菌内毒素检查法本法系利用鲎试剂来检测或量化由革兰阴性菌产生的细菌内毒素,以判断供试品中细菌内毒素的限量是否符合规定的一种方法。
细菌内毒素检查包括两种方法,即凝胶法和光度测定法,后者包括浊度法和显色基质法。
供试品检测时,可使用其中任何一种方法进行试验。
当测定结果有争议时,除另有规定外,以凝胶限度试验结果为准。
本试验操作过程应防止内毒素的污染。
细菌内毒素的量用内毒素单位(EU)表示,1EU与1个内毒素国际单位(IU)相当。
细菌内毒素国家标准品系自大肠埃希菌提取精制而成,用于标定、复核、仲裁鲎试剂灵敏度、标定细菌内毒素工作标准品的效价,干扰试验及检查法中编号B和C溶液的制备、凝胶法中鲎试剂灵敏度复核试验、光度测定法中标准曲线可靠性试验。
细菌内毒素工作标准品系以细菌内毒素国家标准品为基准标定其效价,用于干扰试验及检查法中编号B和C溶液的制备、凝胶法中鲎试剂灵敏度复核试验、光度测定法中标准曲线可靠性试验。
细菌内毒素检查用水应符合灭菌注射用水标准,其内毒素含量小于0.015EU/ml(用于凝胶法)或0.005EU/ml(用于光度测定法),且对内毒素试验无干扰作用。
试验所用的器皿需经处理,以去除可能存在的外源性内毒素。
耐热器皿常用干热灭菌法(250℃、30分钟以上)去除,也可采用其他确证不干扰细菌内毒素检查的适宜方法。
若使用塑料器皿,如微孔板和与微量加样器配套的吸头等,应选用标明无内毒素并且对试验无干扰的器具。
供试品溶液的制备某些供试品需进行复溶、稀释或在水性溶液中浸提制成供试品溶液。
必要时,可调节被测溶液(或其稀释液)的pH值,一般供试品溶液和鲎试剂混合后溶液的pH值在6.0~8.0的范围内为宜,可使用适宜的酸、碱溶液或缓冲溶液调节pH值。
酸或碱溶液须用细菌内毒素检查用水在已去除内毒素的容器中配制。
缓冲液必须经过验证不含内毒素和干扰因子。
内毒素限值的确定药品、生物制品的细菌内毒素限值(L)一般按以下公L=K/M式中L为供试品的细菌内毒素限值,一般以EU/ml、EU/mg或EU/U(活性单位)表示;K为人每千克体重每小时最大可接受的内毒素剂量,以EU/(kg·h)表示,注射剂K=5 EU/(kg·h),放射性药品注射剂K=2.5 EU/(kg·h),鞘内用注射剂K=0.2 EU/(kg·h);M为人用每千克体重每小时的最大供试品剂量,以ml/(kg·h)、mg/(kg·h)或U/(kg·h)表示,人均体重按60kg计算,人体表面积按1.62㎡计算。
药典三部(2015版)-通则-0832水分测定法

0832 水分测定法第一法(费休氏法)1. 容量滴定法本法是根据碘和二氧化硫在吡啶和甲醇溶液中与水定量反应的原理来测定水分。
所用仪器应干燥,并能避免空气中水分的侵入;测定应在干燥处进行。
费休氏试液的制备与标定(1)制备称取碘(置硫酸干燥器内48小时以上)110g,置干燥的具塞锥形瓶(或烧瓶)中,加无水吡啶160ml,注意冷却,振摇至碘全部溶解,加无水甲醇300ml,称定重量,将锥形瓶(或烧瓶)置冰浴中冷却,在避免空气中水分侵入的条件下,通入干燥的二氧化硫至重量增加72g,再加无水甲醇使成1000ml,密塞,摇匀,在暗处放置24小时。
也可以使用稳定的市售费休氏试液。
市售的费休氏试液可以是不含吡啶的其他碱化试剂,或不含甲醇的其他伯醇类等制成;也可以是单一的溶液或由两种溶液临用前混合而成。
本试液应遮光,密封,阴凉干燥处保存。
临用前应标定滴定度。
(2)标定精密称取纯化水10~30mg,用水分测定仪直接标定;或精密称取纯化水10~30mg,置干燥的具塞锥形瓶中,除另有规定外,加无水甲醇适量,在避免空气中水分侵入的条件下,用费休氏试液滴定至溶液由浅黄色变为红棕色,或用电化学方法[如永停滴定法(通则0701)等]指示终点;另做空白试验,按下式计算:F=WA−B式中F为每1ml费休氏试液相当于水的重量,mg;W为称取纯化水的重量,mg;A为滴定所消耗费休氏试液的容积,ml;B为空白所消耗费休氏试液的容积,ml。
测定法精密称取供试品适量(约消耗费休氏试液1~5ml),除另有规定外,溶剂为无水甲醇,用水分测定仪直接测定。
或精密称取供试品适量,置干燥的具塞锥形瓶中,加溶剂适量,在不断振摇(或搅拌)下用费休氏试液滴定至溶液由浅黄色变为红棕色,或用永停滴定法(通则0701)指示终点;另做空白试验,按下式计算:×100%供试品中水分含量(%)=(A−B)FW式中A为供试品所消耗费休氏试液的体积,ml;B为空白所消耗费休氏试液的体积,ml;F为每1ml费休氏试液相当于水的重量,mg;W为供试品的重量,mg。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
紫外可见分光光度计品种 八角茴香 人工牛黄 山楂叶 川贝母 天南星 玉竹 平贝母 冬葵果 半枝莲 西红花 华山参 红花 麦冬 体外培育牛黄 沙棘 灵芝 阿魏 昆布 金樱子 枸杞子 香加皮 莪术 铁皮石斛 海藻 黄精 银柴胡 淫羊藿 紫草 槐花 雷丸 罂粟壳 地榆
药典有害重金属 山楂 水蛭 丹参 甘草 白芍 西洋参 牡蛎 阿胶 昆布 金银花 珍珠 枸杞子 海螵蛸 海藻 黄芪 蛤壳 蜂胶
药典气相品种 丁香 八角茴香 土木香 千年健 广藿香 小茴香 天然冰片 艾片 艾叶 石斛 亚麻子 豆蔻 乳香 冰片(合成龙脑) 油松节 砂仁 鸦胆子 香薷 麝香
药典蒸散品种 山银花 酸枣仁 马鞭草 巴戟天 四季青 爪子金 地肤子 伊贝母 知母 急性子 桔梗 益母草 浙贝母 通关藤 黄芪 银杏叶 商陆 湖北贝母 路路通 薏苡仁
吕景辉整理
药典黄曲霉品种 大枣 水蛭 地龙 肉豆蔻 全蝎 决明子 麦芽 远志 陈皮 使君子 柏子仁 胖大海 莲子 桃仁 蜈蚣 槟榔 酸枣仁 僵蚕 薏苡仁
药典梯度品种 人参 三七 大豆黄卷 山茱萸 山银花 川牛膝 川乌 制川乌 王不留行 天仙藤 车前子 丹参 乌药 水红花子 功劳木 甘草 北刘寄奴 四季青 生姜 玄参 西洋参 肉苁蓉 决明子 关黄柏 红参 巫山淫羊藿 两头尖 两面针 阿胶 附子 金银花 卷柏 细辛 草乌 制草乌 草豆蔻 重楼 独一味 急性子 柴胡 鹿角胶 淫羊藿 蜂胶 酸枣仁 豨苋草 墨旱莲 羌活 沉香 龟甲胶
