7.1合金的相结构全解
材料科学与材料世界第7章金属和合金的凝固

7.1纯金属的凝固 7.1.1液态金属的结构 7.1.2纯金属的凝固过程 7.1.3凝固的热力学条件 7.1.4晶核的形成 7.1.5晶核的长大 7.2合金的凝固
7.2.1平衡分配系数 7.2.2平衡凝固 7.2.3非平衡凝固
7.2.4固溶体合金凝固时溶质的再分配 7.2.5合金凝固中的成分过冷 7.3铸锭的组织与缺陷 7.3.1铸锭三晶区 7.3.2铸锭的缺陷
材料科学基础
第七章
● r> rk时,晶胚的生长导致系统自由能的降低,晶胚自动长大。 该晶胚可以成为晶核。 该临界尺寸rk称为晶核的 临界半径, 该晶核称为 临界晶核
● r> rk时,晶胚的生长导致系统自由能升高,晶胚自动消失。
由:dΔG/dr = 0,得晶核的临界半径:
形核率:
材料科学基础
第七章
材料科学基础
第七章
下图所示为液态纯金属在缓慢冷却过程中温度-时间关系曲线,即 冷却曲线。由图可见,液态金属在理论凝固温度Tm(金属的熔点) 处,并未开始凝固。只有冷却至Tm温度以下某个温度(Tn)才开 始凝固。通常将这种实际开始凝固温度低于理论开始凝固温度的 现象称为“过冷”,并把理论凝固温度Tm与实际凝固温度Tn之差 ΔT称为过冷度(ΔT=Tm-Tn)。
液态金属中局部规则排列微区和随机高致密区都是很不稳定 的,它们大小不一,处于时聚时散,此起彼伏的状态。这种很 不稳定的现象称为“结构起伏”或“相起伏”。均匀的液态金 属凝固过程中结晶的核心就是在结构起伏的基础上形成的,故 这些结构起伏又称为“晶胚”。
7.1.2纯金属的凝固过程
材料科学基础
第七章
液态金属的凝固过程包括晶核形成和晶核长大两个过程 。
合金相结构PPT课件

二、固溶体
➢ 纯铜的σb 为220MPa, 硬度为40HBS, 断面收 缩率ψ为70%。当加入1%镍形成单相固溶体
后, 强度升高到390MPa, 硬度升高到70HB, 而 断面收缩率仍有50%。所以固溶体的综合机械 性能很好, 常常作为结构合金的基体相。 ➢ 固溶体与纯金属相比, 物理性能有较大的变化, 如电阻率上升, 导电率下降, 磁矫顽力增大。
合金的相结构
1
一、基本概念
1 合金 (1)合金:两种或两种以上的金属,或金属与
非金属经一定方法合成的具有金属特性的物质。 (2)组元:组成合金最基本的物质。(如一元、
二元、三元合金〕,可以是元素,也可以是化合 物。
(3)合金系:给定合金以不同的比例而合成的 一系列不同成分合金的总称。如Fe-C,Fe-Cr等。
2
一、基本概念
2相 (1)相:材料中结构相同、成分和性能均一的组成部分。 (2)组织:由不同形态、大小、数量和分布的相组成的综合体。 如单相、两相、多相合金。金属及合金的组织一般应
用显微镜才能看到,所以常称显微组织。
3
一、基本概念
(2)相的分类 合金中的相按结构可分为固溶体和金属化合物。 固溶体:晶体结构与其某一组元相同的相。 金属化合物(中间相):组成原子有固定比例, 其结构与组成组元均不相同的相。
5
二、固溶体
2、分类 ➢ 按溶质原子在溶剂晶格中的位置, 固溶体可
分为置换固溶体与间隙固溶体两种。 ➢ 按溶质原子在溶剂中的溶解度,固溶体可分为
有限固溶体和无限固溶体两种。 ➢ 按溶质原子在固溶体中分布是否有规律,固溶
体分无序固溶体和有序固溶体两种。 在一定条件(如成分、温度等)下,一些合金的 无序固溶体可转变为有序固溶体。这种转变叫 做有序化。
包晶相图和铁碳合金解读
小结
• 非恒温转变类型
匀晶转变
L
L α
稳定化合物
L Am Bn
L Am Bn
L
L AmBn
非稳定化合物
α AmBn
• 恒温转变类型
分解型 共晶转变 共析转变 偏晶转变 熔晶转变
L
α
L β
L1 L2
α
γ β
L1 L2
δ
L
γ
F % ≈ 1 – 12 % = 88 %
珠光体
强度较高,塑性、韧性和硬度介于 Fe3C 和 F 之间。
(3)亚共析钢 ( C % = 0.4 % )结晶过程
各组织组成物的相对量:
P % = ( 0.4 – 0.0218 ) / ( 0.77 – 0.0218 ) ≈ 51 % F % ≈ 1 – 51 % = 49 %
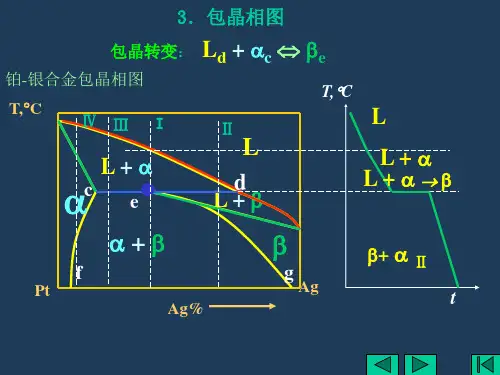
碰到db发生包晶反应: Lb+αd =βp 为恒温反应 结晶过程: L→L+α→L+α+β→α+β →α+β+αⅡ+ βⅡ 匀晶反应+包晶反应+脱溶 转变 室温组织: α+ β+αⅡ+ βⅡ
碰到pb发生包晶反应 : Lb+αD=βP 为恒温反应 结晶过程: L→L+α→L+α+β→L+β →β→αⅡ+ β 匀晶反 应+包晶反应+匀晶反应 +脱溶转变 室温组织:αⅡ+ β
2.
合金的工艺性能与相图的关系
● 铸造性能
液固相线距离愈小,结晶温度范围愈小(如接 近共晶成分的合金),则流动性好,不易形成分散 缩孔。
● 锻造、轧制性能
单相固溶体合金, 变形抗力小,变形均匀, 不易开裂。
7-铁合金生产要点

7 铁合金生产铁合金是指一种或一种以上的金属或非金属元素与铁组成的合金,它主要用作炼钢的脱氧剂和合金元素的添加剂。
例如锰铁是锰与铁的合金,硅铁是硅与铁的合金,硅钙合金是硅与钙组成的合金。
钢铁工业中习惯上把炼钢用的中间合金(不论含铁与否),都叫做铁合金。
由于铁合金的生产工艺比纯金属的制取过程简单,而且又具有比纯金属熔点低、体密大(指体密小的金属如钛、硼等)的优点,有利于炼钢过程中脱氧和合金化的进行。
因此,炼钢脱氧和添加合金元素多以铁合金形式加入。
7.1 铁合金生产概述7.1.1 铁合金的用途(1)用作脱氧剂。
炼钢是用氧化方法去除铁液中的碳、磷等杂质。
在完成这些氧化的任务后,同时钢液中也吸收了氧,如果这些氧存在在钢中就会大大地降低钢的性能。
因此需要添加一些与氧结合力比较强,且其脱氧产物又能顺利从钢液中排除,从而使钢液中的氧含量降低的元素。
这个过程叫做钢的脱氧。
用于脱氧的元素或合金叫做脱氧剂。
常用的脱氧剂有锰、硅、铝等。
这些元素多以铁合金Fe-Mn、Fe-Si和Al等形式加入钢液中。
元素与氧的结合能力越强,在钢中含氧量愈高,其脱氧效果也就越好。
(2)用作合金剂。
合金元素不但能降低钢中杂质的含量.而且还能调整钢的化学成分。
用于调整钢的化学成分使钢合金化的元素或合金叫做合金剂,常用的合金元素有硅、锰、铬、钼、钒、钛、钨、钴、硼、铌等。
不同的合金元素和不同的合金元素含量的钢钟具有不同的特性和用途。
铁合金的产量、品种和质量,直接影响着钢铁工业的发展,其用量一般占钢产量的2%~3%左右。
(3)用于铸造工业,改善铸造工艺和铸件性能。
改变铸铁和铸钢性能的措施之一是改变铸件的凝固条件,在浇铸前加入某些铁合金作为晶核孕育剂,形成晶粒中心,使形成的石墨变得细小分散,晶粒细化,从而提高铸件的性能。
(4)用作还原剂。
硅铁可作为生产钼铁、钒铁等其他铁合金的还原剂;硅铬合金、锰硅合金可分别作为生产中低碳铬铁、中低碳锰铁的还原剂。
固态相变-第7章-有序无序转变

完全无序时
A、B原子占据(1)、 (2)阵点的概率等于A、B原子的相对 个数(浓度)。
2021/3/11
7
从凝聚态物理的范畴来看,有序现象大致可以分为三种类型:
不同原子或离子占据晶格中特定格点;
多原子分子取向性排列
如KH2PO4铁电体、有机分子取向有序、液晶分子的排列取向 有序。
(7-3)
NA(1)+NB(1)=N (1)
NA(2)+NB(2)=N(2)
所以:
2021/3/11
15
PA(1)+PB(1)=1 PA(2)+PB(2)=1 γPA(1)+(1-γ)PA(2)=CA 长程有序度定义
(7-4)
η=(PA (1) -CA)/(1-γ)
(7-5)
根据式(7-4)与式(7-5),所有的几率PA(1) 、PA(2) 、PB (1) 、PB(2) 均可用η和γ来表示:
则A、B原子占据点阵(1)、(2)的几率为:
2021/3/11
14
PA(1)=NA (1) /NA PA (2) =NA (2) /NA PB (1) =NB(1) /NA PB(2) =NB (2) /NB 因为:
(2)
NA(1)+NA(2)=NA
NB(1)+NB(2)=NB
NA+NB=N (1) +N (2) =N
NAB= N * σ=1
当完全无序时,最近邻原子一半是同种原子,一半是异种原 子:
NAB= N * /2 σ=0
2021/3/11
11
有序化的驱动力
从一对AB对转变为AA对和BB对时能量的变化:
合金的结构和相图课件

• 下面以Cu-Ni合金相图为例分析这类相图的 图形及结晶过程特点 。
现在学习的是第十七页,共87页
(1) 相图分析
相图由两条线构 成,上面是液相线,下面 是固相线。
相图被两条线分为三个
相区,液相线以上为液 相区L ,固相线以下为
• 在3点以前为匀晶转变,结晶出单相 固溶体,这种直
接从液相中结晶出的固相称一次相或初生相。
.2
现在学习的是第二十九页,共87页
• 温度降到3点以下, 固溶体被Sn过饱和,由于晶格
不稳,开始析出(相变过程也称析出)新相— 相。
由已有固相析出的新固相称二次相或次生相。
• 形成二次相的过程称二次析出, 是固态相变的一种。
(4)将各临界点标在 以温度为纵坐标,以成分为 横坐标轴的图形中相应合金的成分垂线上,并将意义 相同的临界点连接起来,即得到Cu-Ni合金相图。
现在学习的是第十五页,共87页
现在学习的是第十六页,共87页
1. 匀晶相图
• 组成二元合金的两组元在液态和固态均能无 限互溶的合金系所形成的相图称二元匀晶相 图
现在学习的是第十二页,共87页
三、二元合金相图
• 相图表示了在缓冷条件下不同成分合金的组织随 温度变化的规律,是制订熔炼、铸造、热加工及热 处理工艺的重要依据。
•
利用相图可以表示不同成分的合金、在不同温度
下,由哪些相组成、以及合金在加热或冷却过程中可
能发生的转变等。
•
目前使用的相图几乎都是通过实验测定的。实验
。
③ 液固相线:液相线AEB,固相线 ACEDB。A、B分别为Pb、Sn的 熔点。
铁碳合金相图分析
3. 铁碳合金相图
渗碳体在热力学中上是个亚稳定的相,石墨才是稳定 的相。但在实际中,石墨的表面能很大,形核需要很高的 能垒,一般条件下,碳大多和铁结合成渗碳体,只有在极 缓慢冷却或加入某些合金元素使石墨的表面能降低,碳才 能以石墨的形式存在。
铁碳元素在地壳中占41.2%,储量集中, 易于开采,而且易于从矿石中还原成金属;
铁碳合金的强韧性配合得好;
铁碳合金可形成两个同素异构体,多种组织, 性能变化范围宽;
776℃以下,具有铁磁性; 熔点为1538 ℃,热激活过程可以在不太高的温
度下进行。
可以有意无意地加入其它元素,得到各种各样 的性能。
1. Fe-Fe3C相图
A
1538℃
H
B1493℃
J
L
N 1394℃ γ+ L
1154℃
C
γ
E 1148℃
D
L+Cm F
G 910℃
γ+Cm
M O770℃
αP S
738℃ 727℃
K
α +Cm
Q
230℃
Fe
1
2
3
4
5
6 Fe3C
符 号 温 度/℃ ω(C)/%
说明
A 1538℃ B 1493℃ C 1147℃ D 1227℃ E 1147℃ F 1147℃ G 912℃ H 1493℃
❖ 过共析钢
d1 d2
d3 P S d4
当合金从液相开始冷却:
在d1点温度开始结晶出γ相,直至d2点温度时 结束,得到单相 γ 在d3点温度时,奥氏体 中的碳得到饱和,继续冷却时,奥氏体中析出 二次渗碳体Fe3CⅡ ,呈网状沿奥氏体晶界析出 在d4点温度时,发生共析转变,s点成分的奥氏 体共析分解,形成珠光体。
第七章单相固溶体合金及铸锭的凝固
c1
c2
C0
C0
B%
(b)
K 0 1 此阶段满足:固相结晶排向液相 的溶质量>溶质原子离开界面排 1 向液相的溶质量。 l Rx (2)凝固的稳定阶段(Ⅱ阶段): 0 D 当界面成分是C0,前沿的液相成 分为C0/k时,如图(b)的T5温度和 0 图(c)的第Ⅱ阶段直至Ⅱ阶段结束。 此阶段满足:固相结晶排向液相的溶质量=溶质原子离
图7-1不同KO的相图
(液相线与固相线近似为直线时K0为常数)
二.正常凝固时液-固相线中溶液的分布
研究水平园棒的定向凝固,对于KO<1的相图, 成分为C0 ,假设固相中无扩散,液相中可通过 扩散、对流和搅拌使溶液混合。
液相中溶液的混合分为三种: 完全混合、完全无混合、部分混合。
(一)液相完全混合时固相、液相的溶质分布:
(1)初期阶段:
①由于液相原子扩散速度较 小,边界层成分(CL)i与大体 积液相成分(CL)B相差较大, 且: (CL)B>C0
②固相结晶排出溶质部分进 入大体积液相,使边界层中 的浓度梯度不断增大C KC1x L 如图(d)的第Ⅰ阶段。
Ke1 S 00
d c L d x
定向凝固结论: ① 液相混合越充分,铸锭凝固后溶质分布越不均匀, 区域偏析越严重。 ② 利用定向凝固进行提纯材料,液相混合越充分,提 纯效果越好。
§7.2 固溶体合金的成分过冷
一.成份过冷的产生
①设K0<1的相图,液相完全 无混合,合金成分为C0, 进行完全无混合的单向 凝固如图(a); ②液相中实际的温度分布 图(b)为dT/dx>0,只 受壁模和已凝固的固相 散 热 单向散热所控制;
第七章合金的脱溶沉淀与时效知识分享
强度、硬度较低(HRC30,因C量低),成型性能 好。 时效强化效应,时效后屈服强度为: 1400~3500MPa. 二.铁基合金中的淬火时效 1.铁素体中合金K脱溶 2.奥氏体钢淬火时效现象
§7.6合金的调幅分解
调幅分解定义:由过饱和固溶体分 解产生两种结构相同,成分不同的 固溶体(但一个为溶质富化,一个 为溶质贫化),这种分解按扩散--偏聚机构进行的固态相变。 一.热力学条件 成分在拐点之间的合金(G-C曲线 下凹) 换句话:只有在的范围内的合金才 能进行调幅分解,即RKV范围内。
度越快 (2)溶质浓度的影响 (3)微量元素 3.固溶处理工艺的影响:温度、时间、冷速
§7.3 脱溶后的显微组织
一、连续脱溶及其显微组织 二、非连续脱溶及其显微组织
§7.4合金时效时的性能变化
1.硬度变化 2.时效硬度变化因素 (1)时效过程中固溶体
脱溶,过饱和度下降, 固溶强化降低; (2)基体发生回复与再 结晶; (3)新相的析出。
二.调幅分解过程
是纯扩散过程,一般脱溶分解是下坡扩散,即高浓度向 低浓度扩散,而调幅分解是上坡扩散,低浓度向高浓度 扩散。 三.组织、结构、性能 1.结构特点:分解产物与母相晶体结构相同,仅成分不 同,故新相与母相始终保持共格关系。 2.组织特点:因新相与母相在分解过程中,始终保持共 格关系,必然产生应力场,应变能增加。 (1)择优取向析出 (2)弥散C曲线的形式
形成GP区、过渡相、平衡相需要孕育期;
温度越高,过饱和度下降;
例:T1温度:GP区→β´→β
T2温度:β´→ β
T3温度:β
CAexp( W) KT
哈工大《材料科学基础Ⅱ》(相变)8讲解
过渡相的形成与位错密度有关。
第7章 合金的脱溶分解与时效
7.3 脱溶后的显微组织
一、连续脱溶及其显微组织
在合金脱溶过程中,脱溶物附近基体中的浓度变化为连续的,称 为连续脱溶。
连续脱溶可分为均匀脱溶和非均匀脱溶。 连续均匀脱溶: 脱溶物在固溶体晶内均匀形核,析出物分布比较均匀。 连续非均匀脱溶:
脱溶物在固溶体晶界或晶内滑移面及晶体缺陷处形核,析出物分 布比较均匀。形成的组织与魏氏组织相似。
调幅分解所得到的组织弥散度很大,具有较高的屈服强度和较好的 韧性。
第6章 淬火钢回火时的转变
作业题:
1 概念解释:固溶处理,脱溶,时效,时效合金的回归现 象,调幅分解。 2 以Al-Cu合金为例,说明时效合金的脱溶过程及各种脱 溶物的特征。
第7章 合金的脱溶分解与时效
7.1 脱溶过程和脱溶物结构
三、平衡相的形成
θ’ 相进一步长大,点阵常数变化,界面共格消失,形成稳定化合物 Al2Cu,称为平衡相θ。
θ相的形状:块状
θ相的尺寸:很大 θ相的晶体结构:正方结构,a=0.607nm, c=0.478nm
θ相与基体的界面:不共格
第7章 合金的脱溶分解与时效
时效硬化合金相图
第7章 合金的脱溶分解与时效
固溶体合金加热到略低于固相线的温度,保温足够时间,使溶质原 子充分溶解后立即淬火,得到亚稳定的过饱和固溶体,这种处理称 为固溶处理。 经固溶处理的合金在室温下放 置或加热到一定温度保持,合 金将产生脱溶析出。
析出相往往不是相图的平衡相, 而是亚稳相或溶质原子的偏聚 区。脱溶过程中过饱和固溶体 逐渐变为饱和固溶体。 室温下放置产生的时效称为自 然时效,加热进行的时效称为 人工时效。
材料科学基础
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3) 电性能
超导材料、压电材料
PZT:PbZrO3-PbTiO3
4)光学性能
透明陶瓷、人造宝石
PLZT:La2O3+PZT
人造宝石
4)活化晶格、促进烧结 例:
Al2O3,熔点达2050℃,很难烧结; 加入3%的Cr2O3形成置换型固溶体,可在1860℃烧结;
加入1%~2%TiO2,形成缺位固溶体,可在1600℃烧结
目与原子数目的比值,即e/a。
C电子 e a Z A (1 VB ) Z BVB
离子价相同或离子价总和相等时,才能生成无 限固溶体 如:MgO-NiO、Al2O3-Cr2O3; 钙长石-钠长石、PbZrO3-PbTiO3
4、间隙固溶体
溶质原子分布于溶剂晶格间隙而形成的 固溶体称为间隙固溶体。
(1)晶体结构
晶体结构类型相同,是组元间形成无限固
溶体的必要条件。 例如:
Cr (体心立方) Mn (面心立方)
在-Fe中的最大溶 解度/% 在-Fe中的最大 溶解度/%
12.Cr2O3;PbZrO3-PbTiO3
(2)原子(离子)尺寸因素
第 7 章 合金的相结构与结晶
合金:是指由两种或两种以上的金属或金属
与非金属经熔炼、烧结或其他方法组
合而成并具有金属特性的物质。
组成合金的基本的独立的物质称为组元。
如:碳钢和铸铁、黄铜
7.1 固态合金的相结构
相:是固体材料(合金)中具有同一聚
集状态、同一晶体结构和性质,并
以界面相互隔开的均匀组成部分。
形成间隙型固溶体的条件(影响因素) (1)结构尺寸因素 1)溶质原子的大小 即添加的原子愈小,易形成固溶体,反之亦然。
2)溶剂晶体结构(基质) 一般晶体中空隙愈大,结构愈疏松,易形成固溶体 例1:C和N 在-Fe和-Fe中 (2)电价因素 保持电价平衡(电中性) 例:
硅酸盐固溶体中:Be2++2Al3+
铂(铑)-铂(铑)热电偶,熔点为1450℃; 铂铑-铂 热电偶,熔点为1700℃; 铂铑-铂铑 热电偶,熔点为2000℃以上;
(3)物理和化学性能的变化
固溶体合金随着固溶度的增加,点阵畸变增
大,一般固溶体的电阻率ρ 升高,同时降低电阻
温度系数。
如:
1)Si溶入-Fe中,可提高导磁率; 2)Cr固溶于-Fe中,抗腐蚀;
∴ 形成固溶体后可大大降低烧结温度
5)稳定晶格,阻止某些晶型转变的发生
例:ZrO2
单斜四方
加入CaO后,和ZrO2形成固溶体,无晶型转变
1200C
二、中间相(金属间化合物)
中间相
中间相可以是化合物,也可以是以化合物为基的固溶
体(第二类固溶体或称二次固溶体)。
特点: 中间相通常可用化合物的化学分子式表 示。大多数中间相中原子间的结合方式属 于金属键与其他典型键(如离子键、共价 键和分子键)相混合的一种结合方式。因 此,它们都具有金属性。 如:CuZn、Fe3C、TiC ……
2Si4+
填隙型固溶体实例:
(1)原子填隙 金属晶体中,原子半径小的H、C、B元素 容易进入晶格间隙中形成间隙固溶体,如:钢 (2)阳离子填隙
2 2CaO ZrO Ca Ca Zr i 2OO
(3)阴离子填隙
YF3 YCa Fi 2FF CaF2
一、固溶体
1、定义 固溶体是以某一组元为溶剂,在其晶体
点阵中溶入其他组元原子(溶质原子)所形 成的均匀混合的固态溶体,它保持着溶剂的 晶体结构类型。
2、分类
根据固溶体的不同特点,可将固溶体进行 不同的分类: (1)根据溶质原子在溶剂晶格中所占据的位置
置换固溶体、间隙固溶体
(2)根据溶质原子在溶剂中的固溶能力
(4)原子价因素(离子电价因素)
当原子尺寸因素比较有利时,在某些一价 金属(如Cu、Ag、Au)为基的固溶体中, 原子的电价愈高,其溶解度愈小。
例如:Zn、Ga、Ge和As在Cu中的最大固溶度分 别为:38%、20%、12%和7%。
溶质原子价的影响实质上是“电子浓度”
所决定的。所谓电子浓度就是合金中价电子数
合金相:当金属元素与其他金属元素或非金
属元素组成合金时,会形成一个、两个
或更多的相,统称为合金相。
单相合金:含30%Zn的铜锌合金, 单相
多相合金:含40%Zn的铜锌合金,和’双相
固态下所形成的合金相基本上可分为 固溶体和中间相两大类。 固溶体:也称为一次固溶体或端际固溶体。 置换固溶体、间隙固溶体、有序固溶体 中间相:即化合物 ,金属间化合物 正常价化合物、电子化合物(电子相)、 间隙化合物(尺寸因素化合物)
有序化:有序固溶体加热至某一临界温度时将
转变为无序固溶体,其缓慢冷却至此温度时又 变为有序固溶体,此转变过程称之为固溶体的 有序化。
有序畴(反相畴):
6、固溶体的性质
(1)点阵常数改变
置换固溶体、间隙固溶体 溶质原子浓度
(2)产生固溶强化
通过形成固溶体是金属强化的现象称为固溶强化。
固溶体的强度与硬度往往高于各组元, 而塑性则较低。 例:
尺寸越接近,固溶体越稳定 15%规则:
r1 r2 r r1
<
15%, 固溶度大的无限固溶体
> 15%,固溶度较小的有限固溶体 例:
Ni、Co与-Fe;Cr、V与-Fe
MgO-NiO;MgO-CaO
(3)化学亲合力(电负性因素)
电负性相近 —— 固溶体
电负性差别大 —— 化合物 △X = ±0.4 之间时,易形成无限固溶体
5、有序固溶体(超结构或超点阵)
在一定条件下,溶质原子与溶剂原子 分别占据一定位置,而且每个晶胞中溶质
原子和溶剂原子数之比都是一定的,这样
的固溶体叫做有序固溶体,这种有序结构
叫做超点阵或超结构。
固溶体中溶质原子的分布方式:
完全无序 偏聚(从聚)
部分有序(短程有序)
完全有序(长程有序)
有限固溶体、无限固溶体
(3)根据溶质原子在固溶体中的分布是否有规律 无序固溶体、有序固溶体
3、置换固溶体
当溶质原子溶入溶剂中形成固溶体时,
溶质原子占据溶剂点阵的阵点,或者说溶质
原子置换了溶剂点阵的部分溶剂原子,这种
固溶体就称为置换固溶体。
特点:保持了原溶剂组元的晶体结构
影响固溶度的因素:
晶体结构类型 原子(离子)尺寸因素 化学亲和力(电负性因素) 原子价因素(离子的电价因素)
