肺炎链球菌的实验活动生物危害评估报告
肺炎链球菌生物危害评估报告

肺炎链球菌生物危害评估报告一、细菌的传播与致病肺炎链球菌在自然界中分布广泛,常生活在正常人的鼻腔中,多数不致病或致病力很弱,少数致病力较强。
肺炎链球菌主要引起大叶性肺炎以及气管炎、中耳炎、脑膜炎、胸膜炎、心内膜炎、败血症等疾病。
典型的大叶性肺炎起病急骤,病人有高烧、寒颤,开始时有阵发性干咳,不久有少量粘液痰,随后痰变黄色,呈粘脓性,一般病程1~2周。
二、细菌的生物学特性肺炎链球菌(S.pneumoniae)属链球菌科,链球菌属。
为革兰氏阳性球菌,呈矛尖状,成双排列,标本或液体培养中可连成链状。
有荚膜,无鞭毛,不形成芽胞。
本菌营养要求较高,需在含血液或血清的培养基中生长。
兼性厌氧,C02 5-10%生长最好,且生成的菌落周围有草绿色溶血环。
若于液体培养基中培养24h,呈均匀混浊,后期可因产生自溶而变得澄清。
该菌可分解多种糖类,产酸不产气。
胆汁溶解试验阳性Optochin敏感试验阳性。
其抗原结构包括:荚膜多糖抗原:多糖抗原,型特异性,共85型,Ⅰ~Ⅲ型引起大叶性肺炎;菌体种属特异性抗原为多糖抗原,存在于细胞壁,称C多糖。
在钙离子存在时,C多糖可与正常人血清中称为C-反应蛋白(C reactive protein,CRP)的β球蛋白结合,发生沉淀。
该菌抵抗力较弱,加热56℃,20min即死亡。
而且它对一般消毒剂敏感,对干燥抵抗力较强。
肺炎链球菌可能发生的变异有荚膜变异:即从有荚膜有毒力的光滑(S)型菌变异为失去荚膜毒力减低或消失的粗糙(R)型。
三、细菌的实验室检查1、标本采集包括痰、脓液、血液等标本。
2. 涂片染色镜检革兰氏色染色呈阳性球菌,呈矛头状成双排列,坦面相邻,尖端向外。
若标本可见大量炎性细胞同时存在时有重要的参考价值。
3、荚膜染色阳性。
4、分离培养常采用羊血平板,有助于其溶血特征的识别和进一步鉴定,而且初代分离应置5%~10%CO2的环境下培养。
在血平板上,肺炎链球菌的菌落直径0.5~1.5mm,灰白色、半透明、表面光滑(有些菌株可表现为粘液状)扁平,周围环绕着草绿色溶血环。
检验科实验活动生物危害评估报告

检验科实验活动生物危害评估报告一、引言实验室中的实验活动,尤其是涉及到生物领域的实验活动,可能会存在一定的生物危害性。
为确保实验室和实验人员的安全,进行实验活动前,有必要对实验所涉及的生物危害进行评估,并提前采取相应的防护措施。
本报告就实验活动的生物危害进行评估,并提出相应的防护建议。
二、实验背景本次实验活动旨在研究细菌的增殖过程,通过培养细菌并观察其生长情况和形态变化,分析细菌的增殖速率以及环境对细菌生长的影响。
三、生物危害评估根据实验活动的性质和目的,本次实验涉及到的生物危害主要包括以下几个方面:1.感染风险:实验活动中使用的细菌可能具有一定的致病性,存在感染风险。
误操作、实验器材的不当处理或细菌暴露可能导致感染事件的发生。
2.毒性物质:实验中所使用的细菌培养基、酶切剂等物质可能具有毒性,误接触或吸入可能对实验人员的健康造成危害。
3.遗传物质:实验中使用的细菌包含遗传物质,若遗传物质泄漏或误操作可能对环境和实验人员的健康构成潜在威胁。
根据以上评估,本次实验活动涉及到的生物危害较为明显,需要采取一系列的防护措施以确保实验室和实验人员的安全。
四、防护建议基于生物危害评估结果,下面提出相应的防护建议:1.实验操作人员应经过必要的生物安全培训,熟悉实验室安全操作规程,了解细菌的危害性和应急处理措施。
2.实验操作人员应佩戴个人防护装备,包括实验服、手套、口罩和护目镜,以防止细菌直接接触皮肤、吸入或飞溅进入眼睛和口鼻。
3.实验室应配备安全实验台和生物安全柜,确保实验台面的材质易于清洁,防止细菌滋生和繁殖。
4.细菌实验过程中需要进行严格的无菌操作,避免细菌外泄和污染环境。
5.严格控制细菌培养基的使用和处理,避免误吞食或皮肤接触。
6.在实验过程中避免纯化细菌时的气溶胶产生,可采用安全离心机或其他无菌操作方式。
7.实验后,将实验器材、废弃物进行正确处理,避免细菌污染的扩散。
五、结论本次实验活动涉及到的生物危害较为明显,但通过采取相应的防护措施,可以有效地降低生物危害对实验室和实验人员的危害。
二级实验室病原微生物危害性评估
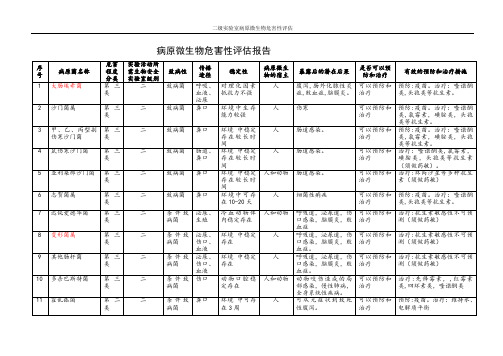
序号
病原菌名称
危害程度分类
实验活动所需生物安全实验室级别
致病性
传播
途径
稳定性
病原微生物的宿主
暴露后的潜在后果
是否可以预防和治疗
有效的预防和治疗措施
1
大肠埃希菌
第三类
二
致病菌
呼吸、血液、泌尿
对理化因素抵抗力不强
人
腹泻,肠外化脓性炎症,败血症,脑膜炎。
可以预防和治疗
预防:疫苗。治疗:喹诺酮类,头孢类等抗生素。
2
沙门菌属
第三类
二
致病菌
粪口
环境中生存能力较强
人
伤寒
可以预防和治疗
预防:疫苗。治疗:喹诺酮类,氯霉素,磺胺类,头孢类等抗生素。
3
甲、乙、丙型副伤寒沙门菌
第三类
二
致病菌
粪口
环境中稳定存在较长时间
人
肠道感染。
可以预防和治疗
预防:疫苗。治疗:喹诺酮类,氯霉素,磺胺类,头孢类等抗生素。
4
鼠伤寒沙门菌
第三类
二
可以预防和治疗
治疗:抗生素敏感性不可预测(须做药敏)
9
其他肠杆菌
第三类
二
条件致病菌
泌尿、伤口、血液
环境中稳定存在
人
呼吸道,泌尿道,伤口感染,脑膜炎,败血症。
可以预防和治疗
治疗:抗生素敏感性不可预测(须做药敏)
10
多杀巴斯特菌
第三类
二
条件致病菌
伤口
动物口腔稳定存在
人和动物
动物咬伤造成的局部感染,慢性肺病,全身系统性疾病。
人
细菌性痢疾
可以预防和治疗
肺炎链球菌实训报告模板

一、实训目的本次实训旨在通过实际操作和理论学习,深入了解肺炎链球菌的性质、生物学特性、致病机制以及相关实验室检测方法。
通过实训,提高学生对微生物学知识的掌握,培养实际操作技能,增强对病原微生物的识别和检测能力。
二、实训时间2023年X月X日至2023年X月X日三、实训地点XX大学微生物实验室四、实训内容1. 肺炎链球菌的形态学观察2. 肺炎链球菌的生化特性鉴定3. 肺炎链球菌的分离纯化4. 肺炎链球菌的致病性检测5. 肺炎链球菌的药物敏感性试验五、实训过程1. 肺炎链球菌的形态学观察(1)实验材料:肺炎链球菌标准菌株、显微镜、玻片、染色液等。
(2)实验步骤:- 将肺炎链球菌接种于玻片上,进行涂片。
- 使用革兰氏染色法对涂片进行染色。
- 使用显微镜观察肺炎链球菌的形态和排列方式。
(3)实验结果:- 观察到肺炎链球菌为革兰氏阳性球菌,呈矛头状成双排列或呈短链状。
2. 肺炎链球菌的生化特性鉴定(1)实验材料:肺炎链球菌标准菌株、生化鉴定管、培养基等。
(2)实验步骤:- 将肺炎链球菌接种于生化鉴定管和培养基上。
- 观察并记录肺炎链球菌的生化反应结果。
(3)实验结果:- 肺炎链球菌能够分解葡萄糖,产生酸性产物,不分解乳糖。
3. 肺炎链球菌的分离纯化(1)实验材料:肺炎链球菌标准菌株、琼脂平板、无菌器械等。
(2)实验步骤:- 将肺炎链球菌接种于琼脂平板上,进行划线分离。
- 将分离后的菌落进行纯化培养。
(3)实验结果:- 成功分离出纯化的肺炎链球菌菌落。
4. 肺炎链球菌的致病性检测(1)实验材料:肺炎链球菌标准菌株、实验动物、注射器等。
(2)实验步骤:- 将肺炎链球菌接种于实验动物体内。
- 观察并记录实验动物的反应。
(3)实验结果:- 实验动物出现肺炎症状,证明肺炎链球菌具有致病性。
5. 肺炎链球菌的药物敏感性试验(1)实验材料:肺炎链球菌标准菌株、药敏纸片、琼脂平板等。
(2)实验步骤:- 将药敏纸片贴于琼脂平板上。
肺炎球菌实验活动风险评估报告

肺炎球菌实验活动风险评估报告1. 介绍本报告旨在评估肺炎球菌实验活动的潜在风险,并提供相应的风险管理建议。
肺炎球菌是一种常见的病原体,与肺炎和其他呼吸道感染有关。
在进行肺炎球菌实验活动时,必须采取预防措施以确保工作人员和实验室环境的安全。
2. 风险评估在肺炎球菌实验活动中,存在以下潜在风险:2.1 感染风险肺炎球菌可通过呼吸道飞沫传播,因此有感染传播的风险。
工作人员在与含有肺炎球菌的样本接触时,可能会被感染。
此外,实验室环境中可能存在空气传播的风险。
感染风险主要存在于未采取适当防护措施的情况下。
2.2 实验物品和设备的风险进行肺炎球菌实验活动时,实验物品和设备的不当使用可能导致一些潜在风险,如溢出、破损或烧伤等。
2.3 实验室环境的风险实验室环境的不适当管理可能会增加肺炎球菌实验活动的风险,如实验室设备不完善、缺乏清洁和正当维护。
3. 风险管理建议为了降低肺炎球菌实验活动的风险,应采取以下风险管理建议:3.1 培训和教育提供足够的培训和教育以确保工作人员了解肺炎球菌实验活动的潜在风险及相应的防护措施。
3.2 个人防护措施提供个人防护装备,如手套、口罩和面罩,以减少感染风险。
3.3 实验室安全规范制定和执行实验室安全规范,包括实验物品和设备的正确使用方法、实验室环境的清洁和维护、空气循环和通风要求等。
3.4 废物处理确保正确处理实验活动产生的废物,包括肺炎球菌样本的处理,以防止疾病传播。
3.5 定期检查和维护定期检查和维护实验室设备,确保其正常运作和安全性。
4. 总结本报告对肺炎球菌实验活动的潜在风险进行了评估,并提供相应的风险管理建议。
通过遵循建议措施,可以减少肺炎球菌实验活动对工作人员和实验室环境的风险,提高实验的安全性和可持续性。
以上是简要的风险评估报告,供参考之用。
实验室病原微生物危害评估报告 (3)

实验室病原微生物危害评估报告病原微生物危害评估报告1. 引言本报告提供了对实验室病原微生物危害的评估,旨在识别潜在的健康和安全风险,并提供相应的建议和措施来降低这些风险。
2. 评估方法评估包括对实验室中的病原微生物的类型和数量进行调查,检查实验室是否有适当的控制措施和安全设施,以及评估员工的培训和意识情况。
3. 病原微生物类型和数量根据实验室提供的信息和样本的分析结果,确定以下病原微生物存在于实验室中:菌落总数(CFU/g),大肠杆菌,沙门氏菌,金黄色葡萄球菌等。
病原微生物数量在合理范围内,但对于某些病原微生物可能存在较高的风险。
4. 控制措施和安全设施实验室内部有适当的控制措施和安全设施,包括但不限于生物安全柜,消毒设备,标志和防护用具,用于控制实验室中的病原微生物的传播和暴露。
5. 员工培训和意识实验室员工接受了相关的培训和教育,了解病原微生物的风险和控制措施,并知道如何正确使用和操作实验室中的设备和工具。
6. 建议和措施为了进一步降低病原微生物危害,建议采取以下措施:- 定期进行病原微生物数量的监测,并根据结果调整和改进控制措施。
- 增加员工的培训和教育,提高他们对病原微生物风险的认识和意识。
- 确保实验室设施和设备的维护和消毒工作得到有效的执行。
- 鼓励员工遵守和执行实验室的安全操作规程,并提供相应的奖惩机制。
7. 结论实验室的病原微生物危害评估结果显示,实验室已采取一定的措施来降低病原微生物的风险。
然而,仍然存在一些潜在的风险,建议采取相应的措施来进一步降低这些风险。
以上建议和措施仅供参考,实验室应根据具体情况制定并执行适用的安全管理计划。
(完整word版)检验科实验活动生物危害评估报告
检验科实验活动生物危害评估报告为保证实验室工作人员在工作中不被危害性生物及物品所侵害,保证危害性物品不外泄,对实验室工作环境进行评估,以鉴定生物安全防护等级,保证生物安全。
一、危害程度分类及生物安全防护水平评估本检验科是为医院诊断、预防、治疗人体疾病或评估人体健康提供信息为目的,对来自人体的材料进行临床生物化学、临床微生物、临床免疫学、临床血液等检验的实验室。
生物源危害主要是由各种检验标本中的微生物,尤其是病原微生物引起的,包括细菌、病毒、寄生虫等,具有潜在危险性,可能引起实验室感染;检验科微生物室还进行一定数量的各种条件致病性细菌及真菌的分离培养工作,工作过程存在病原微生物对实验人员、环境污染的风险;除之以外实验室还存在触电、火灾、化学品腐蚀、偷盗等危险。
根据《实验室生物安全通用要求》,本检验科不涉及《人间传染的病原微生物名录》中高致病性微生物的分离培养及高致病性微生物的菌、毒种的保藏,实验室采用一定防护措施就能控制感染或防范灾害,或者对相应病原体存在有效的免疫方法。
评估我检验科生物安全防护水平按二级实验室(BSL-2)生物安全要求。
二、实验人员和实验室安全防护的一般要求1.吸烟危害评估及防护(1)实验室工作区内绝对禁止吸烟;(2)点燃的香烟是易燃液体的潜在火种;(3)香烟、雪茄或烟斗都是传染细菌和接触毒物的途径。
2. 实验区内食用食物、饮料及其它危害评估及防护(1)实验工作区内不得有食物、饮料及存在“手-口”接触可能的其它物质(2)实验室工作区内的冰箱禁止存放食物。
专用存放食物的冰箱应放置在允许进食、喝水的休息区内。
3.使用化妆品危害评估及防护实验工作区内禁止使用化妆品进行化妆,但允许并建议经常洗手的实验人员使用护手霜。
4. 实验中眼睛和面部的风险评估及防护(1)处理腐蚀性或毒性物质时,须使用安全镜、面罩或其它保护眼睛和面部的防护用品。
(2)工作人员在实验室的危险区内不要佩戴隐形眼镜,除非同时使用护目镜或面罩。
实验室病原微生物危害评估报告模板
病原微生物危害性评估报告第二版文件编号:XXX-XXX-PG生效日期:XXXX年XX月XX日XXX医院XXX科目录鲍曼不动杆菌的生物危害评估1. 细菌的传播与致病1.1鲍曼不动杆菌分布于自然界和医院环境中,是人类皮肤、呼吸道、胃肠道、生殖道的正常菌群,是一种条件致病菌,也科成为重症科室的定植菌,可引起各种感染和医院感染。
是不动杆菌菌种感染率最高的,可引起腹膜炎、脑膜炎、骨髓炎和关节炎菌血症和肺炎等.鲍曼不动杆菌已经发现看多重耐药菌株,耐亚胺培南不动杆菌在中国台湾地区大25%,在澳大利亚和中国大陆地区大20%左右,所以每个分离菌株都应进行药敏试验。
2。
细菌的生物学特性2.1 本菌为革兰阴性球状或球杆菌,约1.0~1。
5μm×1。
5~2。
5μm,单个或成对排列有时成丝状或呈短链状,无芽胞及鞭毛,无动力,有荚膜.严格好氧,在20~30℃生长,大部分菌株最适生长温度33~45℃。
在所有普通综合培养基上均能生长。
2。
2 氧化酶阴性,触酶阳性.3. 细菌的实验室检查3.1 标本采集:来自与临床的各种标本如血液、尿液、脓汁、下呼吸道分泌物以及脑脊液等.3。
2 涂片镜检:细菌培养阳性时,进行革兰染色镜检.3.3 分离培养:接收临床标本后痰、灌洗液、支气管刷检物及脑脊液接种于血平板、中国蓝、巧克力平板上,其他体液及分泌物标本接种于血平板上.3。
4 生化鉴定:氧化酶阴性.4. 细菌的防治4。
1 鉴定出鲍曼不动杆菌的同时进行药敏试验,根据药敏结果与临床实际相结合进行治疗4。
2 在实验室以及病房中注意勤洗手,避免直接接触鲍曼菌株5. 细菌的生物安全防护5。
1操作要求:5。
1。
1 实验时,未经允许,不得随意进入实验室.5.1。
2 不许在工作区域饮食、吸烟、清洗隐型眼镜和化妆。
食物应存放在工作区域以外专用橱柜或冰箱中。
5。
1。
3 所有的操作过程应尽量细心,避免溅出.5.1.4 对于污染的锐器,必须时刻保持高度的警惕,使用过的一次性针、注射器、玻片、加样枪头等放入加有一定浓度的84消毒液锐器盒中浸泡消毒。
肺炎链球菌的临床分布及药敏结果
肺炎链球菌的临床分布及药敏结果王春光目的:了解昆明市儿童医院肺炎链球菌临床分布及药敏情况,为结合临床用药提供依据。
方法:对2013年7月—10月进行微生物病原学培养分离的肺炎链球菌药敏结果进行统计分析。
结果 该院分离的肺炎链球菌主要来自儿童(100%),标本主要来源是痰液(72.72%),其次是血液(22.72%),其他(4.56%)。
肺炎链球菌的耐药率:青霉素86.4%,氨苄西林0%,头孢曲松40.9%,美罗培南54.5%,庆大霉素0%,环丙沙星0%,左旋氧氟沙星0%,氧氟沙星4.5%,克林霉素95.5%,红霉素95.5%,万古霉素0%,氯霉素27.3%,四环素90.9%。
结论 应该积极对儿童预防接种肺炎链球菌疫苗,青霉素对该菌耐药性较高。
肺炎链球菌(Streptococcus Pneumoniae, SP)是儿科社区获得性感染的主要病原菌之一,主要寄生在人类上呼吸道,为条件致病菌,约40% ~ 70% 正常人鼻咽部有本菌存在。
可通过飞沫、分泌物传播,对人的健康构成了一定的威胁,WHO估计,每年大约有160万人死于SP感染,其中5岁以下儿童占43.8%~62.5%,且大多数分布在发展中国家。
更为严重的是,在过去青霉素等抗菌药物是治疗肺炎链球菌感染的有效手段,但随着抗菌药物的大量使用或使用不合理,耐青霉素菌株和多重耐药菌株持续增加,已成为临床抗感染治疗的新难题。
肺炎链球菌疫苗是预防其感染、延缓耐药菌株产生和传播的有效措施。
SP感染严重威胁着儿童的健康,避免抗生素滥用是目前公认的较好的控制SP耐药发生和发展的主要途径。
为了解近年来肺炎链球菌的耐药情况,为临床合理使用抗生素提供依据,特对昆明市儿童医院2013年7月~10月临床分离的非重复的22株肺炎链球菌的耐药性进行回顾性分析,现将结果报道如下。
一、资料与方法(一)一般资料2013年7月—10月分离自昆明市儿童医院患儿的肺炎链球菌感染菌株22株。
其中16株来自痰液,5株来自血培养,1株来自其他。
肺炎链球菌课程设计
肺炎链球菌课程设计一、课程目标知识目标:1. 学生能够理解肺炎链球菌的基本概念,掌握其分类、形态结构及生活习性。
2. 学生能够阐述肺炎链球菌与人类健康的关系,了解肺炎链球菌感染的途径和危害。
3. 学生掌握肺炎链球菌的检测方法,了解实验室诊断及防治措施。
技能目标:1. 学生能够运用所学知识,分析肺炎链球菌感染的案例,并提出合理的防治建议。
2. 学生能够运用生物学实验技能,进行肺炎链球菌的检测实验,提高实验操作能力。
3. 学生能够通过查阅资料、讨论交流,提高自主学习能力和团队合作能力。
情感态度价值观目标:1. 学生能够认识到微生物在自然界和人类生活中的重要作用,培养对微生物的探究兴趣。
2. 学生能够关注肺炎链球菌感染对人类健康的危害,增强健康意识,养成良好卫生习惯。
3. 学生能够通过学习肺炎链球菌的相关知识,培养科学思维和批判性思维,提高解决问题的能力。
本课程针对初中年级学生,结合生物学课程内容,以肺炎链球菌为主题,旨在帮助学生掌握微生物知识,提高实验操作技能,培养科学素养。
课程目标具体、可衡量,便于教师进行教学设计和评估,同时激发学生的学习兴趣,提高其知识运用和问题解决能力。
二、教学内容1. 肺炎链球菌基本概念:介绍肺炎链球菌的分类、形态结构、生活习性及生物学特性。
教材章节:《生物学》第四章第三节“细菌与真菌”2. 肺炎链球菌与人类健康:阐述肺炎链球菌感染途径、危害及其在人体内的作用机制。
教材章节:《生物学》第四章第四节“微生物与人类健康”3. 肺炎链球菌检测方法:介绍实验室常用的肺炎链球菌检测方法,如细菌培养、生化试验、PCR检测等。
教材章节:《生物学》第五章第一节“生物技术在医学领域的应用”4. 肺炎链球菌防治措施:阐述肺炎链球菌感染的预防、控制和治疗方法。
教材章节:《生物学》第四章第五节“传染病的预防与控制”5. 实践活动:肺炎链球菌检测实验,分组进行实验操作,观察和分析实验结果。
教材章节:《生物学》第五章第二节“生物学实验技能”教学内容安排和进度:第一课时:肺炎链球菌基本概念、与人类健康的关系第二课时:肺炎链球菌检测方法、防治措施第三课时:实践活动——肺炎链球菌检测实验教学内容具有科学性和系统性,紧密结合教材,旨在帮助学生掌握肺炎链球菌相关知识,提高实验操作技能,培养学生的科学素养。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
肺炎链球菌的实验活动生物危害评估报告
一、细菌的传播与致病
肺炎链球菌在自然界中分布广泛,常生活在正常人的鼻腔中,多数不致病或致病力很弱,少数致病力较强。
肺炎链球菌主要引起大叶性肺炎以及气管炎、中耳炎、脑膜炎、胸膜炎、心内膜炎、败血症等疾病。
典型的大叶性肺炎起病急骤,病人有高烧、寒颤,开始时有阵发性干咳,不久有少量粘液痰,随后痰变黄色,呈粘脓性,一般病程1~2周。
二、细菌的生物学特性
肺炎链球菌 (S.pneumoniae)属链球菌科,链球菌属。
为革兰氏阳性球菌,呈矛尖状,成双排列,标本或液体培养中可连成链状。
有荚膜,无鞭毛,不形成芽胞。
本菌营养要求较高,需在含血液或血清的培养基中生长。
兼性厌氧,C02 5-10%生长最好,且生成的菌落周围有草绿色溶血环。
若于液体培养基中培养24h,呈均匀混浊,后期可因产生自溶而变得澄清。
该菌可分解多种糖类,产酸不产气。
胆汁溶解试验阳性Optochin敏感试验阳性。
其抗原结构包括:荚膜多糖抗原:多糖抗原,型特异性,共85型,Ⅰ~Ⅲ型引起大叶性肺炎;菌体种属特异性抗原为多糖抗原,存在于细胞壁,称C多糖。
在钙离子存在时,C多糖可与正常人血清中称为C-反应蛋白(C reactive protein,CRP)的β球蛋白结合,发生沉淀。
该菌抵抗力较弱,加热56℃,20min即死亡。
而且它对一般消毒剂敏感,对干燥抵抗力较强。
肺炎链球菌可能发生的变异有荚膜变异:即从有荚膜有毒力的光滑(S)型菌
变异为失去荚膜毒力减低或消失的粗糙(R)型。
三、细菌的实验室检查
1、标本采集包括痰、脓液、血液等标本。
2. 涂片染色镜检革兰氏色染色呈阳性球菌,呈矛头状成双排列,坦面相邻,尖端向外。
若标本可见大量炎性细胞同时存在时有重要的参考价值。
3、荚膜染色阳性。
4、分离培养常采用羊血平板,有助于其溶血特征的识别和进一步鉴定,而且初代分离应置5%~10%CO2的环境下培养。
在血平板上,肺炎链球菌的菌落直径0.5~1.5mm,灰白色、半透明、表面光滑(有些菌株可表现为粘液状)扁平,周围环绕着草绿色溶血环。
培养或放置24h以上的培养物还会由于肺炎链球菌的自溶作用而致菌落中央塌陷而边缘隆起,而呈脐窝状。
5、鉴定试验
①胆汁溶菌试验:本试验的原理基于胆盐能够通过活化肺炎链球菌的自溶酶而溶解肺炎链球菌,但不能溶解草绿色链球菌。
常用的方法包括快速平板法和标准试管法。
前者取一接种环2%去氧胆酸钠溶液加于血平板待鉴定菌的菌落上,置35℃孵育15~30min,菌落溶解消失为阳性。
而后者则是在1ml待鉴定菌18~24h 培养液中加入2滴10%去氧胆酸钠溶液,35℃孵育5-10min后鉴定菌管由混浊变为透明者为阳性。
②Optochin试验用以与其他草绿色链球菌相鉴别。
用接种环将单个待鉴定菌落均匀涂于血平板上,用含量为5μg的optochin纸片贴于接种区中央,35℃需氧培养过夜,抑菌圈 >18mm的为阳性。
本菌为阳性。
6、小鼠毒力试验若用有毒力的菌株接种小鼠,接种后12-36h,小鼠死亡。
四、细菌的防治
肺炎链球菌感染关键在于养成良好的卫生习惯,保持环境卫生。
必要时对体弱儿童及老年人可用疫苗进行预防注射,如用细菌荚膜多糖制备的多糖疫苗进行预防,效果较好。
病人在发热期间,应卧床休息,吃容易消化的食物,多喝水。
磺胺类药物、青霉素等对肺炎等疾病的治疗较为有效。
五、细菌的生物安全防护
根据《病原微生物生物实验室生物安全管理条例》中的有关规定,人间传播的微生物名录(待颁布)肺炎链球菌属于三类,BSL-2。
相关的防护事宜包括:(1)操作要求
1、实验时,未经实验室主任同意,限制或禁止进入实验室。
2、不许在工作区域饮食、吸烟、清洗隐型眼镜和化妆。
食物应存放在工作区域以外专用橱柜或冰箱中。
3、所有的操作过程应尽量细心,避免产生和溅出气溶胶。
4、对于污染的锐器,必须时刻保持高度的警惕,包括针、注射器、玻片、加样器等。
5、注射和吸取感染材料时,只能使用针头固定注射器或一次性注射器(即注射器和针头是一体的)。
用过的一次性针头必须弯曲、切断、破碎、重新套上针头套、从一次性注射器上去掉,或在丢弃前进行人工处理,要不将之小心放入不会被刺穿的、用于收集废弃锐器的容器中。
非一次性锐器必须放置在坚壁容器中,转移至处理区消毒,最好高压杀菌。
6、打碎的器皿不能直接用手处理,必须用其它工具处理,如刷子和簸箕、夹子或镊子。
盛污染的针头、锐器、碎玻璃的容器在倒掉前,应按照相关的规定进行消毒。
7、所有的培养物、储存物及其它规定的废物在释放前,均应使用可行的消毒方法进行消毒,如高压灭菌。
转移到就近实验室消毒的物料应置于耐用、防漏容器内,密封运出实验室。
离开该系统进行消毒的物料,在转移前应包装,其包装应符合有关的法规。
8、溅出或偶然事件中,明显暴露于传染源时,要立即向实验室主任报告。
进行适当的医学评估、观察、治疗,保留书面记录。
9、按日常程序、在有关传染源的工作结束后、尤其是传染源溅出或洒出后、或受到其他传染源污染后,实验室设备和工作台面应当使用有效的消毒剂消毒。
污染的设备在送去修理、维护前,要按照相关的规定消毒;在离开设施转移前,要按照相关的规定打包运输。
(2)安全设备
1、正确使用和保养生物安全柜、最好是二级生物安全柜、或其他合适的人员防护设施、或物理遏制装置。
2、确定可能形成传染性气溶胶或溅出物的实验过程,包括离心、研磨、匀浆、剧烈震荡或混匀、超声波破裂、开启装有传染源的容器、采集感染标本等。
3、涉及高浓度或大体积的传染源时,若选用密封转头或带安全罩的离心机,若转头或安全罩仅在生物安全柜中打开,则可在开放实验室内离心。
4、当必须在生物安全柜外处理标本时,需采取面部保护措施(跟镜、口罩、面罩、或其他防溅装置),以免传染源或其他有害物溅或洒到面上。
5、在实验室内,必须使用专用的防护性外衣、大褂、罩衫或制服。
人员到非实验室区域时,防护服必须留在实验室内。
防护服可以在实验室内处理,也可以在洗衣房中洗涤,但不能带回家中。
6、可能接触潜在传染源、被污染的表面或设备时,要戴手套。
一次性手套不用清洗、不能重复使用,不能用于接触“洁净”的表面(键盘、电话等),也不应当戴着到实验室外。
要备有带滑石粉的乳胶手套。
脱掉手套后,要洗手。
