第七章:互变异构与双重反应性
乙酰乙酸乙酯互变异构

乙酰乙酸乙酯互变异构
乙酰乙酸乙酯(简称ACE)是一种有机化合物,具有酯的一般性质。
在化学领域,乙酰乙酸乙酯的互变异构现象引起了广泛关注。
本文将详细介绍乙酰乙酸乙酯的互变异构现象、性质及应用领域。
乙酰乙酸乙酯的基本性质如下:
1.分子结构:乙酰乙酸乙酯的分子式为C6H10O2,分子量为114.13。
2.物理性质:乙酰乙酸乙酯为无色透明液体,沸点为126-128℃,熔点-20.5℃,折射率1.4125。
3.化学性质:乙酰乙酸乙酯具有较强的反应性,易于水解、酯化、醚化等反应。
乙酰乙酸乙酯的互变异构现象主要表现在其结构中的羰基上。
在乙酰乙酸乙酯分子中,羰基的酮式和烯醇式相互转化,形成互变异构体。
这种互变异构现象对乙酰乙酸乙酯的性质产生了显著影响。
在乙酰乙酸乙酯的互变异构过程中,酮式和烯醇式的相对稳定性会发生变化。
酮式较为稳定,具有较高的反应性,易于发生加成、还原等反应;烯醇式相对不稳定,但其活泼性较高,易于进行亲核取代反应。
乙酰乙酸乙酯在化工领域具有广泛的应用,如:
1.作为香料和调味剂的原料:乙酰乙酸乙酯具有水果香气,可用于调配食品香料、饮料添加剂等。
2.作为有机合成原料:乙酰乙酸乙酯可通过氧化、水解等反应制备其他有机化合物,如乙酰乙酸、乙醇等。
3.药物合成:乙酰乙酸乙酯可用于合成某些药物,如抗生素、抗病毒药物等。
总之,乙酰乙酸乙酯是一种具有广泛应用的有机化合物。
其互变异构现象对其性质和反应活性产生了显著影响。
酮-烯醇互变异构

酮-烯醇互变异构酮-烯醇互变异构:酮与一种称为烯醇的形式处于平衡状态。
烯醇这个名字源于这样一个事实,烯醇是含羰基( C = O )的基团,如醛或酮和醇羟基( OH )的组合。
这两种形式之间的相互转换是由一种叫做互变异构的过程产生的。
这两种异构体通过分子中氢和双键位置的变化而相互关联。
因此,互变异构现象描述了酮和烯醇之间的平衡,这种平衡通过改变电子和氢的键合位置而相互转化,从而产生两种异构体。
这一过程是酮、醛和酯的典型过程,一般来说,相互转化是缓慢的。
含羰基化合物的异构体优于烯醇形式,酮形式占主导地位,大于99 %。
这些比例的控制可以通过催化来实现,特别是通过酸或碱。
糖是碳原子的多羟基链(包含许多OH基团),其另外具有醛或酮官能团。
一般来说,所有糖的特征是碳:氢:氧的比例为1 : 2 : 1。
随后,碳水化合物具有在反应性羟基和羰基碳之间进行内部或分子内反应的能力。
羟基是亲核的;它拥有一个孤电子对,它可以贡献给羰基碳,从而形成一个键。
羰基碳易于形成这种键,因为它的电子受到双键氧的牵引作用。
氧比碳更能吸引成对的电子;据说它更具电负性。
当糖中的单个亲核羟基攻击醛或酮时,分别产生称为半缩醛或半缩酮的产物。
前缀hemi -表示反应的可逆性。
它们也称为缩醛或吡喃糖。
由于化学键形成所产生的闭环效应,这些是环状的。
请注意,攻击醛产生半缩醛会产生6元环。
在糖中,这被称为醛糖。
或者,如果羟基攻击酮以产生半缩酮,则所得产物是称为酮糖或呋喃糖的5元环。
另一个需要注意的惯例是“D -”和“L -”。
前缀“D -”用于表示光学异构体(具有围绕中心原子的不对称基团的异构体)旋转平面偏振光的方向。
d - '异构体的手性( C5 )中心的OH指向右侧;l - '异构体的手性( C5 )中心的OH指向左侧。
在糖中,糖的线性和环状半缩酮或半缩醛平衡存在;线性形式的糖可以经历酮-烯醇互变异构。
这发生在醛糖和酮糖形式之间的相互转化过程中。
07 第七章 有机化学反应的基本问题

第二部分有机化学反应一、全面了解有机化合物的化学性质1.认识并掌握基本反应类型。
2.认识并掌握基本反应历程。
3.全面认识反应活性、选择性、立体化学规律。
4.设计简单的合成路线。
(不作要求)5.掌握重要化合物的鉴别反应。
二、关于有机化合物的反应1.每种类型的有机化合物都能发生什么类型的反应?——第二、三、四章已经初步讲解2.这些反应都有什么具体特点?反应条件如何?反应快慢如何?反应如果有多种可能,应该朝哪个方向进行?选择性如何?会不会形成立体异构的产物?1)热力学的问题:反应能否进行以及反应程度。
2)动力学的问题:反应速率如何,活性与选择性。
3)立体化学的问题:反应的立体化学特征。
三、基本的学习要求1.给出反应物和条件,能准确写出产物。
2.给出反应物和产物,能准确给出反应所需要的反应条件。
3.给出产物和反应条件,能正确地写出反应物。
4.给出完整的反应方程式,能提出合理的反应机理。
5.能分析不同反应物和试剂的反应活性。
6.能利用这些反应设计合理的合成路线。
(不作要求)第七章有机化学反应的基本问题(Basic Problems of Organic Reactions)7.1 键的解离能与反应中的焓变(热效应)1.成键——放能;断键——吸能。
2.化学键的均裂与异裂:均裂和异裂所需要的能量有所不同的,而且异裂反应往往在溶液中进行,受溶剂作用的影响很大。
本章着重讨论均裂反应——烷烃的自由基卤代反应。
HӨ)。
3.一般将键的均裂所需要的能量称为键的解离能(△d4.如果在某一个反应中,形成化学键所释放的能量大于断裂原有化学键所需要的能量,则总反应表现为放热反应;反之则为吸热反应。
5.焓变(Enthalpy change ):等压条件下系统变化的热效应,记为∆ H 。
1)焓变是一个容量函数,与物质的量成正比。
2)焓变是状态函数,与温度、压力有关。
通常采用标准状态下的摩尔焓变(△HӨ)值来分析体系变化的热效应。
3)反应的焓变可以实验测定,也可以通过键的解离能(表7-1)或平均键能(表7-2)计算得出。
第七章配位聚合

第七章配位聚合一、名称解释配位聚合:指单体分子首先在活性种的空位处配位,形成某些形式(σ-π)的配位络合物。
随后单体分子插入过渡金属(Mt)-碳(C)中增长形成大分子的过程,所以也可称作插入聚合。
络合聚合:与配位聚合的含义相同,可以互用。
络合聚合着眼于引发剂有络合配位能力,一般认为配位聚合比络合聚合意义更明确。
定向聚合:也称有规立构聚合,指形成有规立构聚合物的聚合反应,配位络合引发剂是重要的条件。
异构体:分子式相同,但原子相互联结的方式或顺序不同,或原子在空间的排布方式不同的化合物叫做异构体。
构象异构:由单键内旋转造成的立体异构现象。
立体构型异构:原子在大分子中不同空间排列所产生的异构现象。
对映异构:又称手性异构,由手性中心产生的光学异构体R型和S型。
顺反异构:由双键引起的顺式和反式的几何异构,两种构型不能互变。
全同立构:将碳-碳主链拉直成锯齿形,使处在同一平面上,取代基处于平面的同侧,或相邻手性中心的构型相同。
间同立构:若取代基交替地处在平面的两侧,或相邻手性中心的构型相反并交替排列,则称为间同立构聚合物。
全同聚合指数:一致立构规整度的表示方法,指全同立构聚合物占总聚合物的分数。
立构规整度:立构规整聚合物占聚合物总量的百分数。
二、选择题1. 氯化钛是α-烯烃的阴离子配位聚合的主引发剂,其价态将影响其定向能力,试从下列3种排列选出正确的次序( A )A TiCl3(α,γ,δ) > α- TiCl3-AlEtCl2>TiCl4B TiCl2>TiCl4>TiCl3(α,γ,δ)C TiCl4>TiCl3(α,γ,δ) > TiCl22. 下列聚合物中哪些属于热塑性弹性体(d和e)(a) ISI (b)BS (c) BSB (d)SBS (e) SIS3. 下列哪一种引发剂可使乙烯、丙烯、丁二烯聚合成立构规整聚合物?(1)n-C4H9Li/正己烷(2)萘钠/四氢呋喃(3) TiCl4-Al(C2H5)3(4) α- TiCl3-Al(C2H5) 2Cl(5)π-C3H5NiCl (6) (π-C4H7)2Ni4. 下列哪一种引发剂可使丙烯聚合成立构规整聚合物?(D)(A)n-C4H9Li/正己烷(B)萘钠/四氢呋喃(C) TiCl4-Al(C2H5)3(D) α- TiCl3-Al(C2H5) 2Cl三、简答题1. 聚乙烯有几类?如何合成?结构与性能有什么不同?与生产方法有何关系?答:聚乙烯主要有三类:低密度聚乙烯(LDPE),高密度聚乙烯(HDPE),线形低密度聚乙烯(LLDPE)。
智慧树知道网课《有机化学(中国农业大学)》课后章节测试满分答案

第一章测试1【单选题】(10分)提出杂化轨道理论的科学家是:A.鲍林B.拜尔C.范特霍夫D.凯库勒2【单选题】(10分)有机物中碳的杂化态有几种:A.3种B.1种C.4种D.2种3【单选题】(10分)有机物中的π-键的描述正确的是:A.可自由旋转B.有机物结构中的所有化学键可同时为π-键C.不能自由旋转D.键能高于σ键,易发生化学反应4【单选题】(10分)苯的熔点和沸点比环己烷高,从分子间作用力的角度解释,哪条正确:A.苯是极性分子B.苯的分子量大,色散力大C.苯分子间有氢键作用D.苯分子间色散力大5【单选题】(10分)有机分子的极性取决于:A.键能B.键级C.键长D.分子对称性6【单选题】(10分)在醛酮分子中,碳-氧双键中的电性效应为:A.诱导效应和共轭效应B.超共轭效应C.诱导效应D.共轭效应7【单选题】(10分)甲基自由基的中心原子的杂化态为A.sp4B.spC.sp3D.sp28【单选题】(10分)乙醇生成乙醚的反应属于:A.均裂反应B.消除反应C.缩合反应D.氧化还原9【单选题】(10分)丁烷有两个异构体正丁烷和异丁烷,此处的异构体含义为:A.构像异构B.官能团异构C.构型异构D.构造异构10【单选题】(10分)有机物中C-C键的自由旋转,产生异构为:A.构造异构B.镜像异构C.官能团异构D.构像异构第二章测试1【单选题】(10分)烷烃分子结构中连有氢数目最多的碳是:A.伯碳B.季碳C.仲碳D.叔碳2【单选题】(10分)丁烷的典型构像中,能量最高者为:A.部分交叉构像B.全交叉构像C.全重叠构像D.部分重叠构像3【单选题】(10分)影响烷烃熔点和沸点的根本性的原因是:A.分子间取向力的大小B.分子间紧密堆积的程度C.分子间色散力大小D.分子的对称性4【单选题】(10分)在烷烃的卤代反应中,碘代反应很少的原因是:A.碘单质价格昂贵B.选择性太差C.剧烈放热,难于控制D.反应吸热,难以进行5【单选题】(10分)下列自由基最不稳定的是:A.乙基自由基B.叔叔丁基自由基C.异丙基自由基D.苄基自由基6【单选题】(10分)环丙烷的分子构型特征为:A.C-C键可以自由旋转B.C-C键的杂化轨道重叠程度比开链烷烃小C.碳为sp3杂环态D.C-C键的强度与开链烷烃中接近7【单选题】(10分)下列特征不是环己烷椅式构象特征的是:A.骨架碳构成两个平行的平面B.骨架上的氢分为直立氢和平伏氢两类C.骨架上十二个氢性质相同D.中间四个碳构成一个平面,两端的碳位于平面两侧8【单选题】(10分)下列取代环己烷存在优势构像的是:A.顺1甲基-2-乙基环己烷B.反1,3-二甲基环己烷C.顺1,2-二甲基环己烷D.顺1,4-二甲基环己烷9【单选题】(10分)1,2-二甲基环丙烷与Br2反应,生成的主要产物为:A.AB.CC.DD.B10【单选题】(10分)下列烷烃发生一氯代反应,只能生成一种产物的是:A.CB.DC.D.B第三章测试1【单选题】(10分)乙烯分子的结构特征为:A.为平面分子B.结构中有一条π键,一条σ键C.碳原子显示电正性D.是极性分子2【单选题】(10分)按照次序规则,最大的原子或基团是:A.乙炔基B.C.乙烯基D.Cl3【单选题】(10分)含四个碳的开链单烯烃的所有构造异构体数目是:A.3个B.5个C.7个D.4个4【单选题】(10分)下列碳正离子最为稳定的是:A.B.C.D.5【单选题】(10分)下列分子命名需要使用Z/E命名法的是:A.B.C.D.6【单选题】(10分)下列结构能使溴水褪色的是:A.B.C.D.7【单选题】(10分)烯烃的臭氧化还原反应中,还原剂是:A.锌粉B.铁粉C.铝粉D.氢气8【单选题】(10分)双烯合成反应属于:A.氧化反应B.协同反应C.自由基反应D.亲电加成9【单选题】(10分)能与丁烯二酸酐反应的底物是:A.B.C.D.10【单选题】(10分)烯烃的α-氢卤代反应:A.产物符合马氏规则B.产物是反马氏规则的C.为亲电加成反应D.为自由基反应第四章测试1【多选题】(10分)1.判别下列化合物那些有芳香性()A.1B.7C.3D.2E.4F.6G.52【单选题】(10分)2.下列化合物中苯环上电子云密度低于苯的是()A.苯甲醛B.苯胺C.苯酚D.苯甲醚3【单选题】(10分)3.下面碳正离子中存在的共轭效应有(不考虑超共轭)()A.p- 共轭B.⎛-p共轭C.- 共轭D.- 和p- 共轭4【单选题】(10分)下列分子中能形成分子内氢键的是()A.间硝基苯酚B.邻羟基苯甲酸C.对硝基苯酚D.对羟基苯甲酸5【单选题】(10分)乙基苯在光照条件下进行氯化,一氯代产物中的主要产物是()A.DB.BC.CD.A6【单选题】(10分)甲苯卤代得苄基氯应属于什么反应()A.亲核取代反应B.游离基反应C.亲电取代反应D.亲电加成反应7【单选题】(10分)下列化合物进行硝化反应时最容易的是()A.硝基苯B.甲苯C.氯苯D.苯8【单选题】(10分)下列化合物不能被酸性KMnO4作用下氧化成苯甲酸的是()A.乙苯B.叔丁苯C.环己基苯D.甲苯9【单选题】(10分)下列化合物中能进行付克烷基化的是()A.CB.DC.AD.B10【单选题】(10分)下列化合物进行亲电取代反应时,新引入的取代基进入原取代基间位的是()A.BB.AC.DD.C第五章测试1【多选题】(10分)下列Fischer投影式中,哪个是同乳酸分子一样的()A.BB.CC.AD.D2【单选题】(10分)化合物的构型是()A.2R,4EB.2S,4ZC.2R,4ZD.2S,4E3【单选题】(10分)Fischer投影式是R型还是S型?下列各结构式中哪些同上面这个投影式不是同一化合物?()A.DB.AC.CD.B4【单选题】(10分)下列化合物无旋光性的是()A.B.C.D.5【单选题】(10分)与的关系是()A.相同化合物B.对映异构体C.互变异构体D.非对映异构体6【单选题】(10分)下列化合物具有手性的是()A.DB.AC.BD.C7【单选题】(10分)下列化合物中无旋光性的是()A.CB.AC.DD.B8【单选题】(10分)薄荷醇理论上所具有的立体异构体数目应为()A.2种B.4种C.16种D.8种9【单选题】(10分)左旋仲丁醇和右旋仲丁醇的下列参数中,哪一项是不同的()A.比旋光度B.溶解度C.熔点D.沸点10【单选题】(10分)判断下述分子中存在的对称因素:()A.有对称中心B.有对称轴C.有两个对称面D.有一个对称面第六章测试•第1部分•总题数:101【单选题】(10分)化合物的系统命名是A.4—氯戊烷B.2—氯戊烷C.2—甲基—1—氯丁烷D.4—甲基—4—氯丁烷2【单选题】(10分)化合物的系统命名是A.1—甲基—3—氯环己烯B.1—甲基—5—氯环己烯C.1—氯—3—甲基环己烯3【单选题】(10分)判断下列卤代烃与NaCN在DMSO溶剂中反应(S N2)的活性顺序最快的是()A.AB.CC.B4【单选题】(10分)下列卤代烃进行亲核取代反应活性最强的是A.4—氯—1—戊烯化合物B.2—氯丙烷C.氯乙烯D.苄氯5【单选题】(10分)比较下列化合物与AgNO3反应速率,最快的是A.B.C.D.6【单选题】(10分)下列化合物属于叔卤代烃的是()A.BB.AC.DD.C7【单选题】(10分)反应的主产物是:A.B.C.D.8【单选题】(10分)可选用下列哪种试剂鉴别3-溴-2-戊烯和4-溴-2-戊烯?A.溴水B.Lucas试剂C.AgNO3/EtOH溶液D.KMnO4溶液9【单选题】(10分)反应的主产物是:A.B.C.D.10【单选题】(10分)反应的主产物是:A.B.C.D.第七章测试1【单选题】(10分)下列化合物酸性最强的是A.H2OB.C.CH3CH2OHD.2【单选题】(10分)下列醇与金属Na反应,活性最大的是A.甲醇B.异丙醇C.乙醇D.叔丁醇3【单选题】(10分)化合物在强酸催化下进行分子内脱水反应,生成的主要产物是A.B.C.D.4【单选题】(10分)化合物的正确命名是A.Z-1-羟基-3-戊烯B.Z-3-戊烯-1-醇C.E-3-戊烯-1-醇D.E-1-羟基-3-戊烯5【单选题】(10分)反应的主产物是A.B.C.D.6【单选题】(10分)下列化合物中沸点最高的是A.正己醇B.氯己烷C.正己烷D.乙醚7【单选题】(10分)可以用来鉴别苄醇,乙醇和异丙醇的试剂是A.Tollen试剂B.Lucas试剂C.硫酸D.硝酸银的乙醇溶液8【单选题】(10分)下列化合物属于伯醇的是A.CB.AC.DD.B9【单选题】(10分)下列化合物中酸性最强的是A.2-甲基苯酚B.2-硝基苯酚C.2,4,6-三硝基苯酚D.2,4-二硝基苯酚10【单选题】(10分)化学反应的主产物是A.化学反应的主产物是B.C.D.第八章测试1【单选题】(10分)下面结构的正确的系统命名是?A.6-异丙基-4-辛酮B.1,1-二甲基-4-庚酮C.异丁基丙基酮D.2-甲基-5-庚酮E.7-甲基-4-辛酮2【单选题】(10分)下面哪个结构式代表了环己酮和它的互变异构体?A.IVB.IC.IIID.IIE.V3【单选题】(10分)简单的烯醇要比酮式异构体不稳定,原因是?A.烯醇中的碳碳双键没有酮中的碳氧双键稳定B.在烯醇式结构中存在较大的张力C.烯醇不是手性的D.在酮式结构中有更少的原子是共平面的E.实际上,简单的烯醇更稳定4【单选题】(10分)下面哪个试剂能完成下面的转化?A.全部都能B.Pt/H2C.LiAlH4,乙醚D.Zn(Hg),HCl,回流5【单选题】(10分)把HCl气体通入戊醛的甲醇溶液将形成下面哪个化合物?A.。
华中科技大学有机化学第七章对映异构现象
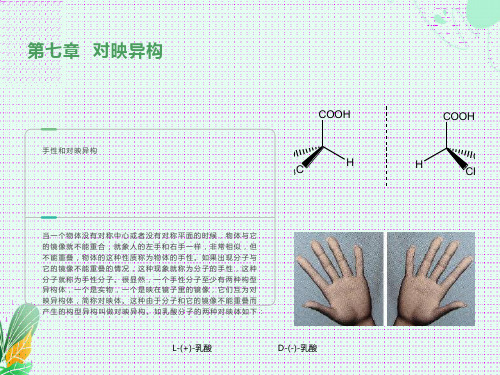
D-(+)-甘油醛 L-(-)-甘油醛
02
单击此处添加小标题
(-)-β-溴乳酸 D-(-)-乳酸
03
单击此处添加小标题
其它的旋光化合物的构型以甘油醛为标准比较得到。凡是由D-甘油醛通过化学反应得到的化合物或可转变为D-甘油醛的化合物,只要在转变过程中原来的手性碳原子构型不变,其构型即为D型。同样,与L-甘油醛相关的即为L型。例如:
左旋酒石酸 右旋酒石酸 内消旋酒石酸 (-)-酒石酸 L-(+)-酒石酸 meso-酒石酸
01
02
L-(+)-酒石酸为天然产物,D-(-)-酒石酸是人工合成的,它们两个互为对映体,有相同的熔点(170oC), 在120毫升水中都只能溶解139克,酸性强度也相同,比旋光度大小相同,方向相反。 虽然内消旋体和外消旋体都没有旋光性,但它们的物理性能和化学性能有很大区别,它们与D或者L酒石酸对映体的性能也完全不同。 内消旋体是一个单一分子,由于分子内有一个对称平面而没有旋光性;而外消旋体是两个对映体的等量混合物,旋光度相互抵消而不具有旋光性,可以再分离为两个旋光度相反的化合物。 从理论上讲,凡含有两个相同的不对称碳原子的化合物都有三种立体异构体,一对对映体和一个内消旋体。
2-氨基丙酸
腺嘌呤的互变异构
腺嘌呤的互变异构1.引言1.1 概述腺嘌呤是一种重要的有机化合物,在生物体中起着关键的生理功能。
它是核苷酸的组成部分,与DNA和RNA的合成密切相关,也参与了多种细胞代谢过程。
腺嘌呤分子结构特殊,存在多种异构体,并且这些异构体之间能够通过互变异构的方式相互转化。
本文将深入探讨腺嘌呤的结构和性质,以及腺嘌呤的异构体及其互变异构过程。
首先,我们将对腺嘌呤的化学结构进行详细解析,包括分子式、键合方式等方面的内容。
同时,对腺嘌呤的物理性质也将进行阐述,包括其溶解性、熔点等方面的特性。
通过对腺嘌呤的结构和性质的全面了解,我们可以更好地理解其在生物体中的功能和作用。
随后,将重点介绍腺嘌呤的异构体及其互变异构过程。
腺嘌呤的异构体主要包括亮氨酸和异亮氨酸两种形式,它们在结构上存在微小的差别,但对生物体的影响却是有着显著差异的。
这些异构体之间能够通过互变异构的方式相互转化,这种转化过程是一个动态平衡的过程,受到多种因素的调控和影响。
我们将详细讨论这些影响因素,并探究它们对腺嘌呤互变异构的具体作用机制。
最后,在结论部分,我们将总结腺嘌呤的互变异构过程及其重要性。
通过深入研究腺嘌呤的互变异构,我们可以更好地理解其在生物体中的作用机制,并为未来的研究提供启示和方向。
同时,我们也将探讨腺嘌呤互变异构在药物设计和生物工程领域的应用前景,并提出未来研究的重点和方向。
通过本文的撰写,我们希望能够为读者提供对腺嘌呤互变异构的全面认识,并为相关领域的研究和应用提供有益的参考。
希望读者通过本文的阅读,能够对腺嘌呤的互变异构有更清晰的认识,从而为未来的研究和应用做出更有价值的贡献。
1.2 文章结构文章结构部分的内容可能包括以下内容:文章结构部分旨在介绍整篇文章的章节组成和各章节的内容安排。
该部分不仅可以帮助读者快速了解文章的大致框架,还能引导读者在阅读过程中有一个清晰的思路。
本文主要分为引言、正文和结论三个部分。
首先,引言部分将简要介绍腺嘌呤的互变异构这一主题的背景与意义。
化学反应中的异构化反应与异构化机理
化学反应中的异构化反应与异构化机理化学反应是物质转变的过程,其中包含着各种各样的反应类型。
其中,异构化反应是一类常见而重要的反应类型,指的是分子结构的未改变下,其构型或立体结构发生改变的反应过程。
这种反应不仅在有机化学中普遍存在,也可以在无机化学和生物化学中观察到。
本文将重点探讨异构化反应的机理以及其在化学反应中的重要性。
一、异构化反应的定义与类型异构化反应是指分子结构保持不变,立体结构或构型发生改变的反应过程。
根据反应的不同类型,可以将异构化反应分为构象异构化反应和分子内异构化反应两种。
1. 构象异构化反应构象异构化反应指的是分子结构内部原子的相对位置发生改变,从而形成新的构象异构体的反应。
这种反应可以通过键的旋转、键的破裂和重新连接等方式实现。
例如,烷烃的旋转异构化反应就是一种常见的构象异构化反应。
2. 分子内异构化反应分子内异构化反应是指在分子内部原子或官能团的排列可能性发生改变,从而使得分子结构发生变化的反应。
这种反应通常涉及共轭烯烃的互变异构化反应、环反应和位异构化反应等。
二、异构化反应的机理异构化反应的机理通常与反应前后的分子构象有关。
在构象异构化反应中,由于化学键的旋转、键的破裂和重新连接等变化,分子的构象发生改变。
而在分子内异构化反应中,通常存在反应物分子内部原子或官能团的位置可能性变化,从而使得分子构象发生转变。
在构象异构化反应中,旋转键的破裂和重新连接是最为常见的变化方式。
这种反应可以通过合适的反应条件,如温度、溶剂和催化剂的选择等来促进。
例如,烷烃的旋转异构化反应通常需要高温和金属催化剂的存在。
对于分子内异构化反应,通常存在一些具体的反应机理和路径。
例如,共轭烯烃的互变异构化反应中,通常涉及环的开裂、亲电或亲核试剂的加成以及环的重构等步骤。
这些步骤共同作用导致了分子结构的转变。
三、异构化反应的重要性异构化反应在化学反应中有着重要的地位和作用。
首先,异构化反应可以大大丰富和扩展分子的构象空间,从而增加了分子的多样性和功能性。
有机化学中的酮烯互变异构反应
有机化学中的酮烯互变异构反应酮烯互变异构反应是有机化学中一类重要的转化反应,指的是酮与烯烃之间发生异构变化的过程。
这种反应在有机合成中有广泛的应用,常用于构建有机分子的碳-碳和碳-氧键连接,从而实现复杂分子的合成。
本文将介绍酮烯互变异构反应的机理、应用以及相关的研究进展。
一、酮烯互变异构反应的机理酮烯互变异构反应的机理主要涉及烯烃的π-键与酮中的羰基之间的共轭作用。
一般情况下,酮中的π-电子云与烯烃中的π-电子云形成共轭体系,从而促使酮和烯烃之间的异构变化。
这种共轭作用可以通过酮烯互变异构反应中的过渡态理论来解释,即酮与烯烃之间通过反应活化能最低的中间体进行异构化。
二、酮烯互变异构反应的应用1. 碳-碳键构建:酮烯互变异构反应可以实现碳-碳键的构建,特别是在合成有机分子的过程中。
通过该反应,可以将烯烃与酮连接起来,形成新的碳-碳键,从而扩展有机分子的结构和功能。
2. 碳-氧键构建:酮烯互变异构反应还可以用于构建碳-氧键。
其中一个典型的例子是巴比尔反应,该反应将酮与含氧官能团的烯烃反应,生成含有醚键的产物。
这种反应在天然产物合成和药物合成中有重要的应用。
3. 不对称催化:近年来,酮烯互变异构反应在不对称催化领域的应用得到了广泛的关注。
通过设计合适的手性配体,可以实现酮烯互变异构反应的不对称催化,合成手性酮或烯烃产物。
这种手性酮或烯烃是药物分子和天然产物分子的重要结构单元,对于研究手性药物和生物活性物质具有重要意义。
三、酮烯互变异构反应的研究进展近年来,酮烯互变异构反应的研究取得了许多进展。
其中一个重要的研究方向是发展新的催化剂和反应条件,以提高反应的效率和选择性。
例如,一些金属还原剂和有机光催化剂已被成功应用于酮烯互变异构反应,使得反应的效率和选择性得到显著提高。
此外,一些研究人员还致力于发展不同类型的酮烯互变异构反应。
例如,一些方法可以实现烯烃中不同位置的选择性反应,从而合成具有多个官能团的化合物。
乙酰乙酸乙酯的互变异构现象示教法
乙酰乙酸乙酯的互变异构现象示教法乙酰乙酸乙酯的互变异构现象乙酰乙酸乙酯是一类重要的有机化合物,在有机化学中具有重要的应用价值。
它们通常以各种形式存在,具有易异构性,可以通过变温、加压、紫外照射等方式发生互变异构反应。
互变异构反应是一种常见的有机反应,其特点是原料物质不改变,但产物的构型却发生了变化。
有机化合物中的互变异构反应是指通过改变温度、加压或紫外照射等因素,使有机物质中的分子结构发生改变,从而产生新的分子结构,从而产生新的有机物质。
乙酰乙酸乙酯可以在苯胺-乙醇体系中发生互变异构反应。
当温度升高或加压时,乙酰乙酸乙酯中的乙酰基可以脱水而形成乙酰基的活性亚甲基碳中心,乙酰基的正电荷会对这个活性中心产生电子屏蔽作用,这时乙酰基便可以通过氢键方式与苯胺分子中的氨基结合,形成新的异构体。
乙酰乙酸乙酯也可以通过紫外照射来发生互变异构反应。
在一定的紫外光强度下,乙酰乙酸乙酯中的碳-氢键可以被射线破坏,乙酰基就会形成活性亚甲基碳中心,然后与苯胺分子中的氨基结合,形成新的异构体。
乙酰乙酸乙酯的互变异构现象是一种常见的有机反应,也是有机化学研究的重要内容,它可以为有机合成提供新的方法。
因此,要正确理解互变异构反应,首先要研究乙酰乙酸乙酯的互变异构现象,了解其反应模式及机理,从而为有机合成提供参考。
乙酰乙酸乙酯的互变异构现象,可以通过实验来示教。
首先,用烧瓶加入苯胺和乙醇,搅拌均匀,然后加入适量的乙酰乙酸乙酯混合物,搅拌均匀,加热至反应温度,观察反应物的变化情况,并用分光光度计测定产物的含量。
然后,改变反应温度、加压或紫外照射,观察反应物是否有变化,用分光光度计测定新产物的含量,从而得出互变异构反应的结果。
通过实验,可以更加直观地了解乙酰乙酸乙酯的互变异构现象,进而让学生更好地理解有机反应的机理,为有机合成提供新的方法。
因此,乙酰乙酸乙酯的互变异构现象示教既可以让学生更好地理解有机反应,也可以为有机合成提供参考。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
B + C=C OH
H C
C O
B
C=C OH
这一历程表示,失去质子和得到质子是分步进行的。一般酸性较强的 物质或在极性强的溶剂中,有利于这一历程进行。
在酸催化下,则是借助“O”的质子化来催化进行的
H C C O +H
+
H C C OH
+
C C OH + H
+
2、双分子质子移变历程
历程:
R CH CH CH R' + SOCl2 OH R CH CH CH R' O O S Cl RCH CH CH R' + SO 2 Cl
对于环状化合物来说,用SOCl2处理,除发生分子内移变外,顺反异构仍然保持:
OH Cl CH3 H CH3 H H
OH Cl H CH3 H H CH3
历程:
CH2=CHCH2COO
-
CH3CH=CHCOO
-
第二节 互变异构转变历程和类型
正离子移变 :分子中原子或原子团以正离子形式发生转移,这种过程 称正离子移变。 负离子移变:分子中的原子或原子团以负离子形式发生转移,这种过 程称负离子移变。 一、质子移变历程 1、单分子质子移变历程
B+ H C C O _ + HB + C C O
(主要,稳定)
OH
-
(次要,不稳定)
O CH CH C CH CH2CH3 O
CHO +
O
CH3 C CH=CH CH3
OH
-
CH CH CH CH C CH3
(主要)
第四节 与酮-烯醇互变异构相关的互变异构
1、三碳系:
C C C H C C H C
(双键位移)
2、硝基-酸式硝基系
O N O C H O N OH C
化合物
CH3COCH(CH3)COOEt CH3COCH(Et)COOEt C CH3COCH(C6H5)COOEt C6H5COCH2COOEt C6H5COCH(Et)COOEt HCOCH(COOEt)2 D CH3COCH(COOEt)2 C2H5COCH(COOEt)2
烯醇的含量,%
4 3 30 21 4 94 69 44
一、三碳系(双键位移)
H C C C H C
-
C
C
CH3 CH CH COOH
OH CH2 CH CH COOH 0 100C
(98%,共轭)
(2%)
CH3
CH2 CH2 CH CH C N
EtO
-
CH3
CH2 CH CH CH2 C N
(86%,共轭)
(14%)
二、亚硝基-异亚硝基(肟)互变异构
CH C CH R' [B] O
-
当有过量酮存在下,则是平衡控制产物
动力学控制易生成取代较少的烯醇,而平衡控制则有利于生成取代 基较多的产物;前者因为空间位阻小,后者由于生成的烯醇更稳定 :
表: 烯醇式混合物的组分
混合物
O CH3 CH3
产物1
O
-
产物2
O CH3
-
动力学 热力学
O
28 94
O
-
72 6
R CH N C R' R' R'' EtO
-
R CH N R' CH
R' R''
当化合物酸性很弱时,物质不能象上述的历程那样出现负离子,而是 质子由一个位置转移到另一个位置是协同进行的。
EtO
-
DOEt
EtOH R
EtO
-
R H R'' C N C R' R'''
R'' C N CD R'''
R'
O O COOEt O COCH3 CHO O
0.02 7.4 29 48
从上表分析得出以下结论: 1、平衡状态下,丙酮以及其它简单酮几乎全部以酮式存在,如丙 酮、 环戊、环己酮等。
2、在表A部分中,当丙酮中H被羧乙酯(-COOEt)取代时,含 量增加;若被乙酰基取代,增加的幅度更大(表B部分)。 a、羧乙酯基或乙酰基的吸电子效应,使α -碳上氢酸性增强,有 利于烯醇式平衡产物的生成, b、β 二酮及β -二酯类的烯醇式烯醇是由于形成分子内氢键及 碳碳双键与碳基共轭而稳定。
第七章
互变异构与双重反应性
第一节 概 述
一、互变异构
又称平衡异构现象,即在室温下,不同官能团异构体处于动态平衡, 能很快的相互转变,是一种特殊的官能团异构。1885年,有化学家拉尔 (Laar)第一个提出这个术语。
二、互变异构和同分异构间的界限
CH3 CH2CH2Br 250C
0
CH3CHCH3 Br
次要
OH PhCH C CHCH3
次要
主要
2、烯醇式混合物组分的动力学和热力学控制 动力学控制:产物的组成受到氢的相对活泼性控制。
O RCH2 Ka OH RCH2 C CHR' [A] [A] = [B] Ka Kb C CH2R' Kb OH RCH C CH2R' [B]
若在〔A〕和〔B〕之间可以建立平衡,即〔A〕、〔B〕可以相互 转化,则建立了平衡控制,即热力学控制 :
C C C X Y
-
C C C X
-
(X=Y or X=Y )
Y
三、分子内历程
R' CH CH CH R O OH O C + C O H R' CH CH CH R HO C O O C O
用取代丙烯醇和亚硫酰氯反应,也可以发生分子内负离子移变:
R CH CH CH R' + SOCl2 OH RCH CH CH R' Cl
C6 H4 C
邻苯二甲酸单酯在酸催化下的互变异构就是分子内的负离子移变。
第三节、酮-烯醇式互变异构
采用库尔特-迈依尔(Kart-Meyer)法可以测定酮化物中烯醇式 含量,常温下,下列酮烯醇式含量如下表: 丙酮 2.5×10-4% 环戊酮 48×10-4% 环己酮 2.5×10-2%
库尔特-迈依尔测定法简介:
OH N C C O H N C OH N H N O C C C C H N C O NH
HO C N C
N H
亚胺醇式
酰胺式
这类一个变化可以用来很好的解释一些反应的产物,如:
CH3 OCH CH 3 Cl + Cl NHNH C R Cl O CH3 OCH CH 3 Cl N Cl O C O N C R
O C Cl
历程:
CH3 OCH CH 3 Cl O NHNH C Cl R Cl CH3 OCH CH 3 Cl NHN C OH R Cl O C Cl
CH3 OCH CH 3 Cl NN C Cl O Cl C OH R
CH3 OCH CH 3 Cl N Cl O C O + HCl N C R
O RCH2 Ka OH RCH2 C CHR' [A] K [A] = K [B] C CH2R' Kb OH RCH C CH2R' [B]
质子催化下的〔A〕、〔B〕之间的相互转化:
R R R R R R R R
C C CH2 R' [A] O
-
+
CH C CH2 R' O
CH C CH2 R' + O
H
O CH3 C CH2
O C CH3
CH3
O C CH
O C
CH 3
3、在C、D、E、F的数据表明,在体系中,烷基的存在,降低烯醇式 的含量。因为R的+I效应。
C CH C O R O or R C CH2 C O O
4、在C和F数据表明,苯基存在有利于烯醇式的生成:由于烯醇和苯环 产生了大共轭体系的原故 5、较大环烯醇含量较高,原因不明。
二、负离子移变过程(转移基团为负离子)
1、单分子历程:
C C C X + C C C X C C C X
特点:形成碳正离子中间体
2、双分子历程
C X C C X
-
C X
-
C
C X
特点:协同历程
3、分子内历程
R CH CH=CH O C C6H4C O R' OH
+
-
R
O
CH
C O
CH
O
CH R' O
第五节
一、单分子历程:
R CH CH CH2 X
负离子移变
R CH CH CH2 X
历程:
R CH CH CH2 X R [CH CH CH2 ] X
+
R CH CH CH2 X
例如
OH CH2 200C OH
0
CH2
例如:
O CH2 OCCH3
0
O OCCH3 25C CH2
例如:
C6H5 CH CH CH2 OCOCH3 C6H5 CH CH CH2OCOCH3
CH N O C N OH
在脂肪族亚硝基混合物中几乎全部是肟式结构,也就是说,脂肪醛和 酮肟,不会转化为亚硝基混合物,但在芳香族混合物中,则是一个平衡体 系:
NO N OH
OH
O
光谱实验证明:固态时为醌式结构,而溶液时为两种异构体的平衡产物, 但在这种互变异构体中,与烯醇式不同的是,平衡总是偏向于肟这一边 。
