铁盐和亚铁盐的鉴别及其转化
合集下载
铁盐和亚铁盐的检验和转化(课件PPT)

11、学会学习的人,是非常幸福的人。——米南德 12、你们要学习思考,然后再来写作。——布瓦罗14、许多年轻人在学习音乐时学会了爱。——莱杰
15、学习是劳动,是充满思想的劳动。——乌申斯基 16、我们一定要给自己提出这样的任务:第一,学习,第二是学习,第三还是学习。——列宁 17、学习的敌人是自己的满足,要认真学习一点东西,必须从不自满开始。对自己,“学而不厌”,对人家,“诲人不倦”,我们应取这种态度。——毛泽东
低价氧化剂 高价 高价 还原剂 低价
●课前小准备分分类
还原剂
氧化剂
氯水
铁粉
铜粉
vc
双氧水Βιβλιοθήκη KMnO4VC实验二: Fe3+转化为Fe2+
问: Fe3+如何能转化为 Fe
Fe2+ ?
Vc等
问:如何证明已实现了 Fe3+到Fe2+ 的转化?
实验方案: Fe3+转化为Fe2+
1: 1mLFeCl3 +1滴KSCN +几滴VC溶液 2: 1ml FeCl3 + 1滴KSCN溶液+铁粉后振 荡
红了,分析原因?
●抢答学以致用2
【通用名】朴雪口服液 【企业名称】哈药集团制药六厂 【药品成分】 乳酸亚铁、维生素 【功能主治】营养性贫血者。 【贮藏】密封,置遮光阴凉处
QQ此Q验4132:维药::补如人如为生品铁何体何什还素已口用补用么是C经服化铁化补F一完液e学补学血起3全+有方充?的剂服变少法的方要用质量证F法配?e失变明2检合+ 效质?
Fe3+ 氧化性: 2Fe3+ + Fe = 3Fe2+
●抢答学以致用1
15、学习是劳动,是充满思想的劳动。——乌申斯基 16、我们一定要给自己提出这样的任务:第一,学习,第二是学习,第三还是学习。——列宁 17、学习的敌人是自己的满足,要认真学习一点东西,必须从不自满开始。对自己,“学而不厌”,对人家,“诲人不倦”,我们应取这种态度。——毛泽东
低价氧化剂 高价 高价 还原剂 低价
●课前小准备分分类
还原剂
氧化剂
氯水
铁粉
铜粉
vc
双氧水Βιβλιοθήκη KMnO4VC实验二: Fe3+转化为Fe2+
问: Fe3+如何能转化为 Fe
Fe2+ ?
Vc等
问:如何证明已实现了 Fe3+到Fe2+ 的转化?
实验方案: Fe3+转化为Fe2+
1: 1mLFeCl3 +1滴KSCN +几滴VC溶液 2: 1ml FeCl3 + 1滴KSCN溶液+铁粉后振 荡
红了,分析原因?
●抢答学以致用2
【通用名】朴雪口服液 【企业名称】哈药集团制药六厂 【药品成分】 乳酸亚铁、维生素 【功能主治】营养性贫血者。 【贮藏】密封,置遮光阴凉处
QQ此Q验4132:维药::补如人如为生品铁何体何什还素已口用补用么是C经服化铁化补F一完液e学补学血起3全+有方充?的剂服变少法的方要用质量证F法配?e失变明2检合+ 效质?
Fe3+ 氧化性: 2Fe3+ + Fe = 3Fe2+
●抢答学以致用1
亚铁盐与铁盐的相互转化

亚铁盐与铁盐的相互转化
亚铁盐和铁盐是两种常见的铁化合物,在一定条件下,它们可以相互转化。
亚铁盐指的是铁的+2氧化态,例如亚铁离子(Fe2+)。
铁盐包括铁的不同氧化态,如三价铁(Fe3+)的盐,例如三氯化铁(FeCl3)。
在适当的条件下,亚铁盐和铁盐之间可以通过氧化还原反应相互转化。
以下是一些常见的亚铁盐和铁盐的相互转化示例:
1.亚铁盐氧化为铁盐: 2Fe2+ + O2 -> 2Fe3+
在有氧条件下,亚铁盐可以被氧气氧化为三价铁盐。
这是一个电子转移过程,其中亚铁离子(Fe2+)失去电子变为三价铁离子(Fe3+)。
2.铁盐还原为亚铁盐: 2Fe3+ + 2e- -> 2Fe2+
在还原条件下,三价铁盐可以接受电子并还原为二价亚铁盐。
这个反应是亚铁离子(Fe2+)接受电子,将三价铁(Fe3+)还原为二价亚铁(Fe2+)。
需要注意的是,亚铁盐和铁盐的相互转化取决于氧化还原反应的条件和环境。
例如,氧气、光、温度和pH值等因素都可以影响这些反应的进行。
此外,不同的铁化合物可能在不同的条件下发生转化,因此具体的反应条件需要根据具体的化合物和反应进行调整。
铁盐与亚铁盐的检验与转化公开课省名师优质课赛课获奖课件市赛课一等奖课件

返回原处
知识梳理
魔术体验 ①怎样用KSCN法检验补铁剂中旳Fe2+?
课外拓展
②为何琥珀酸亚铁补血剂与维C同服有利于
结束
吸收?
自我检验
魔术欣赏
魔术探密 为了检验某FeCl2溶液是否变质,
魔术解密
可向溶液中加入
( C)
返回原处 知识梳理 魔术体验
A.NaOH溶液 B.铁片
课外拓展 C.KSCN溶液
结 束 D.石蕊溶液
魔术欣赏
检验Fe3+旳措施:
魔术探密 魔术解密
鉴别措施
返回原处 直接观色
知识梳理 加NaOH溶液
Fe3+
棕黄色 立即产生红褐色沉淀
魔术体验 课外拓展 结束
加KSCN溶
红色
液
具有Fe3+旳溶液,滴加KSCN,溶液
变红
。
KSCN是检验旳Fe3+旳特效试剂。
探究试验一 Fe2+怎样转化为Fe3+
魔术欣赏 魔术探密 魔术解密
魔术探密 氢氧化钠溶液
魔术解密
返回原处
知识梳理 魔术体验 课外拓展 结束
2ml FeCl3
Fe(OH)3 沉淀
反应原理: Fe3+ + 3OH-== Fe(OH)3 ↓
试验探究2:KSCN法(硫氰化钾)
魔术欣赏 魔术探密 魔术解密
KSCN溶液
返回原处
知识梳理 FeCl3 溶液
魔术体验
课外拓展
结束
[观察现象]: 溶液呈现红色。
子?
课外拓展
结束
魔术欣赏 魔术探密 魔术解密 返回原处 知识梳理 魔术体验 课外拓展 结束
Fe3+与Fe2+旳检验 和转化
知识梳理
魔术体验 ①怎样用KSCN法检验补铁剂中旳Fe2+?
课外拓展
②为何琥珀酸亚铁补血剂与维C同服有利于
结束
吸收?
自我检验
魔术欣赏
魔术探密 为了检验某FeCl2溶液是否变质,
魔术解密
可向溶液中加入
( C)
返回原处 知识梳理 魔术体验
A.NaOH溶液 B.铁片
课外拓展 C.KSCN溶液
结 束 D.石蕊溶液
魔术欣赏
检验Fe3+旳措施:
魔术探密 魔术解密
鉴别措施
返回原处 直接观色
知识梳理 加NaOH溶液
Fe3+
棕黄色 立即产生红褐色沉淀
魔术体验 课外拓展 结束
加KSCN溶
红色
液
具有Fe3+旳溶液,滴加KSCN,溶液
变红
。
KSCN是检验旳Fe3+旳特效试剂。
探究试验一 Fe2+怎样转化为Fe3+
魔术欣赏 魔术探密 魔术解密
魔术探密 氢氧化钠溶液
魔术解密
返回原处
知识梳理 魔术体验 课外拓展 结束
2ml FeCl3
Fe(OH)3 沉淀
反应原理: Fe3+ + 3OH-== Fe(OH)3 ↓
试验探究2:KSCN法(硫氰化钾)
魔术欣赏 魔术探密 魔术解密
KSCN溶液
返回原处
知识梳理 FeCl3 溶液
魔术体验
课外拓展
结束
[观察现象]: 溶液呈现红色。
子?
课外拓展
结束
魔术欣赏 魔术探密 魔术解密 返回原处 知识梳理 魔术体验 课外拓展 结束
Fe3+与Fe2+旳检验 和转化
铁盐和亚铁盐的相互转换
• [资料在线] 亚硝酸盐在血液中能与Fe2+反应 生成Fe3+使血红蛋白丧失携氧功能,导致组 织缺氧,最后使呼吸中枢麻痹、窒息死亡。
• [问]发生亚硝酸盐中毒,如何急救?请给出 急救方案
中毒的早期,毒物还在胃内,可以洗胃。呼吸 困难时可以输氧、输液和补充维生素C等。
含铁食品
实验桌上放有一瓶久置的待测液,为验证FeCl2 溶液的变质情况,请同学们利用实验桌上已有
C、H2、CO等
认真观察右图硫酸亚铁溶液的试剂瓶底 部,你觉得是什么?为什么这样子做?
答:底部放的是铁粉。 目的:防止Fe2+被氧化成Fe3+
Fe+2Fe3+=3Fe2+
• 硫酸亚铁片 【主要成分】乳酸亚铁、维生素C
维生素C作用是:作还原剂。
使较难被吸收的三价铁 还原为易吸收的二价铁, 促进肠道内铁的吸收。
的实验试剂及仪器进行鉴别,并完善以下猜测:
猜测1:溶液没有变质,没有 离子,其使用的试剂
是
,现象为
。
猜测2:溶液已变质,含有 离子,其使用的试剂
是
,现象为
。
猜测3:溶液已部分变质,含有 、 离子,其使用的
试剂及顺序是
,现象为
。
阅读:资料卡片——铜盐
图 3-21 出土的古代铜制品上往往覆盖着一层 铜绿[主要成分是Cu2(OH)2CO3]
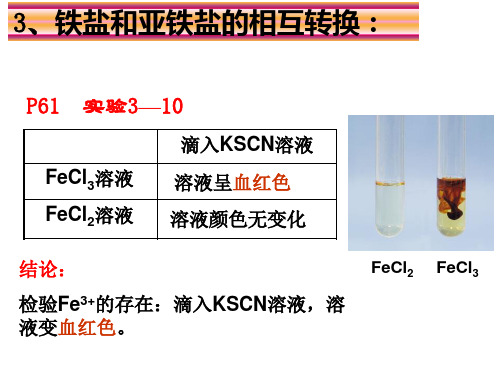
3、铁盐和亚铁盐的相互转换:
P61 实验3—10
滴入KSCN溶液
FeCl3溶液 FeCl2溶液
溶液呈血红色 溶液颜色无变化
结论:
检验Fe3+的存在:滴入KSCN溶液,溶 液变血红色。
FeCl2
FeCl3
铁盐与亚铁盐教学设计

从实验中寻找答案
让学生带着好奇心
进行下面知识的学习。
让学生亲自动手实验,通过观察实验现象,得出实验结论,体会化学学科的奥秘。
培养学生归纳整理实验现象,动手能力
培养学生归纳总结能力
让学生亲自动手实验,通过观察实验现象,得出实验结论,体会化学学科的奥秘。
让学生觉得学化学的趣味性
通过应用的讲解,使学生体会到化学学科的特点,从生活中走向化学,再从化学回到生活。
【总结提问】
通过实验探究,得出结论:Fe2+转化为Fe3+需要加入氧化剂,那么发过来,Fe3+如何转化为Fe2+呢?
【演示实验2】
在FeCl3和KSCN的混合溶液中加入Fe粉,振荡试管。
【提问】
还有什么还原剂也可以实现Fe3+到Fe2+的转化呢?
可提供的试剂:
维C溶液、Cu粉、KI溶液
【总结】
Fe3+转化为Fe2+需要加入还原剂
四、教学过程
教学环节
教师活动
学生活动
设计意图
【板块1】
导入课题
魔术—
茶水的颜色变化
【板块2】
温故知新
提出Fe3+的检验方法的
【板块3】
铁盐和亚铁盐相互转化
1.Fe3+→Fe2+
2.Fe2+→Fe3
【板块4】
铁盐和亚铁盐的应用
【板块5】
课程收获
【板块6】
揭秘魔术
【板块7】
拓展应用
【板块8】
魔术祝福
【表演魔术】
观看视频:切苹果实验
通过本节课所学知识解释生活常识
听老师讲解,丰富知识。
积极思考,归纳总结
让学生带着好奇心
进行下面知识的学习。
让学生亲自动手实验,通过观察实验现象,得出实验结论,体会化学学科的奥秘。
培养学生归纳整理实验现象,动手能力
培养学生归纳总结能力
让学生亲自动手实验,通过观察实验现象,得出实验结论,体会化学学科的奥秘。
让学生觉得学化学的趣味性
通过应用的讲解,使学生体会到化学学科的特点,从生活中走向化学,再从化学回到生活。
【总结提问】
通过实验探究,得出结论:Fe2+转化为Fe3+需要加入氧化剂,那么发过来,Fe3+如何转化为Fe2+呢?
【演示实验2】
在FeCl3和KSCN的混合溶液中加入Fe粉,振荡试管。
【提问】
还有什么还原剂也可以实现Fe3+到Fe2+的转化呢?
可提供的试剂:
维C溶液、Cu粉、KI溶液
【总结】
Fe3+转化为Fe2+需要加入还原剂
四、教学过程
教学环节
教师活动
学生活动
设计意图
【板块1】
导入课题
魔术—
茶水的颜色变化
【板块2】
温故知新
提出Fe3+的检验方法的
【板块3】
铁盐和亚铁盐相互转化
1.Fe3+→Fe2+
2.Fe2+→Fe3
【板块4】
铁盐和亚铁盐的应用
【板块5】
课程收获
【板块6】
揭秘魔术
【板块7】
拓展应用
【板块8】
魔术祝福
【表演魔术】
观看视频:切苹果实验
通过本节课所学知识解释生活常识
听老师讲解,丰富知识。
积极思考,归纳总结
铁盐和亚铁盐的检验和转化

普通高中《化学1》(人教版)第三章 第二节
铁盐和亚铁盐
检验和转化
温故旧知
氧化还原反应
价态规律
转换规律
最高价: 氧化性 最低价: 还原性 中间价: 氧化、还原性
低价氧化剂 高价 高价 还原剂 低价
●课前小准备分分类
还原
双氧水
KMnO4
VC
学习目标
1、通过实验学会Fe3+和Fe2+的检验方法。
●抢答学以致用1
问题情景:小明在用实验室早先配好的 FeCl2溶液做实验时,却遇到了很多问题, 请帮忙解决。
QQ氰 变的QQ1转2:存红化3:4方向:除:化实如了钾亚法此为去验何,溶铁?溶F此室将e盐分液离液C溶应F析时溶l子中3e液溶如C原,液反滴中液l何2因?溶溶应入F?储?液液e?硫3+
●抢答学以致用2
2、运用氧化还原规律及实验掌握Fe2+和Fe3+ 的相互转化。
FeCl3溶液
FeCl2溶液
KSCN溶液 (硫氰化钾)
Fe3++3SCN-=Fe(SCN)3(红色)
实验一: Fe3+和Fe2+的灵敏检验方法
点滴板中完成 1:2-3滴FeCl3 + 1滴KSCN溶液 2:2-3滴FeCl2 + 1滴KSCN溶液
【通用名】朴雪口服液 【企业名称】哈药集团制药六厂 【药品成分】 乳酸亚铁、维生素 【功能主治】营养性贫血者。 【贮藏】密封,置遮光阴凉处
Q合Q明Q检Q432:维此1::验如F:如为人e生药补何2何什+体素品还铁用用么补C已是口化化补一铁经F服学学血e起补完3液方+的剂服充?全有法方要用的变少证法配? 质量失变效质?
开心交流
铁盐和亚铁盐
检验和转化
温故旧知
氧化还原反应
价态规律
转换规律
最高价: 氧化性 最低价: 还原性 中间价: 氧化、还原性
低价氧化剂 高价 高价 还原剂 低价
●课前小准备分分类
还原
双氧水
KMnO4
VC
学习目标
1、通过实验学会Fe3+和Fe2+的检验方法。
●抢答学以致用1
问题情景:小明在用实验室早先配好的 FeCl2溶液做实验时,却遇到了很多问题, 请帮忙解决。
QQ氰 变的QQ1转2:存红化3:4方向:除:化实如了钾亚法此为去验何,溶铁?溶F此室将e盐分液离液C溶应F析时溶l子中3e液溶如C原,液反滴中液l何2因?溶溶应入F?储?液液e?硫3+
●抢答学以致用2
2、运用氧化还原规律及实验掌握Fe2+和Fe3+ 的相互转化。
FeCl3溶液
FeCl2溶液
KSCN溶液 (硫氰化钾)
Fe3++3SCN-=Fe(SCN)3(红色)
实验一: Fe3+和Fe2+的灵敏检验方法
点滴板中完成 1:2-3滴FeCl3 + 1滴KSCN溶液 2:2-3滴FeCl2 + 1滴KSCN溶液
【通用名】朴雪口服液 【企业名称】哈药集团制药六厂 【药品成分】 乳酸亚铁、维生素 【功能主治】营养性贫血者。 【贮藏】密封,置遮光阴凉处
Q合Q明Q检Q432:维此1::验如F:如为人e生药补何2何什+体素品还铁用用么补C已是口化化补一铁经F服学学血e起补完3液方+的剂服充?全有法方要用的变少证法配? 质量失变效质?
开心交流
铁盐与亚铁盐的性质PPT

亚铁盐的用途
作为补铁剂
亚铁盐可用于治疗缺铁性 贫血,补充人体所需的铁 元素。
作为还原剂
亚铁盐具有较强的还原性, 可用于还原染料、药物等 有机化合物。
作为催化剂
亚铁盐在某些化学反应中 可作为催化剂,促进反应 进行。
03
铁盐与亚铁盐的相互转化
氧化还原反应
铁盐与亚铁盐在溶液中可以通过氧化还原反应相互转化。在氧化剂的作用下,亚铁 盐中的亚铁离子(Fe2+)被氧化成铁盐中的铁离子(Fe3+),反之亦然。
04
铁盐与亚铁盐的检测方法
滴定法
总结词
滴定法是一种通过滴定实验来测定物质 浓度的பைடு நூலகம்法,适用于铁盐和亚铁盐的检 测。
VS
详细描述
滴定法的基本原理是利用化学反应中溶液 浓度的变化引起滴定剂消耗量的变化,通 过滴加标准溶液至反应完全,根据消耗的 滴定剂的量来计算待测物质的浓度。对于 铁盐和亚铁盐的检测,通常采用高锰酸钾 滴定法和重铬酸钾滴定法等。
比色法
总结词
比色法是一种通过比较颜色来测定物质浓度的方法,适用于铁盐和亚铁盐的检 测。
详细描述
比色法的基本原理是利用物质在特定波长下的颜色吸收特性,通过比较标准溶 液和待测溶液的颜色深度,计算待测物质的浓度。对于铁盐和亚铁盐的检测, 通常采用邻菲啰啉比色法等。
分光光度法
总结词
分光光度法是一种通过测量物质对光的吸收程度来测定物质浓度的方法,适用于铁盐和 亚铁盐的检测。
铁盐与亚铁盐的性质
• 铁盐的性质 • 亚铁盐的性质 • 铁盐与亚铁盐的相互转化 • 铁盐与亚铁盐的检测方法 • 铁盐与亚铁盐的分离提纯
01
铁盐的性质
物理性质
01
铁盐和亚铁盐的相互转化

2+ 3+ +2Cl氯水 2Fe + Cl = 2Fe 2) FeCl3溶液(FeCl2) 2 ;
2+ = Cu + Fe2+ Fe 粉 Fe + Cu 3)FeCl2溶液(CuCl2) 。
4.证明某溶液只含有Fe2+而不含 Fe3+的实验方法是( BC ) A、先滴加氯水,再滴加KSCN溶 液后显红色 B、先滴加KSCN溶液,不显红色, 再滴加氯水后显红色 C、滴加NaOH溶液,先产生白色 沉淀,后变灰绿,最后显红褐色 D、只需滴加KSCN溶液 练习
(1)总结Fe3+、Fe2+、铁 单质之间的转化关系 (2)阳光课堂
下一章 远方的 下一
——向前、向前……
【拓展】我们知道血红蛋白中的铁元素是 Fe2+,所以当人体出现缺铁性贫血时,应该 补Fe2+。这是市场上常见的硫酸亚铁补血口 服液。 (1)取一滴药品,稀释,设计实验证明该 药物中铁元素是Fe2+。 (2)用所提供的氧化剂让其迅速变质,并 设计实验方案检验。 (3)本品药物介绍:与维生素C同服可促进 本品的吸收。请解释原因
实 验 药 品 : FeSO4 溶 液 、 KSCN 溶 液 、
KMnO4酸性溶液、3%H2O2溶液
实验现象记录
实验操作 现象 离子方程式
FeCl2+KMnO4
FeCl2+H2O2
溶液先是变 为浅黄色, 加了KSCN后 变为红色,
5Fe2++8H++MnO4-=5Fe3+ + Mn2+ +4H2O 2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常见的氧化剂: Cl2、H2O2、HNO3、KMnO4等
常见的还原剂: 金属单质(Zn到Cu)、S2-、I-等
8
Fe2+和Fe3+的相互转化
3.思考讨论
(1)为什么实验室在配制FeCl2或FeSO4溶液时,通 常还要往溶液中加入铁钉或铁粉? 答:防止Fe2+被氧化成Fe3+ Fe+2Fe3+=3Fe2+ (2)是否可以利用它们氧化性或者是还原性来鉴别 Fe2+和Fe3+呢?
6
Fe2+和Fe3+的相互转化
1.从化合价的角度分析铁盐和亚铁盐的性质
Fe元素常见的三种价态
0
+2
+3
因此: Fe2+ 既有氧化性又有还原性 但是偏重于还原性 Fe3+ 具有氧化性
二者之间 如何进行 转化呢
7
Fe2+和Fe3+的相互转化
2.转化方法
2+ Fe
-e+e-
加氧化剂 加还原剂
3+ Fe
人教版必修①第三章
第二节几种重要的金属化合物
铁盐和亚铁盐的 鉴别及其转化
我们补的是什么呢?
Fe
Fe2+
Fe3+
2
Fe2+和Fe3+的鉴别
1.颜色
溶液的颜色也是类似的 Fe2+:浅绿色
Fe3+:棕黄色
3
Fe2+和Fe3+的鉴别
2.NaOH溶液
在两支试管中分别加入少量的FeCl3 和FeSO4溶液,然 后滴加NaOH溶液
4
Fe2+和Fe3+的鉴别
2.NaOH溶液
Fe3+ : 生成红褐色沉淀 Fe2+ : 生成白色沉淀并立即转变
为绿色,最后变为红褐色
还有其他更简便的方法吗?
5
Fe2+和Fe3+的鉴别
3.KSCN溶液
用2支试管分取少量的FeCl3 和FeSO4溶液,然后滴入 KSCN溶液
结论: Fe2+: 没有明显的现象 Fe3+: 变血红色
9
课堂小结
鉴别方法
直接观察颜色 与KSCN溶液 与NaOH溶液反应
利 用 不变红
白色沉淀迅速变灰绿色 最后呈红褐色
Fe3+
黄色 变红
立即产生红褐色沉淀 Cu被腐蚀溶液变蓝色
与铜片 与淀粉 KI试纸
无明显现象 试纸不变蓝
试纸变蓝
10
