非结构性碳水化合物的测定方法
碳水化合物的分类与糖类的实验检测方法

重点回顾
01 分类
介绍了碳水化合物的分类方法及特点
02 实验检测方法
详细讨论了糖类的实验检测方法
03 代谢途径
分析了碳水化合物在生物体内的代谢途径
进一步研究
作用机制
深入了解碳水化 合物在生物体内
的作用机制
健康指导
指导公众如何更 好地选择和摄入
碳水化合物
开展实验
开展相关实验, 验证碳水化合物
的作用与效果
● 04
第四章 碳水化合物在生物 体内的功能
能量来源
碳水化合物是生物体 内最主要的能量来源。 通过糖酵解和呼吸作 用 产 生 的 AT P 为 生 物 体提供能量。在细胞 内,葡萄糖等碳水化 合 物 分 解 产 生 的 AT P 是细胞进行各种生命 活动的能源之一。
结构材料
纤维素
构成细胞壁的重 要物质
● 05
第五章 糖类与健康
糖类摄入与健康
合理摄入糖类对维持 身体健康很重要,但 过量摄入糖类会导致 肥胖、糖尿病等疾病。 建议每日摄入适量的 糖类,注意饮食的平 衡。
碳水化合物选择与血糖控制
选择低GI食 物
有助于血糖稳定
控制食物量
避免过量摄入
避免高糖饮 食
减少血糖波动
糖类的替代品
人工糖代用品
尿糖检测
尿糖检测是通过检测 尿液中是否含有糖类 物质来判断糖尿病患 者的血糖控制情况。 这种检测方法常用于 医院或个人家庭检测, 通过简单的试纸测试 即可得出初步结论。
还原糖检测
01 还原性
具有还原性的糖类
02 化学反应
还原糖和非还原糖的区别
03 实验操作
实验室中的还原糖检测步骤
酶法检测
《精编》碳水化合物的测定

《精编》碳水化合物的测定碳水化合物是人体重要的能量来源之一,也是构成食物的一种基本营养素。
因此,测定食物中的碳水化合物含量对于了解食物的营养价值以及补充身体所需的能量具有重要意义。
本文将介绍几种常见的测定食物中碳水化合物含量的方法。
1. 布氏液测试法布氏液测试法是一种常用的半定量测定食物中碳水化合物含量的方法。
其原理是利用碳水化合物中含有的还原糖,在加热加强酸条件下还原布氏液中的铜离子(Cu2+),从而生成红色沉淀。
沉淀的颜色和沉淀量与碳水化合物的含量成正比。
此方法的优点是操作简单,不需要特殊仪器,但是误差较大,不能准确测定样品中碳水化合物的含量。
2. 救琼斯试剂法救琼斯试剂法是利用碳水化合物中乙醛、酮等羰基物质与美拉德反应中的救琼斯试剂(3,5-二硝基水杨酸)发生的化学反应来定量测定食物中碳水化合物的含量。
具体操作方法是将样品加入救琼斯试剂中,加热后使样品与试剂充分反应生成紫色化合物,通过比色法测定产生的紫色物质的吸收度来测定碳水化合物的含量。
此方法优点是准确度高,适用于各种食物,但是需要使用紫外可见光谱仪进行测定。
3. 酚硫酸法酚硫酸法是一种常用的定量测定食品中总糖含量的方法,在糖中质量分数最高的成分是葡萄糖,因此可以将定量的总糖量视为碳水化合物含量。
操作方法是将样品加入酚硫酸溶液中,加热后将样品经过稀释,通过比色法测定萘乙二酸磷酸锌对产生的紫色物质的吸收度来测定总糖含量。
此方法优点是简单易行,准确度较高,但是不能区分不同种类的糖类物质的含量。
综上所述,碳水化合物的测定方法有多种,可以根据实际情况选择不同的方法,对食物中的碳水化合物含量进行检测,以了解食物的营养价值,选择合适的食品供给身体所需的能量。
食品中碳水化合物检测项目(科标检测)
GB/T 22221-2008 3 乳糖 GB 5413.5-2010
食品中果糖、葡糖糖、蔗糖、麦芽糖、乳 糖的测定 高效液相色谱法 食品安全国家标准婴幼儿食品和乳品中乳 糖、蔗糖的测定
低聚糖检测项目 序号 检测项目 蔗果三糖 1 低聚果糖 蔗果四糖 蔗果五糖 异麦芽糖 2 低聚异麦芽 异麦芽三糖 糖 潘糖 异麦芽四糖 3 4 5 大豆低聚糖 棉籽糖 水苏糖 离子色谱法 离子色谱法 离子色谱法 离子色谱法 离子色谱法 离子色谱法 离子色谱法 离子色谱法 离子色谱法 选定食品产品中反式低聚半乳糖的测定 ——离子色谱法 品中的聚葡萄糖——离子色谱法 检测方法名称
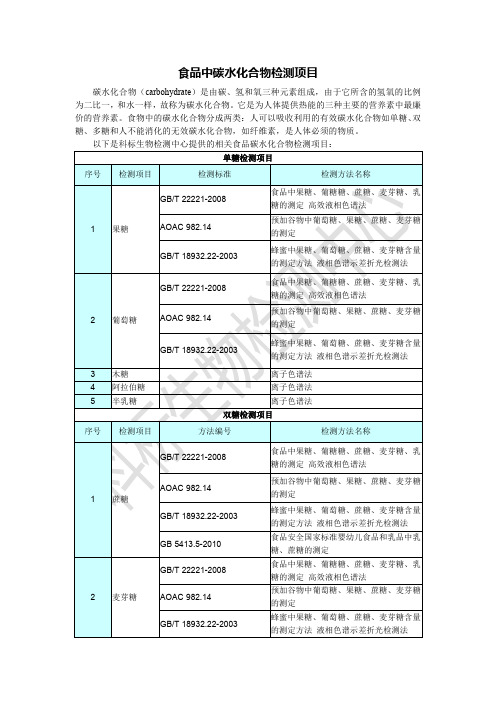
食品中碳水化合物检测项目
碳水化合物(carbohydrate)是由碳、氢和氧三种元素组成,由于它所含的氢氧的比例 为二比一,和水一样,故称为碳水化合物。它是为人体提供热能的三种主要的营养素中最廉 价的营养素。食物中的碳水化合物分成两类:人可以吸收利用的有效碳水化合物如单糖、 双 糖、多糖和人不能消化的无效碳水化合物,如纤维素,是人体必须的物质。 以下是科标生物检测中心提供的相关食品碳水化合物检测项目:
低聚半乳糖 AOAC 2001.02 聚葡萄糖 AOAC 2000.11
膳食纤维检测项目 序号 1 2 3 4 5 检测项目 膳食纤维 总膳食纤维 不溶性膳食纤维 AOAC 991.43 可溶性膳食纤维 膳食纤维 GB/T 22224-2008 方法编号 GB/T 5009.88-2008 检测方法名称 食品中膳食纤维的测定 食品中总膳食纤维、不溶性膳食纤维、可 溶性膳食纤维的测定 酶重量法 MES TRIS 缓冲 食物中的膳食纤维的测定 酶重量法和酶 重量法-液相色谱测定 含有抗性麦芽糊精(简称:RMD)的食物中 6 总膳食纤维 AOAC2001.03 的膳食纤维总量 酶-重量法和液相色谱法 测定 7 8 不溶性膳食纤维 GB 5413.6-2010 不溶性膳食纤维 GB/T 9822-2008 食品安全国家标准婴幼儿食品和乳品中不 溶性膳食纤维的测定 谷物不溶性膳食纤维测定法
碳水化合物的测定

(5) 结果计算
m m2 50 V1 V2 100 1000 100 %
式中ω -----以转化糖计,总糖的质量分数,%; m2-----直接滴定法中10mL碱性酒石酸铜相当于转化糖量, mg,或高锰酸钾法中查表得出相当的转化糖量,mg; m-----样品质量,g; V1-----样品处理液总体积,mL; V2-----测定总糖量取用水解液体积,mL;
5.1 概述 5.2 食品中还原糖的测定 5.3 总糖的测定
滴定必须在沸腾条件下进行
一是可以加快还原糖与的反应速度;二是次甲基蓝 变色反应是可逆的,还原型次甲基蓝遇空气中氧时 又会被氧化为氧化型。此外,氧化亚铜也极不稳定, 易被空气中氧所氧化。 保持反应液沸腾可防止空气进入,避免次甲基蓝和 氧化亚铜被氧化而增加耗糖量。
(1)原理
总糖的测定的原理是样品经除去蛋白质后, 加稀盐酸在加热条件下使蔗糖水解转化为还原糖, 再以直接滴定法或高锰酸钾法测定。
(2)仪器
① 恒温水浴。 ② 其他同还原糖测定。
Байду номын сангаас
样品处理
(4) 测定方法 蔗糖水解(样品及蔗糖标准液) 还原糖法 测定
① 样品处理:按还原糖测定法中的方法进行。 ② 样 品 中 总 糖 量 测 定 : 吸 取 5 0 ml 样 品 处 理 液 于 100mL容量瓶中,加6mol/L盐酸5mL,在68~70℃ 水浴中加热15min,冷却后加2滴甲基红指示剂,用 200g/L(体积分数)氢氧化钠中和至中性,加水至刻 度,混匀,按还原糖测定方法中直接滴定法进行测定。
碱性酒石酸铜溶液的标定
① 称取105℃烘干至恒量的纯蔗糖1.0000g, 以蒸馏水溶解,移入500mL容量瓶中,稀释 至刻度,摇匀。此标准液1mL相当纯蔗糖2mg。 ② 吸取蔗糖标准液50mL于100mL容量瓶中, 加 6 mol/L 盐 酸 5 mL 在 6 8 ~ 7 0 ℃ 水 浴 中 加 热 1 5 min, 冷 却 后 加 2 滴 甲 基 红 指 示 剂 , 用 200g/L氢氧化钠中和至中性,加水至刻度, 摇匀。此液1mL相当于1mg蔗糖。
非结构性碳水化合物的测定方法

水稻糖花比的测定方法一.茎鞘非结构性碳水化合物(NSC)测定参考酶解方法。
准确称取0.5g左右的粉碎样品,加入20mL水,煮沸,使淀粉糊化后, 再添加上淀粉酶专用磷酸缓冲液(KH2PO4,12.08g/L,Na2HPO4·12H2O,7.96g/L, NaNO3,0.1g/L)20mL,加入耐热性ɑ-淀粉酶(和光公司生产)1.5mg和淀粉转葡萄糖苷酶AMYLO-GLUCOSIDASE(SIGMA公司制造)0.5mg制备成的悬浮液。
40℃水浴24h振荡培养后,再行过滤。
残留物与样本的重量差即为非结构性碳水化合物。
二.茎鞘非结构性碳水化合物(NSC)采用蒽酮比色法测定。
1.可溶性糖总量的测定称取O.1g水稻干样于150mL三角瓶中,加20mL80%乙醇,用带有长玻璃管的橡皮塞塞紧,80℃水浴浸提30min(每隔lOmin摇动一次),取出冷却,将清液过滤至150mL三角瓶中,残渣再用80%乙醇提取两次(每次lOmL、15min),再将清液滤至三角瓶中,向三角瓶中加0.25g活性炭80℃水浴脱色30min,冷却过滤至50mL容量瓶中用80%乙醇定容,取2mL提取液于25mL容量瓶中加0.5mL蒽酮试剂和5mL浓硫酸,摇匀,沸水浴中逐管保温lmin后620nm处比色。
将残渣及滤纸于80℃烘干,以备测定淀粉。
2.淀粉含量的测定将提取可溶性糖以后的干燥残渣及滤纸剪碎放入150mL三角瓶中,加20mL热蒸馏水,沸水浴中煮沸15min,加9.2mol/L高氯酸2ml提取15min,冷却过滤至50mL容量瓶中,用I2-KI溶液检验,如有蓝色颗粒重复提取,过滤定容,取滤液2mL,加0.5mL蒽酮试剂和5mL浓硫酸,盖上塞子微微摇动,出现絮状物时剧烈摇动,然后立即放入沸水浴中确保逐管加热lmin,自然冷却至室温620nm比色,以空白提取液为对照。
糖花比=抽穗期茎鞘中非结构性碳水化合物(包括可溶性糖和淀粉)mg/颖花数,表示灌浆始期每朵颖花具有的物质积累。
碳水化合物的测定

4)如何对样品提取液进行澄清? 为了除去色素、少量蛋白质、可溶性果胶、有机
酸、氨基酸等物质,需加入一定量澄清剂,混匀沉淀, 静置后过滤得到澄清的提取液。
5)使用澄清剂要注意的问题: ① 应根据样液的种类、干扰成分的种类及含量进行 选择,同时还要考虑所采用的分析方法。 如用直接滴定法测定时不能用硫酸铜-氢氧化钠 溶液,以免在样液中引入Cu2+;用高锰酸钾滴定法测 定时不能用乙酸锌-亚铁氰化钾溶液,以免在样液中 引入Fe2+。 ②澄清剂的用量要适当。用量太少,达不到澄清的目 的;用量太多,会使检测结果产生误差。 ③用醋酸铅作澄清剂时要除铅。但除铅剂在保证使铅 完全沉淀的前提下尽量少用。
(4)AL(OH)3乳剂是辅助澄清剂。 (5)CuSO4-NaOH这种澄清剂用于牛乳
等样品。
(二).澄清剂 4.澄清剂的用量
在一般操作时,加澄清剂量多少一定要恰当。
(三).常用的除铅剂
K2CrO4(铬酸钾); Na2CrO4(铬酸钠); Na2HPO4(磷酸氢二钠); Na2SO4(硫酸钠);[使用时可加少量固体
(一).还原糖的测定方法
1 直接滴定法(斐林氏溶液法)
1.3 方法
(3)测定
样品溶液预测:吸取5.0ml碱性酒石酸
铜甲液及5.0ml乙液,置于150ml锥形瓶中, 加水10ml,加入玻璃珠2粒,控制在2min 内加热至沸,趁沸以先快后慢的速度,从 滴定管中滴加样品溶液,并保持溶液沸腾 状态,待溶液颜色变浅时,以每两秒1滴 的速度滴定,直至溶液蓝色刚好褪去为终 点,记录样液消耗体积。
ቤተ መጻሕፍቲ ባይዱ
1 直接滴定法(斐林氏溶液法)
1.5注意事项!
1) 本方法测定的是一类具有还原性质的糖,包括葡 萄糖、果糖、乳糖、麦芽糖等,只是结果用葡萄糖 或其他转化糖的方式表示,所以不能误解为还原糖 =葡萄糖或其他糖。
碳水化合物的测定

碳水化合物的测定概述碳水化合物是生物界三大物质之一(Pro, Fat),是自然界最丰富的有机物质。
碳水化合物主要存在于植物界,如谷类食物和水果蔬菜的主要成分是CH2O。
碳水化合物统称为糖类,它包含了单糖、低聚糖及多糖,是大多数食品中重要组成成分,也是人和动物体的重要能源。
单糖、双糖、淀粉能为人体所消化吸收,提供热能,果胶、纤维素维持人体健康具有重要作用。
一、碳水化合物的化学组成、分类和性质1、化学组成(chemical composition)碳水化合物是C、H、O三元素组成一类多羟基醛或多羟基酮化合物,而且绝大多数氢原子是氧原子的两倍。
即氢与氧为2:1。
它们的比例与水分的组成相同(水分子H2O)。
因此被人们称为“碳水化合物”即写成CH2O。
它们可用通式C n(H2O)m表示,好像碳的水化物。
但是笼统地说糖类称为CH2O是不太确切的。
比如,我们熟悉的甲醛,它的分子式为CH2O,醋酸C2H4O2,乳酸C3H6O3,从它们的结构上讲都类似于H与O=2:1的关系。
按照这个比例它们都应属于碳水化合物,但是以上几个物质都没有糖类的特性,所以它们不是碳水化合物。
又比如,C5H10O4去氧核糖,还有鼠李糖C6H12O5。
这些属于糖类,但不符合上面的比例。
因此称碳水化合物是C、H、O组成,通式为C n(H2O)m是不确切的,但是历史上一直沿用下来,而且人们也习惯了,所以至今仍然采用。
2、分类 chemical classification按照有机化学可分成三类,它是根据在稀酸溶液中水解情况分类。
化学分类:1、单糖2、低聚糖(蔗糖、乳糖、麦芽糖) -------有效碳水化合物3、多糖营养性多糖(淀粉、糖原)4、构造性多糖(纤维素、半纤维素、木质素、果胶)-------无效碳水化合物现代营养工作者分为两大类:营养角度分:有效碳水化合物、无效碳水化合物(膳食纤维)有效碳水化合物:对人体有营养(提供能量)性的称做有效碳水化合物无效碳水化合物:膳食纤维:指人们的消化系统或者消化系统中的酶不能消化、分解、吸收的物质,但是消化系统中的微生物能分解利用其中一部分。
食品理化分析碳水化合物的测定

检查滴定管,更换橡皮、润滑油 标定:葡萄糖(或转化糖)标液装管,滴定AB混合液, 三次平行,V0 ,计算A: A = ρ × V0
1.0g硬糖,加水溶解, 加澄清剂(乙酸锌溶液和 亚铁氰化钾溶液),定容250mL, 过滤(弃去初滤液)
•滤液装管滴定 AB混合液, 一次预测, 三次平行V1 ,
• 吸取25mL滤液+2.5mL盐酸, 70℃水浴15min,冷却,调中性, 定容100mL,装管,滴定, 一次预测,三次平行V2 ,
(代替GB/T 5009.8—2003)
《食品中蔗糖的测定》 第一法 高效液相色谱法 第二法 酸水解法
1.原理 样品脱脂后,用水或乙醇提取,提取 液经澄清处理以除去蛋白质等杂质,再用 盐酸进行水解,使蔗糖转化为还原糖。然 后按还原糖测定方法分别测定水解前后样 品液中还原糖含量,两者差值即为由蔗糖 水解产生的还原糖量,乘以一个换算系数 即为蔗糖含量。
(二)高锰酸钾滴定法
1.原理 样液+碱性酒石酸铜溶液(二价铜)反应→氧 化亚铜沉淀→过滤,+过量的酸性硫酸铁溶液(三 价铁盐)→还原为亚铁盐→用高锰酸钾标准溶液 滴定 根据高锰酸钾溶液消耗量可计算出氧化亚铜的 量,再从检索表中查出与氧化亚铜量相当的还原 糖量,即可计算出样品中还原糖含量。
2.适用范围及特点
该法不受半纤维素、多缩戊糖、果胶质
等多糖的干扰,适合于这类多糖含量高 的样品,分析结果准确可靠,但操作复 杂费时。
(三)旋光法 1.原理 淀粉具有旋光性,在一定条件下旋光 度的大小与淀粉的浓度成正比。用氯化钙 溶液提取淀粉,使之与其他成分分离,用 氯化锡沉淀提取液中的蛋白质后,测定旋 光度,即可计算出淀粉含量。 2.适用范围及待点 本法适用于淀粉含量较高,而可溶性糖 类含量很少的谷类样品,如面粉、米粉等。 操作简便、快速。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
水稻糖花比的测定方法
一.茎鞘非结构性碳水化合物(NSC)测定参考酶解方法。
准确称取0.5g左右的粉碎样品,加入20mL水,煮沸,使淀粉糊化后, 再添加上淀粉酶专用磷酸缓冲液(KH2PO4,12.08g/L,
Na2HPO4·12H2O,7.96g/L, NaNO3,0.1g/L)20mL,加入耐热性ɑ-淀粉酶(和光公司生产)1.5mg和淀粉转葡萄糖苷酶
AMYLO-GLUCOSIDASE(SIGMA公司制造)0.5mg制备成的悬浮液。
40℃水浴24h振荡培养后,再行过滤。
残留物与样本的重量差即为非结构性碳水化合物。
二.茎鞘非结构性碳水化合物(NSC)采用蒽酮比色法测定。
1.可溶性糖总量的测定
称取O.1g水稻干样于150mL三角瓶中,加20mL80%乙醇,用带有长玻璃管的橡皮塞塞紧,80℃水浴浸提30min(每隔lOmin摇动一次),取出冷却,将清液过滤至150mL三角瓶中,残渣再用80%乙醇提取两次(每次lOmL、15min),再将清液滤至三角瓶中,向三角瓶中加0.25g活性炭80℃水浴脱色30min,冷却过滤至50mL容量瓶中用80%乙醇定容,取2mL提取液于25mL容量瓶中加0.5mL蒽酮试剂和5mL浓硫酸,摇匀,沸水浴中逐管保温lmin后620nm处比色。
将残渣及滤纸于80℃烘干,以备测定淀粉。
2.淀粉含量的测定
将提取可溶性糖以后的干燥残渣及滤纸剪碎放入150mL三角瓶中,加20mL热蒸馏水,沸水浴中煮沸15min,加9.2mol/L高氯酸2ml提取
15min,冷却过滤至50mL容量瓶中,用I2-KI溶液检验,如有蓝色颗粒重复提取,过滤定容,取滤液2mL,加0.5mL蒽酮试剂和5mL浓硫酸,盖上塞子微微摇动,出现絮状物时剧烈摇动,然后立即放入沸水浴中确保逐管加热lmin,自然冷却至室温620nm比色,以空白提取液为对照。
糖花比=抽穗期茎鞘中非结构性碳水化合物(包括可溶性糖和淀粉)mg/颖花数,表示灌浆始期每朵颖花具有的物质积累。
