肿瘤学研究进展(1989-2001)
ZEB1-AS1及其相关基因ZEB1在肿瘤免疫微环境中的作用研究进展

ZEB1-AS1及其相关基因ZEB1在肿瘤免疫微环境中的作用研究进展闫睿怡,周艺玲,何琳莉川北医学院基础医学与法医学院病理学教研室,四川南充637000【摘要】锌指E -盒结合同源异形盒1-反义链1(ZEB1-AS1)属于长链非编码RNA (Lnc RNA)家族,是E 盒锌指蛋白1基因(ZEB1)的反义蛋白产物,可通过上调ZEB1的活性促进肿瘤浸润、转移,其表达的失调与多种肿瘤的发生、发展密切相关,有望成为肿瘤治疗的重要分子靶点。
近年来,大量研究表明ZEB1-AS1及其相关基因ZEB1可通过调节肿瘤免疫微环境影响肿瘤恶性进展及治疗效果。
本文主要阐述ZEB1-AS1及ZEB1与肿瘤相关免疫细胞、炎症相关细胞因子、炎性信号通路之间的相互作用,为肿瘤的靶向及免疫治疗提供新思路。
【关键词】锌指E -盒结合同源异形盒1-反义链1;E 盒锌指蛋白1;肿瘤免疫微环境;免疫细胞;长链非编码RNA【中图分类号】R730.3【文献标识码】A【文章编号】1003—6350(2023)20—3033—04Research progress on the role of ZEB1-AS1and its related gene ZEB1in tumor immune microenvironment.YAN Rui-yi ,ZHOU Yi-ling,HE Lin-li.Department of Pathology,School of Basic Medicine and Forensic Medicine,North Sichuan Medical College,Nanchong 637000,Sichuan,CHINA【Abstract 】Zinc finger E-box binding homeobox 1-antisense 1(ZEB1-AS1)belongs to the long non-coding RNA (Lnc RNA)family,which is the antisense protein product of the ZEB1.It can promote tumor invasion and metasta-sis by upregulating the activity of ZEB1,and the disorder of its expression is closely related to the occurrence and devel-opment of a variety of tumors,which is expected to become an important molecular target for tumor treatment.In recent years,a large number of studies have shown that ZEB1-AS1and its related gene ZEB1can affect tumor malignant pro-gression and treatment effect by regulating the tumor immune microenvironment.This paper mainly describes the inter-action between ZEB1-AS1and ZEB1and tumor-associated immune cells,inflammation-related cytokines,and inflam-matory signaling pathways,so as to provide new ideas for tumor targeting and immunotherapy.【Key words 】ZEB1-AS1;ZEB1;Tumor immune microenvironment;Immune cells;Long non-coding RNA (Lnc RNA)doi:10.3969/j.issn.1003-6350.2023.20.033基金项目:2022年四川省南充市市校科技战略合作专项资金项目(编号:22SXQT0197);四川省大学生创新创业训练计划项目(编号:S202210634124)。
肿瘤生物学特征研究进展(2000年-2022年)

肿瘤生物学特征研究进展(2000年-2022年)Douglas Hanahan and Robert A. Weinberg于2000年1月7号在《Cell》上发表综述:The Hallmarks of Cancer. 在该综述中,两位最先提出了肿瘤的六大生物学特征,这些基础特征包括:持续不断的增殖信号;躲避生长抑制;抵抗细胞死亡;永不停止的复制能力;引发血管新生的能力;侵袭与转移的能力。
跟这些特征密切相关的还有基因组的不稳定,基因组的不稳定导致了基因的多样性从而加速了这六大特征的获得。
炎症也对其中的多个特征的产生有促进作用。
肿瘤的这六大特征(正是这些独特的、辅助性的能力使肿瘤细胞实现了生长、转移、传播)提供了一个理解肿瘤细胞生物学坚实基础。
这些基础特征构成了我们系统性理解肿瘤—这种复杂的新生冗余物的基础逻辑框架。
D Hanahan , et al. doi: 10.1016/s0092-8674(00)81683-9.2011年3月4号,Douglas Hanahan和Robert A. Weinberg在《Cell》上发表综述:Hallmarks of Cancer:The Next Generation。
论述了过去10年肿瘤学中的热点和进展,阐述了肿瘤细胞的10大基本特征:Sustaining Proliferative Signaling(持续的增殖信号); Evading Growth Suppressors(逃避生长抑制信号); Resisting Cell Death(抵抗细胞死亡); Enabling Replicative Immortality(能够无限复制);Inducing Angiogenesis(诱导血管生成); Activating Invasion and Metastasis(侵袭和远处转移);Genome Instability and Mutation(基因组不稳定和突变);Tumor-Promoting Inflammation(炎症促发肿瘤);Reprogramming Energy Metabolism(代谢重编程);Evading Immune Destruction(免疫逃逸)。
肿瘤科新技术与研究进展

肿瘤科新技术与研究进展近年来,肿瘤科领域不断涌现出一系列令人瞩目的新技术和研究进展。
这些创新和突破为肿瘤的早期诊断、治疗和预防提供了新思路和新方法,为广大患者带来了希望和福音。
本文将对一些重要的肿瘤科新技术和研究进展进行介绍和分析。
一、肿瘤早期诊断技术的突破早期诊断对于肿瘤患者的治疗非常重要,它可以提高治疗成功率,降低死亡风险。
在肿瘤科领域,涌现出了一系列令人振奋的早期诊断技术,为临床医生提供了更精确、更可靠的诊断手段。
1.肿瘤标志物的检测肿瘤标志物是一种在肿瘤患者体内特异性产生的物质,在肿瘤的早期诊断中具有重要价值。
通过检测肿瘤标志物的水平,可以帮助临床医生进行肿瘤的筛查、诊断和疾病进展的监测。
常见的肿瘤标志物包括CEA、CA125、PSA等。
2.影像学技术的发展影像学技术是肿瘤早期诊断中不可或缺的一环。
近年来,随着医学影像学的飞速发展,各种先进的影像学技术相继问世,如计算机断层扫描(CT)、磁共振成像(MRI)、正电子发射计算机断层扫描(PET-CT)等。
这些技术的应用,使医生能够更准确地了解肿瘤的形态、位置和生长情况,为早期诊断提供了更丰富的信息。
二、肿瘤治疗技术的创新突破随着科技的进步和研究的深入,肿瘤治疗技术也得到了革命性的突破,为患者提供了更多治疗选择和更好的治疗效果。
1.靶向治疗技术靶向治疗技术是近年来肿瘤治疗的一个重要突破。
它是通过针对肿瘤细胞表面的分子靶点,选择性地杀灭肿瘤细胞而不对正常细胞产生明显的损害。
这种治疗方法具有高效、准确的特点,能够有效控制肿瘤的生长和转移。
常见的靶向治疗药物包括靶向蛋白激酶抑制剂、单克隆抗体等。
2.免疫治疗技术免疫治疗技术是近年来肿瘤治疗中备受关注的一种新兴治疗方式。
它通过激活或增强人体自身免疫系统的抗肿瘤作用,来攻击和清除肿瘤细胞。
免疫治疗具有精准、低毒性的特点,被认为是肿瘤治疗的重要突破。
常见的免疫治疗方法包括白细胞介素-2(IL-2)治疗、免疫检查点抑制剂治疗等。
肿瘤学最新进展

肿瘤学最新进展随着科学技术的不断进步,肿瘤学已经取得了一些重大的突破和进展。
这些最新的突破不仅改变了我们对癌症的认识,也为未来的癌症治疗开辟了新的道路。
以下就是近期肿瘤学领域的部分重要进展。
一、基因疗法的进步基因疗法一直是肿瘤治疗的主要前沿技术。
近年来,科研人员通过研究,已经发现许多影响癌症的关键基因,如BRCA基因、TP53基因等,这些基因的突变能够引发肿瘤的发生和发展。
目前,基因疗法如CRISPR-Cas9技术等已经进入临床试验阶段,预计在未来能够为癌症治疗带来巨大的希望。
二、免疫疗法的施展免疫疗法是近年来肿瘤学领域的一孚众望的治疗策略。
免疫疗法主要通过激活患者自身的免疫系统来攻击癌细胞。
目前,电源抗体、基因改造的T细胞(CAR-T)等免疫疗法已经广泛应用于临床,为许多绝症带来了希望。
三、肿瘤微环境的研究重视肿瘤微环境,指的是肿瘤细胞以及它们周围的细胞、基质和分子组成的环境,在癌症发生、发展和治疗中都起着极其关键的作用。
近年来,人们对肿瘤微环境的重视日益提升,研究者对如何利用肿瘤微环境来做药物治疗也进行了深入研究。
四、并发症的管理肿瘤并发症,如疼痛、恶心、消瘦和抑郁等,会极大影响癌症患者的生活质量。
因此,如何有效管理这些并发症越来越受到重视。
目前,针对癌症并发症的多模态管理已经被广泛引入临床实践中。
五、早期筛查与预防早期筛查和预防也是近年来肿瘤学领域争相追求的方向。
现在,有许多癌症可以通过早期筛查进行早期发现,同时,基于基因和环境风险因子的个性化癌症预防也已成为可能。
总的来说,本文探讨的这些领域,无疑是走在肿瘤治疗尖端的科技成果,它们为肿瘤疾病的防治带来了崭新的可能和未来。
然而,癌症防治仍然面临多种挑战,期待更多科研成果的产生,为国人和全人类的健康保驾护航。
肿瘤学最新进展
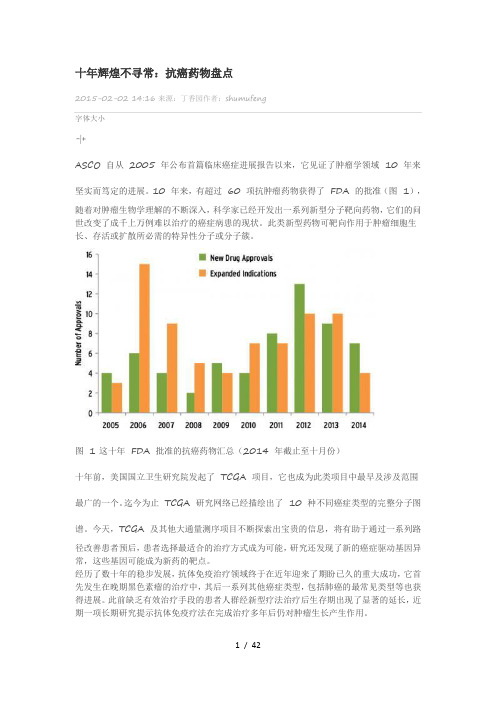
十年辉煌不寻常:抗癌药物盘点2015-02-02 14:16来源:丁香园作者:shumufeng字体大小-|+ASCO 自从2005 年公布首篇临床癌症进展报告以来,它见证了肿瘤学领域10 年来坚实而笃定的进展。
10 年来,有超过60 项抗肿瘤药物获得了FDA 的批准(图1),随着对肿瘤生物学理解的不断深入,科学家已经开发出一系列新型分子靶向药物,它们的问世改变了成千上万例难以治疗的癌症病患的现状。
此类新型药物可靶向作用于肿瘤细胞生长、存活或扩散所必需的特异性分子或分子簇。
图 1 这十年FDA 批准的抗癌药物汇总(2014 年截止至十月份)十年前,美国国立卫生研究院发起了TCGA 项目,它也成为此类项目中最早及涉及范围最广的一个。
迄今为止TCGA 研究网络已经描绘出了10 种不同癌症类型的完整分子图谱。
今天,TCGA 及其他大通量测序项目不断探索出宝贵的信息,将有助于通过一系列路径改善患者预后,患者选择最适合的治疗方式成为可能,研究还发现了新的癌症驱动基因异常,这些基因可能成为新药的靶点。
经历了数十年的稳步发展,抗体免疫治疗领域终于在近年迎来了期盼已久的重大成功,它首先发生在晚期黑色素瘤的治疗中,其后一系列其他癌症类型,包括肺癌的最常见类型等也获得进展。
此前缺乏有效治疗手段的患者人群经新型疗法治疗后生存期出现了显著的延长,近期一项长期研究提示抗体免疫疗法在完成治疗多年后仍对肿瘤生长产生作用。
另一种免疫疗法致力于重组自身的免疫细胞以攻击肿瘤细胞,它对于特定的血液肿瘤以及一系列实体肿瘤同样表现出色。
过去的十年间首款癌症疫苗也得以问世(宫颈癌Gardasil 疫苗)。
探索其他类型癌症疫苗的试验也正在进行中。
最后,大规模的筛查研究带来了新的重要证据,表明对于一些常见癌症如肺癌、乳腺癌以及前列腺癌可推进筛查实践。
靶向治疗迅速发展最近的十年间,我们看到由FDA 批准的新型靶向治疗药物有了稳步且迅猛的增加,远远超过新型化疗药物的研发速度(图2)。
肿瘤学的最新研究进展

肿瘤学的最新研究进展肿瘤学是研究肿瘤的发生、发展、转移和治疗等方面的学科。
近年来,随着科学技术的不断进步和医学研究的深入,肿瘤学领域也取得了许多令人瞩目的研究进展。
本文将介绍肿瘤学的一些最新研究成果。
1. 微环境与肿瘤发生肿瘤微环境是指肿瘤细胞周围的细胞、生化物质和细胞外基质等环境因素。
最新研究表明,肿瘤微环境在肿瘤的发生和发展过程中起着重要作用。
研究人员发现,肿瘤微环境中的免疫细胞和血管新生等因素与肿瘤的恶化和转移有密切关系。
针对肿瘤微环境的治疗成为了一种新的肿瘤治疗策略。
2. 免疫疗法的突破免疫疗法是利用激活患者自身免疫系统来抑制或杀灭肿瘤细胞的一种治疗方法。
最近几年,免疫疗法在肿瘤学中取得了重大突破。
例如,抗CTLA-4和PD-1的抗体疗法被广泛应用于多种恶性肿瘤的治疗中,取得了显著的疗效。
此外,个体化免疫疗法和CAR-T细胞疗法等也成为研究热点。
3. 基因组学和肿瘤精准医学基因组学是研究基因组结构和功能的学科,而肿瘤精准医学是根据患者的基因组信息来个体化治疗肿瘤的一种方法。
最新研究表明,基因组学在肿瘤学领域的应用已经取得了重大突破。
通过对肿瘤基因组的分析,可以发现患者的突变信息,从而选择更加有效的治疗方法。
个体化治疗在某些肿瘤中已经取得了显著的成功,为肿瘤患者带来了希望。
4. 组织工程学和人工智能在肿瘤研究中的应用组织工程学是一门利用细胞、生物材料和工程技术等手段来重建和修复组织的学科,而人工智能是模拟人类智能行为的一种技术。
最新研究表明,组织工程学和人工智能在肿瘤研究中发挥了重要作用。
通过组织工程学技术,研究人员可以构建肿瘤模型,来研究肿瘤的生长和转移机制。
而人工智能则可以帮助科学家更好地分析和挖掘肿瘤数据,提高肿瘤研究的效率和准确性。
总结随着科学技术的不断进步,肿瘤学领域的研究也取得了许多令人振奋的成果。
微环境的研究、免疫疗法的突破、基因组学和肿瘤精准医学的应用以及组织工程学和人工智能的发展,都为肿瘤的治疗和预防带来新的可能。
肿瘤学的前沿研究进展和应用

研究目的:提高肿瘤诊断和治疗水平,改善患者生存质量,降低肿瘤发病率和死亡率
研究方法:包括实验研究、临床研究、流行病学研究和治疗提供科学依据
肿瘤是导致人类死亡的主要原因之一
肿瘤学研究有助于了解肿瘤的发生、发展、转移和治疗
肿瘤学研究有助于提高肿瘤患者的生存率和生活质量
信号分子:发现新的信号分子及其在肿瘤发生发展中的作用
信号调控:研究信号转导的调控机制,为肿瘤治疗提供新的靶点
信号阻断:开发针对信号转导通路的抑制剂,用于肿瘤治疗
肿瘤学应用
肿瘤诊断和检测技术应用
影像学检查:CT、MRI、PET等
病理学检查:组织切片、细胞学检查等
分子生物学检测:基因测序、生物标志物检测等
肿瘤的研究投入:肿瘤研究需要大量的资金和人力投入,需要更多的支持和合作
肿瘤学研究的未来展望
添加标题
添加标题
添加标题
添加标题
技术发展:基因编辑、细胞治疗、人工智能等
研究方向:个性化医疗、靶向治疗、免疫治疗等
挑战与机遇:攻克肿瘤耐药性、提高治疗效果、降低副作用等
国际合作:加强国际合作,共享研究成果,推动肿瘤学研究进展
肿瘤基因组学的最新研究成果
肿瘤基因组学的定义和研究范围
肿瘤基因组学的研究方法和技术
肿瘤基因组学在肿瘤治疗中的应用和前景
肿瘤干细胞研究进展
肿瘤干细胞的定义和特性
肿瘤干细胞在肿瘤发生、发展和转移中的作用
肿瘤干细胞的研究方法和技术
肿瘤干细胞治疗的最新进展和挑战
肿瘤细胞信号转导研究进展
信号转导通路:揭示肿瘤细胞信号转导的机制和通路
放射治疗:利用放射线杀死肿瘤细胞
化学治疗:使用化学药物杀死肿瘤细胞
肿瘤预防和干预措施应用
肿瘤学前沿杂志收录范围

肿瘤学前沿杂志收录范围
《肿瘤学前沿杂志》收录范围
肿瘤学前沿杂志,作为一本权威的学术期刊,专注于肿瘤学领域的最新研究进展和前沿技术。
它以全球视野,聚焦于肿瘤学的多个方向,为读者提供丰富的内容,帮助读者了解肿瘤学领域的最新动态。
该杂志的收录范围广泛,涵盖了肿瘤学的多个研究领域。
以下是一些主要的收录范围:
1. 肿瘤病因与发病机制:探讨肿瘤的起源、发展过程以及与环境、遗传等因素之间的关系。
2. 肿瘤诊断与分期:介绍各种肿瘤的诊断方法和技术,包括肿瘤标志物的检测、影像学诊断、组织学检查等。
3. 肿瘤治疗:介绍肿瘤治疗的各种方法,如手术治疗、放疗、化疗、靶向治疗、免疫治疗等,以及各种治疗的研究进展和新技术的应用。
4. 肿瘤预防与早期筛查:介绍肿瘤预防的方法和策略,以及早期筛查的技术和进展。
5. 肿瘤转移与复发:探讨肿瘤的转移机制和复发原因,并介绍预防和治疗转移与复发的方法。
6. 肿瘤免疫学:介绍肿瘤免疫学的最新研究进展和免疫治疗的应用。
7. 肿瘤基因组学:介绍肿瘤基因组学的研究方法和技术,并介绍肿瘤基因组学在肿瘤诊断和治疗中的应用。
8. 肿瘤干细胞研究:介绍肿瘤干细胞的研究进展和在肿瘤治疗中的应用。
9. 肿瘤生物学:介绍肿瘤细胞的生理特征、分子机制和信号通路等。
10. 肿瘤微环境:介绍肿瘤微环境的研究进展和对肿瘤发展的影响。
以上仅是《肿瘤学前沿杂志》收录范围的一部分,该杂志还包括其他相关领域的研究内容。
通过阅读该杂志,读者可以了解到肿瘤学领域最新的研究成果和前沿技术,为肿瘤学研究提供参考和指导。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
肿瘤学进展(1889-2001)里程碑11889年Seed and soil hypothesis 种子与土壤假说决定哪个器官将会遭受癌症播散的因素究竟是什么?这个问题引起了西方伦敦医院和皇家医院的一个助理外科医生--Stephen Paget的思考,并于1889年发表了一篇文章详细分析了引起癌症转移的"种子和土壤"假说。
即:癌细胞通过血液和淋巴可以播种到其它组织并能使其周围细胞癌症化;并通过分析了735个乳腺癌病例,证实了癌症转移灶不是随机的,而是一些特定器官可以提供适合特定转移灶生长的环境。
虽然这个理论被忽视了很多年,但是,在1980年,Ian Hart 和Isaiah Fidler使种子和土壤假说得到了空前的繁荣,这个时候临床观察也确证了一些器官更易于发生转移。
Hart 和Fidler做了黑色素细胞瘤的动物实验,并用放射性标记技术证实了癌细胞需要从环境中得到一些营养才能生长。
这个思想在今天仍旧激励科学家从分子水平上研究种子与土壤假说的转移机制。
里程碑21890年Cancer as a genetic disease 肿瘤是一种遗传性疾病癌症的遗传学基础是现代癌症研究的基石。
1890年,David von Hansemann详细描述了13个不同腺癌样本的有丝分裂像,发现每个样本都存在异常分裂像,于是推断这些异常的细胞分裂是癌症细胞中染色质内含物或多或少的原因。
在20世纪初,zoologist Theodor Boveri研究了异常有丝分裂和恶性肿瘤的关系。
他的一个重要的创新是设计了一个海胆卵操作实验,该实验可以诱导多级有丝分裂和染色体异常分离。
他发现并命名了有丝分裂纺锤体,推测染色体是遗传物质的载体,对于每个个体在质上都是相似的。
他认为异常分裂导致染色体不平衡分离,这在多数情况下会产生有害基因。
一次偶然中发现染色体的不正确联合会产生能够遗传的有无限增殖能力的恶性细胞。
这些奠定了癌症是遗传性疾病的基础。
同时,Boveri还用自己的观点解释了和癌症相关的许多现象,并且提出了很多大胆的设想和推测,诸如目前我们所说的细胞周期检查点、肿瘤抑癌基因和癌基因。
他甚至想象毒药、射线、物理损伤、病原体、慢性炎症和组织修复都可能会间接促进染色体异常分离或导致染色体不平衡的其它情况,进而与癌症的的发生密切相关。
随着这些惊人的假设,Boveri还阐明了在一种组织中会出现不同类型的肿瘤、隐形染色体等位基因丢失、癌症易感性的遗传度、癌症在发生和进展上的步骤相似、癌细胞对放疗敏感。
这些观点已经广泛接受。
后来,一些研究者发现了致癌物可以作为诱变剂,这使癌症的遗传学基础更引人注目。
1960年Ph染色体的发现使此观点得到了更大的支持。
与Boveri假说密切相关的观点是在癌症细胞中,染色体不稳定可以促使染色体异常和突变积累。
首次证明癌症细胞基因组不稳定的是Robert Schimke和他的同事,他们发现癌细胞的耐药基因易于发生不稳定扩增。
目前该观点已经广泛接受,染色体不平衡、突变率增加和其它形式的基因组不稳定都和人类癌症的发展有关。
随着研究的深入,我们正在试图解释von Hansemann的设想,即:染色体异常和基因组不稳定是癌症发生的始动因素。
里程碑31909年Immune surveillance 免疫监视免疫系统有惊人的能力来检测出外源物质,而保留自身。
Paul Ehrlich深信癌细胞中,突变累积和改变的基因扩模式也能使免疫系统像清除炎症物质那样破坏癌细胞,并于1909年提出免疫系统可以抑制肿瘤的发展。
但是试图开展的免疫治疗却没有得到Ehrlich设想的那样成功。
在1957年,Richmond Prehn 和Joan Main证实并得出结论肿瘤免疫只对化学致癌物引起的肿瘤起作用,对自发产生的肿瘤却无效。
从此,开始了这方面的大量研究。
Harold Hewitt及其同事对这些研究做了总结认为自发性肿瘤是非免疫源的。
此外,Osias Sutman 在1974年的报道提出在化学致癌物引起的肿瘤中免疫监视有效是不正确的。
然而,Aline van Pel和Thierry Boon发现预防接种可以引起肿瘤特异性免疫反应,这使肿瘤免疫的研究得到了重新振作,但是他们没有得到有效的免疫反应。
Pierre van der Bruggen从技术上得到了突破,并证实肿瘤抗原能激发肿瘤特异性免疫反应。
2001年,Robert Schreiber重新开始了免疫监视的研究,认为免疫系统对肿瘤细胞产生了一个选择压力或者免疫编辑,造成免疫源的减少最终逃离免疫介导的根除。
最近,Gerald Willimsky和Thomas Blankenstein提出在老鼠中散发性肿瘤不是失去了免疫源性,而是产生免疫耐受逃离了免疫根除,但是,和肿瘤生长相关的模式仍旧没有明确。
然而,Ehrlich的设想仍旧鼓舞着肿瘤免疫领域的研究,特别是对作为肿瘤治疗中一个有潜力的免疫治疗领域。
里程碑41910年Viruses and cancer 病毒与肿瘤From hens to eternity病毒可以导致癌症,这个观点已经过时了。
但是,逆转录病毒的研究使癌症领域得到了许多重要的发现。
Peyton Rous公认是该领域之父,他的突破性工作始于1910年,在一个母鸡上发现了一个梭形细胞肉瘤,并鉴定出了鲁斯肉瘤病毒RSV。
当时,他的重要发现并没有得到重视,直到1966年,在他77岁时,Rous才因该研究获得了诺贝尔奖。
1969年,Robert Huebner 和George Todaro开始了一系列研究,认为多数癌症都是由逆转录病毒基因表达造成的。
虽然他们的观点并不完全正确,但是,他们的工作促使了第一个逆转录病毒致癌基因src的鉴定。
因此,这些突破性工作为癌症领域的其它发现铺平了道路。
里程碑51915年Hormones and cancer 激素与肿瘤激素可以影响癌症的发生发展,目前被我们普遍接受,然而,从最早观察到激素对一些癌症病人有益到发展起来以内分泌器官为靶的第一种药物,已经经历了一百年。
虽然现在我们知道激素可以好几种癌症,但是对雌二醇和乳腺癌关系的研究就产生了很多重要的里程碑。
1915年,Abbie Lathrop 和Leo Loeb首次提出激素和肿瘤的发生有关,他们对黄体酮和癌症关系的研究具有划时代意义,但是,直到八年之后,Edgar Allen 和Edward Doisy才鉴定出黄体分泌的那种物质是雌二醇。
接下来的25年中,Abraham Lilienfeld等人研究了女性生殖系统和乳腺癌的关系,提出雌二醇是一种致癌物。
Elwood Jensen于1958年发现了雌二醇受体(ER),1971年他的一项研究(肾上腺切除术对人类乳腺癌影响)是该领域的一场大革命,提出抗雌二醇符合物可以作为避孕药,并促进了制药业的发展。
Michael Harper和Arthur Walpole于1967年研究并详细描述了ICI,46,474(它莫酚)等避孕药,但是直到V.Craig Jordan的研究才使这些药物被临床采纳。
1992年,Bernard Fisher及其同事对它莫酚作为乳腺癌外科手术辅助药物的研究才明确了它莫酚可以预防人类乳腺癌的发生。
从此,它莫酚作为不同肿瘤类型的选择性用药纷纷展开,这些药物的成功发展是该领域中的第一个里程碑。
里程碑61937年Cancer stem cells 肿瘤干细胞虽然肿瘤干细胞的观点到20世纪60年代才得到广泛认可,但是直到20世纪90年代中期才分离出这些细胞。
我们对CSC的多数理解都源于造血恶性肿瘤的研究。
1937年,Uacob Furth 首次提到了CSC,当时,对白血病源于病毒还是细胞存在争议,但是他们首次发明了定量方法来测量克隆潜能。
Robert Bruce和Hugo Van der Gaag运用集落形成实验(CFU-S)使CSC的概念明确化。
然而,直到1994年,John Dick及其同事分离并纯化出了CSC。
目前对实体瘤的研究使CSC的观念不再局限于造血恶性肿瘤。
实体瘤干细胞的分离使研究者更加坚信癌症治疗的靶不是肿瘤细胞的混合群落,而是少数具有自我更新能力的CSC。
目前,我们正在努力阐明CSC的调节机制。
里程碑71939年Angiogenesis 血管发生1939年,Gordon Ide和他的同事在研究肿瘤周围的血管时发现重量可能会产生一种血管生长刺激物质。
1945年,Glenn Algire等从动力学上对此进行了更深入的研究,发现血供不足的情况下肿瘤不能有效生长,因此,可以通过抑制血供系统来治疗肿瘤。
1968年,MelvinGreenblatt和Philippe Shubik证实Ide提出的血管生长刺激物质确实存在,而且在理论上也能鉴定出来。
Judah Folkman等于1971年从肿瘤萃取液中分离出了肿瘤血管生成因子TAF,并提出如果抑制了TAF的活性可以阻滞恶性肿瘤的生长,这使对该领域的研究热潮再次升起。
但是,直到18年以后,Napoleone Ferrara才纯化并鉴定出血管内皮生长因子(VEGF)基因,随后克隆并进行了功能上的研究,而且,他们用封闭性抗体为VEGF刺激肿瘤血管发生和生长提供了最终的证据。
基于这些研究,2004年美国食品和药物管理局批准了贝伐单抗来治疗转移性结直肠癌。
里程碑81950年Smoking and cancer 吸烟与肿瘤20世纪的前半个时期,香烟制造业在西方发展迅速,同时男性肺癌的患病率也增长迅速。
英国流行病学家Richard Doll和Tony Bradford Hill提出多数肺癌都是由吸烟造成的,这个观点目前已被我们广泛接受。
接下来,展开了一些肺癌与吸烟关系的病例对照研究,1950年,Doll和Hill在英国医学杂志上发表文章并得出结论--吸烟是肺癌的一个重要的原因。
具有里程碑意义的是他们设计的一个前瞻性研究克服了偏移的影响。
当时的研究都认为吸烟与男性肺癌有关,而且比其它因素都重要。
在香烟中鉴定处理致癌物以及明确了致癌机制,尽管这些数据无可争辩,但是世界有10亿男性每天都吸烟,但是每年死于肺癌的男性只有1.2百万。
里程碑91953年Two-hit hypothesis 二次突变假说20世纪的前半个时期,遗传突变可以导致癌症的观点已经深入人心(见里程碑2),病毒能够致癌也广泛接受,并且也开始用遗传模式来解释癌症发生的年龄分布。
20世纪50年代和60年代,许多研究运用数学模式进行癌症流行病学研究发现必须到一定的年龄发生的成功突变才会致癌。
Carl Nordling认为至少需要大约七次突变,1957年,Peter Armitage和Richard Doll进一步研究认为体细胞两次突变会导致癌症发生。
