糖尿病论文神经性耳聋论文:伴有糖尿病及神经性耳聋的线粒体脑肌病1例
线粒体脑肌病1例报道及文献复习

线粒体脑肌病1例报道及文献复习患者,男,16岁,因“耳痛、听力下降、视物不清2个月,加重伴发热、抽搐6 d”入院。
患者于2月前无明原因出现右耳疼痛,并听力下降,视物模糊,在当地医院就诊以“鼓膜炎”给予抗感染治疗,症状略好转,听力有所恢复。
6 d前患者上述症状加重,来我院行眼科检查双眼无光感,脑CT示双枕叶低密度影,边界欠清,双基底节区脑内多发钙化影。
当天患者出现发热,最高体温达39℃,间断发作数次抽搐,发作时四肢强直,双眼上视,牙关紧闭,意识丧失,持续时间约2~3 min,经抗癫痫治疗后好转。
急诊以“视听障碍、抽搐原因待查”收住院。
其父母健康,非近亲婚配,无遗传家族史。
体格检查:体温38.5℃,脉搏116次/min,呼吸21次/min,血压120/75 mm Hg。
少年男性,身材矮小,营养中等,神志清,心肺腹部查体未见异常。
神经系统检查:双眼无光感,双眼球位置居中,向各方向活动受限,瞳孔等大等圆,光反射存在,双耳听力下降。
四肢肌肉轻度萎缩,肌力4级,不能耐受疲劳,腱反射消失,双侧Babinski征(+),Chaddock征(+),弓形足。
辅助检查:血常规:WBC15.43×109/L,中性粒细胞92.5%,RBC4.16×1012/LPLT471.1×109/L,ESR30 mm/L,肌酶谱AST 45 u/LCK MB 53 u/LLDH 482 u/L HBDH 456 u/L, 腰穿脑脊液压力110 mmH2O,清亮无色,蛋白定性(±),白细胞计数0.004×109/L,微量总蛋白559 mg/L,微量白蛋白247 mg/L,微量球蛋白311.8 mg/L,糖、氯化物及脑脊液细胞学检查正常。
肌电图:胫、腓、尺、正中神经传导速度正常。
心电图:窦性心律,T波异常,左室高电压。
头颅MRI:双枕顶叶及左颞叶T1低信号,T2高信号,边界欠清。
肌肉活检NADH染色在细胞边缘可见RRF纤维,COX染色可见一些肌纤维着色浅淡。
线粒体糖尿病1例报告

线粒体糖尿病1例报告线粒体糖尿病是一种罕见的遗传性疾病,它是由线粒体DNA或线粒体相关基因突变引起的。
该疾病通常表现为糖尿病、耳聋、眼肌麻痹和心肌病等症状。
本文将介绍一例线粒体糖尿病患者的病例及其临床表现、诊断、治疗和护理过程,以便临床医生更好地了解该疾病及其治疗。
患者为男性,今年40岁,主要就诊于内分泌科。
患者主要症状为多尿和多饮,伴有乏力、视力模糊、尿频等。
患者家族中存在糖尿病史,因此高度怀疑患者可能存在遗传性疾病。
经过详细检查和相关基因检测,最终确诊为线粒体糖尿病。
患者进行了全面的身体检查,包括血糖、眼底、心电图、听力等各项指标检测。
临床表现方面,患者的血糖控制较差,糖化血红蛋白高,出现了典型的糖尿病症状,包括多尿、多饮、乏力等。
患者还出现了进行性耳聋和视力下降的症状,眼底检查显示了典型的视网膜病变,心电图显示心电图异常,提示心肌受累。
患者还反复出现感染及慢性疲劳,且对胰岛素治疗难以达到理想的疗效。
患者临床表现典型,与线粒体糖尿病的临床特点相符。
诊断方面,根据患者的临床表现和家族史,再结合相关基因检测的结果,最终确诊为线粒体糖尿病。
基因检测显示患者存在线粒体DNA的突变,进一步支持了临床诊断。
患者的诊断需要多学科的参与,包括内分泌科、遗传科、眼科、耳鼻咽喉科、心脏科等,以便全面评估患者的病情。
治疗方面,线粒体糖尿病目前尚无特效治疗方法,一般采用对症治疗和支持性治疗。
患者需要进行血糖监测和胰岛素治疗,以控制血糖水平。
同时需要进行视力和听力康复训练,以减轻耳聋和视力下降对生活的影响。
对于心脏功能受累的患者,需要定期心脏功能评估并给予相应治疗。
由于线粒体糖尿病对患者生活质量的影响较大,因此对患者的心理护理也至关重要。
护理方面,护理人员需要对患者的病情进行全面评估,包括疾病的严重程度、病情的发展趋势、对治疗的反应等。
需要加强对患者的教育,帮助患者和家人了解疾病的特点和发展趋势,指导患者合理饮食和运动,帮助患者合理使用药物,同时加强心理护理,帮助患者树立战胜疾病的信心。
伴小脑萎缩的线粒体脑肌病MELAS一例
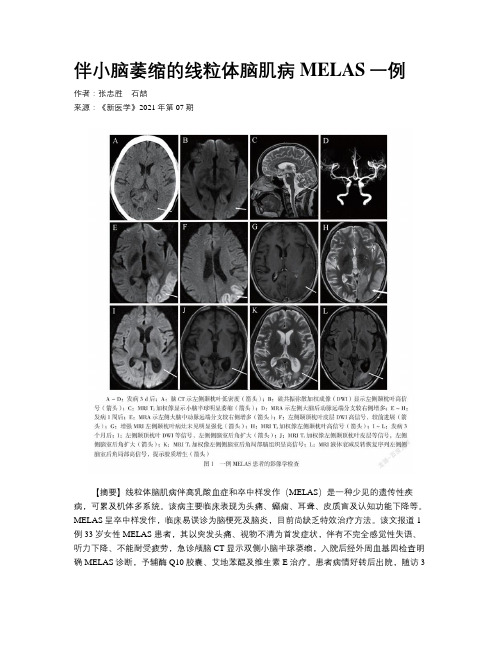
伴小脑萎缩的线粒体脑肌病MELAS一例作者:张忠胜石喆来源:《新医学》2021年第07期【摘要】线粒体脑肌病伴高乳酸血症和卒中样发作(MELAS)是一种少见的遗传性疾病,可累及机体多系统。
该病主要临床表现为头痛、癫痫、耳聋、皮质盲及认知功能下降等。
MELAS呈卒中样发作,临床易误诊为脑梗死及脑炎,目前尚缺乏特效治疗方法。
该文报道1例33岁女性MELAS 患者,其以突发头痛、视物不清为首发症状,伴有不完全感觉性失语、听力下降、不能耐受疲劳,急诊颅脑CT显示双侧小脑半球萎缩,入院后经外周血基因检查明确MELAS诊断,予辅酶Q10胶囊、艾地苯醌及维生素E治疗。
患者病情好转后出院,随访3个月病情稳定。
该病例提示临床医师应提高对MELAS的认识,注意鉴别诊断,避免漏诊或误诊。
【关键词】线粒体脑肌病;小脑萎缩;卒中样发作;病例报告MELAS syndrome complicated with cerebellar atrophy: a case report Zhang Zhongsheng, Shi Zhe. Department of Neurology, the 6th Affiliated Hospital of Guangzhou Medical University (Qingyuan People’s Hospital), Qingyuan 511518, China Corresponding author, Shi Zhe, E-mail:155****************【Abstract】Mitochondrial encephalomyopathy, lactic acidosis and stroke-like episodes (MELAS) is a rare hereditary disease, which can involve with multiple systems. The main clinical manifestations of MELAS consist of headache, epilepsy, deafness, cortical blindness and cognitive decline, etc. MELAS presents with a stroke-like episode, which is easily misdiagnosed as cerebral infarction and encephalitis. No specific treatment has been available at present. In this article, one 33-year-old female with MELAS was reported, presenting with sudden headache and blurred vision as the first symptoms, accompanied by incomplete sensory aphasia, hearing loss,and intolerance of fatigue, etc. Emergency brain CT scan showed bilateral cerebellar atrophy. The diagnosis of MELAS was confirmed by peripheral blood genetic examination. Coenzyme Q10 capsules, idebenone tablets and vitamin E were given. The patient was discharged after improvement of the disease and remained physically stable after 3 months of follow-up. This case prompts that doctors should deepen the understanding of MELAS, pay attention to differential diagnosis and avoid missed diagnosis or misdiagnosis.【Key words】Mitochondrial encephalomyopathy;Cerebellar atrophy;Stroke-like episode;Case report線粒体脑肌病是一种由线粒体DNA或核DNA缺陷导致线粒体结构和功能障碍,使肌纤维和脑神经细胞ATP生成不足而引起的肌肉和(或)脑的病变。
2018年诊治病例分享:一例线粒体脑肌病的诊治

2018年诊治病例分享:一例线粒体脑肌病的诊治患者,女性,60岁。
因“突发头晕9天,意识障碍、肢体抽搐8天“入院。
9日前凌晨睡眠中患者突感头晕,自身不稳。
伴恶心呕吐,为胃内容物,非喷射性,伴腹痛,呈稀水样便3次,里急后重感,便后腹痛缓解。
随后出现吐词不清,双耳听力丧失。
无视物旋转,无饮水呛咳、吞咽困难,无肢体活动不利,无大小便失禁,无头痛发热,无黑曚晕厥,无心慌胸闷。
外院就诊,头颅CT示双颞叶低密度,予静脉补液治疗(具体不详)症状缓解后回家。
8日前上午反复出现赘述,目光呆滞,下午再次诊治收治入院,治疗措施不详,症状无改善。
夜间突发意识丧失伴四肢抽搐,双上肢屈曲,双下肢伸直,口吐白沫,双眼上翻,舌咬伤,外院考虑痫性发作,予抗癫痫处理后,约8分钟左右缓解。
脑电图提示慢波异常,5日前腰椎穿刺潘氏试验阳性,白细胞计数8/ul、红细胞计数4500/ul,氯126.0mmol/l、葡萄糖3.27mmol/l、腺苷脱氨酶0.3IU/L、脑脊液蛋白定量0.4g/L。
头颅核磁增强双侧颞叶对称性异常信号。
拟诊病毒性脑炎,予阿昔洛韦、地塞米松、人免疫球蛋白等治疗,病情无好转,2日前出现双眼视力下降,意识模糊,不能言语,四肢可见不自主活动。
转中大医院进一步诊治。
既往有运动不耐受。
双耳听力下降7年,使用助听器4年;腹泻、便秘交替7年;6年前因“子宫肌瘤”行子宫次全切除术;发现血糖升高4年,空腹血糖波动在7-8mmol/l,未诊治。
30年前顺产一子后“产后大出血”。
患者母亲瘦小,60岁左右出现双耳听力下降,两年前去世(去世之前有4个月不能进食),死因不明;有一个妹妹,两个弟弟,其中一个弟弟身材矮小。
查体:T36.0℃,P106次/分,R21次/分,BP135 /96mmHg。
胸廓对称,听诊双肺呼吸音粗,未闻及罗音。
心率106次/分,律齐,未闻及杂音。
腹软,无压痛反跳痛,双下肢无肿胀。
意识模糊,查体不合作。
双侧瞳孔等大等圆,直径约3mm,对光反射迟钝,眼球运动自如,可见自发粗大水平眼球震颤,快相水平向左。
线粒体损伤与糖尿病发病的相关机制论文

体内主要的抗氧化剂——还原型谷胱甘肽合成时
的关键辅助因子,NADPH耗竭导致还原型谷胱甘
粒体跨膜电位变化,并减少线粒体内ca2+沉积,表明
UCP2在调节线粒体caz+超载中发挥一定作用【8]。研 究也发现,UCP2的激活及表达可对抗游离脂肪酸
肽合成减少。同时,葡萄糖自身氧化生成的活性氧 簇增多,晚期糖基化终末产物增加,氧化还原电位 增加。高血糖还可以驱动过多的电子进入线粒体电
is important place of metabolism and energy
Corresponding author:Zhang Zhenwen.Emaif:yzzzw@medmail.COrn.cn
【Abstract】Mitochondfia
an
synthesis.Dysfunction of
new
ideas for
the treatment of diabetes.
protein 2;
【Key words】
Autophagy
Mitochondria;Diabetes mellitus;Reactive
oxygen
species;Uncoupling
(Int JEndocrinof Metab。2014。34:271—273)
核苷酸递氢体(FADH2),参与细胞氧化磷酸化产生 ATP,这一过程所需的丙酮酸90%以上由葡萄糖产生。 线粒体功能障碍将引起ATP产生不足,导致对
K+通道与ca2+通道的调节作用减弱,进而抑制胰岛 B细胞中胰岛素囊泡的胞吐和释放。线粒体缺陷本 身也可引起脂联素分泌下降,导致多种组织葡萄糖 的生物利用度下降。Kizhakekuttu等[31在研究中发 现,相比非糖尿病者,2型糖尿病患者动脉内线粒体
线粒体糖尿病1例报告

线粒体糖尿病1例报告线粒体糖尿病(MIDD)是一种罕见的遗传性疾病,由于线粒体DNA中的突变导致糖尿病和多系统受累。
它是一种成年早期出现的糖尿病,通常伴随着神经系统和心脏等多系统的并发症。
本文将介绍一例线粒体糖尿病的患者情况,并对其诊断和治疗进行分析和讨论。
患者李某,男,49岁,因频发口干、口渴、多饮、多尿1年余,伴有进行性视力下降6个月入院就诊。
患者父亲有糖尿病史,母亲无糖尿病。
体格检查:血压130/80mmHg,心率80次/分,双侧浅表淋巴结无肿大,肝、脾未及,神经系统检查:双侧视神经乳头水肿,视力双眼仅能分辨手动查视。
实验室检查:空腹血糖14.8mmol/L,糖化血红蛋白9.8%,空腹胰岛素110μU/mL。
心电图:窦性心律,T波低平。
本例患者的临床表现和实验室检查提示其患有糖尿病伴有视神经受累。
考虑到其父亲有糖尿病史、母亲无糖尿病史,患者临床表现严重,且视神经受累,临床医生怀疑该患者糖尿病可能与遗传有关。
考虑线粒体遗传性疾病的可能性,对患者进行了线粒体基因突变筛查,结果显示患者存在线粒体DNA 3243A>G点突变。
根据患者的临床表现和基因检测结果,确诊其患有线粒体糖尿病。
线粒体糖尿病是一种遗传性疾病,目前尚无特效治疗方案。
针对糖尿病的治疗,患者使用胰岛素进行血糖控制,而对于眼部的症状,进行了相应的治疗,但效果并不显著。
患者伴有心脏等多系统受累,需密切监测其心脏功能及病情进展。
以上病例提示,临床医生在诊断疑难病例时需要全面考虑患者的家族史、疾病表现、实验室检查以及基因检测结果。
对于线粒体糖尿病这样的遗传性疾病,家族史和遗传因素非常重要,对疾病的诊断和治疗具有重要意义。
希望通过本例的介绍,能够加深临床医生对线粒体糖尿病的认识,提高对这类疾病的警惕性,及早进行诊断和治疗。
同时也呼吁加强对线粒体疾病的科研,深入研究其病因和治疗方法,为患者提供更好的诊疗服务。
线粒体糖尿病1例报告

线粒体糖尿病1例报告本病例报告描述了一位年轻女性的线粒体糖尿病(m.3243A>G突变),包括疾病诊断、遗传咨询和治疗管理。
病例简介患者为一名27岁的女性,主要症状是反复发作的视力下降和肌无力,面部松弛和说话不清楚,近期出现糖尿病表现。
家族中有数名亲属患有视神经病变、听神经病变、心肌病等疾病史。
患者在首次就诊时被怀疑可能有遗传性疾病,进一步患者和家属的问诊和遗传学检查中发现患者为线粒体遗传疾病,常染色体遗传性一般没有家族成员多代的患者,而线粒体遗传性多与家族成员有密切关系。
检查结果基于上述症状和家族史,患者接受了一系列检查。
血液检查显示血糖值为14.8mmol/L,同时检查了肾功能、肝功能和甲状腺功能均正常。
眼科检查中,患者的视神经旁路电位(mfERG)显示视网膜的视网膜班光和6个环分别下降超过60%。
颈部核磁共振成像(MRI)检查提示颈椎椎间盘突出。
脑电图检查未见明显异常。
而通过尿液检测蛋白item红细胞、尿白细胞、胆红素、亚硝酸盐、葡萄糖、氨基酸以及半羧酸从而诊断患者存在肾小球和肾小管损伤。
进一步的分子生物学检测发现患者的细胞线粒体基因组DNA(mtDNA)中有m.3243A>G突变,是线粒体疾病最常见的突变之一。
诊断和遗传咨询根据症状、体检和分子遗传学检查结果,患者被诊断为线粒体糖尿病,继发性糖尿病和视力下降,归根结底是由于线粒体DNA基因突变引起的线粒体能量代谢障碍。
这种疾病的诊断不仅需要医生对临床症状的合理解释和评估,还需要进行详细的家族史和遗传咨询。
家族遗传史的评估和遗传咨询是诊断线粒体疾病的重要步骤。
患者和家属应该接受一定的遗传咨询,了解病情、疾病的遗传模式和风险评估,以便作出更好的医疗决策。
治疗及管理线粒体疾病目前还没有特效治疗方法,而患者的治疗和管理主要集中在辅助措施和对症治疗上。
主要的治疗手段是改善患者的生活方式和预防并发症。
对于该患者,治疗方案包括限制糖分和脂肪食物,适度运动,视力康复治疗,以及对糖尿病的治疗和监测。
线粒体糖尿病1例报告

线粒体糖尿病1例报告线粒体糖尿病是一种罕见的遗传性疾病,主要由于线粒体DNA突变导致线粒体功能障碍而引起的。
本文通过一例线粒体糖尿病患者的临床表现、诊断和治疗来介绍该疾病。
病例:一名55岁的女性患者,因反复发作的糖尿病、肌肉无力和进行性视力丧失于我科就诊。
患者病史回顾发现,患者9年前出现糖尿病症状,经过饮食控制和口服降糖药物治疗,病情得到控制。
3年前开始出现进行性视力丧失,眼科检查提示视神经萎缩。
患者同时感到四肢乏力,进行性加重,行走困难,查体示双上肢轻度肌无力,下肢较重;进行性视力减退,眼底无明显异常,视野缺损范围较大。
血糖控制不良,多次妊娠史,疑有中毒等母系家族病史。
检查:患者血糖控制不良,空腹血糖11.8mmol/L,糖化血红蛋白8.6%,视网膜无明显异常,视野检查示双眼视野缺损范围较大;血清乳酸、肌酸酐、转氨酶上升。
头颅MRI示双侧颞顶部脑白质异常信号,髓质脱失;肌电图提示肢间神经病变。
行腹部CT示胰管、胆管、肝门及胰腺无明显异常;心脏彩超显示双心房扩大;眼科底荧光造影示双眼视网膜动脉闭塞,并发视网膜病变。
诊断:根据患者临床表现和相关辅助检查,结合母系家族史,考虑线粒体糖尿病可能。
经遗传咨询和线粒体基因测序发现线粒体DNA 3243 A→G 突变,最终诊断为线粒体糖尿病。
治疗:患者经过多学科会诊,制定治疗方案为:输入代谢疾病科、眼科、康复科、心脏内科等多个科室,进行综合治疗。
口服二甲双胍控制血糖,视力康复治疗包括维生素B1等营养神经治疗,视网膜激光治疗等;加强营养支持,行康复训练,同时规避药物及诱发病因。
患者疗程中症状得到缓解,复查视力、心脏功能良好,定期随访及调整治疗方案。
通过以上病例报告,了解到线粒体糖尿病的临床表现、诊断和治疗方案,希望可以引起更多医生对该病的重视,并能够及时发现和治疗该罕见疾病。
希望未来能有更多的临床科研对线粒体糖尿病的治疗和康复进行深入研究,提高患者的生活质量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
糖尿病论文神经性耳聋论文:伴有糖尿病及神经性耳聋的线
粒体脑肌病1例
线粒体遗传病是线粒体dna缺陷造成能量代谢障碍的遗传性疾病,发病率较低,该类疾病在遗传及临床表现上的具有很大的异质性,容易误诊。
现报告伴有糖尿病及神经性耳聋的线粒体脑肌病1例,资料如下:
1 病例
患者,男性,34岁,因“头痛,发热3天”入院。
患者于入院前3天出现头痛,为全头持续性胀痛,伴发热,体温波动于37.4℃左右,无头晕及恶心呕吐,无抽搐及精神异常,患者症状持续无缓解,后出现视物不清。
既往:右耳中耳炎术后10余年,逐渐出现右耳聋,左耳听力减退1年余,糖尿病史2年。
平素体质较差,容易疲劳,难以耐受体力劳动。
父母非近亲婚配,兄长有糖尿病史。
查体:身高164cm,体重54kg。
神清流利,双瞳孔等大等圆,左:右=3:3mm,光反射(+),眼球活动充分,无眼震,视野检查不合作,额纹及鼻唇沟均对称,双耳听力减退,伸舌居中,咽反射(+),四肢肌力v-级,肌张力正常,共济检查协调,深浅感觉正常,四肢腱反射(++),双巴氏征(-)。
头ct:正常;脑电图:异常脑电图;实验室检查:空腹血糖:9.48mmol/l;电解质、肝肾功能及凝血功能正常,血乳酸
2.8mmol/l(0.4-1.7mmol/l) ;血梅毒血清学及艾滋病初筛
试验阴性;抗核抗体系列正常,esr15mm/h,crp0.18 mg/dl;甲状腺功能及肿瘤系列未见异常;血液病毒系列:巨细胞病毒igg增高,余未见异常;弓形虫igm(<100iu/ml)。
腰椎穿刺:脑脊液压力146cmh2o, wbc2*106,rbc2*106,glu 5.73mmol/l, cl 120nmmol/l, pr33.1mg/dl,igg5.78mg/dl,乳酸4.6mmol/l(1.1-1.8mmol/l);抗酸染色、墨汁染色及结核抗体阴性;脑脊液培养无需氧及厌氧菌生长。
脑脊液病毒系列未见异常。
2周后复查腰椎穿刺:脑脊液压力正常,脑脊液生化、细胞学及细菌学检查均未见异常。
纯音及阻抗检查提示:左耳神经性耳聋,右耳混合性耳聋,头mri平扫提示左侧顶枕叶皮层异常信号影。
增强mri:左侧顶枕叶病灶未见明显强化,头mra:颅内血管未见明显异常,mrs提示病灶区乳酸峰增高,考虑线粒体脑病。
反复肌肉活检发现破碎红纤维。
院外基因检查提示:线粒体dna 3243a-g点突变。
给予维生素b族及atp、辅酶q10及辅酶a改善细胞代谢治疗,患者头痛症状逐渐缓解,仍有视物变形。
2 讨论
线粒体病是由于线粒体结构及功能异常所致的一种多
系统受累的疾病,如果同时累及骨骼肌和中枢神经系统,则称为线粒体脑肌病(me)。
线粒体脑肌病临床表现复杂,主要分为以下几种类型,线粒体脑肌病伴乳酸酸中毒及卒中样发作(melas)、肌阵挛性癫痫伴破碎红纤维,慢性进行性眼
外肌麻痹及kearns-sayre综合征。
melas表现为乳酸中毒及脑卒中样发作,是由于遗传缺陷引起的线粒体代谢酶缺陷,氧化磷酸化代谢脱偶联引起mtdna突变,影响线粒体转运rna。
该病主要临床特点:(1)常于10~40岁发病,儿童及青少年多见; (2)肢体近端无力,运动不能耐受, 伴轻度肌缩; (3)以卒中样发作为特点,可表现为偏瘫、失语、偏盲、视物模糊等; (4)局限性或全面性癫样发作,发作性头痛、呕吐、精神症状或意识障碍; (5)上述临症状反复发作,可逐渐出现智能下降、痴呆;(6)伴有发育异常, 如身材矮小、发际低、弓形足、神经性聋等。
(7)肌肉病理学检查发现破碎红纤维。
(8)影像学检查:头部mri改变[1]主要累及枕、顶、颞叶,大多不在同一血管支配范围内,病灶多位于皮质与皮质下, 呈 t1wi 低信号, t2wi 及flair 高信号,呈皮质层状受累的特点; 慢性或恢复期病灶缩小或消失;随着病情的反复发作、迁延、新老病灶可以交替出现;mrs可见lac峰明显增高,naa峰不同程度降低。
该例患者病例特点为:青年男性,糖尿病史及家族史;有卒中样发作症状,活动不耐受,神经性耳聋;血清及脑脊液乳酸浓度高于正常;脑电图异常;头mri可见左侧枕叶皮层长t1、长t2信号影,dwi上为高信号影,mra血管检查未见异常,病灶分布区不符合血管支配,mrs提示乳酸峰增高,naa峰减低;反复肌肉活检见破碎红纤维;院外基因检查提
示为3243a-g点突变。
根据临床、病理及基因检查结果确诊为melas,患者伴有糖尿病及神经性耳聋,为伴有糖尿病及神经性耳聋的melas。
国内此类患者仅见2例报道,该患者经基因检查为3243a-g点突变,与国外报道的病例一致[2]。
国外研究证实,3243a-g点突变出现于80%临床表现典型的患者,其他部位突变包括mt-tl1尤其是mt-nd5亦可以出现该病。
ballinger等[3]报道了一线粒体缺失的母系遗传表型为糖尿病及耳聋,患者无明显线粒体肌病表现。
参考文献
[1] 董松申,王佳薇.线粒体脑病的mri表现及误诊分析.吉林医学,2010,31(21):3541~3542.
[2] van den ouweland jm , lemkes hh, ruitenbeek w et al. mutation in mitochondrial trnal eu (uur) gene in a large pedigree with maternally transmitted type 2 diabetes mellitus and deafness. n at genet, 1992, 1: 368 .
[3]ballinger sw, et al.maternally transmitted diabetes and deafness associated with 10.4kb mitochondrial dna deletion.nature genetics,
1992,1:11.。
