生物化学复习总结之呼吸链
呼吸链--生物化学.doc

第七章生物氧化1、生物氧化(biological oxidation):物质在体内进行氧化称生物氧化。
主要指营养物质在体内分解时逐步释放能量,最终生成CO2和水的过程。
生物氧化又称组织呼吸或细胞呼吸。
生物氧化释放的能量:主要(40%以上)用于ADP的磷酸化生成A TP,供生命活动之需。
其余以热能形式散发用于维持体温。
2、生物氧化内容(1)生物体内代谢物的氧化作用、代谢物脱下的氢与氧结合成水的过程。
(2)生物体内二氧化碳的生成。
(3)能量的释放、储存、利用(ATP的代谢——A TP的生成与利用)。
3、生物氧化的方式——遵循一般氧化还原规律。
(1)失电子:代谢物的原子或离子在代谢中失去电子,其原子正价升高、负价降低都是氧化。
(2)脱氢:代谢物脱氢原子(H=H++e)的同时失去电子。
(3)加氧:向底物分子直接加入氧原子或氧分子的反应使代谢物价位升高,属于氧化反应。
向底物分子加水、脱氢反应的结果是向底物分子加入氧原子,也属于氧化反应。
4、生物氧化的特点(1)在温和条件下进行(37℃,中性pH等);(2)在一系列酶催化下完成;(3)能量逐步释放,部分储存在A TP分子中;(4)广泛以加水脱氢方式使物质间接获得氧;(5)水的生成由脱下的氢与氧结合产生;(6)反应在有水环境进行;(7)CO2由有机酸脱羧方式产生。
5、物质体外氧化(燃烧)与生物氧化的比较(1)物质体内、体外氧化的相同点:物质在体内外氧化所消耗的氧量、最终产物、和释放的能量均相同。
(2)物质体内、体外氧化的区别:体外氧化(燃烧)产生的二氧化碳、水由物质中的碳和氢直接与氧结合生成;能量的释放是瞬间突然释放。
5、营养物氧化的共同规律糖类、脂类和蛋白质这三大营养物的氧化分解都经历三阶段:分解成各自的构件分子(组成单位)、降解为乙酰CoA、三羧酸循环。
第一节 ATP生成的体系一、呼吸链(respiratory chain):代谢物脱下的氢原子(2H)通过多种酶和辅酶所催化的连锁反应逐步传递,最终与氧结合生成水。
生化名词解释
名词解释1、呼吸链:呼吸链又叫电子传递链,是由位于线粒体内膜(真核)中的一系列电子传递体按标准氧化还原电位,由低到高顺序排列组成的一种能量转换体系。
2、生物氧化:能源物质在活细胞中氧化分解,释放化学能并转化为生物能的生化过程,称 为生物氧化,又叫细胞氧化或细胞呼吸。
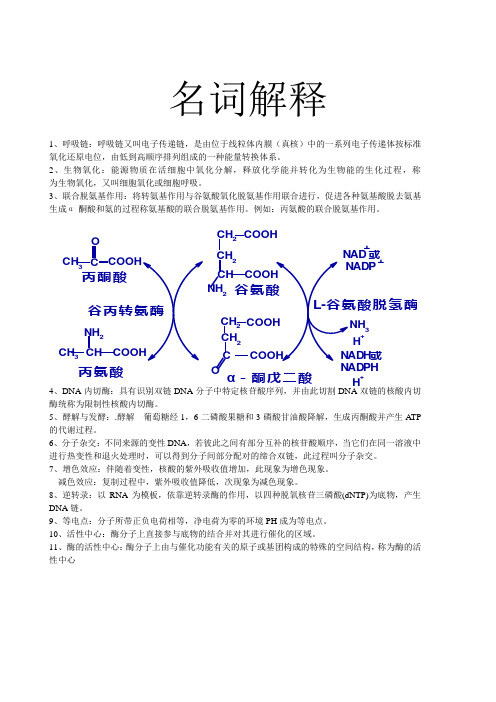
3、联合脱氨基作用:将转氨基作用与谷氨酸氧化脱氨基作用联合进行,促进各种氨基酸脱去氨基生成α-酮酸和氨的过程称氨基酸的联合脱氨基作用。
例如:丙氨酸的联合脱氨基作用。
4、DNA 内切酶:具有识别双链DNA 分子中特定核苷酸序列,并由此切割DNA 双链的核酸内切酶统称为限制性核酸内切酶。
5、酵解与发酵:.酵解 葡萄糖经1,6-二磷酸果糖和3-磷酸甘油酸降解,生成丙酮酸并产生ATP的代谢过程。
6、分子杂交:不同来源的变性DNA ,若彼此之间有部分互补的核苷酸顺序,当它们在同一溶液中进行热变性和退火处理时,可以得到分子间部分配对的缔合双链,此过程叫分子杂交。
7、增色效应:伴随着变性,核酸的紫外吸收值增加,此现象为增色现象。
减色效应:复制过程中,紫外吸收值降低,次现象为减色现象。
8、逆转录:以RNA 为模板,依靠逆转录酶的作用,以四种脱氧核苷三磷酸(dNTP)为底物,产生DNA 链。
9、等电点:分子所带正负电荷相等,净电荷为零的环境PH 成为等电点。
10、活性中心:酶分子上直接参与底物的结合并对其进行催化的区域。
11、酶的活性中心:酶分子上由与催化功能有关的原子或基团构成的特殊的空间结构,称为酶的活性中心C COOH CH COOH CH 2COOH C COOH O CH 2CH 2COOH CH COOH NH 2CH 2谷氨酸NH 2CH 3CH 3O 丙氨酸丙酮酸谷丙转氨酶NA D NA DP 或NA DH 或NA DPH H +++H +NH 3L-谷氨酸脱氢酶α-酮戊二酸。
种子092 呼吸链

表示无机硫原子
铁硫蛋白类
铁硫蛋白类( 铁硫蛋白类 ( iron-sulfur protein) 又称非血红 ) 素铁蛋白(nonheme iron protein), 是一类含铁硫络 素铁蛋白 , 合物的蛋白质。 合物的蛋白质。
+
NAD
+
+ FMNH 2
延胡索酸 + FADH 2
此类酶所表现出的催化活性与某些金 属离子的存在有密切关系,如NADH脱氢酶 和琥珀酸脱氢酶等含有几个非血红素铁原 子,这些铁原子能与硫原子结合形成铁硫 蛋白或铁硫中心,依赖铁的价态改变(Fe2+ ↔ Fe3+)来传递电子。
(3)铁硫蛋白类(Fe—S)
(四)细胞色素氧化酶(复合体Ⅳ (四)细胞色素氧化酶(复合体Ⅳ)
由 cyt.a和a3 组成。复合物中除了含有铁卟啉外, 还含有2个铜原子(CuA,CuB)。Cyta与CuA相配 合,cyta3与CuB相配合,当电子传递时,细胞色素 的Fe3+ Fe2+间循环,同时Cu2+ Cu+间循环,将 电子从cytc直接传递给O2。 功能:将电子从细胞色素C传递给O2,同时 发生质子的跨膜移位。
交替氧化酶是抗氰呼吸链的末端氧化酶, 交替氧化酶是抗氰呼吸链的末端氧化酶,该 单位酶由核基因编码,是一种非血红素铁蛋白, 单位酶由核基因编码,是一种非血红素铁蛋白, 以同源二聚体形式结合于线粒体内膜上, 以同源二聚体形式结合于线粒体内膜上,并且两 个单位之间通过一个二硫键相连。 个单位之间通过一个二硫键相连。 交替氧化酶与植物开花、种子萌发、果 植物开花、种子萌发、 植物开花 实成熟和植物的抗病性有密切的关系。 实成熟和植物的抗病性有密切的关系。
呼吸链生物化学

第七章生物氧化1、生物氧化(biological oxidation):物质在体内进行氧化称生物氧化。
主要指营养物质在体内分解时逐步释放能量,最终生成CO2和水的过程。
生物氧化又称组织呼吸或细胞呼吸。
生物氧化释放的能量:主要(40%以上)用于ADP的磷酸化生成A TP,供生命活动之需。
其余以热能形式散发用于维持体温。
2、生物氧化内容(1)生物体内代谢物的氧化作用、代谢物脱下的氢与氧结合成水的过程。
(2)生物体内二氧化碳的生成。
(3)能量的释放、储存、利用(ATP的代谢——A TP的生成与利用)。
3、生物氧化的方式——遵循一般氧化还原规律。
(1)失电子:代谢物的原子或离子在代谢中失去电子,其原子正价升高、负价降低都是氧化。
(2)脱氢:代谢物脱氢原子(H=H++e)的同时失去电子。
(3)加氧:向底物分子直接加入氧原子或氧分子的反应使代谢物价位升高,属于氧化反应。
向底物分子加水、脱氢反应的结果是向底物分子加入氧原子,也属于氧化反应。
4、生物氧化的特点(1)在温和条件下进行(37℃,中性pH等);(2)在一系列酶催化下完成;(3)能量逐步释放,部分储存在A TP分子中;(4)广泛以加水脱氢方式使物质间接获得氧;(5)水的生成由脱下的氢与氧结合产生;(6)反应在有水环境进行;(7)CO2由有机酸脱羧方式产生。
5、物质体外氧化(燃烧)与生物氧化的比较(1)物质体内、体外氧化的相同点:物质在体内外氧化所消耗的氧量、最终产物、和释放的能量均相同。
(2)物质体内、体外氧化的区别:体外氧化(燃烧)产生的二氧化碳、水由物质中的碳和氢直接与氧结合生成;能量的释放是瞬间突然释放。
5、营养物氧化的共同规律糖类、脂类和蛋白质这三大营养物的氧化分解都经历三阶段:分解成各自的构件分子(组成单位)、降解为乙酰CoA、三羧酸循环。
第一节 ATP生成的体系一、呼吸链(respiratory chain):代谢物脱下的氢原子(2H)通过多种酶和辅酶所催化的连锁反应逐步传递,最终与氧结合生成水。
呼吸链

呼吸链是指存在于线粒体内膜上的,按一定顺序排列的一系列酶或辅酶,其作用是以传递电子和质子的形式传递代谢脱下的氢原子(2H),最后是活化的氢和活化的氧结合生成水,该传递链进行的连锁反应与细胞摄取氧的呼吸过程有关,故称为呼吸链,也叫电子传递连。
(一)呼吸链的组成呼吸链的4个酶复合体和2个游离存在的电子传递体(CoQ和Cyt c)组成,他们按照上图的顺序排列。
1.图中显示的复合体Ⅰ,即NADH-Q还原酶(NADH-Q reductase),又称为NADH脱氢酶,只是一个具有相对分子质量880kDa的大蛋白质分子,含有42条多肽链,其中含有的辅基有黄素单核苷酸(FMN)、Fe-S簇(至少六种,且与蛋白质结合后称为铁-硫蛋白),功能是催化一对电子从NADH传递给CoQ,一对电子从复合物Ⅰ传递时伴随着4个质子被传递到膜间隙。
发生反应:NADH +Q+5H N+ →QH2 + 4H p+NAD+2.图中显示的紫色小体,即辅酶Q,又称泛醌,它以不同形式在电子传递链中起到传递电子的作用,处在中心地位,它在呼吸链中是一种和蛋白质结合不紧密的辅酶,这使得他在黄素蛋白和细胞色素类之间能够作为一种特殊灵活的电子载体起作用。
3.图中显示的复合体Ⅱ,即琥珀酸-Q还原酶,他是嵌在线粒体内膜的酶蛋白,完整的酶还包括柠檬酸中氧化为延胡索酸的琥珀酸脱氢酶,功能是催化电子从琥珀酸传递给辅酶Q,复合物Ⅱ传递电子时不伴随氢的传递。
4.图中显示的复合体Ⅲ,即细胞色素还原酶,他的作用是催化电子是从GH2转移到细胞色素c,其血红素辅基的铁原子,在电子传递中发生2价和3价之间价态的可逆变化,细胞色素还原酶每传递一对电子,同时传递4个H+到膜间隙。
发生如下反应:QH2+2细胞色素c1(氧化态)+2H N+→Q+ 2细胞色素c1(氧化态)+4H p+5.图中显示的蓝色小体,即细胞色素c,它是一个相对分子质量为13kDa的较小球形蛋白质,它是唯一能溶于水的细胞色素,当他的单一血红素单位接受了来自复合体Ⅲ的一个电子后,细胞色素移动到复合体Ⅳ而将电子提供给位于复合体Ⅳ中的双核铜中心,在复合体Ⅲ和Ⅳ之间起传递电子的作用。
呼吸链

抑制剂
抑制剂
1.鱼藤酮、安密妥、杀粉蝶菌素:阻断电子从NADH到辅酶Q的传递。鱼藤酮是极毒的植物物质,可作杀虫剂。 2.抗霉素A:从链霉素分离出的抗生素,抑制从细胞色素b到c1的传递。 3.氰化物、叠氮化物、CO、H2S等,阻断由细胞色素aa3到氧的传递。
谢谢观看
(a)单个铁与半胱氨酸硫相连 (b)2Fe-2பைடு நூலகம் (c)4Fe-4S
铁硫蛋白中的铁可以呈两价(还原型),也可呈三价(氧化型),由于铁的氧化、还原而达到传递电子作用。
在呼吸链中它多与黄素蛋白或细胞色素b结合存在。
泛醌
图1呼吸链泛醌(ubiquinone,UQ或Q),亦称辅酶Q(coenzyme Q),为一脂溶性苯醌,带有一很长的侧链, 是由多个异戊二烯(isoprene)单位构成的,不同来源的泛醌其异戊二烯单位的数目不同,在哺乳类动物组织中 最多见的泛醌其侧链由10个
复合体Ⅱ
由琥珀酸脱氢酶(一种以FAD为辅基的黄素蛋白)和一种铁硫蛋白组成,将从琥珀酸得到的电子传递给辅酶Q。
辅酶Q
是呼吸链中唯一的非蛋白氧化还原载体,可在膜中迅速移动。它在电子传递链中处于中心地位,可接受各种 黄素酶类脱下的氢。复合体Ⅲ辅酶Q:细胞色素C氧化还原酶复合体,是细胞色素和铁硫蛋白的复合体,把来自辅 酶Q的电子,依次传递给结合在线粒体内膜外表面的细胞色素C。
铁硫蛋白
铁硫蛋白(iron-sulfur proteins,Fe-S),又称铁硫中心,其特点是含铁原子。铁是与无机硫原子或是 蛋白质肽链上半胱氨酸残基的硫相结合,常见的铁硫蛋白有三种组合方式(a)单个铁原子与4个半胱氨酸残基上 的巯基硫相连。(b)两个铁原子、两个无机硫原子组成(2Fe-2S),其中每个铁原子还各与两个半胱氨酸残基 的巯基硫相结合。(c)由4个铁原子与4个无机硫原子相连(4Fe-4S),铁与硫相间排列在一个正六面体的8个顶 角端;此外4个铁原子还各与一个半胱氨酸残基上的巯基硫相连。
高中生物竞赛-呼吸链与氧化磷酸化

一、呼吸链(respiratory chain)
1. 基础描述: 整个氢的传递和电子的传递过程以及参与这一系列
催化反应的酶与辅酶及其他中间递体一个接一个,组成 链状反应体系,如同接力棒一样,这种形式的反应称为 呼吸链(电子传递链)。
递氢体:呼吸链中参与传递H的辅酶或辅基。 递电子体:呼吸链中参与传递电子的辅酶或辅基。
种唯一的非蛋白组分,有一个长的异戊二烯侧链,因广泛存 在得名。是呼吸链中参入到线粒体内膜的电子传递体和质子 转移体,连接复合体Ⅰ( Ⅱ)和复合体Ⅲ。
CoQ在呼吸链中接受黄素酶的H,本身被还原为氢醌, 再把H传递给Cyt体系被氧化,接受1e变为半醌自由基,接受 2e变为氢醌(QH2)。
一、呼吸链(respiratory chain)
到线粒体内,同时合成好的ATP也必须能运出线粒体在细胞 质中水解供能。
腺苷酸转位酶(Adenine nucleotide translocase)是内膜上的 酶,为反向转运体,可以把ADP转运到线粒体内,也能把合 成的ATP从线粒体运到胞液。
二、氧 化 磷 酸 化
2. 腺苷酸和磷酸转位酶 ATP—ADP反向转运体
一、呼吸链(respiratory chain)
一、呼吸链(respiratory chain)
一、呼吸链(respiratory chain)
3. 酶复合体:
一、呼吸链(respiratory chain)
3. 1 复合体Ⅰ :NADH-CoQ氧化还原酶 2个组分: FMN、 铁—硫中心
一、呼吸链(respiratory chain)
一、呼吸链(respiratory chain)
生物化学复习总结之呼吸链

氧化磷酸化 (Oxidative Phosphorylation)
生物氧化过程中,代谢物脱下的氢经呼吸链氧化
为水时所释放的能量转移给ADP形成ATP的过程。实
际上是氧化作用与氧化作用过程释放的能量用于形成
ATP的过程(磷酸化作用)两种作用的偶联反应。
ATP必须运输出线粒体
ATP 离开, ADP进入线粒体- 通过一种“转位酶” 。ATP离开是有利 的,因为细胞液比基质要 “+”。然而ATP出去和ADP进入有1个负电 荷的净转移——相当于有1个质子进入基质。 所以每1个ATP的输出 消耗1个H+ 。1个ATP合成大概需要消耗3 H+ 。于是,合成及加上 输出 1 ATP = 4H+
复合物Ⅳ:细胞色素C到O2
• 复合物Ⅳ又称细胞色素氧化酶
• 功能:在呼吸链的最后一步,把Cyt c的电子转移给 O2,使其还原生成H2O。
• 结构:The complex has a large molecule(分子) (MW
204 kD) and consists more than ten subunits (13); 电子传递的顺序为:Cyt c-CuA-a-a3-CuB-O2,每4 e通过复 合物时,酶从基质中消耗4个“底物”H+,生成2H2O,每通 过1 e,利用氧化还原反应的能量泵出1 H+到内膜外空间。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
细胞色素(cห้องสมุดไป่ตู้tochromes)
• 细胞色素都是膜结合蛋
白。 • 不同种类的细胞色素的辅 基结构及与蛋白质连接的 方式是不同的 • 不同的血红素有不同的特 征吸收谱带; • 血红素的氧化态与还原态 的光吸收是不同的。 • 唯一水溶性的细胞色素; • 分子量为~13,000;
Cytochrome C
复合物Ⅱ :琥珀酸到泛醌
呼吸链上还有其他底物的电子流经Q,但不 经过复合物II: – 脂酰CoA脱氢酶 – 3-磷酸甘油脱氢酶 往往将这些由FAD作为辅基的脱氢酶统称 为琥珀酸脱氢酶类。
复合物Ⅲ :泛醌到Cyt c
(细胞色素bc1复合物或CoQ: Cyt c氧化还原酶)
又称细胞色素bc1复合物,或泛醌:细胞色
底物水平磷酸化
(Substrate Level Phosphorylation)
• 底物分子首先因脱氢、脱水等作用形成一种高能中间 化合物; • 高能中间化合物是由于底物氧化时底物内分子重排形 成的; • 高能键通过转磷酰基给ADP,转移时有非常大的平衡 常数和一个大的ΔGº’ 负值;
• 一分子高能中间化合物只能形成一个ATP;
• 基质水平磷酸化是酵解过程中获取能量的唯一方式。
氧化磷酸化
(Oxidative Phosphorylation)
生物氧化过程中,代谢物脱下的氢经呼吸链氧化
为水时所释放的能量转移给ADP形成ATP的过程。实 际上是氧化作用与氧化作用过程释放的能量用于形成 ATP的过程(磷酸化作用)两种作用的偶联反应。
F1F0-ATP合酶抑制剂
解偶联剂
ATP/ADP交换体抑制剂
的活性基团。 铁硫中心的结构:最简单的是单铁原子与4个Cys的SH相连;更复杂的是有2个或4个铁原子。Rieske铁 硫蛋白则为1个铁原子与两个His残基相连。 蛋白含有的铁是非血红素铁,它借铁的价态变进行电子 传递,氧化型与还原型的的颜色不同,Fe3+为红、 绿,而Fe2+为无色. 注意:铁硫蛋白在电子传递链中,虽然起到传电子的作用, 但这不是传递链中一个单独的组分,往往是与其它组分 结合在一起共同起传递电子的作用。
NAD+及与NAD+偶联的脱氢酶 NAD+是一种流动的电子传递体。
黄素及与黄素偶联的脱氢酶 辅酶Q 属于一种流动的电子传递体。
铁硫蛋白 细胞色素 细胞色素c是一种流动的电子传递体
氧气
呼吸链的组成及其作用机制
吡啶核苷酸与吡啶核苷酸型脱氢酶
吡啶核苷酸型脱氢酶,属脱氢酶类,包括脱氢酶复合物, 但它们的辅酶大多相同,主要有两种:
呼吸链四个复合物的电子和质子流动总图
NAD-Q还原酶
琥珀酸-Q还原酶
细胞色素还原酶
细胞色素氧化酶
电子传递链中的复合体
• 复合体Ⅰ:NADH脱氢酶复合体
也称NADH: 泛醌氧化还原酶,是一个大的 酶复合物,由42条不同的多肽链组成,包括 含FMN黄素蛋白和至少6个铁硫中心。高分
辨率电子显微镜显示复合物Ⅰ为L形,L的一
辅酶Q(Coenzyme Q,CoQ)
脂溶性醌类化合物,有一个长的异戊二烯侧链,因广泛 存在得名,又称泛醌(Ubiquinone) 。位于线粒体内膜。
辅酶Q为电子和质子载体。CoQ在呼吸链中接受脱氢酶
传递过来的H,本身被还原为氢醌,再把电子传递给Cyt 体系而被氧化,接受1 e变为半醌自由基,接受2e变为 氢醌(QH2)。
NAD+(CoI ): Nicotinamide AdenineDinucleotide
NADP+(CoII): Nicotinamide Adenine Dinucleotide Phosphate
分子中起递氢作用的是烟酰胺,能反复氧化和还原,起到接
受氢和提供氢的作用而传递氢。
根据NAD(P)+的光谱变化进行测定
素c氧化还原酶。 作用:偶联催化电子由氢醌到Cyt c的转移
和质子由膜内基质向膜外空间的运输。
复合物Ⅲ :泛醌到Cyt c
(细胞色素bc1复合物或CoQ: Cyt c氧化还原酶)
结构:复合物Ⅲ和Ⅳ结构的确定(1995-1998,X-
射线晶体学)是线粒体电子转移研究的里程碑。复
合物Ⅲ是一个由相同单体组成的二聚体,每个单体
CoQ不仅接受NADH脱氢酶的H,还接受线粒体内其
它脱氢酶的H,如琥珀酸脱氢酶,脂酰CoA脱氢酶及 其它黄素脱氢酶脱下的H,在电子传递链中处于中心 地位。
细胞色素(cytochromes)
• 结构:细胞色素是一类色蛋白,以血红素为辅基
• 功能:在电子传递链中起传递电子的作用; 通过血红素
中Fe原子的价态变化传递电子(血红蛋白与肌红蛋白的 血红素不发生价态变化) • 血红素结构是划分细胞色素的依据 a, a3, b, c, c1….. • 都是膜结合蛋白,只有Cyt c是可溶的
个臂在膜内,另一臂伸展到基质中。
复合体Ⅰ:NADH脱氢酶复合体
复合物Ⅰ催化两个同时发生的偶联过程:
(1)NADH + H+ + Q NAD+ + QH2
(2)4个质子由基质转到内膜外
因此,复合物Ⅰ是由电子转移能所驱动的质子
泵,结果内膜基质面变负,内膜外侧变正。
复合物Ⅱ :琥珀酸到泛醌
也称琥珀酸脱氢酶,是TCA循环中唯一的一个 线粒体内膜结合的酶,虽比复合物Ⅰ小而简单,但 含有两类辅基和至少4种不同的蛋白,1个蛋白与 FAD及有4个铁原子的Fe-S中心共价结合;1个铁硫 蛋白。电子由琥珀酸流向FAD,然后通过Fe-S中心 到泛醌。
• 位于线粒体内膜的外测; • 每次接受和传递一个电子
电子传递链各组分的排列顺序
The order of the electron-transferring chain
从NADH→O2的电子传递顺序:
NADH →FP1→4FeS →CoQ→(2FeS) ↓ Cyt b→Cyt c1→Cyt c ↓ Cyt a a3→O2
磷氧比(P/O)
氧化磷酸化的效率可以通过测定P/O值来确定。P/O值
是指电子传递过程中,每消耗1摩尔氧原子所生成的 ATP的摩尔数。消耗的氧原子数目相当于传递给氧气 的电子数的1/2,消耗的无机磷酸等于氧化磷酸化产生 的ATP。 细胞内的氧化磷酸化是受到严格调控的,调控的手 段主要是它与电子传递之间的反馈。确切的说是ADP 浓度控制,这种由ADP对氧化磷酸化的调节被称为呼 吸控制。 代谢物脱下的2H经NADH氧化呼吸链被氧化为水时, 生成3ATP(P/O≈3),而经琥珀酸氧化呼吸链氧化为 水时,生成2ATP(P/O≈2)。
呼吸链的组成及其作用机制
黄素脱氢酶类
• 是一类不需氧的含黄素的脱氢酶; • 种类多,酶蛋白不同,辅基有两种: 黄素单核苷酸(Flavin Mononucleotide,FMN); 黄素腺嘌呤二核苷酸(Flavin Adenine Dinucleotide, FAD)
• 此类酶催化由NADH分子上脱氢(NADH脱氢酶,酶
蛋白称为FP1),生成FMNH2,或催化由琥珀酸分 子上脱氢(琥珀酸脱氢酶,酶蛋白称为FP2)生成 FADH2。
呼吸链的组成及其作用机制
铁-硫中心(Iron-sulfur Centers, 铁硫蛋白) 铁硫中心(Fe-S):铁硫蛋白中铁与无机硫原子(Fe
与S等量)和/或蛋白质中Cys残基的硫原子相连所形成
氧化磷酸化的抑制剂
抑制类型 呼吸链抑制剂 抑制剂名称 鱼藤酮、安米妥、杀粉菌素 萎锈灵 抗霉素A 氰化物、CO、H2S、叠氮化物 Aurovertin 寡霉素、venturicidin DCCD DNP、FCCP 缬氨霉素 生热素 苍术苷、米酵菌酸 作用位点或作用机制 复合体I 复合体II 复合体III 复合体IV 抑制F1 抑制F0 阻止质子通过质子F0通道 脂溶性质子载体 钾离子载体,破坏电势能 质子通道 抑制线粒体基质内的 ATP 与细胞质内 的ADP之间交换
ATP必须运输出线粒体
ATP 离开, ADP进入线粒体- 通过一种“转位酶” 。ATP离开是有利 的,因为细胞液比基质要 “+”。然而ATP出去和ADP进入有1个负电 荷的净转移——相当于有1个质子进入基质。 所以每1个ATP的输出 消耗1个H+ 。1个ATP合成大概需要消耗3 H+ 。于是,合成及加上 输出 1 ATP = 4H+
含有11个不同的亚基。
复合物Ⅳ:细胞色素C到O2
• 复合物Ⅳ又称细胞色素氧化酶
• 功能:在呼吸链的最后一步,把Cyt c的电子转移给 O2,使其还原生成H2O。 • 结构:The complex has a large molecule(分子) (MW 204 kD) and consists more than ten subunits (13); 电子传递的顺序为:Cyt c-CuA-a-a3-CuB-O2,每4 e通过复 合物时,酶从基质中消耗4个“底物”H+,生成2H2O,每通 过1 e,利用氧化还原反应的能量泵出1 H+到内膜外空间。
呼吸链(电子传递链)
电子传递(electron transfer): 底物脱下的氢和电子经过 系列载体的序列氧化还原反应,最终把电子和氢质子传 递给受体的过程,称之为电子传递。 电子传递链(electron transfer chain): 由一系列递氢体 和递电子体组成的氧化还原反应链,称之为电子传递链。 参与底物氧化的电子传递链也叫做呼吸链( respiration chain)。 递氢体:电子传递链中同时参与传递H+与电子的辅酶或 辅基。 递电子体:电子传递链中参与传递电子的辅酶或辅基。
