化学反应原理自测试题11页word
《化学反应原理》试卷及答案分析.docx

《化学反应原理》第 I 卷(选择题共 41 分)一、选择题(本题包括10 个小题,每小题 2 分,共 20 分,每小题只有一个答案符合题意)1.以油类为溶剂的防锈漆称为油基防锈漆,由于环保方面的原因,目前要推广使用水基防锈漆,但水基漆较易溶解O2,在干燥之前易导致金属表面产生锈斑,为此要在水基漆中加入缓蚀剂,以下可作为缓蚀剂添加的是()A. KMnO 4B. NaNO 2C.FeCl3D. HNO 32.下列说法中,正确的是()A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH 会增大B.在测定BaSO4沉淀的量前,先洗涤BaSO4沉淀,洗涤剂选择水或稀硫酸时的效果相同C.AgCl 悬浊液中加入KI 溶液,白色沉淀变成黄色,证明此条件下K sp(AgCl) > K sp(AgI) D.加水稀释酸溶液时,所有离子的浓度都降低3.广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。
根据上述信息,下列说法不正确的是()A. CaO 2的水解产物是 Ca(OH) 2和 H2O2B.PCl3的水解产物是 HClO 和 PH3C. NaClO 的水解产物之一是HClO D. Mg 3 N2的水解产物是两种碱性物质4. t0HA 与一元碱 BOH 溶液。
C 时,水的离子积为 K ,该温度下混合可溶性一元酸w下列有关混合液的关系式中,可确认溶液一定呈中性的是()A. pH = 7B. c(A- ) > c(B +)C.c (OH - ) =D.c (H+ )- c(OH - ) = c(A- )- c(B+) 5.有关下列装置图中的叙述正确的是()A.这是电解NaOH 溶液的装置B.这是一个原电池装置,利用该装置可长时间的观察到Fe(OH) 2沉淀的颜色C. Pt 为正极,其电极反应为: O--+ 2H O + 4e= 4OH22D.这是一个原电池装置,Pt 为负极, Fe 为正极6.已知胆矾溶于水使溶液温度降低,室温下将1mol无水硫酸铜制成溶液释放出热量为Q1kJ,又知胆矾分解的化学方程式为:CuSO4·5H2O(s)= CuSO4 (s)+5H 2O(l) ;△ H= +Q 2(Q2>0 ),则 Q1、 Q2的关系为()A. Q1 <Q 2B. Q1 >Q 2C. Q1 =Q 2D.无法确定7.分别取 pH=3 的两种一元酸HA 和 HB 溶液 10mL ,加入等量(过量)的镁粉,充分反应后,收集H2的体积在相同状况下分别为V1和 V2,若 V1>V 2,下列说确的是()A.将原酸溶液都稀释到1L, pH 都增大到5B.在相同条件下,NaA 水溶液的碱性弱于NaB 水溶液的碱性C. HB 一定是强酸D.反应开始时二者生成H2的速率相同8.已知 NaHSO 3溶液呈酸性、 NaHCO 3溶液呈碱性。
高中化学《化学反应原理》练习题(附答案解析)

高中化学《化学反应原理》练习题(附答案解析)学校:___________姓名:___________班级:___________一、单选题1.对于已建立化学平衡的可逆反应,当改变条件使化学平衡向正反应方向移动,下列有关叙述正确的是 ( )①生成物的质量分数一定增加; ②生成物的产量一定增加; ③反应物的转化率一定增大; ④反应物浓度一定降低;⑤正反应速率一定大于逆反应速率; ⑥使用了合适的催化剂; A .①②B .②⑤C .③④D .④⑥2.下列说法中,正确的是( ) A .K w 随温度、浓度的改变而改变B .凡是能自发进行的化学反应,一定是△H <0、△S >0C .对已达到化学平衡的反应,改变压强,平衡常数(K )一定改变D .Ksp 只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关3.近年来随着中国科技的崛起,中国电动汽车也随之获得迅猛发展,下列说法错误的是( ) A .电动汽车行驶时电池将化学能转化为电能 B .电动汽车行驶时电池的正极发生氧化反应 C .电动汽车充电时电池将电能转化为化学能 D .电动汽车充电时电池的阴极发生还原反应4.在反应C(s)+CO 2(g)=2CO(g)中,能使反应速率加快的是( ) ①增大压强 ②升高温度 ③将C 粉碎 ④通CO 2气体 ⑤加入足量木炭粉 A .①②③B .①②④C .①②③④D .全部5.下列反应不是吸热反应的是( ) A .2高温C+CO 2COB .()22Ba OH 8H O ⋅与4NH Cl 的反应C .铝热反应D .煅烧石灰石制取生石灰6.下列说法正确的是()A.化学反应速率是对可逆反应而言,非可逆反应无法计量化学反应速率B.在可逆反应中,正反应的反应速率是正值,逆反应的反应速率是负值C.在同一化学反应中,用不同物质来表示反应速率,其数值可能相同D.化学反应速率是单位时间内反应物或生成物物质的量的变化7.下列说法正确的是()A.上图所示的是一个放热反应B.加入催化剂v(正)增大、v(逆)减小C.燃烧热是生成1molH2O放出的热量D.只有活化分子才能发生有效碰撞8.电解饱和食盐水的实验中,在U型管的两端分别滴加无色酚酞试液,通电一会儿的现象为()A.产生黄绿色气泡的电极一端溶液变红B.产生无色气泡的电极一端溶液变红C.两端均变红D.两端均不变红9.在测定中和热的实验中,使用下列用品不是为了减小实验误差的是()A.碎泡沫塑料B.环形玻璃棒C.硬纸板D.两个量筒10.某课题组以纳米Fe2O3作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图所示),下列说法正确的是()A.该电池可以用水溶液作为电解质溶液B.该电池不能重复使用C.Fe2O3电极在充电时发生还原反应D.负极的电极反应式为2Li-2e-+O2-=Li2O11.下列事实能说明醋酸属于弱电解质的是()①中和10mL1mol/LCH3COOH溶液需要10mL1mol/LNaOH溶液②物质的量溶液相同时,完全相同的两块锌粒分别跟盐酸和醋酸反应,前者的速率快③0.01mol/L醋酸溶液的pH大于2④0.1mol/LCH3COONa溶液显碱性A.①②③B.②③④C.②③D.①④12.在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是()A.平均反应速度:甲<乙B.平衡时C的物质的量:甲>乙C.平衡时C的转化率:甲>乙D.平衡时混合气体密度:甲<乙二、填空题13.已知:(1)为了证明HF是弱酸,甲、乙、丙三位同学分别设计以下实验进行探究。
化学反应原理第一章测试卷试题

念书破万卷下笔若有神《化学反响原理》第一章测试题(相对原子质量:H 1 C 12 O 16 )一、选择题(此题包含10 小题,每题 5 分,共 50 分,每题只有一个正确答案)1.以下说法不正确的选项是A.化石燃料在任何条件下都能充分焚烧B.化石燃料在焚烧过程中能产生污染环境的CO、 SO2等有害气体C.直接焚烧煤不如将煤进行深加工后再焚烧的成效好D.固体煤变成气体燃料后,焚烧效率将提升2.以下选项中说明乙醇作为燃料的长处的是①焚烧时发生氧化反响②充分焚烧的产物不污染环境③乙醇是一种重生能源④焚烧时放出大批热量A .①②③B .①②④C.①③④ D .②③④3.将来新能源的特色是资源丰富,在使用时对环境无污染或污染很小,且能够重生。
以下属于将来新能源标准的是①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能A .①②③④B .⑤⑥⑦⑧C.③⑤⑥⑦⑧ D .③④⑤⑥⑦⑧4.以下反响既属于氧化复原反响,又是吸热反响的是A .铝片与稀盐酸反响B .氢气复原三氧化钨C.Ba(OH)2·8H 2O与NH 4Cl反响 D .甲烷在氧气中的焚烧反响5.已知葡萄糖焚烧热是2804 kJ·mol -1,当它氧化生成1g 液态水,放出的热量是A . 26.0 kJ B.51.9 kJ C.155.8 kJ6.已知: 101 kPa 时辛烷的焚烧热为5518 kJ ·mol-1,强酸与强碱在稀溶液中发生反响时的中和热为57.3 kJ ·mol -1,则以下热化学方程式书写正确的选项是①C8H18(l) + O2(g)=== 8CO2(g) + 9H2O (l) H=+5518 kJ·mol-1②C8H 18 2 2(g) + 9H2 O (l)H=–5518 kJ ·mol-1 (l) + O (g)=== 8CO③H++ OH—= H2O H=–57.3 kJ ·mol-1④ NaOH (aq) + H2 SO4(aq) == Na2SO4(aq) + H 2O(l) H=+57.3 kJ ·mol-1A .①③B.②③C.②④ D .只有②7.已知以下热化学方程式:C(s)+O2 (g)=CO 2(g)ΔH= -393.5 kJ/mo12H2 (g)+O 2(g)=2H 2O(g)ΔH= -483.6 kJ/mo1现有 0.2mol 的炭粉和氢气构成的悬浊气、固混淆物在氧气中完好焚烧,共放出63.53 kJ 热量,则炭粉与氢气的物质的量之比为A . 1∶ 2B . 2∶3C.1∶1 D .3∶ 28.已知1mol白磷(P4) 转变成 4mol 红磷,放出 73.6 kJ 热量,又知: P 4(白,s)+5O 2(g) = 2P 2O 5(s) H 1,4P (红, s )+5O 22 5 (s)H 2。
(完整word)《化学反应原理》模块测试题(含答案),推荐文档

《化学反应原理》模块测试题可能用到的相对原子质量:H-1 C-12 O-16 Cu-64第Ⅰ卷(共42分) 一、选择题(每小题2分,共22分。
每小题只有一个选项符合题意)1、已知反应X+Y= M+N 为放热反应,,对该反应的下列说法中正确的 A 、X 的能量一定高于M B 、Y 的能量一定高于NC 、X 和Y 的总能量一定高于M 和N 的总能量D 、因该反应为放热反应,故不必加热就可发生2、在pH=1的无色溶液中,下列离子能大量共存的是( ) A .NH 4+、Ba 2+、NO 3—、CO 32—B .Fe 2+、OH —、SO 42—、MnO 4—C .Na +、Fe 3+、Cl —、AlO 2—D .K +、Mg 2+、NO 3-、SO 42—3、在密闭容器里,A 与B 反应生成C ,其反应速率分别用A v 、B v 、C v 表示,已知2B v =3A v 、3C v =2B v ,则此反应可表示为( )A 、2A+3B=2CB 、A+3B=2C C 、3A+B=2CD 、A+B=C 4、可以将反应Zn+Br 2 = ZnBr 2设计成蓄电池,下列4个电极反应 ①Br 2 + 2e -= 2Br -②2Br - - 2e -= Br 2 ③Zn – 2e -= Zn 2+④Zn 2++ 2e -= Zn其中表示充电时的阳极反应和放电时的负极反应的分别是( )A .②和③B .②和①C .③和①D .④和①5、相同温度下等物质的量浓度的下列溶液中,pH 值最小的是 ( ) A .Cl NH 4B .34HCO NHC .44HSO NHD .424SO )(NH6、下列说法正确的是( )A 、物质的溶解性为难溶,则该物质不溶于水B 、不溶于水的物质溶解度为0C 、某离子被沉淀完全是指该离子在溶液中的浓度为0D 、绝对不溶解的物质是不存在的7、化学电池可以直接将化学能转化为电能,化学电池的本质是 ( )A .化合价的升降B . 电子的转移C .氧化还原反应D .电能的储存8、随着人们生活质量的不断提高,废电池必须集中处理的问题被提到议事日程,首要原因是( ) A 、利用电池外壳的金属材料B 、防止电池中汞、镉和铅等重金属离子对土壤和水源的污染C 、不使电池中渗泄的电解液腐蚀其他物品D 、回收其中石墨电极9、在一密闭容器中进行如下反应:2SO2(气)+O2(气)2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是()A.SO2为0.4mol/L、O2为0.2mol/L B.SO2为0.25mol/LC.SO2、SO3均为0.15mol/L D.SO3为0.4mol/L10、下列对化学平衡移动的分析中,不正确...的是()①已达平衡的反应C(s)+H2O(g) CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动②已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动A.①④B.①②③C.②③④D.①②③④11、可以充分说明反应P(g)+Q(g) R(g)+S(g)在恒温下已达到平衡的()A.反应容器内的压强不随时间改变B.反应容器内P、Q、R、S四者浓度之比为1:1:1:1 C.P的生成速率和S的生成速率相等D.反应容器内的气体总物质的量不随时间变化二、选择题(每小题2分,共20分。
高考化学化学反应原理综合练习题含答案.doc
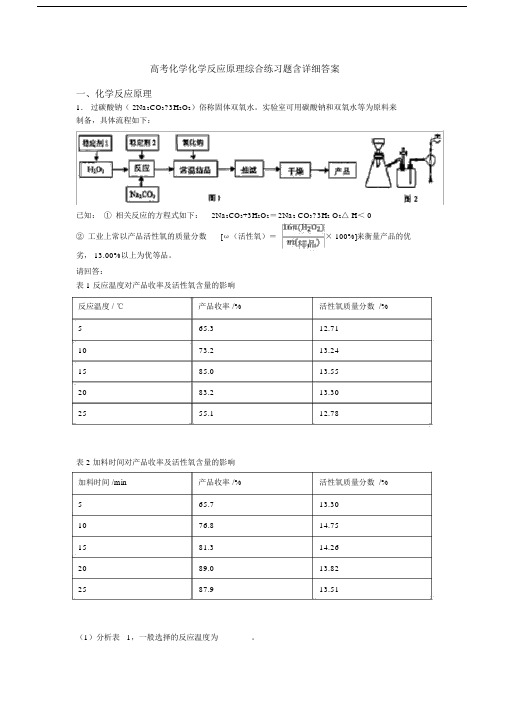
高考化学化学反应原理综合练习题含详细答案一、化学反应原理1.过碳酸钠( 2Na2CO3?3H2O2)俗称固体双氧水。
实验室可用碳酸钠和双氧水等为原料来制备,具体流程如下:已知:①相关反应的方程式如下:2Na2CO3+3H2O2=2Na2 CO3?3H2 O2△ H< 0② 工业上常以产品活性氧的质量分数[ω(活性氧)=× 100%]来衡量产品的优劣, 13.00%以上为优等品。
请回答:表 1 反应温度对产品收率及活性氧含量的影响反应温度 / ℃产品收率 /% 活性氧质量分数 /%5 65.3 12.7110 73.2 13.2415 85.0 13.5520 83.2 13.3025 55.1 12.78表 2 加料时间对产品收率及活性氧含量的影响加料时间 /min 产品收率 /% 活性氧质量分数 /%5 65.7 13.3010 76.8 14.7515 81.3 14.2620 89.0 13.8225 87.9 13.51(1)分析表1,一般选择的反应温度为_____。
(2)分析表 2,加料时间对产品收率也有很大影响,时间太短或太长均不利于生产,加料时间太短导致产品收率较低的原因是_____。
(3)结晶过程中加入氯化钠,作用是_____。
(4)下列关于抽滤操作,正确的是_____。
A.准备略大于漏斗内径的滤纸,以盖住布氏漏斗瓷板上的小孔B.用倾析法先转移溶液,待溶液快流尽时再转移沉淀C.洗涤沉淀时,加入少量水并开大水龙头,重复操作2~ 3 次D.用玻璃棒轻轻刮下抽滤得到的固体,晾干后保存在试剂瓶中(5)使用图 2 所示装置抽滤,中途需停止抽滤时,最佳操作为_____。
(6)产品出厂前需测定活性氧的质量分数,现将0.1000g 某厂的产品(所含杂质均不参与反应)溶于水配成溶液,加入10.00mL1.000mol ?L﹣1的稀硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量_____,用 0.1000mol ?L﹣1的 Na2 2 3标准溶液滴定,若该S O产品的活性氧质量分数为13.60%,则达到滴定终点时共消耗标准液的体积为_____mL。
有机化学反应机理的试题

有机化学反应机理的试题一、选择题:1.以下哪组反应物与产物的分子结构不符合Lewis键合原理?A) CH3-CHOH-CH3 → CH3-COH+H2B) CH3COOC2H5+NH3 → CH3CONH2+C2H5OHC) CH3COOH+NH3 → CH3CONH2+H2OD) CH3COOC2H5+NH3 → CH3CONH2+C2H5OH2.下列哪种反应机理是一个电子转移过程?A) 亲核攻击B) 脱离和合成C) 钮烯—烯D) 还原氧化3.以下关于甲烷燃烧反应机理的描述中,哪个是正确的?A) 甲烷与氧气反应生成一氧化碳和二氧化碳。
B) 甲烷经过链传递反应生成反应性较强的自由基。
C) 甲烷燃烧反应是一个核生成反应。
D) 甲烷的燃烧反应中没有高能化学键出现。
二、填空题:1. (3分) 以下是苯环上可能发生的反应之一:_________ 反应产物为苯环结构中的一个碳原子上引进了一个氢原子。
2. (3分) 下图是治疗心绞痛的一种药物分子的反应机理图,请根据图中所示的反应步骤填写下列句子中的空白:首先,药物分子和心绞痛的病理靶标发生_________ 反应,在此反应中药物分子失去了分子中的_______ 基团。
然后,得到的产物分子会与其他分子发生_______ 反应,从而完成心绞痛的治疗过程。
三、解答题:1. (10分) 请以苯酚醛为例解释亲核取代反应的机理,并画出反应机理图。
2. (10分) 请以诺贝尔奖获得者Suzuki的作用反应为例,说明亲电取代反应的机理,并画出反应机理图。
四、综合题:1. (20分) 解释以下反应机理中的术语:A) 钮烯—环加成反应B) 钮烯—烯反应C) pKa值D) Michael加成反应2. (20分) 解释以下反应机理中的术语:A) 光气B) 拉克-楞次催化剂C) 羟基自由基D) Knoevenagel缩合反应以上就是有机化学反应机理的试题。
请根据题目中的要求,用适合的格式书写你的答案,并在审阅后提交给相关人员。
《化学反应原理》测试题(含答案)

高二化学总复习《化学反应原理》检测题(总分:100分考试时间:90分钟)可能用到的相对原子质量:H 1 C 12 O 16 Na 23第I卷(选择题共50分)本卷每小题只有一个选项符合题意,每小题2分,共50分1.下列物质属于强电解质的是()A.氯化钠B.乙醇C.醋酸D.铜2.下列反应中,属于放热反应的是()A.CaCO,受热分解B.盐酸和NaOH溶液反应C.C与CO2反应D.Ba(OH)2·8H2O与NH4C1反应3.下列物质的水溶液显碱性的是()A.HClO B.NaCl C.FeCl3D.CH3 COONa4.下列溶液一定显酸性的是()A.含H+的溶液B.c(OH一)<c(H+)的溶液C.pH<7的溶液D.能与金属Al反应放出H2的溶液5.工业上常用电解法冶炼的金属是()A.Al B.Fe C.Cu D.Ag6.新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
下列属于能源的是()①煤②石油③太阳能④生物质能⑤氢能A.①②③B.①②⑤C.②③⑤D.③④⑤7.用石墨作电极,电解1 mol/L下列物质的溶液,pH保持不变的是()A.HCl B.NaOH C.Na2SO4D.NaCl8.下列各组离子在溶液中可以大量共存的是()A.H+、NH4+、CO32-B.Fe3+、Cl-、NO3-C.Na+、OH-、HCO3-D.Al3+、OH-、NO3-9.下列关于铜电极的叙述,正确的是()A.铜锌原电池中,铜是正极B.用电解法精炼粗铜时,粗铜作阴极C.在镀件上电镀铜时,可用金属铜作阴极D.电解稀硫酸制H2、O2时,铜作阳极10.下列说法不正确的是()A.电解池是将电能转化成化学能的装置B.化学键断裂时吸收能量,形成时放出能量C.增大反应物的浓度,可增加单位体积内活化分子数,从而使反应速率增大D.含0.1mol H2SO4的浓硫酸与含0.2 mol NaOH的溶液混合;放出的热量即为中和热11.下列说法正确的是()A.天然物质都比人造物质好B.通过化学变化一定能改变物质的性质C.氧化还原反应中不一定有电子转移 D.所有化学反应进行得越快、越彻底越好12.下列关于强、弱电解质的叙述,正确的是()A.强电解质全部是离子化合物B.强电解质在稀的水溶液中完全电离C.强电解质在水中的溶解度一定大于弱电解质在水中的溶解度D.强电解质溶液的导电能力一定很强,弱电解质溶液的导电能力一定很弱13.下列叙述不正确的是()A.钢铁在干燥的空气中不易被腐蚀B.可以用船尾连锌块的方法来保护船身C.金属的电化学腐蚀比化学腐蚀更普遍D.用铝质铆钉铆接铁板,铁板易被腐蚀14.表示下列变化的化学用语不正确的是()A.氨水显碱性:NH 3·H2O NH4++OH-B.硫酸氢钠溶液显酸性:NaHSO4=Na++H++SO42-C.Na 2S溶液显碱性:S2-+2H2O H2S+2OH-D.FeCl 3溶液显酸性:Fe3++3H2O Fe(OH)3+3H+‟15.下列事实不能用平衡移动原理解释的是()A.工业合成氨时使用催化剂B.配制FeCl3溶液时加入少量的盐酸C.在NaOH溶液中由水电离出的c(H+)<1×10-7mol/LD.AgCl在水中的溶解度大于在饱和NaCl溶液中的溶解度16.0.1 mol/L的CH 3COOH溶液中存在平衡:CH3COOH CH3COO-+H+。
最新化学反应原理自测试题

化学反应原理自测试题月考一复习题一、有机化合物组成、结构、命名1.下列各组物质不属于同分异构体的是( )A.2,2—二甲基丙醇和2—甲基丁醇B.邻氯甲苯和对氯甲苯C.2—甲基丁烷和戊烷 D.甲基丙烯酸和甲酸丙酯2.0.1 mol某有机物的蒸汽跟过量O2混合后点燃,生成13.2gCO2和5.4gH2O,该有机物跟金属钠反应放出H2,又能跟新制Cu(OH)2悬浊液加热时生成红色沉淀,还能跟乙酸反应生成酯类化合物,该酯类化合物的结构简式可能是( )。
A.CH3一CH(OCH3)一CHO B.C.D.3.下列各化合物的命名正确的是( )。
A.1,3—二丁烯B. 3—丁醇C.甲基苯酚D.2—甲基丁烷4.蛭得净M是一种抗血吸虫病药,其结构简式为:,下列说法错误的是( )。
A.M可看作是酚类化合物B.M可看作是芳香族化合物C.M可看作是磷酸的酚酯D.M不能发生加成反应5.《化学教育》报道了数起人因食用有“瘦肉精”的猪肉和内脏,而发生急性中毒的恶性事件。
这足以说明,目前由于奸商的违法经营,已使“瘦肉精”变成了“害人精”。
“瘦肉精”的结构可表示为:下列关于“瘦肉精”的说法正确的是( )。
A.摩尔质量为313.5 g B.属于芳香烃C.分子式为C12H19Cl3N2O D.不能发生加成反应6.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中—定不存在同分异构体的反应是( )。
A.异戊二烯()与等物质的量的Br2发生加成反应B.2一氯丁烷()与NaOH乙醇溶液共热发生消去HCl分子的反应C.甲苯在—定条件下发生硝化生成—硝基甲苯的反应D.2,2—二甲基丙烷和氯气等物质的量反应7.下列文字表述与反应方程式对应且正确的是( )A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓B.用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑C.利用腐蚀法制作印刷线路板: Fe3++Cu=Fe2++Cu2+D.实验室用液溴和苯在催化剂作用下制溴苯:8.下列有机反应中,不属于取代反应的是( )A.B.C.D.9.美军为打击躲藏在阿富汗山洞中的恐怖分子,使用了一种名为BLU—82的高效能燃料空气炸弹。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
月考一复习题一、有机化合物组成、结构、命名1.下列各组物质不属于同分异构体的是( )A.2,2—二甲基丙醇和2—甲基丁醇B.邻氯甲苯和对氯甲苯C.2—甲基丁烷和戊烷 D.甲基丙烯酸和甲酸丙酯2.0.1 mol某有机物的蒸汽跟过量O2混合后点燃,生成13.2gCO2和5.4gH2O,该有机物跟金属钠反应放出H2,又能跟新制Cu(OH)2悬浊液加热时生成红色沉淀,还能跟乙酸反应生成酯类化合物,该酯类化合物的结构简式可能是( )。
A.CH3一CH(OCH3)一CHO B.C.D.3.下列各化合物的命名正确的是( )。
A.1,3—二丁烯B. 3—丁醇C.甲基苯酚D.2—甲基丁烷4.蛭得净M是一种抗血吸虫病药,其结构简式为:,下列说法错误的是( )。
A.M可看作是酚类化合物B.M可看作是芳香族化合物C.M可看作是磷酸的酚酯D.M不能发生加成反应5.《化学教育》报道了数起人因食用有“瘦肉精”的猪肉和内脏,而发生急性中毒的恶性事件。
这足以说明,目前由于奸商的违法经营,已使“瘦肉精”变成了“害人精”。
“瘦肉精”的结构可表示为:下列关于“瘦肉精”的说法正确的是( )。
A.摩尔质量为313.5 g B.属于芳香烃C.分子式为C12H19Cl3N2O D.不能发生加成反应6.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中—定不存在同分异构体的反应是( )。
A.异戊二烯()与等物质的量的Br2发生加成反应B.2一氯丁烷()与NaOH乙醇溶液共热发生消去HCl分子的反应C.甲苯在—定条件下发生硝化生成—硝基甲苯的反应D.2,2—二甲基丙烷和氯气等物质的量反应7.下列文字表述与反应方程式对应且正确的是( )A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓B.用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑C.利用腐蚀法制作印刷线路板: Fe3++Cu=Fe2++Cu2+D.实验室用液溴和苯在催化剂作用下制溴苯:8.下列有机反应中,不属于取代反应的是( )A.B.C.D.9.美军为打击躲藏在阿富汗山洞中的恐怖分子,使用了一种名为BLU—82的高效能燃料空气炸弹。
这种炸弹爆炸时,除产生高温外,还可使山洞内的氧气耗尽,致使所有生物窒息死亡而山洞不致完全崩塌,以便后续军队进入山洞鉴别死者身份。
燃料空气弹所装炸药的成分之—是环氧乙烷(),试回答下列问题:(1)环氧乙烷属于烃衍生物中的( )。
A.醇类B.酮类C.环酮D.环醚(2)工业上可用乙醇为原料在Cu或Ag的催化下脱氢合成环氧乙烷,试用化学方程式表示上述过程_________________________________。
(3)爆炸时,环氧乙烷先变成雾状分散在空气中,然后燃爆,反应的生成物为CO2、CO和H2O。
用化学方程式表示上述过程_________________________________。
10.有机物X(分子式为C4H6O5)广泛存在于许多水果中,尤以苹果、葡萄、西瓜、山楂内为多。
经测定该有机物具有下列性质(见下表),请根据题目要求填空:(1)x的性质推测X结构中有关官能团的结论①足量的金属钠反应生氢气②X与醇或羧酸在浓硫酸加热条件下均能生成有香味的产物二、有机反应、有机推断、计算1.据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:。
对该物质判断正确的是( )。
A .晶体的硬度与金刚石相当B .能使酸性高锰酸钾溶液褪色C .不能发生加成反应D .不能使溴水褪色2.下列物质在催化剂作用下和氢气加成不能得到2—甲基戊烷的是( )。
A .CH 3CH =C(CH 3)CH 2CH 3 B .CH 3CH =CHCH(CH 3)2 C .(CH 3)2C =CHCH 2CH 3D .HCCCH 2CH(CH 3)23.CCTV 《科技博览》报道,2004年3月中科院首创用CO 2合成可降解塑料聚二氧化碳。
下列相关说法合理的( )。
A .聚二氧化碳塑料是通过加聚反应制得的B .聚二氧化碳塑料与干冰互为同素异形体C .聚二氧化碳塑料与干冰都属于纯净物D .聚二氧化碳塑料的使用会产生白色污染4.鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。
已知角鲨烯分子中含有30个碳原子及6个C =C 且不含环状结构,则其分子式为( );A .C 30H 60B .C 30H 56C .C 30H 52D .C 30H 505.法国化学家伊夫·肖万获发现了烯烃里的碳—碳双键会被拆散、重组,形成新分子,这种过程被命名为烯烃复分解反应。
烯烃复分解反应可形象地描述为交换舞伴(如图11所示)。
烯烃复分解反应中的催化剂是金属卡宾(如CH 2=M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈。
随后它们“交换舞伴”,组合成两个新分子,其中—个是新的烯烃分子,另一个是金属原子和它的新舞伴。
后者会继续寻找下一个烯烃分子,再次“交换舞伴”。
把C 6H 5CH 2CH =CH 2与CH 2=M 在一定条件下混合反应,下列产物不可能存在的是( )。
图11A .C 6H 5CH 2CH =MB .CH 2=CH 2C .C 6H 5CH 2 CH 2 C 6H 5D .C 6H 5CH 2CH =CH CH 2 C 6H 56.有机物X 、Y 分子式不同,它们只含C 、H 、O 元素中的两种或三种,若将x 、Y 不论以何种比例混合,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变。
X 、Y 可能是( )。
A .C 2H 4、C 2H 60B .C 2H 2、C 6H 6 C .CH 2O 、C 3H 6O 2D .CH 4、C 2H 4O 27.国际奥委会公布的违禁药物目前有138种。
某种兴奋剂的结构为关于它的说法中正确的( )。
A .从结构上看,它属于芳香烃B .它的分子中所有的碳原子共平面C .该物质的分子式为C 14H 22ClNO 2D .1 mol 该物质最多能与2 mol 氢氧化钠反应 8.聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之—,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点。
下边是聚丙烯酸酯的结构简式,它属于( )。
①无机化合物;②有机化合物;③高分子化合物;④离子化合物;⑤共价化合物。
A .①③④B .①③⑤C .②③⑤D .②③④9.两种有机物以一定比例混合,一定条件下在a LO 2(足量)中燃烧,充分反应后恢复到原状态,再通过足量Na 2O 2层,得到气体仍是aL ,下列混合有机物中符合此条件的( )。
A .CH 4、C 2H 4B .CH 3OH 、CH 3COOHC .C 2H 6、HCHOD .HCHO 、CH 3COOCH 3N O NHCH 3CH 310.某芳香族有机物的分子式为C 8H 8O 2,它的分子(除苯环外不含其他环)中不可能有( )。
A .一个羟基 B .一个醛基 C .两个醛基 D .一个羧基 11.苏丹红是很多国家禁止用于食品生产的合成色素,其结构简式如图。
关于苏丹红说法错误的是( )。
A .分子中含一个苯环和一个萘环B .属于芳香烃C .能被酸性高锰酸钾溶液氧化D .能溶于苯12.中国石油吉林石化公司双苯厂发生爆炸事故,大量硝基苯泄漏,引起松花江水受污染,安全生产和环保问题再次引起人们的关注。
下列关于硝基苯的叙述正确的是( )。
A .硝基苯是一种油状物质,会浮在水面上B .实验室制硝基苯需要用水浴加热C .硝基苯中毒是由蒸气吸入或误食引起的,与皮肤接触不会引起中毒D .硝基苯是由苯酚和硝酸直接反应生成的 13.下列各物质中,互为同系物的是( )。
B .HCOOCH 3,和CH 3COOHC .油酸和软脂酸14.4—甲基—2—乙基—1—戊烯经催化加成所得产物名称为( )。
A .4—甲基——2—乙基戊烷 B .2,5—二甲基戊烷 C .2—乙基—4—甲基戊烷D .2,4—二甲基己烷15.已知分子式为C 12H 12的物质A 结构简式为。
A 苯环上的二溴代物有9种同分异构体,由此推断A 苯环上的四氯代物的同分异构体数目有( )。
A .9种B .10种C. 11种D .12种16.近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。
图20是以煤为原料生产聚乙烯(PVC)和人造羊毛的合成线路。
请回答下列问题:(1)写出反应类型:反应①,反应②。
(2)写出结构简式:PVC ,C 。
(3)写出A→B的化学方程式。
(4)与D互为同分异构体且可发生碱性水解的物质有种(不包括环状化合物),写出其中一种的结构简式。
17.化合物A最早发现于酸牛奶中,它是人体糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。
A在某种催化剂存在下进行氧化,其产物不能发生银镜反应。
在浓硫酸存在下,A可发生如图21所示的反应。
回答下列问题:(1)写出B、D两种化合物的结构简式:B:;D:。
(2)写出下列化学反应方程式:A→E:;A→F:。
(3)反应类型:A→E : ;A→F: 。
18.有机物A、B、C、D、E能发生如图22所示的转化。
请回答下面有关问题:(1)写出A、B、C、D、E的名称。
(2)写出反应②的化学方程式,属于有机反应的哪一个类型:。
(3)说明反应⑤的产物在日常生活中常作为购物的方便袋,但不能作为食品袋的原因:,同时产物也是“白色污染”的祸根之一,其原因是。
19.现有A、B两种链状饱和一元醇的混合物0.3 mol,其质量为13.8g.已知A和B碳原子数均不大于4,且A<B。
(1)混合物中A可能的分子式是;B可能的分子式是。
(2)若n(A):n(B)=1:1时,A的名称是,B的名称是。
(3)若n(A):n(B)≠l:1时,A的结构简式为,B的结构简式为。
则n(A):n(B)=。
20.在400℃、101.3 kPa时,3 L某烃A在m L氧气中完全燃烧,燃烧后测得气体体积为(m+6)L(气体体积均在同温同压下测定)。
试回答下列问题:(1)烃A的组成应满足的条件是。
(2)当m=27时,烃可能的分子式(只要求写出三种可能的分子式)是、、。
(3)通过计算确定:若烃A在常温常压下为气态物质时, m的取值范围。
三.有机物的测定1.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物是( )。
2.由E(Fe)制备的E(C2H5)2的结构如,其中氢原子的化学环境完全相同。
但早期人们却错误地认为它的结构为:核磁共振法能够区分这两种结构。
在核磁共振氢谱中,正确的结构有种峰,错误的结构有种峰。
3.下列有机物分子中不含手性碳原子的是。
4.分子式为C3H6O2的二元混合物,如果在核磁共振氢谱上观察到氢原子给出的峰有两种情况。
