弱酸、弱碱的解离常数表
强碱弱酸盐的水解平衡常数

强碱弱酸盐的水解平衡常数盐类在溶液中,与水作用而改变溶液的酸碱性的反应叫作盐类的水解。
水解常数的大小表示盐的水解达到平衡时,水解程度的大小,水解常数的大小取决于盐中弱酸或弱碱的解离常数的大小。
既不含H+又不含OH-的盐溶于水而显酸碱性,是由于盐的一个或两个离子和水中的H+和OH-结合,从而使水的电离平衡移动的结果,盐的组分离子与溶液中水电离出的H+和OH-作用产生弱电解质的反应称盐类的水解。
分类:盐的组分离子与水发生反应而改变溶液的酸度,涉及质子的转移,所以也是一种酸碱反应。
弱酸强碱盐的水解常数NaAc、KCN、Na2CO3、NaClO3等属于弱酸强碱盐,以NaAc为例,在NaAc水溶液中,同时存在以下反应NaAc的水解作用实质是Ac-与H2O作用生成弱酸HAc的反应。
弱酸强碱盐的水解,实质上是酸根离子发生了水解。
水解过程用离子方程式表示为:Ac-+ H2O ⇌HAc + OH-,当水解达到平衡时:Kh为水解反应的平衡常数,即水解常数。
对于一元弱酸强碱盐的水解反应,(Kw是水的离子积常数,Ka是弱酸的解离常数),在常温下水的离子积常数Kw为一常数,故弱酸强碱盐的水解常数值Kh取决于弱酸的电离常数Ka的大小,Ka越小,即酸越弱,则Kh越大,说明该盐的水解程度越大,反之,Ka越大,Kh越小,水解程度越小。
弱酸甲酸Ka=1.8×10^-3;醋酸Ka=1.76×10^-5;Kb=5.68×10^-10碳酸Ka1=4.30×10^-7Ka2=5.61×10^-11磷酸Ka1=7.52×10^-3Ka2=6.23×10^-8Ka3=2.2×10^-13Kb1=1.33×10^-12Kb2=1.6 ×10^-7Kb3=4.54×10^-2草酸Ka1=3.5×10^-2 Ka2=4×10^-6弱碱一水合氨Kb=1.8×10^-5水(水可以认为既是弱酸,又是弱碱)K=1.8*10^-16从本质上来认识弱酸强碱盐的水解常数以CH3COONa为例来说明水解的离子方程式:CH3COO- +H2O =(可逆号)CH3COOH + OH- 水解常数表达式:Kh=C(CH3COOH )*C(OH-)/C(CH3COO-)C(OH-)=Kw/C(H+) 代人上式Kh=C(CH3COOH )*Kw/C(H+)*(CH3COO-)再看CH3COOH的电离常数Ka=C(H+)*(CH3COO-)/C(CH3COOH ) 所以Kh=Kw/KaKw=10的-14次方,Ka=1.76*10的-5次方其它一元弱酸强碱盐的水解常数都可以根据这个公式进行计算。
有机酸无机酸PKa值表

肼(联氨) 羟 氨
8.86 3.96 2.43 1.4 4.75 6.02 14.9 8.04 3.02 7.52 3.02
氢氧化铅 氢氧化锌
4. 有机碱在水溶液中的解离常数(25oC) Dissociation Constants of Organic Bases in Aqueous Solution (25oC)
-3 -8
亚碲酸
2. 有机酸在水溶液中的解离常数(25oC) Dissociation Constants of Organic Acids in Aqueous Solution(25oC)
序号 (No.) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 名称(Name) 甲 酸 乙 酸 乙醇酸 草 酸 化学式 (Chemical formula) HCOOH CH3COOH CH2(OH)COOH (COOH)2 CH2(NH2)COOH CH2ClCOOH CHCl2COOH CCl3COOH CH3CH2COOH CH2═CHCOOH CH3CHOHCOOH HOCOCH2COOH HC≡CCOOH HOCH2CHOHCOOH CH3COCOOH CH3CHNH2COOH CH2NH2CH2COOH CH3(CH2)2COOH (CH3)2CHCOOH CH2═CHCH2COOH CH2═C(CH2)COOH HOCOCH═CHCOOH HOCOCH═CHCOOH HOCOCH(OH)CH(OH)COOH CH3(CH2)3COOH (CH3)2CHCH2COOH CH3CH2CH═CHCOOH CH3CH═CHCH2COOH CH2═CHCH2CH2COOH HOCO(CH2)3COOH
常见酸碱水中的解离常数

常见酸碱水中的解离常数弱酸、弱碱的解离常数Dissociation Constants of Weak Acids and Weak Bases1. 无机酸在水溶液中的解离常数(25o C)Dissociation Constants of Mineral Acids in Aqueous Solution (25o C)序号名称(Name) 化学式(Chemical formula) K a p K a (No.)1 偏铝酸HAlO2 6.3×10-1312.22 亚砷酸H3AsO3 6.0×10-109.223 砷酸H3AsO46.3×10-3 (K1) 2.2 1.05×10-7 (K2) 6.98 3.2×10-12 (K3) 11.54 硼酸H3BO35.8×10-10 (K1) 9.24 1.8×10-13 (K2) 12.74 1.6×10-14 (K3) 13.85 次溴酸HBrO 2.4×10-98.626 氢氰酸H CN 6.2×10-109.217 碳酸H2CO34.2×10-7 (K1) 6.385.6×10-11(K2) 10.258 次氯酸HClO 3.2×10-87.59 氢氟酸HF 6.61×10-4 3.1810 锗酸H2GeO31.7×10-9 (K1) 8.78 1.9×10-13 (K2) 12.7211 高碘酸HIO4 2.8×10-2 1.5612 亚硝酸HNO2 5.1×10-4 3.2913 次磷酸H3PO2 5.9×10-2 1.2314 亚磷酸H3PO35.0×10-2 (K1) 1.3 2.5×10-7 (K2) 6.615 磷酸H3PO47.52×10-3 (K1) 2.12 6.31×10-8 (K2) 7.2 4.4×10-13 (K3) 12.3616 焦磷酸H4P2O73.0×10-2 (K1) 1.524.4×10-3 (K2) 2.36 2.5×10-7 (K3) 6.65.6×10-10 (K4) 9.2517 氢硫酸H2S 1.3×10-7 (K1) 6.88 7.1×10-15 (K2) 14.1518 亚硫酸H2SO31.23×10-2 (K1) 1.91 6.6×10-8 (K2) 7.1819 硫酸H2SO4 1.0×103 (K1) -31.02×10-2 (K2) 1.9920 硫代硫酸H2S2O32.52×10-1 (K1) 0.6 1.9×10-2 (K2) 1.7221 氢硒酸H2Se 1.3×10-4 (K1) 3.89 1.0×10-11(K2) 1122 亚硒酸H2SeO32.7×10-3 (K1) 2.57 2.5×10-7 (K2) 6.623 硒酸H2SeO41×103 (K1) -3 1.2×10-2 (K2) 1.9224 硅酸H2SiO31.7×10-10 (K1) 9.77 1.6×10-12 (K2) 11.825 亚碲酸H2TeO32.7×10-3 (K1) 2.57 1.8×10-8 (K2) 7.742. 有机酸在水溶液中的解离常数(25o C)Dissociation Constants of Organic Acids in Aqueous Solution (25o C)序号(No .) 名称(Name)化学式K a p K a(Chemical formula)1 甲酸HCOOH 1.8×10-4 3.752 乙酸CH3COOH 1.74×10-5 4.763 乙醇酸CH2(OH)COOH 1.48×10-4 3.834 草酸(COOH)25.4×10-2(K1) 1.27 5.4×10-5(K2) 4.275 甘氨酸CH2(NH2)COOH 1.7×10-109.786 一氯乙酸CH2ClCOOH 1.4×10-3 2.867 二氯乙酸CHCl2COOH 5.0×10-2 1.38 三氯乙酸CCl3COOH 2.0×10-10.79 丙酸CH3CH2COOH 1.35×10-5 4.8710 丙烯酸CH2═CHCOOH 5.5×10-5 4.2611 乳酸(丙醇酸) CH3CHOHCOOH 1.4×10-4 3.8612 丙二酸HOCOCH2COOH 1.4×10-3(K1) 2.852.2×10-6(K2) 5.6613 2-丙炔酸HC≡CCOOH 1.29×10-2 1.8914 甘油酸HOCH2CHOHCOOH 2.29×10-4 3.6415 丙酮酸CH3COCOOH 3.2×10-3 2.4916 α-丙胺酸 CH3CH NH2COOH 1.35×10-109.8717 β-丙胺酸CH2NH2CH2COOH 4.4×10-1110.3618 正丁酸CH3(CH2)2COOH 1.52×10-5 4.8219 异丁酸(CH3)2CHCOOH 1.41×10-5 4.8520 3-丁烯酸CH2═CHCH2COOH 2.1×10-5 4.6821 异丁烯酸CH2═C(CH2)COOH 2.2×10-5 4.6622 反丁烯二酸(富马酸)HOCOCH═CHCOOH9.3×10-4(K1) 3.033.6×10-5(K2)4.4423 顺丁烯二酸(马来酸)HOCOCH═CHCOOH1.2×10-2(K1) 1.925.9×10-7(K2)6.2324 酒石酸HOCOCH(OH)CH(OH)COOH 1.04×10-3(K1) 2.98 4.55×10-5(K2) 4.3425 正戊酸CH3(CH2)3COOH 1.4×10-5 4.8626 异戊酸(CH3)2CHCH2COOH 1.67×10-5 4.7827 2-戊烯酸CH3CH2CH═CHCOOH 2.0×10-5 4.728 3-戊烯酸CH3CH═CHCH2COOH 3.0×10-5 4.5229 4-戊烯酸CH2═CHCH2CH2COOH 2.10×10-5 4.67730 戊二酸HOCO(CH2)3COOH 1.7×10-4(K1) 3.77 8.3×10-7(K2) 6.0831 谷氨酸HOCOCH2CH2CH(NH2)COOH7.4×10-3(K1) 2.13 4.9×10-5(K2) 4.31 4.4×10-10 (K3) 9.35832 正己酸CH3(CH2)4COOH 1.39×10-5 4.8633 异己酸(CH3)2CH(CH2)3—COOH 1.43×10-5 4.8534 (E)-2-己烯酸H(CH2)3CH═CHCOOH 1.8×10-5 4.7435 (E)-3-己烯酸CH3CH2CH═CHCH2COOH 1.9×10-5 4.7236 己二酸HOCOCH2CH2CH2CH2COOH 3.8×10-5(K1) 4.42 3.9×10-6(K2) 5.4137 柠檬酸HOCOCH2C(OH)(COOH)CH2COOH 7.4×10-4(K1) 3.13 1.7×10-5(K2) 4.76 4.0×10-7(K3) 6.438 苯酚C6H5OH 1.1×10-109.9639 邻苯二酚(o)C6H4(OH)23.6×10-109.45 1.6×10-1312.840 间苯二酚(m)C6H4(OH)23.6×10-10(K1) 9.3 8.71×10-12(K2) 11.0641 对苯二酚(p)C6H4(OH)2 1.1×10-109.9642 2,4,6-三硝基苯酚2,4,6-(NO2)3C6H2OH 5.1×10-10.2943 葡萄糖酸CH2OH(CHOH)4COOH 1.4×10-4 3.8644 苯甲酸C6H5COOH 6.3×10-5 4.245 水杨酸C6H4(OH)COOH 1.05×10-3(K1) 2.98 4.17×10-13(K2) 12.3846 邻硝基苯甲酸(o)NO2C6H4COOH 6.6×10-3 2.1847 间硝基苯甲酸(m)NO2C6H4COOH 3.5×10-4 3.4648 对硝基苯甲酸(p)NO2C6H4COOH 3.6×10-4 3.4449 邻苯二甲酸(o)C6H4(COOH)21.1×10-3(K1) 2.96 4.0×10-6(K2) 5.450 间苯二甲酸(m)C6H4(COOH)22.4×10-4(K1) 3.62 2.5×10-5(K2) 4.651 对苯二甲酸(p)C6H4(COOH)22.9×10-4(K1) 3.543.5×10-5(K2)4.4652 1,3,5-苯三甲酸C6H3(COOH)37.6×10-3(K1) 2.12 7.9×10-5(K2) 4.1 6.6×10-6(K3) 5.1853 苯基六羧酸C6(COOH)62.1×10-1(K1) 0.68 6.2×10-3(K2)2.213.0×10-4(K3) 3.52 8.1×10-6(K4) 5.094.8×10-7(K5) 6.323.2×10-8(K6) 7.4954 癸二酸HOOC(CH2)8COOH 2.6×10-5(K1) 4.59 2.6×10-6(K2) 5.5955乙二胺四乙酸(EDTA)CH2—N(CH2COOH)2 1.0×10-2(K1) 2∣ 2.14×10-3(K2) 2.67CH2—N(CH2COOH)2 6.92×10-7(K3) 6.165.5×10-11(K4) 10.263. 无机碱在水溶液中的解离常数(25o C)Dissociation Constants of Mineral Bases in Aqueous Solution (25o C)序号(No .) 名称(Name)化学式K b p K b(Chemical formula)1 氢氧化铝Al(OH)3 1.38×10-9(K3) 8.862 氢氧化银AgOH 1.10×10-4 3.963 氢氧化钙Ca(OH)23.72×10-3 2.43 3.98×10-2 1.44 氨水NH3+H2O 1.78×10-5 4.755 肼(联氨)N2H4+H2O 9.55×10-7(K1) 6.02 1.26×10-15(K2) 14.96 羟氨NH2OH+H2O 9.12×10-98.047 氢氧化铅Pb(OH)29.55×10-4(K1) 3.02 3.0×10-8(K2) 7.528 氢氧化锌Zn(OH)29.55×10-4 3.024. 有机碱在水溶液中的解离常数(25o C)Dissociation Constants of Organic Bases in Aqueous Solution (25o C)序号(No.)名称(Name) 化学式(Chemical formula) K b p K b 1 甲胺CH3NH2 4.17×10-4 3.382 尿素(脲)CO(NH2)2 1.5×10-1413.823 乙胺CH3CH2NH2 4.27×10-4 3.374 乙醇胺H2N(CH2)2OH 3.16×10-5 4.55 乙二胺H2N(CH2)2NH28.51×10-5(K1) 4.07 7.08×10-8(K2) 7.156 二甲胺(CH3)2NH 5.89×10-4 3.237 三甲胺(CH3)3N 6.31×10-5 4.28 三乙胺(C2H5)3N 5.25×10-4 3.289 丙胺C3H7NH2 3.70×10-4 3.43210 异丙胺i-C3H7NH2 4.37×10-4 3.361,3-丙二胺NH2(CH2)3NH22.95×10-4(K1) 3.5311 3.09×10-6(K2) 5.511,2-丙二胺CH3CH(NH2)CH2NH25.25×10-5(K1) 4.2812 4.05×10-8(K2) 7.39313 三丙胺(CH3CH2CH2)3N 4.57×10-4 3.3414 三乙醇胺(HOCH2CH2)3N 5.75×10-7 6.2415 丁胺C4H9NH2 4.37×10-4 3.3616 异丁胺C4H9NH2 2.57×10-4 3.5917 叔丁胺C4H9NH2 4.84×10-4 3.31518 己胺H(CH2)6NH2 4.37×10-4 3.3619 辛胺H(CH2)8NH2 4.47×10-4 3.3520 苯胺C6H5NH2 3.98×10-109.421 苄胺C7H9N 2.24×10-5 4.6522 环己胺C6H11NH2 4.37×10-4 3.3623 吡啶C5H5N 1.48×10-98.8324 六亚甲基四胺(CH2)6N4 1.35×10-98.8725 2-氯酚C6H5ClO 3.55×10-6 5.4526 3-氯酚C6H5ClO 1.26×10-5 4.927 4-氯酚C6H5ClO 2.69×10-5 4.5728 邻氨基苯酚(o)H2NC6H4OH 5.2×10-5 4.28 1.9×10-5 4.7229 间氨基苯酚(m)H2NC6H4OH 7.4×10-5 4.13 6.8×10-5 4.1730 对氨基苯酚(p)H2NC6H4OH 2.0×10-4 3.73.2×10-6 5.531 邻甲苯胺(o)CH3C6H4NH2 2.82×10-109.5532 间甲苯胺(m)CH3C6H4NH2 5.13×10-109.2933 对甲苯胺(p)CH3C6H4NH2 1.20×10-98.9234 8-羟基喹啉(20℃) 8-HO—C9H6N 6.5×10-5 4.1935 二苯胺(C6H5)2NH 7.94×10-1413.136 联苯胺H2NC6H4C6H4NH25.01×10-10(K1) 9.3 4.27×10-11(K2) 10.37。
酸碱解离平衡

多元酸在水中是分步电离的,以氢硫酸的解离为例:
H2S H+ + HS-
[H ][HS ] Ө K1 1.1 107 [H 2S]
HS-
H+ + S2-
2 [H ][S ] 13 Ө K2 1.3 10 [HS ]
在常温常压下,H2S 气体在水中的饱和浓度约为 0.10
平衡常数表达式 KӨ =[H+][OH-],称其为水的离子
积常数,经常用 KwӨ 表示。常温下 KwӨ =1.0×10–14。
KwӨ 与反应的 ΔrGmӨ 有关系,由 KwӨ 可求得上述反应
的ΔrGmӨ值。
2
溶液的 pH
pH=-lg[H+] pOH=-lg[OH-]
因为常温下: KwӨ =[H+][OH-] =1.0×10–14 故常温下有 : pH+pOH=14
但当某温度下,水的离子积常数 KwӨ不等于 1.0×10–
14,p
KwӨ 不等于14时,中性溶液中 pH = pOH ,但都不 pH = pOH 是中性溶液的根本标志。
等于 7。
3
酸碱指示剂 借助于颜色的改变来指示溶液pH的物质叫做酸碱指
示剂。酸碱指示剂通常是一种复杂的有机物,并且都是弱
酸或弱碱。 例如甲基橙指示剂就是一种有机弱酸:
[H+] = [HS-] = 3.32×10–5 mol· dm–3
第二步电离平衡
2
Ө
HS-
5
H+ + S2-
2
[H ][S ] 3.32 10 [S ] 2 K2 [S ] 5 [HS ] 3.32 10
故 [S2–]= 1.3×10–13 mol· dm–3
弱酸和弱碱的解离平衡

(
NH
+ 4
)
=x {c}
=
7.510 -6 0.10
=
0.0075
%
影响盐类水解的因素
①盐的浓度: c盐↓ , 水解度增大。h =
Kh c(盐)
② 温度:水解反应为吸热反应,△rHm >0 ,
T↑, Kh ↑,水解度增大。 总之,加热和稀释都有利于盐类的水解。
③溶液的酸碱度:加酸可以引起盐类水解平衡
思考:其相关常数等于多少?
25 0 C , pKa + pK b = 14
NH
+的解离度就是所谓的盐
4
类的水解度。
水解平衡时盐水解部分 的浓度
水解度 =
100%
盐的初始浓度
c 0 - c eq
=
100%
c0
例4-4:计算 0.10mol·L-1 NH4Cl溶液的pH和
NH
+ 4
的解离度。
解: Ka (NH4+ )
=
Kw Kb (NH3 )
的移动,例如加酸能抑制下述水解产物的生成。
SnCl2 + H2O Sn(OH)Cl(s) + HCl Bi(NO 3 )3 + H2O BiONO 3 (s) + 2HNO3 SbCl3 + H2O SbOCl(s)+ 2HCl
2 强碱弱酸盐(离子碱)的水解
NaAc , NaCN……一元弱酸强碱盐的水 溶液呈碱性,因为弱酸阴离子在水中发生水 解反应。如在NaAc水溶液中:
无关。
③ 对于二元弱酸,若 c(弱酸)一定时,
c(酸根离子)与 {c (H3O+)}2 成反比。
PH和磷酸电离产物及一些弱酸,弱碱的电离常数(室温)

分析化学中三元弱酸的分布公式为
M = [H+]^3+[H+]^2Ka1+[H+]Ka1Ka2+Ka1Ka2Ka3
x3 = [H3A]/c= [H+]^3/M
x2 = [H2A-]/c= [H+]^2Ka1/M
x1 = [HA2-]/c= [H+]Ka1Ka2/M
x0 = [A3-]/c=Ka1Ka2Ka3/M
其中x2表示磷酸二氢根,x1表示磷酸一氢根,x0表示磷酸根。
[H+]表示氢离子浓度,也就是10^(-pH)
Ka1=10^(-pKa1),Ka2=10^(-pKa2),Ka3=10^(-pKa3)
通过计算,可以得到
当pH=4时,阴离子的种类主要是磷酸二氢根(占总含磷微粒的98.6%)
当pH=10时,阴离子主要是磷酸一氢根(占总含磷微粒的99.4%)
当pH=13时,阴离子主要是磷酸根(占总含磷微粒的83.1%)
一些弱酸,弱碱的电离常数
弱酸
名称
化学式
Ka﹙b﹚
pKa(b)
硼酸
H₃BO₃
5.8×10ˆ-10(Ka1)
9.24
碳酸
H₂CO₃
4.5X10ˆ﹣7(Ka1)
4.7X10ˆ-11(Ka2)
6.35
10.33
氢氟酸
HF
7.2X10^-4
3.14
亚硝酸
HNO₂
5.1X10^-4
3.29
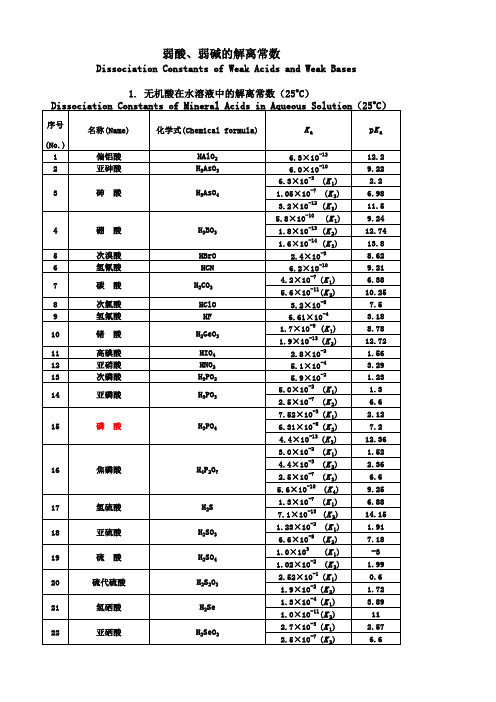
有机酸无机酸PKa值表
38
苯酚
39
邻苯二酚
C6H5OH (o )C6H4(OH)2
40
间苯二酚
41
对苯二酚
42 2,4,6-三硝基苯酚
43
葡萄糖酸
44
苯甲酸
45
水杨酸
46
邻硝基苯甲酸
47
间硝基苯甲酸
48
对硝基苯甲酸
49
邻苯二甲酸
(m )C6H4(OH)2
(p )C6H4(OH)2 2,4,6-(NO2)3C6H2OH CH2OH(CHOH)4COOH
2 2.67 6.16 10.26
3. 无机碱在水溶液中的解离常数(25oC) Dissociation Constants of Mineral Bases in Aqueous Solution (25oC)
序号 (No.)
名称(Name)
化学式 (Chemical formula)
Kb
pK b
14
三乙醇胺
(HOCH2CH2)3N
5.75×10-7
6.24
15
丁胺
C4H9NH2
4.37×10-4
3.36
16
异丁胺
C4H9NH2
2.57×10-4
3.59
17
叔丁胺
C4H9NH2
4.84×10-4
3.315
18
己胺
H(CH2)6NH2
序号 (No.)
名称(Name)
化学式(Chemical formula)
Kb
pK b
1
甲胺
CH3NH2
4.17×10-4
3.38
2
尿素(脲)
CO(NH2)2
弱电解质的电离平衡常数

弱电解质的电离平衡常数电离平衡常数是描述溶液中弱电解质电离程度的重要物理量。
对于弱电解质来说,其电离平衡常数通常用酸解离常数(Ka)或碱离解常数(Kb)来表示。
本文将分别从酸解离常数和碱离解常数两个方面来探讨弱电解质的电离平衡常数。
一、酸解离常数(Ka)酸解离常数(Ka)是描述酸在溶液中电离程度的指标。
对于弱酸HA,其在水溶液中可以发生如下电离反应:HA ⇌ H+ + A-其中HA为未电离的弱酸,H+为产生的氢离子,A-为产生的酸根离子。
酸解离常数(Ka)的定义为:Ka = [H+][A-]/[HA]其中[H+]表示溶液中的氢离子浓度,[A-]表示溶液中的酸根离子浓度,[HA]表示溶液中的弱酸浓度。
酸解离常数越大,说明弱酸的电离程度越高,反之,酸解离常数越小,说明弱酸的电离程度越低。
弱酸的电离程度主要受到以下因素的影响:1. 分子内的键能:键能越强,电离程度越低;2. 分子结构:分子结构中含有共轭体系或芳香环的弱酸,电离程度较高;3. 溶剂的性质:溶剂中的极性越大,电离程度越高;4. 温度:温度升高会增加电离程度。
二、碱离解常数(Kb)碱离解常数(Kb)是描述碱在溶液中电离程度的指标。
对于弱碱B,其在水溶液中可以发生如下电离反应:B + H2O ⇌ BH+ + OH-其中B为未电离的弱碱,BH+为产生的碱根离子,OH-为产生的氢氧根离子。
碱离解常数(Kb)的定义为:Kb = [BH+][OH-]/[B]其中[BH+]表示溶液中的碱根离子浓度,[OH-]表示溶液中的氢氧根离子浓度,[B]表示溶液中的弱碱浓度。
碱离解常数越大,说明弱碱的电离程度越高,反之,碱离解常数越小,说明弱碱的电离程度越低。
弱碱的电离程度主要受到以下因素的影响:1. 分子内的键能:键能越强,电离程度越低;2. 分子结构:分子结构中含有孤对电子或共轭体系的弱碱,电离程度较高;3. 溶剂的性质:溶剂中的极性越大,电离程度越高;4. 温度:温度升高会增加电离程度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.21 3.52 5.09 6.32 7.49 4.59 5.59 2 2.67 6.16 10.26
(K 4)
3. 无机碱在水溶液中的解离常数(25oC) Dissociation Constants of Mineral Bases in Aqueous Solution (25oC) 序号 化学式 Kb pK b 名称(Name) (No. (Chemical formula) -9 Al(OH)3 1 氢氧化铝 8.86 1.38×10 (K 3) -4 2 氢氧化银 AgOH 3.96 1.10×10 -3 2.43 3.72×10 Ca(OH)2 3 氢氧化钙 -2 1.4 3.98×10 -5 NH3+H2O 4 氨 水 4.75 1.78×10 5 6 7 8 肼(联氨) 羟 氨 N2H4+H2O NH2OH+H2O Pb(OH)2 Zn(OH)2 9.55×10 (K 1) 1.26×10
-15 -7
6.02 14.9 8.04 3.02 7.52 3.02
(K 2 )
氢氧化铅 氢氧化锌
9.12×10-9 9.55×10-4(K 1) 3.0×10-8(K 2) 9.55×10
o -4
4. 有机碱在水溶液中的解离常数(25 C) Dissociation Constants of Organic Bases in Aqueous Solution (25oC) 序号 (No. 1 2 3 4 5 6 7 8 9 10 11 名称(Name) 甲胺 尿素(脲) 乙胺 乙醇胺 乙二胺 二甲胺 三甲胺 三乙胺 丙胺 异丙胺 1,3-丙二胺 化学式(Chemical formula) CH3NH2 CO(NH2)2 CH3CH2NH2 H2N(CH2)2OH H2N(CH2)2NH2 (CH3)2NH (CH3)3N (C2H5)3N C3H7NH2 i -C3H7NH2 NH2(CH2)3NH2
-7 -3 -8 -2 -8
次氯酸 氢氟酸 锗 酸
高碘酸 亚硝酸 次磷酸 亚磷酸
(K 2 ) (K 1 ) (K 2 ) (K 3 ) (K 1 ) (K 2 ) (K 3 ) (K 4) (K 1 ) (K 2) (K 1 ) (K 2 ) (K 1 ) (K 2 ) (K 1 ) (K 2)
7.52×10 15 磷 酸 H3PO4 6.31×10 4.4×10 3.0×10 16 焦磷酸 H4P2O7 4.4×10 2.5×10 5.6×10 17 18 19 20 氢硫酸 亚硫酸 硫 酸 H2S H2SO3 H2SO4 H2S2O3 1.3×10 7.1×10
1.7×10 (K 2) 4.0×10 (K 3) 1.1×10-10 -10 3.6×10 1.6×10-13 3.6×10-10(K 1) 8.71×10-12(K 2) 1.1×10 5.1×10-1 -4 1.4×10 6.3×10-5 -3 1.05×10 (K 1) 4.17×10-13(K 2) 6.6×10 -4 3.5×10 3.6×10-4 1.1×10-3(K 1) 4.0×10-6(K 2) 2.4×10 (K 1) 2.5×10 (K 2) 2.9×10 (K 1) 3.5×10 (K 2) 7.6×10 (K 1)
Ka
6.3×10-13 -10 6.0×10 -3 6.3×10 (K 1 ) 1.05×10-7 (K 2) 3.2×10 5.8×10
-12
pK a 12.2 9.22 2.2 6.98 11.5 9.24 12.74 13.8 8.62 9.21 6.38 10.25 7.5 3.18 8.78 12.72 1.56 3.29 1.23 1.3 6.6 2.12 7.2 12.36 1.52 2.36 6.6 9.25 6.88 14.15 1.91 7.18 -3 1.99 0.6 1.72
-1 -6
53
苯基六羧酸
C6(COOH)6
6.2×10-3(K 2) 53 苯基六羧酸 C6(COOH)6 3.0×10 (K 3) 8.1×10-6(K 4) 4.8×10 (K 5) 3.2×10 (K 6) 54 癸二酸 HOOC(CH2)8COOH CH2—N(CH2COOH)2 55 乙二胺四乙酸 (EDTA) ∣ CH2—N(CH2COOH)2 2.6×10-5(K 1) 2.6×10-6(K 2) 1.0×10 (K 1) 2.14×10 (K 2) 6.92×10-7(K 3) 5.5×10
2. 有机酸在水溶液中的解离常数(25oC) Dissociation Constants of Organic Acids in Aqueous Solution(25oC) 序号 化学式 Ka pK a 名称(Name) (No. (Chemical formula) 1 甲 酸 HCOOH 3.75 1.8×10-4 -5 CH3COOH 2 乙 酸 4.76 1.74×10 -4 CH2(OH)COOH 3 乙醇酸 3.83 1.48×10 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 草 酸 (COOH)2 CH2(NH2)COOH CH2ClCOOH CHCl2COOH CCl3COOH CH3CH2COOH CH2═CHCOOH CH3CHOHCOOH HOCOCH2COOH HC≡CCOOH HOCH2CHOHCOOH CH3COCOOH CH3CHNH2COOH CH2NH2CH2COOH CH3(CH2)2COOH (CH3)2CHCOOH CH2═CHCH2COOH CH2═C(CH2)COOH HOCOCH═CHCOOH HOCOCH═CHCOOH HOCOCH(OH)CH(OH)COOH 5.4×10-2(K 1) 5.4×10 (K 2) 1.7×10 1.4×10-3 -2 5.0×10 2.0×10-1 1.35×10-5 -5 5.5×10 -4 1.4×10 1.4×10-3(K 1) 2.2×10 (K 2) 1.29×10 -4 2.29×10 3.2×10-3 1.35×10-10 4.4×10-11 1.52×10-5 1.41×10-5 2.1×10-5 2.2×10 9.3×10-4(K 1) 3.6×10-5(K 2) 1.2×10 (K 1) 5.9×10 (K 2) 1.04×10 (K 1) 4.55×10 (K 2)
甘氨酸 一氯乙酸 二氯乙酸 三氯乙酸 丙 酸 丙烯酸 乳酸(丙醇酸) 丙二酸 2-丙炔酸 甘油酸 丙酮酸 a -丙胺酸 b -丙胺酸 正丁酸 异丁酸 3-丁烯酸 异丁烯酸 反丁烯二酸(富马 酸) 顺丁烯二酸(马来 酸) 酒石酸
25 26 27 28 29 30
正戊酸 异戊酸 2-戊烯酸 3-戊烯酸 4-戊烯酸 戊二酸
弱酸、弱碱的解离常数 Dissociation Constants of Weak Acids and Weak Bases 1. 无机酸在水溶液中的解离常数(25oC) Dissociation Constants of Mineral Acids in Aqueous Solution(25oC) 序号 (No. 1 2 3 名称(Name) 偏铝酸 亚砷酸 砷 酸 化学式(Chemical formula) HAlO2 H3AsO3 H3AsO4
-3 -5 -4 -5 -4 -3 -10
邻苯二酚 间苯二酚 对苯二酚 2,4,6-三硝基苯酚 葡萄糖酸 苯甲酸 水杨酸 邻硝基苯甲酸 间硝基苯甲酸 对硝基苯甲酸 邻苯二甲酸 间苯二甲酸 对苯二H3(COOH)3
7.9×10-5(K 2) 6.6×10 (K 3) 2.1×10 (K 1)
柠檬酸 苯 酚
HOCOCH2C(OH)(COOH)CH2COOH C6H5OH (o )C6H4(OH)2 (m )C6H4(OH)2 (p )C6H4(OH)2 2,4,6-(NO2)3C6H2OH CH2OH(CHOH)4COOH C6H5COOH C6H4(OH)COOH (o )NO2C6H4COOH (m )NO2C6H4COOH (p )NO2C6H4COOH (o )C6H4(COOH)2 (m )C6H4(COOH)2 (p )C6H4(COOH)2
CH3(CH2)3COOH (CH3)2CHCH2COOH CH3CH2CH═CHCOOH CH3CH═CHCH2COOH CH2═CHCH2CH2COOH HOCO(CH2)3COOH
1.4×10 1.67×10-5 -5 2.0×10 3.0×10-5 -5 2.10×10 1.7×10-4(K 1) 8.3×10 (K 2) 7.4×10 (K 1)
(K 3 ) (K 1 ) (K 2 ) (K 3 )
-10 -13 -14
4 5 6 7 8 9 10 11 12 13 14
硼
酸
H3BO3 HBrO HCN H2CO3 HClO HF H2GeO3 HIO4 HNO2 H3PO2 H3PO3
1.8×10 1.6×10
次溴酸 氢氰酸 碳 酸
2.4×10-9 -10 6.2×10 4.2×10-7 (K 1) 5.6×10-11(K 2) 3.2×10 -4 6.61×10 1.7×10-9 (K 1) 1.9×10-13 (K 2) 2.8×10 5.1×10-4 -2 5.9×10 -2 5.0×10 (K 1 ) 2.5×10
3 -11 -3 -7
3.89 11 2.57 6.6 -3 1.92 9.77 11.8 2.57 7.74
(K 2) (K 1) (K 2) (K 1)
1.2×10-2 (K 2) 1.7×10 1.6×10
-10 -12 -3 -8
(K 1) (K 2) (K 1 ) (K 2 )
亚碲酸
2.7×10 1.8×10
31 32 33 34 35 36
