人教版九年级化学常见化学式总结
人教版九年级化学化学式汇总.doc
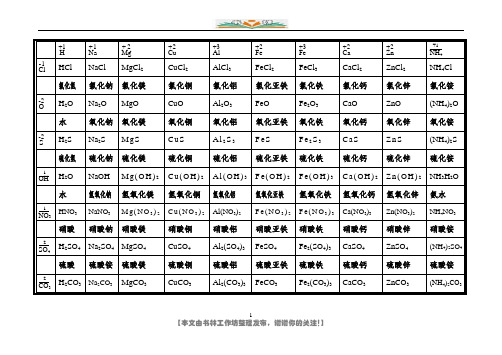
1H +1Na +1Mg +2Cu +2Al +3Fe +2Fe +3Ca +2Zn +2+1NH 4Cl -1HCl NaCl MgCl 2 CuCl 2 AlCl 3 FeCl 2 FeCl 3 CaCl 2 ZnCl 2 NH 4Cl氯化氢 氯化钠 氯化镁 氯化铜 氯化铝 氯化亚铁 氯化铁 氯化钙 氯化锌 氯化铵 O -2H 2O Na 2OMgOCuO Al 2O 3 FeO Fe 2O 3 CaO ZnO (NH 4)2O水 氧化钠 氧化镁 氧化铜 氧化铝 氧化亚铁 氧化铁 氧化钙 氧化锌 氧化铵 S -2H 2S Na 2SM gSC uS A l 2S 3 F e S F e 2S 3 C aS Zn S (NH 4)2S硫化氢 硫化钠 硫化镁 硫化铜硫化铝硫化亚铁硫化铁硫化钙硫化锌硫化铵-1OHH 2O NaOH M g(O H )2 C u (O H )2 A l (OH )3 F e (O H )2 F e (O H )3 C a (OH )2 Zn (O H )2 NH 3H 2O水氢氧化钠氢氧化镁氢氧化铜氢氧化铝氢氧化亚铁氢氧化铁氢氧化钙氢氧化锌氨水-1NO 3 HNO 3NaNO 3M g(N O 3)2 C u (N O 3)2 Al(NO 3)2 F e (N O 3)2 F e (N O 3)3 Ca(NO 3)3Zn(NO 3)2NH 4NO 3硝酸 硝酸钠 硝酸镁 硝酸铜 硝酸铝 硝酸亚铁 硝酸铁 硝酸钙 硝酸锌 硝酸铵-2SO 4 H 2SO 4 Na 2SO 4 MgSO 4CuSO 4 Al 2(SO 4)3 FeSO 4 Fe 2(SO 4)3 CaSO 4 ZnSO 4 (NH 4)2SO 4硫酸 硫酸铵 硫酸镁 硫酸铜 硫酸铝硫酸亚铁硫酸铁 硫酸钙 硫酸锌 硫酸铵-2CO 3 H 2CO 3 Na 2CO 3 MgCO 3CuCO 3Al 2(CO 3)3 FeCO 3Fe 2(CO 3)3CaCO 3ZnCO 3(NH 4)2CO 32碳酸碳酸钠 碳酸镁碳酸铜碳酸铝碳酸亚铁碳酸铁碳酸钙碳酸锌碳酸铵H +1Na +1Mg +2Cu +2Al +3Fe +2Fe +3Ca +2Zn +2+1NH 4Cl -1氯化氢 氯化钠 氯化镁 氯化铜 氯化铝 氯化亚铁 氯化铁 氯化钙 氯化锌 氯化铵 O -2水 氧化钠 氧化镁 氧化铜 氧化铝 氧化亚铁 氧化铁 氧化钙 氧化锌 氧化铵 S -2硫化氢 硫化钠 硫化镁 硫化铜 硫化铝 硫化亚铁 硫化铁 硫化钙 硫化锌 硫化铵 -1OH水氢氧化钠氢氧化镁氢氧化铜氢氧化铝氢氧化亚铁氢氧化铁氢氧化钙氢氧化锌氨水-1NO 3硝酸 硝酸钠 硝酸镁 硝酸铜 硝酸铝 硝酸亚铁 硝酸铁 硝酸钙 硝酸锌 硝酸铵-2SO 4硫酸 硫酸铵 硫酸镁 硫酸铜硫酸铝硫酸亚铁硫酸铁硫酸钙硫酸锌硫酸铵3-2CO 3碳酸碳酸钠 碳酸镁碳酸铜碳酸铝碳酸亚铁碳酸铁碳酸钙碳酸锌碳酸铵H +1Na +1Mg +2Cu +2Al +3Fe +2Fe +3Ca +2Zn +2+1NH 4Cl -1HCl NaCl MgCl 2 CuCl 2 AlCl 3 FeCl 2 FeCl 3 CaCl 2 ZnCl 2 NH 4ClO -2H 2O Na 2O MgO CuO Al 2O 3 FeO Fe 2O 3 CaO ZnO (NH 4)2OS -2H 2S Na 2S M gS C uS A l 2S 3 F e S F e 2S 3 C aS Zn S (NH 4)2S-1OHH 2O NaOH M g(O H )2 C u (O H )2 A l (OH )3 F e (O H )2 F e (O H )3 C a (OH )2 Zn (O H )2 NH 3H 2O-1NO 3 HNO 3NaNO 3M g(N O 3)2 C u (N O 3)2 Al(NO 3)2 F e (N O 3)2 F e (N O 3)3 Ca(NO 3)3Zn(NO 3)2NH 4NO 3-2SO 4 H 2SO 4 Na 2SO 4 MgSO 4CuSO 4Al 2(SO 4)3FeSO 4Fe 2(SO 4)3CaSO 4ZnSO 4(NH 4)2SO 4-2H2CO3Na2CO3MgCO3CuCO3Al2(CO3)3FeCO3Fe2(CO3)3CaCO3ZnCO3(NH4)2CO3 CO34。
人教版九年级上册化学化学方程式汇总+知识点提醒
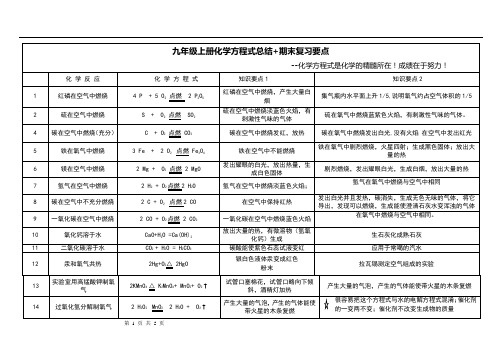
28 甲烷在空气中燃烧CH4 + 2 O2点燃CO2 + 2 H2O发出蓝色火焰(同CO),生成能使澄清石灰水变浑浊的气体在上面加一个干而冷的烧杯,烧杯内壁有水雾29 酒精在空气中燃烧C2H5OH + 3 O2点燃2 CO2 + 3 H2O 产生淡蓝色的火焰集气瓶的内壁有水珠出现,并能使澄清的石灰水变浑浊的气体30 一氧化碳还原三氧化二铁3 CO +Fe2O3 高温 2 Fe + 3 CO2红色的氧化铁粉末逐渐变为黑色,澄清石灰水变浑浊此反应较难配平,可直接记住化学计量数31 碱式碳酸铜的分解Cu2(OH)2CO3△ 2CuO + CO2↑ + H2O 绿色变为黑色,试管内壁有水珠,产生使澄清石灰水变浑浊的气体分解反应,产物有三32 氢气还原氧化铁3H2+Fe2O3高温3H2O+2Fe红棕色粉末变成黑色,有水珠出现氢气验纯试管倾,先通氢气后点灯。
红棕变黑水珠出,熄灯冷却再停氢。
32 碳还原二氧化碳C+CO2高温2CO吸热反应CO2和CO化学性质不同是因为分子构成不同1.化合价及化学式的书写一价氢氯钾钠银二价氧钙钡镁锌三铝四硅五价磷二三铁,二四碳二四六硫都齐全铜汞二价最常见单质为零永不变负一硝酸氢氧根负二硫酸碳酸根负三记住磷酸根正一价的是铵根-3 -4 -3 -3 +5NH3 CH4 NH4+ NH4.NO3 易错:Fe2+:亚铁离子(浅绿色) Fe3+:铁离子(棕黄色)书写化学式步骤:一排序二标价三约简四交叉2.根据化学式计算(1)原子个数比:元素符号右下角数字比(相同的元素的原子个数要合并)例:H2O中氢原子与氧原子个数比为2 ∶ 1(2)计算相对分子质量(Mr)=化学式中各原子的相对原子质量×各原子个数的总和,如Mr(CO2)=12+16×2=44 (注意化学方程式的计算中涉及某物质的相对质量需乘以前面的化学计量数)(3)计算物质组成元素的质量比=各元素的相对原子质量×原子个数之比。
九年级化学常见化学式(人教版)

九年级化学常见化学式(人教版)
氢气 H2 金刚石 C 水 H2O
过氧化氢(双氧 水)H2O2
氧化亚铁 FeO 氧化镁 MgO 氯化铝 AlCl3 氯化钠(食 盐) NaCl 硫酸镁 MgSO4 硫酸钡 BaSO4 碳酸钾 K2CO3 氢氧化亚铁 Fe(OH)2 氢氧化钠 NaOH 硝酸 HNO3 硝酸铝 Al(NO3)3 硝酸铵 NH4NO3 锰酸钾 K2MnO4 尿素 CO(NH2)2
ZnO 氯化银 AgCl 氯化镁 MgCl2 硫酸钠 Na2SO4 硫酸铜 CuSO4 碳酸镁 MgCO3 氢氧化铜 Cu(OH)2 氢氧化锌 Zn(OH)2 硝酸银 AgNO3 硝酸亚铁 Fe(NO3)2 碳酸氢铵 NH4HCO3 甲烷 CH4
HgO 氯化氢 HCl 氯化钙 CaCl2 硫酸铝 Al2(SO4)3 硫酸 H2SO4 碳酸钙 CaCO3 氢氧化钡 Ba(OH)2 氨水 NH3·H2O 硝酸钾 KNO3 硝酸钡 Ba(NO3)2 碳酸氢钠 NaHCO3 乙醇 C2H5OH
氯气 Cl2 铜 Cu 五氧化二 磷 P2O5 三氧化硫 SO3
(三)氧化(二) 铁 Fe2O3氮 NO 二氧化锰 MnO2
(三)氧化(二) 铝 Al2O3 氧化汞
红磷 P 铁 Fe 二氧化氮 NO2 氧化铜 CuO 氧化钡 BaO 氧化钡 BaO 氯化钡 BaCl2 氯化锌 ZnCl2 硫酸锌 ZnSO4 碳酸锌 ZnCO3 碳酸 H2CO3 氢氧化钙 Ca(OH)2 硝酸钙 Ca(NO3)2 硝酸铜 Cu(NO3)2 碳酸铵 (NH4)2CO3 氯酸钾 KClO3 乙酸(醋 酸)CH3COOH
氮气 N2 硫磺 S 一氧化碳 CO 二氧化硅 SiO2 氧化钙 CaO 氧化钠 Na2O 氯化亚铁 FeCl2 氯化钾 KCl 硫酸亚铁 FeSO4 硫酸钙 CaSO4 碳酸钡 BaCO3 氢氧化铝 Al(OH)3 氢氧化钾 KOH 硝酸镁 Mg(NO3)2 硝酸锌 Zn(NO3)2 硫酸铵 (NH4)2SO4 高锰酸钾 KMnO4
九年级上册化学式子总结(精华版全册)

九年级上册化学式子总结(精华版全册)一、化学式的基础知识* 原子:物质最小的单位,由质子、中子和电子组成。
* 元素:由相同类型的原子组成的纯物质。
* 化合物:由两种或多种元素组成的物质。
* 电子结构:描述原子中电子的分布情况,如1s2、2s2、2p6等。
* 原子价:元素在化合物中的正负电荷能力。
* 过渡金属:位于周期表中B族元素,具有多种原子价。
二、化学式的表示方法1. 分子式:用元素符号表示化合物中各元素的种类和原子数。
2. 组成式:在分子式上附加原子价(以圈表示)表示元素的具体原子数。
3. 离子式:用离子符号表示化合物中的离子组成。
4. 平均原子质量:元素在自然界中存在不同同位素的平均质量。
三、离子式与化学方程式1. 离子的符号:正离子写在负离子的前面。
2. 离子反应:正离子与负离子之间发生的反应。
3. 化学方程式:用化学式符号表示化学反应。
四、摩尔与摩尔质量1. 摩尔:物质的量单位,用符号mol表示。
2. 摩尔质量:1摩尔物质的质量,单位为g/mol,可以根据元素的相对原子质量计算。
五、化学式的应用与实践1. 化合物命名:根据化合物成分和原子价决定名称。
2. 配平化学方程式:保持反应前后各种原子的个数相等。
六、化学式在日常生活中的应用1. 化妆品:根据化妆品成分分析化学式,保证使用安全。
2. 医药领域:通过化学方程式研究药物的合成和反应。
3. 食品添加剂:分析化学式,确认添加剂的成分和安全性。
以上是九年级上册化学式子的总结,希望对你有帮助!。
人教版初三化学需要背诵的化学式

人教版初三化学需要背诵的化学式一、介绍化学式是化学元素或化合物的符号表示法,是化学中的基本概念之一。
在初中化学学习中,掌握化学式是非常重要的,不仅是理论学习的基础,也是实验操作的必备知识。
人教版初三化学需要背诵的化学式,涉及到元素的符号、化合物的组成以及化学反应等内容。
二、常见元素的化学式1. 氢:H2. 氦:He3. 铍:Be4. 碳:C5. 氮:N6. 氧:O7. 氟:F8. 钠:Na9. 镁:Mg10. 铝:Al11. 锌:Zn12. 铁:Fe13. 铜:Cu三、常见化合物的化学式1. 氨气:NH32. 氯化钠:NaCl3. 氧化铜:Cu2O4. 二氧化碳:CO25. 一氧化碳:CO6. 亚硝酸盐:NO2-7. 硫酸:H2SO48. 碳酸钠:Na2CO39. 铝矾:Al2(SO4)310. 硫化氢:H2S11. 过氧化氢:H2O212. 白砷:As2O3四、化学反应中的化学式1. 直接组成反应:例如氢气与氧气的反应生成水,化学式为2H2 + O2 → 2H2O2. 分解反应:例如过氧化氢分解成水和氧气,化学式为2H2O2 → 2H2O + O23. 单一置换反应:例如锌与盐酸生成氢气和氯化锌,化学式为Zn + 2HCl → ZnCl2 + H24. 双置换反应:例如氯化钠与硫酸反应生成盐酸和硫酸钠,化学式为NaCl + H2SO4 → HCl + Na2SO45. 酸碱中和反应:例如氢氧化钠与硫酸反应生成水和硫酸钠,化学式为2NaOH + H2SO4 → 2H2O + Na2SO4五、总结人教版初三化学需要背诵的化学式,包括常见元素的化学式、常见化合物的化学式以及化学反应中的化学式。
通过背诵这些化学式,可以帮助学生牢固掌握这些基本的化学知识,为进一步深入学习化学打下坚实的基础。
在日常的学习中,可以通过多种方式来背诵和巩固这些化学式,如制作化学式卡片、做化学式练习题等。
希望学生们能够重视化学式的背诵,从而在化学学习中取得更好的成绩。
初中九年级化学方程式大全总结

初中九年级化学方程式大全总结化学方程式是化学反应的简洁描述,它包括反应物、产物及其化学符号和系数。
在初中九年级化学学习中,化学方程式是一个重要的概念。
本文将总结九年级化学学习中常见的化学方程式,以帮助同学们更好地掌握这一知识点。
一、离子方程式离子方程式是描述溶液中离子反应的化学方程式。
它是由溶液中各种离子的化学符号组成的,反应物和产物之间用箭头隔开。
下面是一些常见的离子方程式:1.酸碱反应方程式酸碱反应方程式酸碱反应方程式在酸碱反应方程式中,酸和碱反应后生成盐和水。
例如:HCl + NaOH → NaCl + H2O2.氧化还原反应方程式氧化还原反应方程式氧化还原反应方程式氧化还原反应方程式描述的是电子的转移过程,反应物中至少有一种物质被氧化,另一种物质被还原。
例如:Zn + HCl → ZnCl2 + H2↑二、分子方程式分子方程式是描述非离子反应的化学方程式,反应物和产物用化学式表示。
分子方程式中不显示溶剂和离子。
下面是一些常见的分子方程式:1.合成反应方程式合成反应方程式合成反应方程式合成反应方程式描述两个或多个物质合成成一个新的化合物的反应。
例如:2H2 + O2 → 2H2O2.分解反应方程式分解反应方程式分解反应方程式分解反应方程式描述一个化合物分解成两个或更多物质的反应。
例如:2KClO3 → 2KCl + 3O2↑三、氧化物方程式氧化物方程式描述氧化物之间或氧化物与其他物质的反应。
下面是一些常见的氧化物方程式:1.酸性氧化物与碱性氧化物反应酸性氧化物与碱性氧化物反应酸性氧化物与碱性氧化物反应酸性氧化物与碱性氧化物反应生成盐和水。
例如:SO2 + 2NaOH → Na2SO3 + H2O2.氧化物与非金属反应氧化物与非金属反应氧化物与非金属反应氧化物与非金属反应生成酸。
例如:CO2 + H2O → H2CO3四、化学反应类型根据反应物和产物的性质变化,化学反应可以分为以下几种类型:合成反应、分解反应、置换反应、氧化反应和还原反应。
九年级常见化学式书写及答案
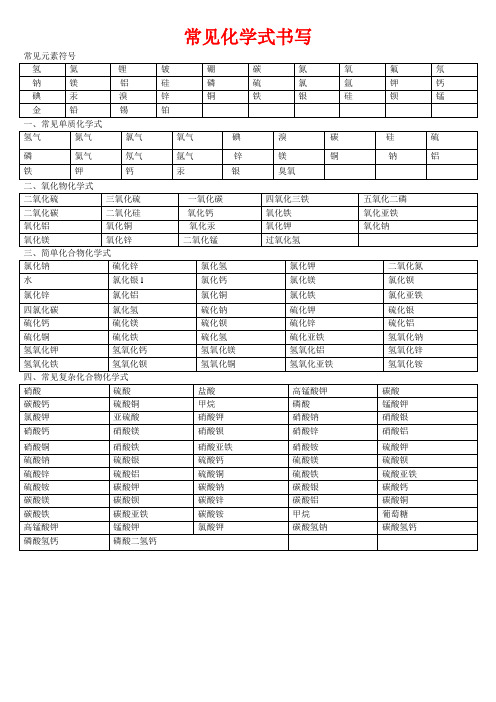
氯化铝AlCl3
氯化铜CuCl2
氯化铁FeCl3
氯化亚铁FeCl2
四氯化碳CCl4
氯化氢HCl
硫化钠Na2S
硫化钾K2S
硫化银Ag2S
硫化钙CaS
硫化镁MgS
硫化钡BaS
硫化锌ZnS
硫化铝Al2S3
硫化铜CuS
硫化铁Fe2S3
硫化氢H2S
硫化亚铁FeS
氢氧化钠NaOH
氢氧化钾KOH
氢氧化钙Ca(OH)2
一、常见单质化学式
氢气H2
氮气N2
氯气Cl2
氧气O2
碘I2
溴Br2
碳C
硅Si
硫S
磷P
氦气He
氖气Ne
氩气Ar
锌Zn
镁Mg
铜Cu
钠Na
铝Al
铁Fe
钾K
钙Ca
汞Hg
银Ag
臭氧O3
二、氧化物化学式
二氧化硫SO2
三氧化硫SO3
一氧化碳CO
四氧化三铁Fe3O4
五氧化二磷P2O5
二氧化碳CO2
二氧化硅SiO2
氧化钙CaO
碳酸钡Ba CO3
碳酸锌Zn CO3
碳酸铝Al2(CO3)3
碳酸铜CuCO3
碳酸铁Fe2(CO3)2
碳酸亚铁FeCO3
碳酸铵(NH4)2CO3
甲烷CH4
葡萄糖C6H12O6
高锰酸钾K2MnO4
锰酸钾K2MnO4
氯酸钾KClO3
碳酸氢钠NaHCO3
碳酸氢钙Ca(HCO3)2
磷酸氢钙CaHPO4
磷酸二氢钙Ca(H2PO4)2
氢氧化亚铁
氢氧化铵
四、常见复杂化合物化学式
常见物质的化学式总结

常见物质的化学式总结
一、单质:
氢气氧气氮气氯气碘碳硅磷硫钠镁铝钾钙锰铁铜锌银汞氦气氖气氩气
二、氧化物
水过氧化氢二氧化碳一氧化碳二氧化氮二氧化硅五氧化二磷氧化钙氧化镁氧化铝二氧化锰氧化亚铁氧化铁四氧化三铁
氧化铜氧化汞
三、氯化物
氯化氢氯化钠氯化镁氯化铝氯化钾氯化钙氯化亚铁氯化铁氯化铜氯化锌氯化银氯化钡氯化铵
四、硝酸及硝酸盐
硝酸硝酸钠硝酸镁硝酸铝硝酸钾硝酸钙硝酸亚铁硝酸铁硝酸铜硝酸锌硝酸银硝酸钡
硝酸铵
五、硫酸及硫酸盐
硫酸硫酸钠硫酸镁硫酸铝硫酸钾硫酸钙硫酸亚铁硫酸铁硫酸铜硫酸锌硫酸银硫酸钡硫酸铵
七、碳酸及碳酸盐
碳酸碳酸钠碳酸钾碳酸钙碳酸钡碳酸氢钠碳酸氢钾碳酸氢钙碳酸氢铵
八、氢氧化物(碱)
氢氧化钠氢氧化钾氢氧化钙氢氧化钡氢氧化铝氢氧化亚铁氢氧化铁氢氧化铜
氨水
九、其他
高锰酸钾锰酸钾氯酸钾甲烷乙醇。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(3)钾、钙、钠三种金属比较活泼,它们直接跟溶液中的水发生反应置换出氢气
初中常见化学式
一、常见单质
氢气
H2
氮气
N2
氯气
Cl2
氧气
O2
臭氧
O3
氦气
He
氖气
Ne
氩气
Ar
碳
C
硅
Si
硫
S
磷
P
碘
I2
溴
Br2
钾
K
钙
Ca
钠
Na
镁
Mg
铝
Al
锌
Zn
铁
Fe
铜
Cu
汞
Hg
银
Ag
二、化合物
1.氧化物
水
H2O
三氧化硫
SO3
一氧化碳
CO
二氧化碳
CO2
五氧化二磷
P2O5
过氧化氢
H2O2
二氧化氮
NO2
二氧化硫
Fe2(SO4)3
硫酸亚铁
FeSO4
硝酸银
AgNO3
硝酸钡
Ba(NO3)2
硝酸铵
NH4NO3
硫酸钡
BaSO4
硫酸铜
CuSO4
硫酸镁
MgSO4
3.常见根(原子团)的化合价
根的名称
铵根
氢氧根
硝酸根
硫酸根
碳酸根
磷酸根
离子符号
NH4+
OH-
NO3-
SO42-
CO32-
PO43-
化合价
+1
-1
-1
-2
-2
-3
SO2
氧化钙
CaO
氧化亚铁
FeO
氧化铁
Fe2O3
四氧化三铁
Fe3O4
氧化镁
MgO
氧化锌
ZnO
二氧化锰
MnO2
氧化汞
HgO
氧化铝
Al2O3
氧化铜
CuO
2.其他化合物
硝酸
HNO3
硫酸
H2SO4
盐酸
HCl
碳酸
H2CO3
硫化氢
H2S
氯化氢
HCl
氢氧化钠
NaOH
氢氧化钾
KOH
氢氧化钙
Ca(OH)2
氢氧化镁
Mg(OH)2
Ag+
氢氧根离子
OH-
碳酸根离子
C032-
镁离子
Mg2+
锌离子
Zn2+
硝酸根离子
N03-
碳酸氢根离子
HCO3-
铝离子
Al3+
铵根离子
NH4+
磷酸根离子
PO43-
四、金属活动性顺序表:
(钾钙钠镁铝锌铁锡铅氢铜汞银铂金)
说明:(1)越左金属活动性就越强,左边的金属可以从右边金属的盐溶液中置换出该金属出来
氢氧化铝
Al(OH)3
氢氧化锌
Zn(OH)2
氢氧化铁
Fe(OH)3
氢氧化亚铁
Fe(OH)2
氢氧化铜
Cu(OH)2
氢氧化钡
Ba(OH)2
氨水
NH3·H2O
氨气
NH3
氯化钠
NaCl
氯化铜
CuCl2
氯化铝
AlCl3
氯化钾
KCl
氯化亚铁
FeCl2
氯化铁
FeCl3
氯化银
AgCl
氯化钙
CaCl2
氯化镁
MgCl2
氯化钡
BaCl2
氯化锌
ZnCl2
碳酸氢铵
NH4HCO3
高锰酸钾
KMnO4
锰酸钾
K2MnO4
氯酸钾
KClO3
硝酸铝
Al(NO3)3硝酸钾KNO3硝酸钠NaNO3
硝酸铁
Fe(NO3)3
硝酸亚铁
Fe(NO3)2
硝酸银
AgNO3
碳酸钠
Na2CO3
碳酸钙
CaCO3
碳酸铵
(NH4)2CO3
碳酸氢钠
NaHCO3
硫酸铁
4常见有机化合物
甲烷
CH4
乙醇
C2H5OH
醋酸
CH3COOH
三、离子符号
名称
符号
名称
符号
名称
符号
名称
符号
钠离子
Na+
钾离子
K+
氯离子
Cl-
高锰酸根离子
Mn04-
钙离子
Ca2+
亚铁离子
Fe2+
氧离子
02-
锰酸根离子
Mn042-
氢离子
H+
铁离子
Fe3+
硫离子
S2-
硫酸根离子
SO42-
铜离子
Cu2+
银离子
