钨的物理性质和化学性质
人教版九年级下册化学 第八单元 金属和金属材料 实验活动4 金属的物理性质和某些化学性质 (2)

4.现有甲、乙、丙三种金属,分别与空气和氧气反应,现象如下表所示:
据此信息,这三种金属活动性由强到弱为
(A )
甲
乙
丙
空气
剧烈燃烧
变黑
变黑
氧气 更剧烈燃烧 变黑 剧烈燃烧
A.甲>丙>乙
B.甲>乙>丙
C.乙>丙>甲
D.丙>乙>甲
5.如图,为了验证镁、铜两种金属活动性大小,应该选择
(A )
A.稀硫酸 B.硫酸镁溶液 C.氯化钠溶液 D.植物油
2.金属的化学性质 (1)金属跟氧气的反应 ①铁在潮湿的空气里(既有 H2O 又有 O2 时)易生锈,铁锈是混合物,主
要成分是 Fe2O3·xH2O。
防锈方法:在铁表面涂一层保护膜(如刷漆或涂油),镀锌等金属或 烤蓝等。
②铁丝在氧气中燃烧:化学方程式为 3Fe+2O2=点==燃==Fe3O4。
(2)金属跟酸的反应 铁与稀硫酸反应:Fe+H2SO4===FeSO4+H2↑ (3)金属跟化合物溶液的反应 铁跟硫酸铜溶液反应:Fe+CuSO4===FeSO4+Cu
易错点:活泼金属与酸反应生成盐和氢气,但浓 H2SO4 和 HNO3 除外, 因为它们有较强的氧化性,与金属反应不产生氢气。
易混点:位于前面的金属能将后面的金属从它们的化合物溶液中置 换出来,若化合物不溶于水就不能置换(K、Ca、Na 除外)。
1.观察镁、铝、铁、铜的颜色和光泽:
金属 颜色和光泽
实验步骤
实验现象
实验结论
分别将打磨后的铁丝、银丝 铁丝表面有红色物质析
插入盛有CuSO4溶液的试管中, 出,银丝表面无现象
观察现象
金属活动性: Fe>Cu>Ag
钨铜材料参数

钨铜材料参数一、钨铜材料的基本介绍钨铜(Copper Tungsten)是一种由钨和铜组成的合金材料。
钨铜合金具有钨的高熔点和高硬度以及铜的良好导电性能,因此被广泛应用于电力、航空航天、电子、热管、大功率半导体器件等领域。
二、钨铜材料的组成与比例钨铜合金中的钨含量通常在50%到90%之间,而剩下的铜则占据剩余的百分比。
钨铜合金的具体组成比例可以根据不同的应用需求进行调整。
在一些特殊应用中,还可以添加其他元素来改变钨铜合金的性能。
三、钨铜材料的物理性质1.密度:钨铜合金的密度为15-18克/立方厘米,密度随着钨含量的增加而增加。
2.熔点:钨的熔点高达3410摄氏度,而铜的熔点为1083摄氏度。
钨铜合金的熔点随钨含量的变化而变化,一般在1500摄氏度以上。
3.热膨胀系数:钨铜合金的热膨胀系数低,对温度变化的敏感性小。
4.硬度:钨铜合金具有很高的硬度,钨的硬度约为钢的9倍,铜的硬度约为钢的3倍。
四、钨铜材料的机械性能1.抗拉强度:钨铜合金的抗拉强度较高,可以达到600-900兆帕,强度与钨含量成正比。
2.抗压强度:钨铜合金的抗压强度也较高,可以达到800-1200兆帕。
3.弹性模量:钨铜合金的弹性模量介于170-240吉帕斯卡之间,弹性模量决定了材料的刚性。
4.屈服强度:钨铜合金的屈服强度较高,一般大于400兆帕。
钨铜合金具有良好的导电性能,可以用作电接触材料。
其导电性能主要取决于铜的含量。
随着铜含量的增加,钨铜合金的导电性能也会提高。
钨铜合金的导电性能一般介于纯钨和纯铜之间。
六、钨铜材料的热传导性能钨铜合金不仅具有良好的导电性能,在热传导性能方面也表现出色。
钨铜合金的热传导系数高,能够有效地将热量传递出去,因此在导热材料领域得到广泛应用。
七、钨铜材料的耐腐蚀性能由于钨具有较高的耐腐蚀性,钨铜合金也具有较好的耐腐蚀性能。
在一些特殊的环境中,钨铜合金可以取代不锈钢等材料,以应对更严酷的腐蚀环境。
八、钨铜材料的应用领域1.电力行业:钨铜合金可用于制造高压开关、接触器和断路器等电力设备的触头材料,具有良好的电弧熔断性能和耐电弧熔蚀性能。
钨及其化合物

钨及其化合物1. 简介钨(符号:W)是一种重金属元素,原子序数为74。
它是地壳中含量很少的元素之一,但在自然界中主要以矿石的形式存在,如钨矿石和钨酸盐。
钨具有高熔点、高密度和良好的耐腐蚀性能,因此被广泛应用于各个领域。
钨及其化合物具有许多重要的应用,包括工业、冶金、电子、化学、医药等领域。
本文将深入探讨钨及其化合物的性质、制备方法以及应用领域。
2. 钨的性质2.1 物理性质钨是一种银白色金属,具有很高的密度(19.3 g/cm³),仅次于铂和金。
它具有很高的熔点(3422 °C)和沸点(5930 °C),使得它在高温环境下表现出优异的稳定性。
此外,钨还具有良好的导电和导热性能。
2.2 化学性质钨是一种非常稳定的元素,不受大多数酸和碱的侵蚀。
它可以与氧、硫、氮等元素形成多种化合物。
钨的最常见的氧化态是+6,但它也可以形成+4和+5的氧化态。
3. 钨化合物3.1 氧化钨(WO₃)氧化钨是一种常见的钨化合物,具有黄色或淡黄色的颜色。
它具有很高的稳定性和光学特性,因此被广泛应用于陶瓷、涂料、染料和催化剂等领域。
3.2 钨酸盐钨酸盐是一类以钨酸根离子(WO₄²⁻)为主要成分的化合物。
它们通常具有良好的溶解性和稳定性,在催化剂、电池、材料科学等领域有重要应用。
4. 钨及其化合物的制备方法4.1 钨的提取钨通常以矿石形式存在,如黑钨矿(FeWO₄)和白钨矿(CaWO₄)。
提取钨的方法包括浮选、重选、浸出等步骤,最终得到钨精矿。
然后,通过化学反应和冶炼过程,将钨精矿转化为纯净的钨金属。
4.2 钨化合物的合成钨化合物的合成方法多种多样,包括溶液法、固相法、气相法等。
具体方法根据目标化合物的性质和应用需求选择。
5. 钨及其化合物的应用领域5.1 工业领域由于钨具有高熔点和高密度,它被广泛应用于工业领域。
例如,钨被用作高温炉、电弧焊接电极、切削工具等。
5.2 冶金领域钨在冶金领域中也有重要应用。
钨及钨合金

真空熔炼
电弧炉、电子束炉熔炼
化学气相沉积( CVD)
高纯 H2(99. 99% )和高 纯 WF6 ( 99. 99% ) 为 原 料 气 体,通 过 化 学 反应 WF6 + 3 H2→W + 6HF还原生成钨原子, 在沉积仿形基体上获得钨沉积层 。沉积过
程结束后通过化学腐蚀或将基体在真空炉 中熔化获得沉积钨制品 。沉积制品形状取 决于沉积基体形状,尺寸精确可控
GTA
(A) (C)
(B)
GTA
GTA
EBW/GTAB
GTAB
GTA
Results for alloyed tungsten
GTA
Ebw
Conclusions
由于大多数钨合金韧脆转变温度都在室温以上,焊前对工件机械加工等处理 需要十分小心。
对于非合金化钨合金的单道焊接需要预热以避免裂纹的产生。
电触头、电 接点以及半 导体支承件 和火箭喷管
氩弧焊接、 等离子焊接 与切削、非 自耗电弧炉 等高温电极
电子管热阴 极、高温放 电电极和氩 弧焊电极
钨合金的制备工艺
粉末冶金
将钨粉与合金元素粉末或其他添加剂粉末充分混 合,再进行压制成形、预结、烧结等工序而成合 金锭坯,并对锭坯进行各种塑性加工可制成棒、 丝、片材等
chamber <5*10-5torr
1hr
pure argon
V=10ipm
I=350A
U=10~15V GTAB
filler metal tungsten and W26% Re(铼)
EBW 5*10-6torr 150KV 20mA
GTA
Results for unalloyed tungsten
金属钨
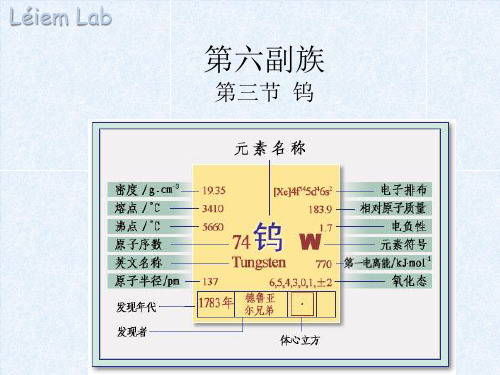
二,金属钨的化学性质
它的防腐性能非常好,大多数无机酸对它的侵 蚀很小.在空气里它的表面上形成一层保护性 的氧化物,但是在高温下它会被完全氧化.钢 里加入少量钨可以大大地增高钢的硬度.
一,钨和单质的反应
(1)钨和卤素反应
钨可以和氟气反应,粉状的钨在200℃反应, 微粉常温下便能和氟气反应,而钨棒在300℃ 才和氟气反应.钨和氟气反应主要牵扯到以下 反应: W+3F2==WF6; 2W+5F2==2WF5; W+3F2==WF5+F 在有氧气存在时,会有四氟氧化钨(WOF4)生成. 六氟化钨为无色体心立方或斜方晶,熔点2℃, 17.1℃沸腾,遇水分解.四氟氧化钨为无色单 斜晶,熔点110℃,沸点185.9℃,极易潮解, 在潮湿空气中转黄,生成氢氟酸及钨酸,不溶 于四氯化碳.
溶解的方程式如下: 氟王水: W+2HNO3+6HF→WF6+2NO↑+4H2O 3W+12HF+6HNO3→3WOF4+6NO↑+9H2O 王水: W+2HNO3→WO3+2NO↑+H2O W+2HCl+2HNO3→WO2Cl2+2NO↑+2H2O 在230℃钨粉可以溶解在90%磷酸中: 12W+H3PO4+36H2O→H3 [P(W3O10) 4]+36H2↑ 钨在碳酸(饱和CO2水溶液),油酸中无显 著侵蚀.
钨的稳定同位素有:182W(丰度26.50%), 183W(丰度14.30%),184W(丰度30.64%), 186W(丰度28.43%)
【三,金属钨】
一,金属钨的物理性质 钨的核性质
钨是一种化学元素,它的化学符号是W,它 的原子序数是74,是一种非常硬的,锡白 色的过渡金属.纯钨很脆,不易加工.含 有钨的矿物有黑钨矿和白钨矿等.钨的物 理特征非常强,尤其是它的熔点非常高, 是所有非合金金属中最高的.纯钨主要用 在电器和电子设备中,它的许多化合物和 合金也被用在许多其它应用中(最常见的 有灯泡的灯丝,在X射线管中以及在高温合 金中也有钨使用).
钨及钨合金

钨及钨合金的焊接
报告人:**
钨及钨合金简介
目录
钨及钨合金的焊接性
钨及钨合金简介
ห้องสมุดไป่ตู้
基本信息
钨 元素周期表第六周期ⅥB族元素,为稀有高熔点金属。元素符号W, 原子序数 74,相对原子质量183.85。致密块状金属钨呈银白色光泽。
表1 钨的主要物理性质
密度 ρ /kg·
m-3
熔点 T/K
沸点 T/K
19300
(293K) 17700
3680±2.0 5930
(熔点温 度的液体)
蒸气压 ρ /kPa
热导率 线胀系数
λ /W·m- α l/K-1 1·K-1
抗拉强度 σ b/MPa
弹性模量 E/MPa
3.38×10-13 (2000K)
7.75×10-7 (2800K)
1800
(未退火丝)
174(300K)
钨合金的高温强度
钨合金分类和用途(按照所添加元素的不同)
钨合金
钨铼合金
钨钼合金
高密度钨 合金
钨铜合金 钨银合金
铈钨合金 镧钨合金 钇钨合金
钍钨合金
电子管、显 像管、灯泡、 高温热电偶
等
电子管热丝、 玻璃封接引 出线和电火 花切割线
陀螺转子、 射线屏蔽材 料、压铸模、 配重材料和 穿甲弹体
钨丝化学式-概念解析以及定义
钨丝化学式-概述说明以及解释1.引言1.1 概述钨丝是一种重要的金属材料,具有广泛的应用前景。
它是由钨元素制成的细丝状物质,因其优异的物理性质和化学性质而在各个领域得到广泛应用。
钨丝的化学式为W,原子序数为74。
钨丝在工业、电子、照明等领域有着重要的作用,并且随着科学技术的发展,钨丝在新兴领域的应用也呈现出不断拓展的趋势。
钨丝的制备方法有多种,其中最常见的方法是通过钨矿石的冶炼和提纯得到纯钨金属,然后再通过拉伸、滚压等加工工艺制成细丝。
钨丝的制备工艺要求严格,需要控制合适的温度、气氛和机械条件,以获得高质量的钨丝产品。
钨丝具有良好的化学稳定性,不易被常见酸碱腐蚀。
同时,钨丝也具有较高的熔点和密度,使其能够在高温、高压环境下稳定地工作。
钨丝还具有良好的耐磨、耐腐蚀性能,使其在电子器件、化学催化剂、热电偶等领域得到广泛应用。
钨丝的物理性质也十分特殊。
它具有很高的熔点,达到了3410摄氏度,使其成为一种理想的熔炼材料。
钨丝还具有较低的热膨胀系数和良好的导电性能,使其在电子元件、电极材料等方面有着广泛的应用。
总之,钨丝作为一种重要的金属材料,具有广泛的应用前景。
其优异的化学性质和物理性质使其在多个领域得到应用,并且随着科技的进步,钨丝的应用领域也将进一步扩展。
因此,对钨丝的深入研究和发展具有重要意义,可以为科技创新和社会发展做出积极贡献。
1.2 文章结构文章结构部分的内容如下:2. 文章结构本文将按照以下结构展开对钨丝化学式的探讨。
首先,我们将在引言部分概述本文的主要内容和目的,并对钨丝化学式的重要性进行简要介绍。
接下来,正文部分将分为三个主要部分展开论述。
在第2.1节中,我们将介绍钨丝的历史背景,包括钨丝的发现和发展历程,以及相关的实验和探索。
我们将回顾钨丝的制备方法,并探讨不同制备方法的优劣之处。
第2.2节将重点关注钨丝的化学性质。
我们将介绍钨丝的化学式及其结构,以及钨丝在不同环境中的反应性和化学性质的变化。
钨(W)
广义的钨合金和狭义的钨合金。广义的钨合金: 含有钨元素的金属材料统称为钨合金,如钨铁 合金、钨铜合金、钨镍合金等;狭义的钨合金: 以钨为基体材料(其中含钨量为85%~99%) 加入少量镍(Ni)、铜(Cu)、铁(Fe)、钴 (Co)、钼(Mo)、铬(Cr)等金属黏结剂 组成的一种合金材料,也被称之为高比重钨合 金或高密度钨合金或重合金.
储氢合金
由于石油和煤炭的储量有限,而且在使用过程 中会带来环境污染等问题,尤其是20世纪70 年代全球石油危机,使氢能作为新的清洁燃料 成为研究热点。在氢能利用过程中,氢的储运 是重要环节。1969年荷兰飞利浦公司研制出 LaNi5储氢合金,具有大量的可逆地吸收、释 放氢气的性质,其合金氢化物LaNi5H6中氢的 密度与液态氢相当,约为氢气密度的1 000倍。
晶体结构及晶格常数Α-W:体心立方 A=3.16524 NM(25℃)
晶胞参数: a = 316.52 pm,b = 316.52 pm,c = 316.52 pm,α = 90°,β = 90°,γ = 90° β-W:立方晶格 a=5.046 nm(630℃以下稳定) 弹性模量:35000—38000 MPa(丝材) 扭力模量:~36000Mpa
高温材料 钨材使用温度高,单纯采用固溶强化方法对提 高钨的高温强度效果不大。但在固溶强化的基 础上再进行弥散(或沉淀)强化,可大大提高高温 强度,以ThO2和沉淀的HfC弥散质点的强化效果 最好。在 1900℃左右W-Hf-C系和W-ThO2系合 金都有着高的高温强度和蠕变强度。在再结晶 温度以下使用的钨合金,采取温加工硬化的方 法,使其产生应变强化,是有效的强化途径。
请老师同学批评指正
谢谢
钨导热系数
钨导热系数钨导热系数导热系数是指物质传递热量的能力,通常用W/(m·K)表示。
钨是一种高熔点金属,具有良好的导热性能,其导热系数随温度的变化而变化。
一、钨的基本概述1.1 钨的性质钨是一种灰白色金属,具有高密度、高硬度、高融点、高强度和耐腐蚀等特性。
它是地球上最稀有的元素之一,也是最重要的工业金属之一。
1.2 钨的应用领域由于其特殊的物理和化学性质,钨在许多领域都有广泛应用。
例如,在电子行业中,钨被用作电极材料;在航空航天工业中,它被用于制造发动机部件和火箭喷嘴;在医学领域中,它被用于制造放射线保护材料等。
二、钨导热系数的基本知识2.1 导热系数的定义导热系数是指单位时间内单位面积上温度梯度方向上传递的热量。
在材料科学中,导热系数是一种重要的物理参数,它反映了材料传递热量的能力。
2.2 钨导热系数的测量方法测量钨导热系数的方法有多种,其中比较常用的是横向热流法和纵向热流法。
横向热流法是指将样品放置在两个恒温环境之间,通过测量样品两端的温度差和加热功率来计算导热系数。
纵向热流法则是将样品置于一个恒温环境中,通过测量样品表面的温度差和加热功率来计算导热系数。
三、钨导热系数与温度的关系3.1 钨导热系数随温度变化的特点钨具有良好的导热性能,但其导热系数随着温度升高而逐渐降低。
这是因为随着温度升高,晶格振动增强,原子之间相互作用减弱,从而影响了电子和声子传输过程。
3.2 钨导热系数与温度变化规律在常温下,钨的导热系数约为174 W/(m·K)。
随着温度升高,钨的导热系数逐渐降低。
当温度达到3000K时,钨的导热系数约为98W/(m·K)。
四、影响钨导热系数的因素4.1 温度如前所述,钨的导热系数随着温度升高而逐渐降低。
4.2 结构和纯度钨的结构和纯度也会影响其导热性能。
晶格结构不同、晶粒尺寸不同以及杂质含量不同都会对钨的导热性能产生影响。
4.3 压力压力也是影响钨导热系数的因素之一。
钨合金球标准-概述说明以及解释
钨合金球标准-概述说明以及解释1.引言1.1 概述钨合金球是一种由钨及其他合金元素组成的球状材料。
钨合金球具有优异的物理和化学性质,因此在许多领域得到广泛应用。
本文旨在介绍钨合金球的标准和相关知识。
钨合金球具有高密度、高熔点、高硬度和优异的耐磨性能。
这些特性使得钨合金球成为许多行业中不可或缺的材料。
例如,在航空航天领域,钨合金球被广泛应用于制造高温部件、航天器的动力系统以及导弹和火箭的导引装置。
此外,钨合金球还被用作核能领域中的重要材料,用于制备核燃料和控制反应堆中的核燃料棒。
钨合金球的制备方法多种多样,常见的方法包括粉末冶金、熔融铸造和化学气相沉积等。
粉末冶金是最常用的制备方法之一,通过粉末冶金可以获得均匀的成分和微观组织,从而保证钨合金球的高质量。
熔融铸造则适用于制备大规模和复杂形状的钨合金球。
化学气相沉积技术则常用于制备纯度较高的钨合金球。
钨合金球的应用领域非常广泛。
除了航空航天和核能领域之外,钨合金球还被广泛应用于电子、军工、化工、医疗器械等领域。
在电子行业,钨合金球被用作电路连接材料和半导体封装材料。
在军工领域,钨合金球则被用于制造弹头、弹壳等重要部件。
在化工领域,钨合金球被用作催化剂和催化载体。
在医疗器械领域,钨合金球被应用于放射治疗和诊断设备中。
综上所述,钨合金球作为一种重要的材料,在各个领域发挥着重要的作用。
本文将对钨合金球的定义、制备方法以及应用领域进行详细介绍,并展望其未来的发展趋势。
通过对钨合金球的研究和应用,我们可以更好地利用其特性,推动相关领域的发展和进步。
文章结构部分的内容可以包括以下几个方面:文章结构的说明- 本篇文章将按照以下结构进行阐述和探讨。
- 首先,我们将在引言部分对钨合金球进行概述,介绍其定义、制备方法以及应用领域。
- 接下来,我们将在正文部分详细介绍钨合金球的定义,包括其成分和特性等。
- 然后,我们将探讨钨合金球的制备方法,包括常见的制备工艺和相关技术。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
钨属于元素周期表第Ⅵ族副族,原子的最外层电子排布是5d46s2,氧化价从+2到+6价。
致密钨呈钢灰色,粗颗粒钨粉显深灰,直至超细钨粉显黑色,并皆具有金属光泽。
其熔点为3410±20℃,密度为19.3g/cm,,沸点为5700±200℃,其熔点是所有金属中最高的。
钨的导电性能好,电子逸出功较小。
在机械性能方面其硬度和抗拉强度极限都与加工及热处理情况杂质含量有密切关系。
常温下,钨在空气中十分稳定,在400℃轻微氧化,高于500-600℃则迅速氧化生成WO3,不与氢气发生作用,因而其热处理过程可在氢气保护下进行。
在氮气中致密钨到2000℃才发生反应。
炽热温度下,能与水蒸气作用生成WO2。
常温下,钨在任意浓度的盐酸、硫酸、硝酸、氢氟酸和王水中都是稳定的。
80~100℃下只与盐酸,硫酸发生微弱反应,硝酸与王水对它有明显的腐蚀,而在氢氟酸和王水混合酸中则迅速溶解。
常温下钨与碱溶液不发生反应,但在氧化剂(如KNO3等)存在下高温熔融,则钨与碱剧烈反应生成钨酸盐。
美国用喷雾干燥-流化床技术制备纳米WC粉体,其中间产物纳米金属钨粉体采用氧化钨(WO3)还原法制备。
此法先用喷雾干燥技术得到AMT粉体[(NH4)6·(H2W12O10)·4H2O],再将AMT粉体在500℃Ar气氛中热解得到黄色的WO3粉体最后用纯度为99.999%的H2还原得到纳米金属W粉体。
当还原温度T<575℃时,得到β-W结构的纳米W粉,平均晶粒度为9nm;当T=575~650℃时,得到份β-W与α-W两种结构共存的纳米W粉体,平均晶粒度为10~15nm;而当T>650℃时,得到α-W结构的纳米W粉体,平均晶粒度为16nm。
Fecht曾指出,高能球磨法可将包括金属钨在内的体心立方(bcc)金属粉细化至纳米尺寸。
Wagner的实验结果表明,用高能球磨方法可制备出平均晶粒尺寸为5nm的金属钨粉体,但因钢球与球磨罐在球磨过程中沾染了W粉体,使其中含有杂质Fe。
如延长球磨时间,纳米W粉不再细化,含Fe量却不断增加直至生成无定型的Fe-W合金。
钨是稀有高熔点金属,属于元素周期系中第六周期(第二长周期)的VIB 族。
钨是一种银白色金属,外形似钢。
钨的熔点高,蒸气压很低,蒸发速度也较小。
它的主要物理性质如下:
元素符号&Nbsp; W
原子序数74
稳定同位素及其所占% 180(0.14);182(26.41);183(14.40);184(30.64);186(28.41)
原子体积9.53 cm3/mol
密度19.35 g/cm3
晶体结构及晶格常数
α-W:体心立方a=3.16524 nm(25℃)
β-W:立方晶格a=5.046 nm(630℃以下稳定)
熔点3410±20℃
沸点5927℃
熔化潜热40.13±6.67kJ/mol
升华热847.8 kJ/mol(25℃)
蒸发热823.85±20.9kJ/mol(沸点)
电阻温度系数0.00482 I/℃
热膨胀系数 4.6 ×10^(-6) ,[20~590℃]
电子逸出功 4.55 eV
热中子俘获面19.2 b
弹性模量35000~38000 MPA(丝材)
扭力模量~36000Mpa
体积模量 3.108×1011-1.579×107t+0.344×103t2 Pa
剪切模量 4.103×1011-3.489×107t+7.55×103t2 Pa
压缩性 2.910-7 cm/kg
钨有两种变型,α和β。
在标准温度和常压下,α型是稳定的体心立方结构。
β型钨只有在有氧存在的条件下才能出现。
它在630℃以下是稳定的,在630℃以上又转化为α钨,并且这一过程是不可逆的。
