冰醋酸含量测定报告
冰醋酸—冰醋酸的测定—中和滴定法

冰醋酸—冰醋酸的测定—中和滴定法仪器设备:试样制备:1.氢氧化钠滴定液(1mol/l):配制:取氢氧化钠适量,加水振摇使溶解成饱和溶液,冷却后,置聚乙烯塑料瓶中,静置数日,澄清后备用。
取澄清的氢氧化钠饱和溶液56ml,加新沸过的冷水使成1000ml,摇匀。
标定:取在105℃干燥至恒重的基准邻苯二甲酸氢钾约0.6g,精密称定,加新沸过的冷水50ml,振摇,使其尽量溶解,加酚酞指示液2滴,用本液滴定,在接近终点时,应使邻苯二甲酸氢钾完全溶解,滴定至溶液显粉红色。
每1ml氢氧化钠滴定液(1mol/l)相当于204.2mg的邻苯二甲酸氢钾。
根据本液的消耗量与邻苯二甲酸氢钾的取用量,算出本液的浓度。
贮藏:置聚乙烯塑料瓶中,密封保存;塞中有2孔,孔内各插入玻璃管1支,1管与钠石灰管相连,1管供吸出本液使用。
2.酚酞指示液:取酚酞1g,加乙醇100ml使溶解。
应用范围本方法采用滴定法测定冰醋酸中冰醋酸的含量。
本方法适用于冰醋酸。
方法原理供试品加新沸过的冷水与酚酞指示液,用氢氧化钠滴定液滴定,根据滴定液使用量,计算冰醋酸的含量。
试剂1. 氢氧化钠滴定液(1mol/l),2. 酚酞指示液,3. 基准邻苯二甲酸氢钾试样制备1.氢氧化钠滴定液(1mol/l):配制:取氢氧化钠适量,加水振摇使溶解成饱和溶液,冷却后,置聚乙烯塑料瓶中,静置数日,澄清后备用。
取澄清的氢氧化钠饱和溶液56ml,加新沸过的冷水使成1000ml,摇匀。
标定:取在105℃干燥至恒重的基准邻苯二甲酸氢钾约0.6g,精密称定,加新沸过的冷水50ml,振摇,使其尽量溶解,加酚酞指示液2滴,用本液滴定,在接近终点时,应使邻苯二甲酸氢钾完全溶解,滴定至溶液显粉红色。
每1ml氢氧化钠滴定液(1mol/l)相当于204.2mg的邻苯二甲酸氢钾。
根据本液的消耗量与邻苯二甲酸氢钾的取用量,算出本液的浓度。
贮藏:置聚乙烯塑料瓶中,密封保存;塞中有2孔,孔内各插入玻璃管1支,1管与钠石灰管相连,1管供吸出本液使用。
冰醋酸(15版中国药典公示稿)

冰醋酸BingcusuanGlacial Acetic AcidC2H4O260.05[64-19-7]本品含C2H4O2不得少于99.0%(g/g)。
【性状】本品为无色的澄明液体或无色的结晶块;有强烈的特臭。
本品与水、乙醇、甘油或多数的挥发油、脂肪油均能任意混合。
凝点本品的凝点(附录ⅥD)不低于14.8℃。
【鉴别】(1)取本品1ml,加水1ml,用氢氧化钠试液中和,加三氯化铁试液,即显深红色;煮沸,即生成红棕色的沉淀;再加盐酸,即溶解成黄色溶液。
(2)取本品少许,加硫酸与少量的乙醇,加热,即发生乙酸乙酯的香气。
【检查】氯化物取本品10ml,加水20ml。
依法检查(附录ⅧA),与标准氯化钠溶液4.0ml制成的对照液比较,不得更深(0.0004%)。
硫酸盐取本品20ml,加1%无水碳酸钠溶液1ml,置水浴上蒸干,依法检查(附录ⅧB),与标准硫酸钾溶液1.0ml制成的对照液比较,不得更深(0.0005%)。
铁盐取本品2ml,置水浴上蒸干,加水15ml,微温溶解后,加水适量使成25ml,依法检查(附录ⅧG),与标准铁溶液1.0ml制成的对照液比较,不得更深(0.0005%)。
甲酸与易氧化物取本品5ml,加水10ml稀释后,分取5ml,加重铬酸钾滴定液(0.01667mol/L)2.5ml与硫酸6ml,放置1分钟,再加水20ml,冷却至15℃,加碘化钾试液1ml,应显深黄色或棕色。
乙醛取本品1.8 ml,精密称定,置10 ml量瓶中,用水稀释至刻度,摇匀,取2.5 ml,置顶空瓶中,加3.2mol/L氢氧化钠溶液2.5ml,立即密封,摇匀,作为供试品溶液; 另取乙醛对照品适量,精密称定,用1.6mol/L醋酸钠溶液稀释制成每1 ml中约含0.01 mg的溶液,精密量取5 ml,置顶空瓶中,密封,作为对照品溶液。
照残留溶剂测定法(中国药典2010年版二部附录ⅧP第二法)测定,以聚乙二醇聚硅氧烷为固定液的毛细管柱为色谱柱: 柱温35℃维持5分钟,以每分钟30℃的速率升温至120℃,维持2分钟;进样口温度200 ℃;检测器温度250℃;顶空平衡温度为80 ℃,平衡时间为30分钟。
7冰醋酸
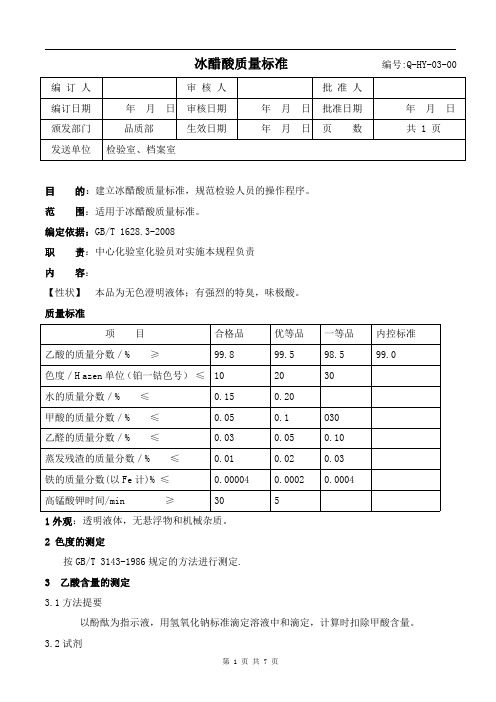
冰醋酸质量标准编号:Q-HY-03-00编订人审核人批准人编订日期年月日审核日期年月日批准日期年月日颁发部门品质部生效日期年月日页数共1页发送单位检验室、档案室目的:建立冰醋酸质量标准,规范检验人员的操作程序。
范围:适用于冰醋酸质量标准。
编定依据:GB/T1628.3-2008职责:中心化验室化验员对实施本规程负责内容:【性状】本品为无色澄明液体;有强烈的特臭,味极酸。
质量标准项目合格品优等品一等品内控标准乙酸的质量分数/%≥99.899.598.599.0色度/H azen单位(铂一钴色号)≤102030水的质量分数/%≤0.150.20甲酸的质量分数/%≤0.050.1O30乙醛的质量分数/%≤0.030.050.10蒸发残渣的质量分数/%≤0.010.020.03铁的质量分数(以Fe计)%≤0.000040.00020.0004高锰酸钾时间/min≥3051外观:透明液体,无悬浮物和机械杂质。
2色度的测定按GB/T3143-1986规定的方法进行测定.3乙酸含量的测定3.1方法提要以酚酞为指示液,用氢氧化钠标准滴定溶液中和滴定,计算时扣除甲酸含量。
3.2试剂3.2.1氢氧化钠标准滴定溶液:c(NaOH)=1mo1/L;3.2.2酚酞指示液:5g/L。
3.3分析步骤用容量约3ml 具塞称量瓶称取约2.5g 试样,精确至0.0002g。
置于已盛有50ml 无二氧化碳水的250ml 锥形瓶中,并将称量瓶盖摇开,加0.5ml 酚酞指示液,用氢氧化钠标准滴定溶液滴定至微粉红色,保持5s 不退为终点。
3.4结果计算乙酸的质量分数以%表示,计算:乙酸%=21305.11001000w m cM V-⨯(实际乙酸%=10010001⨯mcM V)式中:V—试样消耗氢氧化钠标准滴定溶液的体积的数值,单位为毫升(ml);c—氢氧化钠标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);m—试样的质量的数值,单位为克(g);M1—乙酸的摩尔质量的数值,单位为克每摩尔(g/mol)(M,-60.05);1.305-甲酸换算为乙酸的换算系数;W2—按测得的甲酸的质量分数,数值以%表示。
19冰醋酸含量测定

1、 适用范围
本品适用与不含其它酸类物质的冰醋酸,且冰醋酸浓度大于50%适用。
2、 原理
样品在合适的指示剂的存在下,用规定浓度的碱标准溶液滴定,测出消耗规定浓度的碱的体积,计算样品的含量。
3、仪器及装置 3.1 量筒 3.2 移液管
3.3 100mL 具塞锥形瓶 3.4 滴定管 4、操作步骤
4.1量取15ml 无二氧化碳水注入具塞锥形瓶中,称量(称量精确至0.0001g ); 4.2移区1ml 冰醋酸样品到具塞锥形瓶中,再次称量;
4.3加入40ml 无二氧化碳水及2滴10g/L 的酚酞指示剂,摇匀; 4.4用氢氧化钠标准滴定溶液[c(NaOH)=0.5mol/L]滴定至溶液呈粉红色。
计算公式:
V*c*60.05
m*1000
式中:X :乙酸的质量百分含量%
V :氢氧化钠标准滴定溶液的体积ml
c :氢氧化钠标准滴定溶液的实际浓度mol/L 60.05:乙酸的摩尔质量mol/L m :样品的质量g 5、表单:
6、参考标准
本分析方法参考《化学试剂 乙酸(冰醋酸)》GB/T676 2007 (代替GB/T676 1990)
X=
*100。
冰乙酸检测标准

冰乙酸检测标准一、外观检查主要检查样品的色泽、杂质等指标,确保样品符合国家标准的要求。
通常采用视觉观察或借助放大镜进行详细检查。
二、纯度检查按照国家标准要求,通过重量法或酸值法测定冰乙酸的纯度。
重量法是通过称量样品的质量,计算出质量分数;酸值法是通过测定冰乙酸的酸碱反应程度来确定其纯度。
三、水分检查通过卡尔·费休法测定冰乙酸中水分的含量。
该方法利用碘与水反应生成碘化氢,再与卡尔·费休试剂反应生成水,根据试剂的消耗量计算出水分的含量。
四、杂质检查通过比重法或色谱法测定冰乙酸中其他有机物的含量。
比重法是通过测定样品的密度来推算杂质含量;色谱法则是利用色谱柱将杂质分离出来,再通过检测器测定各组分的含量。
五、酿造醋酸比率依照方法标准GB/T 22099-2008 《酿造醋酸与合成醋酸的鉴定方法》,通过测定醋酸的天然度即测试冰醋酸中14C的比活度与标准值的比值进行检测。
天然度越高,酿造醋酸的比率越高。
六、食醋卫生标准主要通过GB/T 5009.41-2003《食醋卫生标准的分析方法》进行检测,以确保样品符合国家卫生标准。
该标准规定了冰醋酸的卫生指标,包括总砷、铅、铜、锌等元素的含量以及菌落总数和大肠菌群数等微生物指标。
七、工业醋酸浓度乙酸也叫醋酸或者冰醋酸,在正常气温下的标准浓度为17.5mol/L,在空气中最大浓度不超过25mg/m3。
工作场所乙酸的最高容许深度为10ppm。
对于工业用冰乙酸,还需特别关注其可能存在的杂质和安全性问题。
在涉及工业用冰乙酸的场所,应采取必要的通风措施,佩戴个人防护用品等措施来保障操作人员的健康和安全。
八、区分食用醋酸和工业乙酸用于区分食用醋酸和工业乙酸(或工业醋酸)的检测标准主要是参照GB 1903-2008《食品添加剂冰醋酸(冰乙酸)》,该标准规定了食用醋酸的要求、试验方法、检验规则和标志、包装、运输、贮存等。
在该标准中,食用醋酸被定义为以食用酒精为原料经醋酸发酵或以化学合成法生产的乙酸,专供配制食醋之用。
醋酸的电离实验报告

醋酸的电离实验报告一、实验目的1、了解弱电解质在溶液中的电离平衡。
2、掌握测定醋酸电离常数的方法。
3、加深对电离平衡概念的理解。
二、实验原理醋酸(CH₃COOH)是一种弱电解质,在水溶液中存在电离平衡:CH₃COOH ⇌ CH₃COO⁻+ H⁺其电离常数表达式为:Ka = CH₃COO⁻H⁺/ CH₃COOH通过测定一定浓度的醋酸溶液的 pH 值,可以计算出溶液中氢离子浓度H⁺。
再根据初始醋酸的浓度,就可以计算出醋酸的电离常数Ka。
三、实验仪器与试剂1、仪器pH 计容量瓶(100 mL)移液管(25 mL)烧杯(50 mL、100 mL)玻璃棒胶头滴管2、试剂冰醋酸(分析纯)蒸馏水四、实验步骤1、配制不同浓度的醋酸溶液用移液管准确量取 250 mL 冰醋酸,注入 100 mL 容量瓶中,用蒸馏水稀释至刻度,摇匀,得到浓度约为 010 mol/L 的醋酸溶液。
用移液管分别吸取上述 010 mol/L 醋酸溶液 500 mL、1000 mL、2500 mL 于三个 100 mL 容量瓶中,用蒸馏水稀释至刻度,摇匀,得到浓度分别约为 0005 mol/L、001 mol/L、0025 mol/L 的醋酸溶液。
2、测定醋酸溶液的 pH 值用 pH 计分别测定上述不同浓度醋酸溶液的 pH 值,记录数据。
每个溶液测定三次,取平均值。
3、数据处理根据 pH 值计算出氢离子浓度 H⁺。
以 H⁺/ c 为纵坐标,H⁺为横坐标作图,通过直线的斜率和截距计算醋酸的电离常数 Ka。
五、实验数据记录与处理1、实验数据记录|醋酸溶液浓度(mol/L)| pH 值(第一次)| pH 值(第二次)| pH 值(第三次)|平均 pH 值| H⁺(mol/L)||::|::|::|::|::|::|| 0005 |_____ |_____ |_____ |_____ |_____ || 001 |_____ |_____ |_____ |_____ |_____ || 0025 |_____ |_____ |_____ |_____ |_____ |2、数据处理以 H⁺/ c 为纵坐标,H⁺为横坐标作图。
工业用冰乙酸中乙酸含量的测定

酸碱滴定法测定工业冰乙酸中乙酸含量 ❖允许差 两次平行测定结果的绝对差值不大于
0.15 %。
六、项目完成效果评价
❖自评:每组选出一名代表介绍本组的实验设计,实 验结果,实验验证的情况;
❖互评:其他组同学对他们的实验提出问题,进行评 价,由组内成员解答。
❖教师评价:教师对自评和互评结果进行评价,并提 出改量的测定
问题:工业冰乙酸中乙酸含量的测定难 点在哪里?
问题:如何根据性质选择合适的方法?
吉化103厂醋酸生产装置
知识点一 关于冰乙酸的基础知识
❖中文名称: 乙酸 ❖英文名称: Acetic acid或Ethanoic acid ❖别 名: 醋酸;冰醋酸 ❖分子式:C2H4O2 CH3COOH ❖结构式:
二、教学任务
1 查阅资料、解读标准、讨论并制定工业 用冰乙酸中乙酸含量测定方案
2 实施测定方案并在实施过程中优化 测定方案
3 完成实际工业产品试样中乙酸含量的 测定,按照GB/T 1628- 要求对其 质量进行评定
三、教学方法
小组讨论法
提问引导法
多媒体教学法
DDiiaaggrraamm 22
讲练结合法
❖方法提要 以酚酞为指示液,用氢氧化钠标准滴定溶液中和滴
定,计算时扣除甲酸含量。 ❖试剂 氢氧化钠标准滴定溶液:c(NaOH) =1 mol/L; 酚酞指示液:5g/L。 ❖分析步骤 用容量约3mL具塞称量瓶称取约2.5g试样,精确至
0.0002g。置于已盛有50 mL 无二氧化碳水的 250 mL 锥形瓶中,并将称量瓶盖摇开,加0.5mL 酚酞指示 液,用氢氧化钠标准滴定溶液滴定至微粉红色,保持 5s不退为终点。
DDiaigargarm am 33
药检检测乙酸含量方法2010317142938403
合成多肽中的醋酸测定方法《中华人民共和国药典 2010版二部》新增附录 VII N:合成多肽中的醋酸测定方法,方法全文如下:本方法系用液相色谱法测定合成多肽中醋酸或醋酸盐的含量。
除另有规定外,按下列方法测定。
对照品溶液的制备取冰醋酸适量,精密称定,用流动相A-流动相B(95:5)的混合溶液定量稀释制成每1ml中约含0.1mg的溶液(对照品溶液的浓度可随供试品中醋酸的含量作适当调整)供试品溶液的制备照各品种项下规定的方法制备(取样量应根据其醋酸含量而定)色谱条件及系统适用性实验用十八烷基键合硅胶为填充剂(250mm×4.6mm,5μm),以磷酸溶液(在1000ml水中加磷酸0.7ml,用氢氧化钠试液调节pH至3.0)为流动相A,甲醇为流动相B;流速为每分钟1.2ml;检测波长为210nm。
按下表进行梯度洗脱。
理论塔板数按醋酸峰计算不低于2000。
醋酸峰的保留时间约在3~4分钟。
梯度洗脱开始后,多肽被洗脱,基线急剧升高。
测定法精密量取对照品溶液和供试品溶液各10μl,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算多肽中的醋酸含量。
博纳艾杰尔科技的Venusil XBP C18色谱柱按照上述方法,用于合成多肽中的醋酸测定,经过对不同品种多肽样品中醋酸的测定,结果非常稳定,准确。
结果见下图。
色谱条件:色谱柱:Agela Venusil XBP-C18柱,100Å,4.6×250mm,5µm (订货号:VX952505-0);流动相A:取0.7ml磷酸,加水至1000ml,以浓氢氧化钠溶液调节pH值至3.0。
流动相B:甲醇;流速: 1.2 ml/min;进样体积:10µl;检测波长210nm。
洗脱梯度:时间(min) 流动相A( %) 流动相B( %)0 95 55 95 510 50 5020 50 5022 95 530 95 5博纳艾杰尔科技 全国服务热线:400-6068-099 service@一、醋酸奥曲肽中醋酸含量测定图1、醋酸对照品溶液色谱图图2、醋酸奥曲肽供试品溶液色谱图博纳艾杰尔科技 全国服务热线:400-6068-099 service@二、 鲑降钙素醋酸含量测定图3、醋酸对照品溶液色谱图图4、鲑降钙素供试品溶液色谱图博纳艾杰尔科技 全国服务热线:400-6068-099 service@三、胸腺法新醋酸含量测定图5、醋酸对照品溶液色谱图图6、胸腺法新供试品溶液色谱图博纳艾杰尔科技 全国服务热线:400-6068-099 service@。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
冰醋酸含量测定报告 Prepared on 22 November 2020
冰醋酸的成分含量测定方法
实验目的:主要是为了测定供应商提供的冰醋酸的浓度含量是否达到标准要求(CH3COOH%>=98%)。
实验器材:烧杯三个(50ml)锥形瓶两个(带活塞1个)(250ml)酸式滴定管1个100g的精密电子秤一个 .滴管2个
实验原料:100ml的冰醋酸(无色透明液体,具有很强的挥发性,刺激性气味)的氢氧化钠(L的NaoH是无色透明液体,有腐蚀性)酚酞指示剂(主要是为了测
定溶液的碱性)蒸馏水(500ml以上)(注意不能用自来水)
实验原理:主要是通过冰醋酸与氢氧化钠的中和反应,酚酞试剂遇碱变色的原理.往稀释的冰醋酸溶液中滴入的NaOH溶液,直至溶液变成微红色。
(通过化学反应,
可知1摩尔的醋酸消耗1摩尔的氢氧化钠。
测出消耗多少体积的氢氧化钠,
就可以算出消耗多少摩尔的氢氧化钠,进而计算出消耗多少质量的醋酸,通
过反应消耗醋酸的质量与样品的质量百分比,就求出样品中醋酸的含量百分
比。
)
化学反应式: NaOH + CH3COOH = CH3COONa + H2O
计算公式:CH3COOH%={N(NaOH)*V(NaOH)*样品重(g)*1000}*100%
实验步骤:1.先在实验室充分准备好此次实验的器材和实验的原料。
(拿一个250ml的锥形瓶(带活塞)到车间的助剂室提取100ml的冰醋酸,并立即盖好塞子。
贴上标签)其他的材料均可在实验室提取。
2. 分别给烧杯编上(1、2、3)号,锥形瓶((装有样品醋酸的为1)、装稀
释的醋酸为2),滴定管(1、2)
3.开电子秤(待电子秤显示数据),接着把烧杯1放到电子称上面称量,调
零。
并关闭好各个电子称的各个门。
4.把装有醋酸的锥型瓶半倾,将滴管1伸进醋酸溶液的中间吸取溶液,接着将
滴管1取出,并盖好锥形瓶1瓶子。
5.先打开电子称的顶门,将滴管1伸入电子秤上空中,滴2-3滴()左右的醋
酸溶液,关好电子秤的顶门,待秤上读数稳定,读取读数,并记录读数g。
6.把滴定管放到烧杯2中,迅速打开电子秤的侧门,将烧杯1取出,并用蒸馏
水进行稀释(将蒸馏瓶嘴贴着烧杯1口环绕注入蒸馏水),导入锥形瓶2
中,25ml左右一次,进行四次,共100ml,
7.关闭电子秤,将其他器材与移到滴定管旁边。
并在滴定管下方放一张白纸,
防止滴定管漏出的NaOH溶液腐蚀试验台。
8.用滴管2吸取酚酞试剂,往锥形瓶2滴入1—2滴酚酞试剂。
9.倒入适量的氢氧化钠溶液到烧杯3.在将烧杯3的氢氧化钠溶液缓慢的倒入滴
定管中,使得滴定管的液面升到刻度10ml左右。
10.将烧杯3沾取滴定管口溢出的NaOH溶液,读取滴定管的数据,并记录V2.
11.将锥形瓶2放到滴定管的正下方,左手控制滴定管的旋转开关(主要是为
了控制滴定管的滴定速度。
)一滴,一滴的放,右手拿着锥形瓶2.晃动锥形
瓶2,使得溶液能够均匀、充分反应,观察锥形瓶2溶液的变化,当发现锥形
瓶里面形成的红色物质消去的时间变长时,要减慢滴定管的滴定速度,最好
就是半滴,半滴的滴定。
当发现锥形瓶2的溶液变成微红色(不能消失)
时,停止滴定,读取并记录滴定管的读数。
并进行数据处理。
12.重复以上实验4次,记录四组数据,算出每一组的CH3COOH%值,求出平
均值。
13.对实验的结果进行数据分析。
14.废液的处理,整理好实验室的卫生,清洗各种实验器具并放好。
实验的注意事项及误差分析:
1.烧杯,锥形瓶,以及滴管都要保证干净,无水。
(否则的话会产生误
差,严重影响实验的测试结果,导致实验的失败。
)
2.吸取、称量醋酸,以及稀释醋酸时要考虑到醋酸的强挥发性,醋酸的挥
发性会导致测试出醋酸的含量比变小。
3.读取滴定管时,视线要与滴定管的液面平齐(注意不要俯视,仰
视。
),要读取液面的最低处,否则也会影响到数据的准确性,使得实验结果产生较大的误差。
4.在控制滴定管滴定氢氧化钠溶液时,要控制好滴定的速度,使得溶液的
液面为微红色,如果液面为红色,甚至是深红色,则会影响测出的结果,导致测出醋酸的含量会变大。
5.左手控制滴定管时,要注意适度的控制好速度调节开关,避免滴定管里
面的液体从开关处漏出,影响结果,同时当氢氧化钠沾到时,要立刻到水龙头处冲水处理。
6.用电子秤称量时要关好电子秤的各个门,防止外来的空气造成数据的不
准确性。
7.当装有稀释醋酸的锥形瓶2移离滴定管上方时,要注意把烧杯2放到滴定管的正下方,防止NaOH溶液滴到实验台上,造成污染和浪费。
