柔红霉素、盐酸多柔比星和盐酸表柔比星的HPLC分析
化疗患者静脉通路管理

化疗患者静脉通路管理
化疗药物在静脉给药过程中意外渗漏的发生率为0.1%~6%。
外渗的后果有多种,可表现为轻度红斑、局部不适或疼痛、组织坏死、皮肤溃疡以及深部结构如肌腱和神经损伤。
根据化疗药物外渗后对组织的损伤程度,可以将化疗药物分为两类:
1.发疱性化疗药物外渗后可以引起局部组织坏死的药物。
如:盐酸多柔比星、盐酸表柔比星、吡柔比星、柔红霉素、放线菌素D、丝裂霉素、长春新碱、长春瑞宾、光辉霉素、氮芥、长春花碱、更生霉素等。
2.非发疱性化疗药物
(1)刺激性化疗药物:外渗后可以引起灼伤或轻度炎症而无坏死的药物。
如卡氮芥、卡铂、奥沙利铂、氮烯咪胺、依托泊苷、链脲霉素、伊立替康、托泊替康、博来霉素等。
(2)无明显刺激作用的药物:如环磷酰胺、异环磷酰胺、甲氨蝶呤、氟脲嘧啶、阿糖胞苷、顺珀、米托蒽醌、平阳霉素、门冬酰胺酶等。
还有一些药物如:紫杉醇、多西他赛、吉西他滨等药物。
虽然在各类文献报道中都没有对外周静脉刺激的报道,但在临床使用的过程中如多西他赛,紫杉醇有皮肤溃烂及坏死现象。
药物外渗后会给患者带来很大的痛苦,所以我们建议化疗要选择中心静脉置管,这样杜绝化疗药物外渗的现象。
在以上的药物中,发疱性的药物是必须做picc置管或中心静脉置管来做,刺激性药物建议用静脉留置针来输入,不主张用钢针输入化疗药物。
另外持续静脉。
脂质体多柔比星治疗淋巴瘤的疗效以及安全性分析

脂质体多柔比星治疗淋巴瘤的疗效以及安全性分析【摘要】目的:探讨观察在治疗淋巴瘤患者的过程中,使用脂质体多柔比星进行治疗的临床疗效,为临床治疗提供依据。
方法:选取2019年10月~2021年2月间接受治疗的淋巴瘤患者共100例为研究对象,所有患者均使用脂质体多柔比星进行治疗,对患者的临床资料进行回顾性分析,统计分析患者的治疗有效率、不良反应发生率以及生存率。
结果:①对于治疗有效率,总治疗有效率为74.00%,其中完全缓解有57例,占比57.00%,不问缓解有17例,占比17.00%。
②在不良反应发生率方面,总不良反应发生率为57.00%,胃肠道不适发生率为40.00%,心电图异常发生率为50.00%,肝损害发生率为31.00%。
③在生存率方面,对选取的患者进行随访发现,一年、两年、三年生存率分别为85.00%(85/100)、75.00%(75/100)、55.00%(55/100)。
结论:对于患有淋巴瘤的患者,使用脂质体多柔比星进行治疗,会加大治疗的疗效,延缓病情的发展,提升患者的生存率,值得临床推广及应用。
【关键词】淋巴瘤;脂质体多柔比星;安全性分析淋巴瘤是起源于淋巴造血系统的恶性肿瘤,主要表现为无痛性淋巴结肿大,肝脾肿大,全身各组织器官均可受累,伴发热、盗汗、消瘦、瘙痒等全身症状,根据瘤细胞分为非霍奇金淋巴瘤(NHL)和霍奇金淋巴瘤(HL)两类【1】,这两类淋巴瘤对患者的免疫系统均会造成非常严重的影响,随着病情的不断恶化,肿瘤在向周边扩散转移,会对患者的生命安全造成及其严重的危害【2】。
因此很多医学科研工作者一直致力于淋巴瘤的研究中,希望可以通过合理的手段延缓患者病情的发展,提高患者的生存几率。
多柔比星能成功地诱导多种恶性肿瘤的缓解,包括急性白血病、淋巴瘤、软组织和骨肉瘤、儿童恶性肿瘤及成人实体瘤,尤其用于乳腺癌和肺癌。
此次研究对道中道(菏泽)制药有限公司的100名淋巴瘤患者进行研究治疗,分析观察在治疗过程中,使用脂质体多柔比星进行治疗的临床疗效,现将具体情况报道如下:1资料与方法1.1一般资料选取2019年10月~2021年2月间收治的接受治疗的淋巴瘤患者共100例为研究对象,所有患者均经过严格的检查和诊断,并符合相关诊断标准。
柔红霉素发酵液的高效液相色谱分析

Z - 制备液相色谱仪经性能测试和 B2型
cr a g p wt m lp ho t r h i m oa h uil te
和长期使用,其性能稳定,适应 性范 围广 泛,效率较高,是一种多功能的制备型液相 色谱仪,适合天然产物中的复杂组分以及合
成产物主副产物的制备分离。
柔红霉素发酵液的高效液相色谱分析
素盐酸盐 6毫克 ( 内含柔红霉素 1 毫克)于
1毫升容量瓶内,加水稀释至刻度。冷藏待 0
用。
3 .发酵液的萃取 ( ) 酸化前发酵液的萃取 取发酵 液 1 2 毫升,加 N O 溶液调节 p aH H至8 8 , ~. 5 加1 毫升正丁醇,超声波处理 1 分钟,离 0
心, 吸取上层正丁醇溶液注射 入柱中 作高效
( 三) 色谱操作条件
部
分
色谱柱:0 6 . 厘米 ( 2 内径) 2厘米不 5 锈钢柱,装填G T 1填料。 Y -C8 流动相:甲醇-0 1 . M醋 酸铵 水 溶液 0
(H . = 53 体积 体积) P 4) 6 5( / 2
流速: 1 毫升/ 分 检测波长:20 3毫微米,0 6 us .A f 1
Z o - eg ag iW a ,i h gs n,h n h-en nW n h Ga g 荻
t n n nW W -yn, ng i ,a g , a i ig u W
Is tt o Maei Mei ,h n e aey nt ue i t a dc i s c dm r a e
黄平芬 张同珍
( 上海医药工业研究院)
〔 提要〕 本文介绍柔红霉素和其同类物质以及它们的甙元的高效液相色谱法。色谱分离在C8 1 烷基键合硅胶柱上以甲醇-00M醋酸铵水溶液 (H42 为流动相,流出液用紫外检测器检测波 .1 p .)
盐酸表柔比星功能介绍
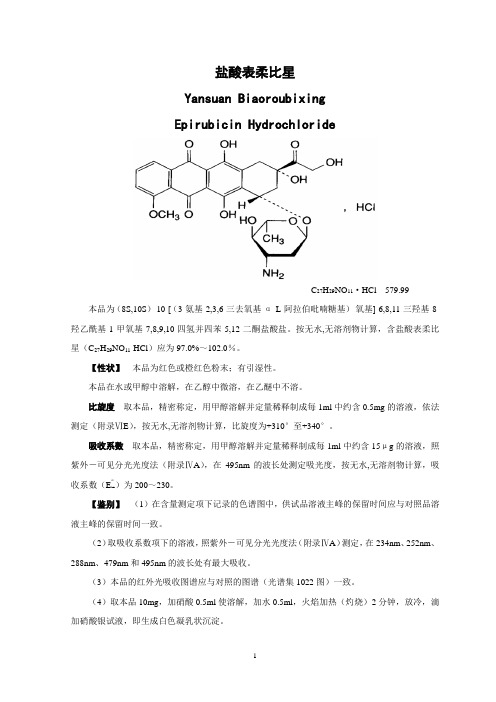
盐酸表柔比星Yansuan BiaoroubixingEpirubicin HydrochlorideC27H29NO11·HCl 579.99 本品为(8S,10S)-10-[(3-氨基-2,3,6-三去氧基-α-L-阿拉伯吡喃糖基)-氧基]-6,8,11-三羟基-8-羟乙酰基-1-甲氧基-7,8,9,10-四氢并四苯-5,12-二酮盐酸盐。
按无水,无溶剂物计算,含盐酸表柔比星(C27H29NO11·HCl)应为97.0%~102.0%。
【性状】本品为红色或橙红色粉末;有引湿性。
本品在水或甲醇中溶解,在乙醇中微溶,在乙醚中不溶。
比旋度取本品,精密称定,用甲醇溶解并定量稀释制成每1ml中约含0.5mg的溶液,依法测定(附录ⅥE),按无水,无溶剂物计算,比旋度为+310°至+340°。
吸收系数取本品,精密称定,用甲醇溶解并定量稀释制成每1ml中约含15μg的溶液,照紫外-可见分光光度法(附录ⅣA),在495nm的波长处测定吸光度,按无水,无溶剂物计算,吸收系数(E1%1cm)为200~230。
【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)取吸收系数项下的溶液,照紫外-可见分光光度法(附录ⅣA)测定,在234nm、252nm、288nm、479nm和495nm的波长处有最大吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集1022图)一致。
(4)取本品10mg,加硝酸0.5ml使溶解,加水0.5ml,火焰加热(灼烧)2分钟,放冷,滴加硝酸银试液,即生成白色凝乳状沉淀。
【检查】酸度取本品,加水制成每1ml中含5mg的溶液,依法测定(附录VI H),pH 值应为4.0~5.5。
溶液的澄清度取本品5份,各10mg,分别加水5ml溶解后,溶液应澄清;如显浑浊,与1号浊度标准液(附录ⅨB)比较,均不得更浓。
同一色谱条件测定柔红霉素、盐酸多柔比星和盐酸表柔比星

1 1 0 0 型高 效液相 色谱 仪包 括包 括G 2 1 7 0 A A型P c 化学工 作站 、 G 1 3 1 I A型四 元梯 度 泵 、 G1 3 1 4 A 型 可 变紫 外检 测 器 ( 美 国Ag i l e n t 公司 ) ; AL C - 1 1 0 0 . 4 精 密 天平( S a r f o r i u s  ̄司) , K Q 2 5 0 D B 型数 控超 声波 清洗 器 ( 昆山超声 仪器 厂 ) 。 柔红 霉素 ( 柔 红霉 素标 准 品 , 中国药 品生 物制 品检 定所 , 批号 : 1 3 0 5 5 9 2 0 0 5 0 1 ) , 盐酸 多柔 比星 ( S i g ma 公司, 批号 : 0 3 8 K1 3 4 9 ) , 注射 用 盐酸表 柔 比星( 盐酸表 柔 比星 样品, 浙 江海正 药 业股份 有 限公司 , 批号 : O 9 O 8 0 3 ) ; 甲醇 、 乙腈为 色谱级 , 水 为重 蒸馏 水 , 其 它试 剂均 为分 析 纯 。 2方法 与 结果 2 . 1色谱 条件 : 色谱 柱 : Ag i l e m HC - C1 8( 2 5 0 mm x4 . 6 m m , 5 m) ; 柱 温: 3 0 " C; 流速: 1 . 0 mL ・ I n 一1 ; 流 动相 : 十二 烷基 硫酸 钠溶 液 ( 1 . 4 4 g + 0 . 6 8 mL H3 P O 4 +H2 0+ 5 0 0 mL,用磷 酸 调p H2 . 2 ) 一乙腈 一甲醇 ( 5 0 0 : 5 0 0 : 6 0 ) , 检测 波长2 5 4 n m; 进样体 积2 Ou L 。 结果 , 在 此条件 下柔 红霉素 与盐 酸多柔 比 星、 盐酸 表柔 比星色谱 峰 可基 线分 离 , 柔 红霉 素保 留时 间1 9 . 7 mi n, 盐 酸 多柔 比 星保 留 时 间1 0 . 9 mi n , 盐酸表 柔 比星保 留时 间 1 2 . 4 mi n 。 该条 件 的建 立为 盐酸 多柔 比星 类化 合物 进行 定性 分 析奠 定 了基 础。 2 . 2样 品溶 液 的制备 : 称 取柔 红霉 素 、 盐酸 多柔 比星和 盐酸 表柔 比 星样品
盐酸多柔比星脂质体注射液化疗后出现皮肤黏膜炎症及神经毒性的1

盐酸多柔比星脂质体注射液化疗后出现皮肤黏膜炎症及神经毒性的1例卵巢癌患者的中西医护理发表时间:2016-04-21T15:17:48.927Z 来源:《中西医结合护理》2015年11月第11期作者:江玲霞[导读] 浙江省中医院盐酸多柔比星脂质体注射液是盐酸多柔比星的脂质体制剂.浙江省中医院浙江杭州 310006[中图分类号] R246.7 [文献标识码] A [文章编号]1672-5018(2015)11-51-01盐酸多柔比星脂质体注射液是盐酸多柔比星的脂质体制剂,该剂型克服了游离的阿霉素药物心脏毒性大的缺陷,脱发、呕吐等毒性反应明显减少,常用于乳腺癌、卵巢癌和多发性骨髓瘤等恶性肿瘤一线化疗药。
其最常见的不良反应为骨髓抑制(药物说明书上指出发生率50%),其他少见的不良反应(发生率<5%)有手掌-足底红斑性感觉迟钝、恶心呕吐、口腔溃疡等。
我科2014年收治1例盐酸多柔比星脂质体注射液化疗后出现皮肤黏膜炎症及神经毒性症状的卵巢癌患者,经积极治疗和中西医对症护理,患者最终痊愈出院,现将护理体会报道如下:1 病例资料患者,女性,63岁,前期肿瘤诊疗于浙江省肿瘤医院进行,2013年5月因腹胀行CT检查和腹水穿刺诊断为卵巢癌。
从2013年6月6日开始于艾素+顺铂方案化疗1次,艾素+卡铂方案化疗4次。
2013年11月5日于浙江省肿瘤医院行全麻下经腹子宫全切+双附件切除+选择性盆腔淋巴结切除+大网膜切除+肠粘连松解术,术后病理示:左卵巢中分化子宫内膜样腺癌伴坏死。
术后予艾素+卡铂方案化疗4次。
化疗后出现肝损,黄疸,CT检查示:肝脾占位性病变,考虑转移性肿瘤可能,肝脏病灶较前增大。
2014年9月17日,2014年10月10日予盐酸多柔比星脂质体注射液化疗,21天后出现“Ⅲ度口腔溃疡,四肢指端麻木伴有轻度运动障碍属Ⅲ度神经毒性,手指指腹、脚趾指腹、四肢指缝、腋下、大腿内侧多发水泡”,于2014年10月31日入住我院治疗。
柔红霉素、盐酸多柔比星和盐酸表柔比星的HPLC分析

【摘要】 目的:建立柔红霉素、盐酸多柔比星和盐酸表柔比星的高效液相色谱分析方法。方法:色谱柱为Agilent HC-C18(250 mm×4.6 mm ,5 m);柱温为30 oC;流速为1.0 mL·min-1;流动相为十二烷基硫酸钠溶液-乙腈-甲醇(500∶500∶60,用磷酸调pH 2.2);检测波长为 254 nm。结果:柔红霉素保留时间19.7 min,盐酸多柔比星保留时间10.9 min,盐酸表柔比星保留时间12.4 min;三种化合物进样量在0.1 2 g范围内与峰面积积分值呈良好线性关系;平均回收率为98.4 %~99.0 %,RSD为0.45 %(n=5);结论:本方法灵敏度高、准确,可以对 盐酸多柔比星类化合物进行定性定量分析。
表2 加样回收率试验结果(n=5) 3 讨论 目前,采用HPLC 法分别测定柔红霉素、盐酸多柔比星和盐酸表柔比星文献报道较多,但采用同一个色谱条件来测定这3 种化合物未见 报道。本试验发现:Agilent HC-C18柱,柱温30 oC,流速1.0mL·min -1 ,流动相SDS-乙腈-甲醇(500∶500∶60,用磷酸调pH2.2), 检测波长254 nm,3 种化合物分离效果很好。初步分析原因在于三种化合物的结构差异性:盐酸多柔比星比柔红霉素C-14位多了一个羟 基,加大了盐酸多柔比星的极性,其保留时间要早于柔红霉素;盐酸表柔比星是盐酸多柔比星结构的异构化,保留时间肯定与盐酸多柔比 星不一致。同时用磷酸调pH2.2使呈弱酸性能够提高柱效及分离度。本方法准确、灵敏度高、重现性好、可用于盐酸多柔比星类化合物的定 性定量分析,盐酸多柔比星制剂的质量控制。 参考文献 [1] Hutchinson CR. Biosynthetic Studies of Daunorubicin and Tetracenomycin C[J]. Chem Rev,1997,97(7):2525~36 [2] Gallo MA, Ward J, Hutchinson CR. The dnrM gene in Streptomyces peucetius contains a naturally occurring frameshift mutation that is suppressed by another locus outside of the daunorubicin-production gene cluster[J]. Microbiology, 1996,142 ( Pt 2):269~75 [3] 胡友佳,朱春宝,朱宝泉.代谢工程研究及其在柔红霉素产生菌中的应用[J].中国医药工业杂志,2007,38(3):164~169 [4] Madduri K, Kennedy J, Rivola G, et al. Production of the antitumor drug epirubicin (4'-epidoxorubicin) and its precursor by a genetically engineered strain of Streptomyces peucetius[J]. Nat Biotechnol,1998,16(1):69~74 [5] 国家药典委员会编. 中华人民共和国药典(一部)[S].2005年版.北京:化学工业出版社,2005:505~505,557~558 作者单位:210009 东南大学附属中大医院 1 210046 南京师范大学生命科学学院 2
盐酸多柔比星脂质体注射液仿制药研究技术指导原则(征求意见稿)

盐酸多柔比星脂质体注射液仿制药1研究技术指导原则2(征求意见稿)34一、概述5盐酸多柔比星脂质体注射液是采用硫酸铵梯度法将盐6酸多柔比星包裹于PEG化脂质体内形成的特殊注射剂。
7本指导原则结合盐酸多柔比星脂质体注射液的制剂特8点,提出仿制药开发过程中药学研究、非临床研究和生物等9效性研究的技术要求,旨在为该仿制药的研发提供技术指导。
10本指导原则仅代表药品监管部门目前对于本品的观点11和认识。
在符合现行法规的要求下,可采用替代的研究方法,12建议提供详细的研究资料或与监管机构进行沟通。
13二、整体研究思路14作为仿制药,应当按照国家局发布的《化学仿制药参比15制剂遴选与确定程序》选择参比制剂。
16盐酸多柔比星脂质体注射液为经静脉注射给药的脂质17体制剂,应基于产品特征,采取逐步递进的对比研究策略,18首先进行仿制药与参比制剂药学和非临床的全面对比研究;19然后进行人体生物等效性研究;必要时进行临床研究。
若药20学研究和(或)非临床研究结果提示仿制药与参比制剂不一21致,建议优化后重新开展研究1。
22作为注射剂仿制药,除满足仿制药注册申报的要求外,23还应符合《化学药品注射剂仿制药质量和疗效一致性评价技24术要求》、《化学药品注射剂仿制药(特殊注射剂)质量和25疗效一致性评价技术要求》等。
26三、技术要求27(一)药学研究281、处方29仿制药的处方应与参比制剂一致,辅料种类和用量通常30应与参比制剂相同2。
31氢化大豆磷脂酰胆碱(HSPC)、胆固醇、甲氧基聚乙二32醇磷脂酰乙醇胺(MPEG-DSPE)是本品的关键成分,应按33相关要求进行登记和关联,或由制剂注册申请人一并提供研34究资料3。
仿制药应与参比制剂选择相同来源(天然的或合35成的)的脂质辅料,制定严格的内控标准,并提供研究资料36证明仿制药所采用的脂质辅料与参比制剂中的脂质辅料相37似(如,各组分比例)。
382、制备工艺39应采用硫酸铵梯度法制备,主要步骤包括:1)空白脂质40体的制备,2)硫酸铵梯度的形成,3)活性药物的装载。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【Abstract】 Objective: To establish a HPLC method for the analysis of Daunorubicin, Doxorubicin and Epirubicin. METHODS: The determination was performed by HPLC using Agilent HC-C18 column (250 mm x4.6 mm ,5 m) with the column temperature maintained at 30 oC. The mobile phase consisted of SDS-acetonitrile-methanol (500∶500∶60, ajust pH 2.2 with H3PO4)at a flow rate of 1.0 mL·min-1 and a UV detection wavelength of 254 nm. RESULTS: The Daunorubicin retention time is 19.7 min ,the Doxorubicin retention time is 10.9 min ,the Epirubicin retention time is 12.4 min; The linear range of the three compounds were 0.1 2 g,and the average recoveries of all stood at 98.4 %~99.0 % and RSD at 0.45 %( n = 5 each); CONCLUSION: This method is sensitive, accurate, and it can be used for the qualitative and quantitative analysis of Daunorubicin, Doxorubicin and Epirubicin.
【Key words】 Daunorubicin; Doxorubicin; Epirubicin; HPLC 【中图分类号】 R414 【文献标识码】 A 【文章编号】1005-0515(2011)01-0025-02
柔红霉素和盐酸多柔比星为蒽环类抗生素[1],盐酸多柔比星是柔红霉素的C-14位的羟化产物[2],盐酸多柔比星氨基糖部分4'位异构化得 到活性相当、但毒性减少的盐酸表柔比星[3],是联合国世界卫生组织推荐的治疗肿瘤化疗的基本药物,在国际和国内市场同类药物中占有 较大的份额。目前盐酸多柔比星类化合物主要是通过化学半合成法[4],问题是化学合成目标产物时可能含有其他的组份,质量控制需要各 组份精确分析,因此定性和定量分析就很重要。2005版药典中有介绍盐酸多柔比星类化合物的分析方法,但没有柔红霉素、盐酸多柔比星 和盐酸表柔比星三种化合物的分析方法,故参照有关文献[5],以高效液相色谱法建立盐酸多柔比星类化合物的分析方法。
【摘要】 目的:建立柔红霉素、盐酸多柔比星和盐酸表柔比星的高效液相色谱分析方法。方法:色谱柱为Agilent HC-C18(250 mm×4.6 mm ,5 m);柱温为30 oC;流速为1.0 mL·min-1;流动相为十二烷基硫酸钠溶液-乙腈-甲醇(500∶500∶60,用磷酸调pH 2.2);检测波长为 254 nm。结果:柔红霉素保留时间19.7 min,盐酸多柔比星保留时间10.9 min,盐酸表柔比星保留时间12.4 min;三种化合物进样量在0.1 2 g范围内与峰面积积分值呈良好线性关系;平均回收率为98.4 %~99.0 %,RSD为0.45 %(n=5);结论:本方法灵敏度高、准确,可以对 盐酸多柔比星类化合物进行定性定量分析。
1 材料 1100型高效液相色谱仪包括包括G2170AA型PC化学工作站、G1311A型四元梯度泵、G1314A型可变紫外检测器(美国Agilent公司); ALC-1100.4精密天平(Sarforius公司);KQ250DB型数控超声波清洗器(昆山超声仪器厂)。柔红霉素(柔红霉素标准品,中国药品生 物制品检定所,批号:130559~200501),盐酸多柔比星(Sigma公司,批号:038K1349),注射用盐酸表柔比星(盐酸表柔比星样品, 浙江海正药业股份有限公司,批号:090803);甲醇、乙腈为色谱级,水为重蒸馏水,其它试剂均为分析纯。 2 方法与结果 2.1 色谱条件:色谱柱:Agilent HC-C18 (250 mm×4.6 mm ,5μm);柱温:30 oC;流速:1.0 mL·min -1 流动相:十二烷基硫酸钠溶 液(1.44 g+0.68 mL H 3PO 4+H 2O+500mL, 用磷酸调pH 2.2)-乙腈-甲醇(500∶500∶60),检测波长254 nm;进样体积20μL。结果,在 此条件下柔红霉素与盐酸多柔比星、盐酸表柔比星色谱峰可基线分离,柔红霉素保留时间19.7 min,盐酸多柔比星保留时间10.9 min,盐酸 表柔比星保留时间12.4 min。该条件的建立为盐酸多柔比星类化合物进行定性分析奠定了基础(色谱见图1)。 2.2 样品溶液的制备:称取柔红霉素、盐酸多柔比星和盐酸表柔比星样品各1 mg,用水溶解配置各自储存液1 mg·mL -1 即1μg·μL -1。
柔红霉素、盐酸多柔比星和盐酸表柔比星的HPLC分析
发表时间:2011-06-03T17:07:26.780Z 来源:《中国健康月刊》20112 [导读] 目的:建立柔红霉素、盐酸多柔比星和盐酸表柔比星的高效液相色谱分析方法。 石 涛1 陈莎莎2 朱宇鹏2 尚广东2 国家重大新药创制 科研项目(No. 2009ZX09503-005)。 江苏省卫生厅医学科技发展基金 项目编号p200801
