注射用盐酸表柔比星新选.
盐酸多柔比星脂质体注射液 质量标准

盐酸多柔比星脂质体注射液质量标准盐酸多柔比星脂质体注射液,是一种用于治疗癌症的药物。
其主要成分是盐酸多柔比星,以及一种称为脂质体的药物传递系统。
在本文中,我们将详细介绍盐酸多柔比星脂质体注射液的质量标准。
1.外观:盐酸多柔比星脂质体注射液应该是无颗粒、无悬浮物和无杂质的透明液体。
其中,脂质体应该是均匀分散在溶液中,并且具有均一的颗粒大小和形状。
2. pH值:盐酸多柔比星脂质体注射液的pH值应该在4.0-7.0之间。
pH值的范围对于药物的稳定性和生物利用度非常重要,过高或过低的pH值可能会影响药物的疗效。
3.盐酸多柔比星含量:盐酸多柔比星脂质体注射液的盐酸多柔比星含量应符合国家药典或企业自行制定的规定。
这是确保该药物在治疗癌症方面提供有效结果的重要指标。
4.脂质体粒径:盐酸多柔比星脂质体注射液中的脂质体应具有一定的粒径范围。
这是由于脂质体的大小会影响其在体内的分布和吸收情况。
通常来说,脂质体粒径应在100-200纳米之间。
5.无菌性:盐酸多柔比星脂质体注射液必须符合无菌性的要求。
这意味着在制造和包装过程中,要严格控制微生物的污染。
如果存在细菌、霉菌或其他致病微生物的污染,可能对患者的健康产生严重影响。
6.稳定性:盐酸多柔比星脂质体注射液在储存和运输过程中应该具有良好的稳定性。
药物的稳定性包括其在不同温度、光照和湿度条件下的物化特性和有效性。
针对盐酸多柔比星脂质体注射液,一般要求其在室温下储存,并且在有效期内保持其活性。
7.溶解度:盐酸多柔比星脂质体注射液的溶解性是十分重要的。
治疗的有效性与药物的溶解度密切相关。
因此,盐酸多柔比星脂质体注射液的溶解性应符合一定的标准,以确保在用药过程中能够得到良好的溶解。
综上所述,盐酸多柔比星脂质体注射液的质量标准涉及到外观、pH值、盐酸多柔比星含量、脂质体粒径、无菌性、稳定性以及溶解度等方面。
只有在这些方面都能达到标准,药物才能发挥其治疗癌症的作用。
不过需要注意的是,具体的质量标准可能因国家药典、公司标准或医疗监管要求而有所不同。
表柔比星注射液

盐酸表柔比星注射液目录编辑本段产品介绍【批准文号】国药准字H20041211【中文名称】盐酸表柔比星注射液【产品英文名称】Epirubicin Hydrochloride for Injection 【生产企业】浙江海正药业股份有限公司【功效主治】用于治疗白血症恶性淋巴瘤多发性骨髓瘤乳腺癌肺癌软组织肉瘤胃癌结肠直肠癌卵巢癌等【化学成分】盐酸表柔比星编辑本段药理作用4位置上的羟基由顺位变为反位为一细胞周期非特异性药物其主要作用部位是细胞核本品的作用机制与其能与DNA结合有关体外培养的细胞加入本品可迅速透入胞内进入细胞核与DNA结合从而抑制核酸的合成和有丝分裂已证实表柔比星具有广谱的抗实验性肿瘤的作用对拓扑异构酶也有抑制作用疗效与阿霉素相等或略高而毒性尤其是心脏毒性低于阿霉素【药物相互作用】1表柔比星可与其他抗肿瘤药物合用但表柔比星用量应减低联合用药时不得在同一注射器内使用2表柔比星不可与肝素混合注射因为二者化学性质不配伍在一定浓度时会发生沉淀反应编辑本段不良反应1与阿霉素相似但程度较低尤其是心脏毒性和骨髓换制毒性;2其他不良反应有:脱发60~90%的病例可发生一般可逆男性有胡须生长受抑;黏膜炎用药的第5~10天出现能常发生在舌侧及舌下粘膜;胃肠功能紊乱如恶心呕吐腹泻;曾有报道偶有发热寒颤荨麻疹色素沉着关节疼痛【禁忌症】1禁用于因用化疗或放疗而造成明显骨髓抑制的病人2已用过大剂量蒽环类药物(如阿霉素或柔红霉素)的病人3近期或既往有心脏受损病史的病人【产品规格】5ml:10mg【用法用量】表柔比星单独用药时成人剂量为按体表面积一次60~90mg/m2联合化疗时每次50~60mg/m2静脉注射根据病人血象可间隔21天重复使用【贮藏方法】遮光,密封保存。
编辑本段注意事项1关于心脏毒性(1)可导致心肌损伤,心力衰竭。
动物实验和短期人体实验表明,表柔比星的心脏霉性比异构体阿霉素小。
比较研究表明,表柔比星和阿霉素引起相同程度心功能减退的蓄积剂量之比为2:1。
注射用盐酸多柔比星说明书

注射用盐酸多柔比星说明书【药品名称】通用名:注射用盐酸多柔比星英文名:Doxorubicin Hydrochloride for Injection汉语拼音:Zhusheyong Yansuan Duoroubixing【成份】本品主要成分为盐酸阿霉素化学名称为:10-[(3-氨基-2,3,6-三去氧-a-L-来苏己吡喃基)-氧]-7,8,9,10-四氢-6,8,11-三羟基-8-(羟乙酰基)-1-甲氧基-5,12-萘二酮的盐酸盐。
其结构式为:分子式:C27H29NO11·HCl分子量:Cas No:25316-40-9辅料:乳糖、氢氧化物【性状】本品为橙红色疏松块状物或粉末。
【适应症】适用于急性白血病(淋巴细胞性和粒细胞性)、恶性淋巴瘤、乳腺癌、肺癌(小细胞和非小细胞肺癌)、卵巢癌、骨及软组织肉瘤、肾母细胞瘤、神经母细胞瘤、膀胱癌、甲状腺癌、前列腺癌、头颈部鳞癌、睾丸癌、胃癌、肝癌等。
【规格】按C27H29NO11·HCl 计算10mg【用法用量】静脉冲入、静脉滴注或动脉注射。
临用前加灭菌注射用水溶解,浓度为2mg/ml。
(1)成人常用量单药为50~ 60mg/m2,每3~ 4周1次或每日20mg/m2,连用3日,停用2~ 3周后重复。
联合用药为40mg/m2,每3周1次或25mg/m2,每周1次,连用2周,3周重复。
总剂量按体重面积不宜超过400mg/m2。
分次用药的心肌毒性、骨髓抑制和胃肠道反应(包括口腔溃疡)较每3周用药一次为轻。
(2)联合化疗①ABVD(阿霉素、博来霉素、长春新碱和达卡巴嗪),主要用于霍奇金淋巴瘤;②CAF(环磷酰胺、阿霉素和氟尿嘧啶),主要用于乳腺癌;③CHOP(环磷酰胺、阿霉素、长春新碱和泼尼松),主要用于非霍奇金淋巴瘤;④FAM(氟尿嘧啶,阿霉素和丝裂霉素),主要用于胃癌;⑤AC(阿霉素和阿糖胞苷),主要用于成人急性髓细胞性白血病;⑥AOP(阿霉素、长春新碱和泼尼松),主要用于淋巴母细胞型急性白血病的诱导缓解;⑦ACP(阿霉素、环磷酰胺和顺铂),主要用于卵巢癌和肺癌以及头颈部癌、膀胱癌等;⑧COAD(环磷酰胺、长春新碱、阿霉素和达卡巴嗪),主要用于软组织肉瘤和成骨肉瘤;⑨CAO(环磷酰胺、阿霉素、长春新碱)主要用于小细胞肺癌。
盐酸表柔比星功能介绍
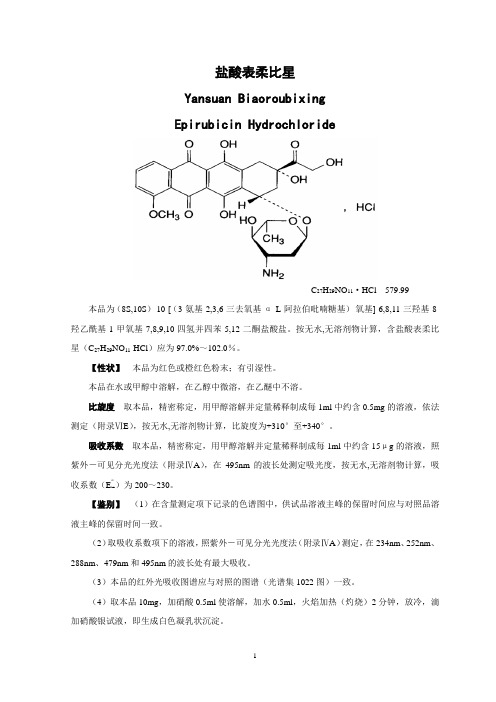
盐酸表柔比星Yansuan BiaoroubixingEpirubicin HydrochlorideC27H29NO11·HCl 579.99 本品为(8S,10S)-10-[(3-氨基-2,3,6-三去氧基-α-L-阿拉伯吡喃糖基)-氧基]-6,8,11-三羟基-8-羟乙酰基-1-甲氧基-7,8,9,10-四氢并四苯-5,12-二酮盐酸盐。
按无水,无溶剂物计算,含盐酸表柔比星(C27H29NO11·HCl)应为97.0%~102.0%。
【性状】本品为红色或橙红色粉末;有引湿性。
本品在水或甲醇中溶解,在乙醇中微溶,在乙醚中不溶。
比旋度取本品,精密称定,用甲醇溶解并定量稀释制成每1ml中约含0.5mg的溶液,依法测定(附录ⅥE),按无水,无溶剂物计算,比旋度为+310°至+340°。
吸收系数取本品,精密称定,用甲醇溶解并定量稀释制成每1ml中约含15μg的溶液,照紫外-可见分光光度法(附录ⅣA),在495nm的波长处测定吸光度,按无水,无溶剂物计算,吸收系数(E1%1cm)为200~230。
【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)取吸收系数项下的溶液,照紫外-可见分光光度法(附录ⅣA)测定,在234nm、252nm、288nm、479nm和495nm的波长处有最大吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集1022图)一致。
(4)取本品10mg,加硝酸0.5ml使溶解,加水0.5ml,火焰加热(灼烧)2分钟,放冷,滴加硝酸银试液,即生成白色凝乳状沉淀。
【检查】酸度取本品,加水制成每1ml中含5mg的溶液,依法测定(附录VI H),pH 值应为4.0~5.5。
溶液的澄清度取本品5份,各10mg,分别加水5ml溶解后,溶液应澄清;如显浑浊,与1号浊度标准液(附录ⅨB)比较,均不得更浓。
注射用盐酸表柔比星说明书

注射用盐酸表柔比星说明书注射用盐酸表柔比星说明书一、商品名称注射用盐酸表柔比星二、药品分类处方药三、药品成分每1毫升含盐酸表柔比星2毫克四、适应症此药适用于治疗以下感染疾病:1. 呼吸道感染,如急性喉炎、急性支气管炎等。
2. 皮肤和软组织感染,如表浅性脓肿、痈、蜂窝织炎等。
3. 泌尿道感染,如肾盂肾炎、尿道炎等。
4. 消化道感染,如胃肠炎、胆囊炎等。
5. 骨骼系统感染,如骨髓炎,化脓性关节炎等。
五、用法用量该药应由医生按病情和患者体重等因素决定用药剂量和疗程,不宜自行调整。
1. 成人和12岁以上儿童:每次0.25毫克/千克,一日2次给药。
2. 特殊人群:(1)肝功能不全患者:应减小剂量或增加给药间隔时间。
(2)肾功能不全患者:根据肾功能状况,调整用药剂量和给药间隔时间,严重肾功能不全应禁用。
(3)老年患者:应注意肾功能变化,酌情调整剂量和给药间隔时间。
(4)儿童患者:剂量应按体重计算,给予成人剂量的半数。
六、注意事项1. 禁忌症:对本药过敏、严重肝功能不全和婴儿期患嗜血细胞减少症等禁用。
2. 孕妇和哺乳期妇女应慎用。
3. 本药物可能出现过敏、肝损伤、肾损伤、血液系统不良等不良反应,如出现不适应立即停药并就医。
4. 在药物使用期间应避免饮酒、吸烟等影响药效的行为。
5. 长期应用本药可能导致细菌耐药性增加,应尽可能遵医嘱使用。
七、药物相互作用1. 与苯扎氯铵合用可增加中枢神经系统毒性。
2. 与卡马西平合用可增强前者的抗高血压作用。
3. 与华法林、保泰松等药物合用可增加出血风险。
八、贮藏方法本药品需存放于干燥,阴凉和避光的环境内,离达到最佳效果的安瓿打开时间不超过24小时。
避免冷藏,不得使用色素变化、浑浊、有颗粒物的溶液。
九、过期时间该药品保质期为2年。
十、包装规格每瓶装2毫升,每盒12瓶。
注射用盐酸表柔比星

注射用盐酸表柔比星ZhusheyongYansuan BiaoroubixingEpirubicinHydrochloride forInjection本品为盐酸表柔比星加适宜赋形剂或/和抑菌剂制成的无菌冻干品。
盐酸表柔比星(CH29NO11·HCl)平均含量应为标示量的90.0%~110.0%。
27【性状】本品为红色或橙红色疏松块状物或粉末;有引湿性。
【鉴别】取本品适量,照盐酸表柔比星项下的鉴别(1)、(4)项试验,显相同的结果。
【检查】酸度取本品适量,加水制成每1ml中含盐酸表柔比星2mg的溶液,依法测定(附录VI H),pH值应为4.5~6.0。
溶液的澄清度取本品5瓶,分别加水制成每1ml中含盐酸表柔比星2mg的溶液,溶液应澄清;如显浑浊,与1号浊度标准液(附录ⅨB)比较,均不得更浓。
有关物质取本品,用含量测定项下的流动相制成每1ml中约含盐酸表柔比星0.5mg 的溶液;作为供试品溶液,精密量取适量,用流动相定量稀释制成每1ml中含盐酸表柔比星5μg的溶液,作为对照溶液,照盐酸表柔比星项下的方法测定。
供试品溶液色谱图中如有杂质峰[如本品含有抑菌剂对羟基苯甲酸甲酯(相对保留时间约0.2)应除外],多柔比星酮按校正后的峰面积计算(相对保留时间约0.3,校正因子0.7)不得大于对照溶液主峰面积(1.0%),多柔比星(相对保留时间约0.8)峰面积不得大于对照溶液主峰面积(1.0%),其他单个杂质峰面积不得大于对照溶液主峰面积的4/5(0.8%),各杂质峰面积(多柔比星酮按校正后的峰面积计算)的和不得大于对照溶液主峰面积的2.5倍(2.5%)。
对羟基苯甲酸甲酯取含量测定项下供试品溶液作为供试品溶液,取对羟基苯甲酸甲酯对照品适量,用含量测定项下的流动相定量溶解并稀释制成每1ml中约含20μg的溶液,作为对照品溶液;照含量测定项下的方法测定,按外标法以峰面积计算,含对羟基苯甲酸甲酯应为标示量的80.0%~120.0%(10mg规格每瓶含对羟基苯甲酸甲酯2mg;50mg规格每瓶含对羟基苯甲酸甲酯10mg)。
注射用盐酸表柔比星说明书--法玛新

注射用盐酸表柔比星说明书【药品名称】通用名称: 注射用盐酸表柔比星(速溶)商品名称:法玛新®英文名称: Epirubicin Hydrochloride for Injection (Rapid Dissolution)汉语拼音: Zhusheyong Yansuan Biaoroubixing(Surong)【成份】化学名称:(7S:9S)-9-羟乙酰基-4-甲氧基-7,8,9,10-四氢-6,7,9,11-四羟基-7-O-(2,3,6-三去氧-3-氨基-α-L-阿拉伯吡喃糖基)-5,12-萘二酮盐酸盐化学结构式:分子式:C27H29NO11⋅ HCl分子量:579.98CAS No.:56390-09-1辅料名称:乳糖、对羟基苯甲酸甲酯【性状】本品为鲜红色或橙红色的疏松块状物,有引湿性。
【适应症】治疗恶性淋巴瘤、乳腺癌、肺癌、软组织肉瘤、食道癌、胃癌、肝癌、胰腺癌、黑色素瘤、结肠直肠癌、卵巢癌、多发性骨髓瘤、白血病。
膀胱内给药有助于浅表性膀胱癌、原位癌的治疗和预防其经尿道切除术后的复发。
【规格】10mg【用法用量】常规剂量:表柔比星单独用药时,成人剂量为按体表面积一次60~120mg/m2,当表柔比星用来辅助治疗腋下淋巴阳性的乳腺癌患者联合化疗时,推荐的起始剂量为100~120mg/m2静脉注射,每个疗程的总起始剂量可以一次单独给药或者连续2-3天分次给药。
根据患者血象可间隔21天重复使用。
优化剂量:高剂量可用于治疗肺癌和乳腺癌。
单独用药时,成人推荐起始剂量为按体表面积一次最高可达135mg/m2,在每疗程的第1天一次给药或在每疗程的第1、2、3天分次给药,3-4周一次。
联合化疗时,推荐起始剂量按体表面积最高可达120mg/m2,在每疗程的第1天给药,3-4周一次。
静脉注射给药。
根据患者血象可间隔21天重复使用。
膀胱内给药:表柔比星应用导管灌注并应在膀胱内保持一小时左右。
在灌注期间,患者应时常变换体位,以保证膀胱粘膜能最大面积地接触药物。
两种溶媒稀释注射用表柔比星用于肝动脉内化疗药灌注介入治疗的观察与分析

龙源期刊网 两种溶媒稀释注射用表柔比星用于肝动脉内化疗药灌注介入治疗的观察与分析作者:孟令爽来源:《健康必读(上旬刊)》2019年第08期【摘 ;要】目的:通过对比两种溶媒在稀释注射用表柔比星用于肝动脉内化疗药灌注介入治疗动脉注射过程中,通过观察药物稀释效果、患者感受的疼痛程度,指导临床选择较为适宜的溶媒,提高医疗护理服务质量。
方法:对我科2017年全年介入手术中配制注射用盐酸表柔比星622组,采用分组对照办法,将2017年01月-2016年06月使用A组溶媒稀释(0.9%生理盐水)300组设定为对照组,2017年07月份-2017年12月份使用b组溶媒稀释(5%葡萄糖注射液)322组设定为试验组。
采用肉眼观察、口诉言词分级法(VRS)记录对药物稀释效果、患者的疼痛程度,数据进行统计学分析。
结果:2种溶媒稀释注射用表柔比星用于动脉内灌注介入治疗肌内注射过程中,药物稀释效果、患者感受的疼痛程度,有显著差异(P值结论:使用5%葡萄糖注射液做稀释注射用表柔比星用于动脉内灌注介入治疗,药物稀释效果显著,明显减轻患者注射的疼痛,提高患者的满意度。
【关键词】注射用表柔比星;动脉灌注;稀释效果;疼痛观察【中图分类号】R47;;;;;;【文献标识码】B; ;;;;【文章编号】1672-3783(2019)08-0276-01药品名称:通用名:注射用盐酸表柔吡星;商品名:法玛新;成份:1.化学名称为:(7S:9S)-9-羟乙酰基-4-甲氧基-7,8,9,10-四氢-6,7,9,11-四羟基-7-O-(2,3,6-三去氧-3-氨基α-L-阿拉伯吡喃糖基)-5,12-萘二酮盐酸盐;其结构式为:分子式:C27H29NO11·HCl;分子量:579.98;CASNo.:56390-09-1;2.辅料:乳糖、对羟基苯甲酸甲酯;性状:本品为鲜红色或橙红色疏松块状物;有引湿性。
规格:以C27H29NO11·HCl计10mg[1]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
注射用盐酸表柔比星
Zhusheyong Yansuan Biaoroubixing
Epirubicin Hydrochloride for Injection
本品为盐酸表柔比星加适宜赋形剂或/和抑菌剂制成的无菌冻干品。
盐酸表柔比星(C27H29NO11·HCl)平均含量应为标示量的90.0%~110.0%。
【性状】本品为红色或橙红色疏松块状物或粉末;有引湿性。
【鉴别】取本品适量,照盐酸表柔比星项下的鉴别(1)、(4)项试验,显相同的结果。
【检查】酸度取本品适量,加水制成每1ml中含盐酸表柔比星2mg的溶液,依法测定(附录VI H),pH值应为4.5~6.0。
溶液的澄清度取本品5瓶,分别加水制成每1ml中含盐酸表柔比星2mg的溶液,溶液应澄清;如显浑浊,与1号浊度标准液(附录ⅨB)比较,均不得更浓。
有关物质取本品,用含量测定项下的流动相制成每1ml中约含盐酸表柔比星0.5mg 的溶液;作为供试品溶液,精密量取适量,用流动相定量稀释制成每1ml中含盐酸表柔比星5μg的溶液,作为对照溶液,照盐酸表柔比星项下的方法测定。
供试品溶液色谱图中如有杂质峰[如本品含有抑菌剂对羟基苯甲酸甲酯(相对保留时间约0.2)应除外],多柔比星酮按校正后的峰面积计算(相对保留时间约0.3,校正因子0.7)不得大于对照溶液主峰面积(1.0%),多柔比星(相对保留时间约0.8)峰面积不得大于对照溶液主峰面积(1.0%),其他单个杂质峰面积不得大于对照溶液主峰面积的4/5(0.8%),各杂质峰面积(多柔比星酮按校正后的峰面积计算)的和不得大于对照溶液主峰面积的2.5倍(2.5%)。
对羟基苯甲酸甲酯取含量测定项下供试品溶液作为供试品溶液,取对羟基苯甲酸甲酯对照品适量,用含量测定项下的流动相定量溶解并稀释制成每1ml中约含20μg的溶液,作为对照品溶液;照含量测定项下的方法测定,按外标法以峰面积计算,含对羟基苯甲酸甲酯应为标示量的80.0%~120.0%(10mg规格每瓶含对羟基苯甲酸甲酯2mg;50mg规格每瓶含对羟基苯甲酸甲酯10mg)。
(含对羟基苯甲酸甲酯时)
水分取本品,照水分测定法(附录VIII M第一法A)测定,含水分不得过4.0%。
含量均匀度以含量测定项下测得的每瓶含量计算,应符合规定(附录X E)。
细菌内毒素取本品适量,依法检查(附录XI E),每1mg盐酸表柔比星中含内毒素的量应小于1.1EU。
降压物质取本品,依法检查(附录ⅪG),剂量按猫体重每1kg注射1mg(以盐酸表柔比星计),应符合规定。
无菌取本品,用0.9%无菌氯化钠溶液使溶解并稀释制成每1ml中含盐酸表柔比星0.4mg的溶液,用薄膜过滤法处理,冲洗液用量每膜不少于300ml,分次冲洗后,以金黄色葡萄球菌为阳性对照菌,依法检查(附录XI H),应符合规定。
其他应符合注射剂项下有关的各项规定(附录I B)。
【含量测定】取本品10瓶,分别加流动相定量制成每1ml中约含盐酸表柔比星0.1mg 的溶液,照盐酸表柔比星项下的方法测定,并求出10瓶的平均含量。
【类别】同盐酸表柔比星。
【规格】按C27H29NO11·HCl计(1)10mg (2)50mg。
【贮藏】遮光,密封,在阴凉处保存。
最新文件仅供参考已改成word文本。
方便更改。
