有机化学实验报告--2-甲基-2氯丙烷的制备
2-甲基-2-氯丙烷制备实验的改进

2-甲基-2-氯丙烷制备实验的改进发表时间:2020-01-08T15:24:47.627Z 来源:《科技新时代》2019年11期作者:王文辉马艳丽李佳倩袁晓刘艳敏李娟* [导读] 对2-甲基-2-氯丙烷的制备方法进行改进。
选择叔丁醇与浓盐酸不同的配比进行反应以寻求最高产率的合适配比;王文辉马艳丽李佳倩袁晓刘艳敏李娟* (河北师范大学汇华学院理学部河北石家庄 050091)摘要:对2-甲基-2-氯丙烷的制备方法进行改进。
选择叔丁醇与浓盐酸不同的配比进行反应以寻求最高产率的合适配比;制备方法中通过增加超声操作,磁力搅拌操作促进反应物充分混合,增加蒸馏操作促使反应平衡向右移动,使反应继续进行,以达到提高产率的目的。
最终选择叔丁醇与浓盐酸以物质的量1:10的比例,制备过程中先室温震荡10min,再超声震荡5min,而后进行蒸馏促进反应继续进行,最后获得59.2%的高产率。
关键词:2-甲基-2-氯丙烷的制备配比超声蒸馏 2-甲基-2-氯丙烷的制备是高校有机化学实验教材的内容之一。
该实验操作简单,旨在掌握由三级醇制备卤代烃的SN1亲核取代的反应原理以及蒸馏操作和分液漏斗的使用方法。
虽然该实验简单易行,但大部分同学获得的产率并不高,达不到教材上的高产率结果。
针对这种情况,现对制备方法进行改进以提高产率。
教材上的实验内容如下[1]:在100ml圆底烧瓶中,放置6.2g叔丁醇和21ml浓盐酸,不断振荡10~15min后,转入分液漏斗,静置,待明显分层后,分去水层。
有机层分别用水、5%碳酸氢钠溶液、水各5ml洗涤。
产品用无水氯化钙干燥后转入蒸馏烧瓶中蒸馏。
收集50~51℃馏分。
在实际操作过程中,同学们获得的产率在40%以下。
为了提高2-甲基-2-氯丙烷的产率,我们对教材上的制备方法进行了如下改进:(1)改变正丁醇与浓盐酸的物质的量的比例,通过不同的配比进行实验,寻找较高产率的最佳配比;(2)由于该反应的关键是使两种反应物充分混合,教材中只是进行单纯的室温震荡15min,这种人工震荡可能达不到使反应物充分接触的目的,所以加入了超声波震荡和磁力搅拌来进行对比;另一方面,为了使反应更多地向右移动,加入蒸馏操作使低沸点的产物(52℃)更多地从反应体系中蒸馏出来,促进反应继续发生。
2-甲基-2-氯丙烷的制备实验报告

2-甲基-2-氯丙烷的制备实验报告
实验目的:
通过烷基化反应合成2-甲基-2-氯丙烷。
实验原理:
2-甲基-2-氯丙烷是一种常用的有机合成中间体,其制备方法主要有SN2取代反应和SN1取代反应。
本实验采用SN2反应进
行制备,该反应是一种亲核取代反应,通过亲核试剂攻击反应物中活泼的卤素,生成亲核试剂与反应物连接的新化合物。
实验步骤:
1. 取一250 mL圆底烧瓶,加入20 g2-氯丙烷。
2. 在烧瓶中加入20 mL乙醇,用玻璃搅拌棒搅拌均匀。
3. 在冰浴条件下,加入15 mL溴化钠水溶液,保持反应温度
在0°C-5°C。
4. 继续在冰浴条件下,逐滴加入10 mL浓氨水,反应时长为
15分钟。
5. 将反应混合物倒入250 mL锥形瓶中,加入适量饱和食盐水,振荡混合均匀。
6. 使用滤纸过滤出有机相,将有机相转移到干净的干式锥形瓶中。
7. 在锥形瓶中加入适量无水氯化钠,沉淀异丙醇。
8. 使用滤纸过滤出有机相,将有机相转移到干燥的胶塞试剂瓶中,保存。
实验结果与讨论:
通过以上步骤,成功制备了2-甲基-2-氯丙烷。
但应注意在反
应过程中保持低温,避免生成副产物。
另外,在反应后的产品中可能还含有少量的杂质,需要进行进一步的纯化以获得较高纯度的产物。
结论:
通过SN2反应,成功合成了2-甲基-2-氯丙烷。
有机化学实验 2-甲基-2-氯丙烷制备

副反应:
CH3
CH3
H3C C CH3 + H3C C CH3
OH
OH
H+ 加热
CH3 H3C C CH3
OH
H+ 加热
CH3 H3C C CH2
CH3 CH3 H3C C O C CH3 + H2O
CH3 CH3
分子间脱水成醚由于分子较大,空间障碍大,使反应 难于进行,通常要在80℃以上才能发生,所以,反应中只 有少量醚产生。分子内脱水成烯也须在浓酸和一定温度下 进行,在此条件下只有少量生成。此外,还有分子重排、 氧化等可能发生的反应,但可以忽略不计。
水层
分分液液 分分液液 分液
分液
有机层
(CH((CC3)H水3HC3层)3O水3)C水3H层(COC层HOHH3HC)H水3((lCCCC层HOHlHHH3C23)H水O3)lC32层HCOOHCOHl(2HCOHHH(C3C2H()O水3CHClCC层HCH3OH)lH333H)2CCC33O(HCCCH=OCHH=O2C(3HHCCOC3HHlHC3H2)(H32H3(C)(CCC3C32(HCCCOCH(有HHOC有H=3OH3机3)(H3)CH机3)H3C3333层CCC3CH)层CH)C3H=OC32CC(CH(C33HlCClO)OH(33HCHCC有CHCHC2HH3有(3H)(HC机=O()C333CC3C(机CC3)HC层3ClCH有)H3HH=O33H层CHC机CH)C333H3))3l2HC层OC23(3)O3C2ClC(CHC(Hl(CO(CHCC有H3CHlH3HH)机)C(33C3H3C3层CC))ll32H33CCCOCH3lHOl)O23C2HOCOH(CC(lCHCHl3H)23HO3)23O
2-甲基-2-氯丙烷的制备

實驗八:製備2-氯-2-甲基丙烷 (2-chloro-2-methylpropane)引言本實驗利用 2-甲基丙-2-醇與濃氫氯酸的反應製備 2-氯-2-甲基丙烷。
若在反應時加入氯化鋅,效果更佳。
此反應的方程式如下:(CH3)3COH + 濃HCl (CH3)3CCl + H2O化學藥品2-甲基丙-2-醇(2-methylpropan-2-ol)、濃氫氯酸、0.5M 氯化鋅溶液、5%碳酸氫鈉溶液、飽和氯化鈉溶液、無水硫酸鈉固體、0.1 M 硝酸銀溶液、乙醇。
儀器/物料快接儀器、量筒、漏斗、防漰沸小粒、燒杯、-10-110 C 溫度計、分液漏斗、小錐形瓶、濾紙、天平步驟2-甲基丙-2-醇易燃,濃氫氯酸具腐蝕性。
進行實驗時必須戴上安全眼鏡。
甲、2-氯-2-甲基丙烷的製備(Preparation of 2-chloro-2-methylpropane)1. 把 10 cm3的 2-甲基丙-2-醇、15 cm3濃氫氯酸和 2 cm3的0.5M氯化鋅溶液先後加進分液漏斗,接著猛烈搖動分液漏斗約 5 分鐘,搖動時須間中打開活栓排氣,然後讓混合液靜置數分鐘。
2.待混合液清晰地分成兩液層後,首先測試哪一個是有機液層,接著摒棄水液層,但有機液層仍保留在分液漏斗內。
3.把10 cm3的 5% 碳酸氫鈉溶液傾進分液漏斗,接著猛烈搖動分液漏斗約1-2 分鐘,搖動時須間中打開活栓排氣,然後讓混合液靜置數分鐘。
接著把水液層摒棄,有機液層仍留在分液漏斗內。
4.用10 cm3的飽和氯化鈉溶液代替 5% 碳酸氫鈉溶液,重複步驟(3)。
5.把有機液層傾進一乾燥的小錐形瓶,加入適量的無水硫酸鈉固體,搖動瓶子直至液體變得清澈。
小心把液體傾入一乾燥的圓底燒瓶中,再加入防漰沸小粒,安裝蒸餾裝置(所有儀器均需先行弄乾)。
6. 利用小本生燈加熱蒸餾,並用一已稱重的乾燥試管收集在約50o C所蒸餾出來的液體,記錄其沸點。
7. 量度餾液的質量,並計算收穫百分率。
《有机化学实验》教学大纲

《有机化学实验》教学大纲一、课程基本信息课程类别:专业基础课(必修)适用专业:化学总学时数:102 学分:3开课学期:一、二开课系部:化学化工学院教学方式:实验及讨论考核方式:考查二、课程的性质、目的和任务有机化学实验作为化学实验科学的重要分支,是化学专业学生(本科)必修的一门独立的专业基础课。
有机化学实验课的主要目的是使学生熟练掌握有机合成化学实验的基础技能,学会正确选择有机化学的合成方法,分离提纯与基本的分析鉴定方法,培养学生实事求是的科学态度和良好的科学素养、工作习惯。
有机化学实验内容主要包括三个方面:第一部分为实验基本技术,包括蒸馏、分馏、水蒸汽蒸馏、熔点测定、重结晶、萃取、升华、色谱法、折光率测定、旋光度测定、无水无氧操作技术、加热、致冷及干燥技术;工具书及手册查阅方法训练;实验报告及研究论文的写作要求。
第二部分为反应与制备,包括卤代反应、威廉逊反应、氧化反应、格式反应、傅-克反应、璜化反应、硝化反应、还原反应、脂化反应、斯克劳普反应、珀金反应;相转化催化、外消旋体的拆分、天然物的提取与纯化、药物分离与鉴定。
第三部分包括连续有机合成实验和英文文献实验。
三、教学的基本要求(一)有机化学实验的基本操作技术有机化学基本操作技术是该课程的基本任务之一,是必须在教学中切实加强的重要环节,包括如下内容:1.玻管的弯曲,拉毛细管,滴管,玻璃钉和搅拌棒的制作。
2.标准磨口仪器的使用及维护。
3.常用仪器的选择及正确装卸。
4.熔点及沸点的测定。
5.回流、蒸馏、分馏、水蒸气蒸馏及减压蒸馏。
6.分液漏斗的使用及液体物质的萃取。
7.索氏提取器的使用及固体物质的提取。
8.固体物质的重结晶及升华。
9.各种过滤方法。
10.液体物质及固体物质的干燥。
11.加热及冷却。
12.机械搅拌。
13.液体物质的折光率测定。
14.旋光度的测定。
15.薄层色谱、纸色谱及柱色谱。
16.理化手册及工具书的查阅及训练。
17.实验报告及研究论文的写作格式与要求。
2-甲基丙二酸二乙酯(2-氯丙酸法)

2-甲基丙二酸二乙酯(氯丙酸法) ClCOOH NaCO 3Cl COONa COONa CN NaOHCOONa COONaH 2SO 4/EtOH COOC 2H 5COOC 2H 51. 中和反应 中和反应在 1000L 反应釜中进行, 2-氯丙酸与 碳酸钠反应,生成 2-氯丙酸钠。
投料摩尔比为 2-氯丙酸:Na 2CO 3=2:1.01,确保2-氯丙酸充分反应。
操作流程为:反应釜连接真空泵,将桶装 2-氯丙酸负压吸入釜内;液体碳酸钠负压吸入高位槽,由高位槽滴入釜内,滴加过程中关闭真空泵;控制滴加速度,使釜内温度保持在 30℃左右;碱液滴加完毕后,搅拌反应 10min ,然后取样化验;从取样口取样,通过气象色谱检验 2-氯丙酸的含量,当 2-氯丙酸含 量低于 0.01%时,反应结束,打开底部阀,料液从底部出料口流入氰化釜。
由于 2-氯丙酸钠属于强碱弱酸盐,可与水发生水解反应,在碱过量条件下, 2-氯丙酸含量低0.01%时, 可以认为 2-氯丙酸完全反应, 对氰化工序无不利影响。
此工序产生吸收池放气口废气 G 1.1和真空泵废气 G 1.2,以及废水 W 1。
真空泵通过水吸收池、 冷凝器与反应釜相连, 水吸收池的作用是吸收从釜中排出的气 体, 冷凝器的作用是减少 2-氯丙酸的挥发量。
中和反应过程中关闭真空泵, 打开放气口,反应产生 CO 2气体,以及随 CO 2排出的 2-氯丙酸,通过水吸收池吸收 后,从吸收池上方的放气口排出,产生废气 G 1.1,主要污染因子为少量随 CO2排出的 2-氯丙酸。
进料过程中关闭放气口, 开启真空泵, 釜内气体通过水吸收池后,从真空泵排出,产生废气 G 1.2,主要污染因子为少量随 CO 2排出的 2-氯丙酸 , 属于无组织排放。
吸收池中的水以及水环真空泵中的喷射水定期排放, 产生废水 W 1,主要成分为2-氯丙酸 ,污染因子为 pH 、COD(2-氯丙酸 ) 、ss 。
有机化学实验报告--2-甲基-2氯丙烷的制备
2-甲基-2氯丙烷的制备
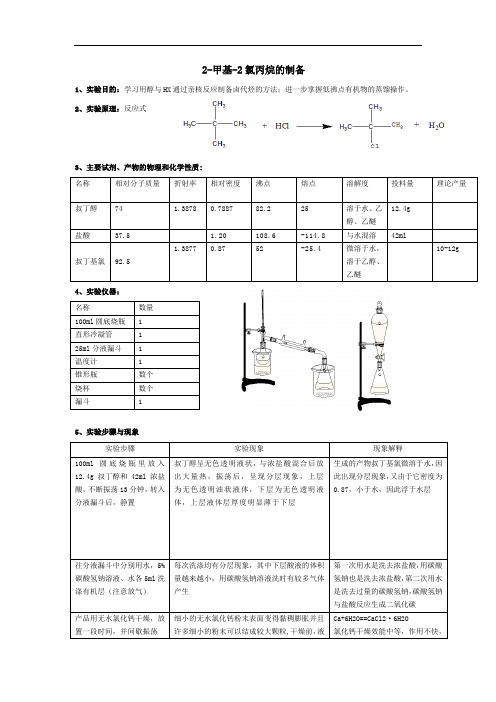
1、实验目的:学习用醇与HX 通过亲核反应制备卤代烃的方法;进一步掌握低沸点有机物的蒸馏操作。
2、实验原理:反应式
3、主要试剂、产物的物理和化学性质:
4、实验仪器:
5、实验步骤与现象
6、产品产率计算
本品理论产量为,实际产量为8g
产率为 8/15.5=51.6%
7、实验结果与讨论
碳酸氢钠是弱碱性物质,即使饱和溶液pH也只8.6左右,用来洗去氯化氢等酸性物质和水溶性物质;短时间不会有明显影响(放置数天可能会有影响,加入碳酸氢钠除酸时浓度计反应时间过长会导致叔丁基氯水解生成叔丁基醇,如果用其他碱性强的物质洗除酸,有可能使叔丁基氯水解损失,降低产率。
本次实验产率不高的原因一方面主要是由于使用分液漏斗操作还不够熟练,损失了一些产物,另一方面是振荡力度不够,可能有些还未反应完全。
并且也由于操作不熟,做实验速度较慢,有点手忙脚乱。
二甲基二氯丙烷的制备的误差分析

二甲基二氯丙烷的制备的误差分析
二甲基二氯丙烷的制备误差分析可能包括以下几个方面:
1. 反应条件误差:反应过程中,温度、pH值、反应时间等反应条件的误差会影响产物的质量和收率。
2. 质量误差:制备二甲基二氯丙烷所使用的原料的纯度、配比、储存方式等因素会影响产物的质量。
3. 操作误差:在实验操作过程中,如加料速度、搅拌时间、采取操作方式等因素,也可能对产物的质量和收率产生影响。
4. 分离纯化误差:在产物分离纯化过程中,如分离器操作不当、干燥条件不够理想等因素也会对产物的质量产生影响。
综上所述,对二甲基二氯丙烷制备误差的分析和改进需要从反应条件、质量控制、操作方式以及后续纯化过程入手,提高实验操作的精度和有效性,进一步提高产物的质量和收率。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2-甲基-2氯丙烷的制备
1、实验目的:学习用醇与HX 通过亲核反应制备卤代烃的方法;进一步掌握低沸点有机物的蒸馏操作。
2、实验原理:反应式
3、主要试剂、产物的物理和化学性质:
4、实验仪器:
5、实验步骤与现象
6、产品产率计算
本品理论产量为,实际产量为8g
产率为 8/15.5=51.6%
7、实验结果与讨论
碳酸氢钠是弱碱性物质,即使饱和溶液pH也只8.6左右,用来洗去氯化氢等酸性物质和水溶性物质;短时间不会有明显影响(放置数天可能会有影响,加入碳酸氢钠除酸时浓度计反应时间过长会导致叔丁基氯水解生成叔丁基醇,如果用其他碱性强的物质洗除酸,有可能使叔丁基氯水解损失,降低产率。
本次实验产率不高的原因一方面主要是由于使用分液漏斗操作还不够熟练,损失了一些产物,另一方面是振荡力度不够,可能有些还未反应完全。
并且也由于操作不熟,做实验速度较慢,有点手忙脚乱。
