环氧乙烷灭菌器技术参数
环氧乙烷灭菌(ISO11135-1)

无菌
无菌状态 无菌保证水品 (SAL)
干扰测 试工作
灭菌实质上就是通过一定方法,将对象物的微生物污染杀灭至 要求水平的过程。
灭菌概念
无菌 Sterile 无菌状态 Sterility 无菌保证水平 Sterility assurance level (SAL) 灭菌 Sterilization
灭菌器
EN 1422:1997+A1:2009 Sterilizers for medical purposes - Ethylene oxide sterilizers - Requirements and test methods YY 0503-2005(NEQ EN 1422:1997) 环氧 乙烷灭菌器
22 0 -6.
23 0 -6.
-8.00
100 368 135 50
lgNt 3.0 2.5 2.1 1.7 1.2 0.概念
D值/D10值
在设定条件下,灭活90%测试微生物所需的时间或辐射剂量。
灭菌过程微生物存活曲线&对数曲线
1100 1000 900 Nt 4.00
8
6
4
2
0
30 44 54 64 70
温度/℃
EO灭菌过程影响因素
总结
1. 一定气体浓度范围内,浓度越高,灭菌效果越好;超过 1000mg/L,灭菌效果的提升不明显; 2. 相对湿度在40%-80%时,灭菌效果没有显著差别;低于 40%,灭菌效果降低明显;高于90%,没有明显的提高, 而且易于产生水滴,反而影响灭菌效果; 3. 温度在30-65℃间,每升高10℃,灭菌效果提升一倍;高于 65℃时,没有显著的灭菌效果提升。
EO灭菌过程影响因素
环氧乙烷灭菌器标准操作流程及评分标准

环氧乙烷灭菌器标准操作流程及评分标准一、操作目的利用环氧乙烷灭菌器对不耐热、不耐湿医用物品进行处理,以达到灭菌效果。
二、物品准备手消毒液、帽子、纸塑包装袋、化学指示胶带、化学指示卡、环氧乙烷气罐、待灭菌物品、物品装载篮筐、生物指示剂三、操作流程报告:我是消毒供应中心护士××,我操作的项目是环氧乙烷灭菌器的标准操作,现物品准备完毕,是否开始,请指示?是!→洗手(六部洗手法)→打开电源及压缩空气开关(7公斤以上)→装入气罐,将气罐插入气罐槽的挡圈内,箭头向下,往下压入,同时向里轻推,使气罐被扣住→放置篮筐,将已装入物品的篮筐放入炉内,将生物指示剂按上前下后位置放在物品中间,关上门,顺时针旋转手柄直到手柄垂直→设置通气时间,按通气时间递增或递减键,每按一次,递增或递减1小时,直到所需的通气时间显示为止(12小时)→开始灭菌循环过程按下“开始”键,开始灭菌/通气循环,整个过程自动运行直至结束。
→灭菌结束后,逆时针旋转炉门手柄到底,30—60秒后,炉腔压力等于大气压力时,门即打开,按下STOP键,灭菌器即处于待机状态,关闭电源,压缩空气开关。
取下环氧乙烷气罐,作为非易燃废弃物丢弃→报告:操作完毕!(口述:1.物品的摆放:物品倾斜放入篮筐,物品间留有空隙,对于纸塑复合材料,务必按纸对纸塑对塑秩序放置。
2.环氧乙烷灭菌器常规测试包的制作:生物指示剂绿色帽端朝向20ml注射器的乳头(中间要留有空隙)。
然后用腹纱包裹注射器,塑封,放入指示卡,贴上3M胶带并注明上前,下后,时间为半年。
将上一次的阳性生物指示剂塑封,同待灭菌物品一起灭菌。
每次灭菌均应放置2支生物指示剂,以监测灭菌效果,生物指示剂应代表被灭菌物品,按上前下后位置放在物品中间。
)四、应知应会1、环氧乙烷气体灭菌的适用范围?答:适用于不耐高温、湿热的诊疗器械的灭菌。
例如:电子仪器、内镜、透析器和一次性使用的诊疗用品等。
环氧乙烷是目前最主要的低温灭菌方法之一。
验证方案(EO灭菌)
XXXXXXXXX公司环氧乙烷灭菌验证报告编制:日期:审核:日期:批准:日期:1、目的一次性使用无菌产品的灭菌是使医疗器械达到无菌使用的必须过程,灭菌过程的有效性和合理性验证和监控是确保产品无菌的可靠保障。
此验证的目的是为了证明XXXXXXXXXXXXXXX公司生产的XXXXXXXXXX的环氧乙烷灭菌过程的有效性和合理性。
2、执行标准EN550/ISO 11135:1994《医疗器械环氧乙烷灭菌确认和常规控制》3、职责3.1XXXXXXXXXX公司生产的XXXXXXXX产品由XXXXXXXX公司进行环氧乙烷灭菌验证。
3.2XXXXXXXXX提供灭菌设备、灭菌造作人员和环氧乙烷。
3.3XXXXXXXXXXX公司提供验证所需的产品和生物指示剂,并且在灭菌后测试BIs。
4、灭菌产品本次灭菌的产品是XXXXXXXXXXXXXXXXX,主要原料为XXXX,包装方式为:内袋:纸塑包装袋,生产厂家为XXXXXXX公司;中包装:使用1层瓦楞,每中包装装载10只产品;大包装:采用3层瓦楞纸,每包装装载8个中包装,即80只产品。
5、生物指示剂本次验证采用XXXXXXXXXX公司生产的环氧乙烷灭菌用生物指示剂,菌种:Bacillus atrophaeus;芽孢含量:1.9×106cfu/片。
符合标准ISO11138-1,2和EN866-1,2。
6、环氧乙烷本次验证使用的纯环氧乙烷由XXXXXXXXXX提供。
7、灭菌设备7.1本次验证的灭菌设备是北京丰台永定消毒设备厂生产的HMQ-6型灭菌器,灭菌舱容积为6M3。
7.2环氧乙烷灭菌器的确认由北京丰台永定消毒设备厂进行,详见《XXXX环氧乙烷灭菌器确认验证报告》。
8、验证小组成员9、微生物性能验证9.1产品装载灭菌产品的包装按照4中所述的规定,堆放模式见附一。
9.2温度传感器的分布依据EN550要求,温度传感器使用贴触式温度探头,数量为11个,分布模式见附二。
9.3生物指示剂的堆放依据EN550要求,本次试验每次放置22片生物指示剂菌片且分别放置在产品正常包装内封好,放置模式见附三,另外作1个阳性对照。
环氧乙烷灭菌器技术参数
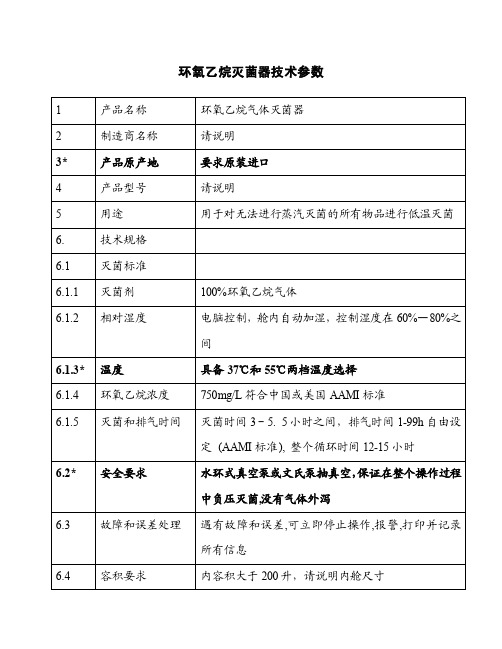
灭菌时自动锁定 单门,手动 高性能、耐高温聚氢硅氢胶材质,使用寿命 3 年以上 设备开始启动后,自动锁门。整个程序结束后,方可 打开门
电脑控制 液晶显示,人机对话,可对操作步骤、运转状况自动 显示 以 英文、 数字及 曲线 实时显 示主要 参数 :温 度 /湿度 / 真空度/时间 具有远程遥控功能,允许操作者在 76 米处遥控操作。 电脑自动检测,如有泄漏,自动转为排气过程,并报 警。
100%环氧乙烷气体 电脑控制,舱内自动加湿,控制湿度在 60%—80%之 间 具备 37℃和 55℃两档温度选择 750mg/L 符合中国或美国 AAMI 标准 灭菌时间 3-5. 5 小时之间,排气时间 1-99h 自由设 定 (AAMI 标准), 整个循环时间 12-15 小时 水环式真空泵或文氏泵抽真空,保证在整个操作过程 中负压灭菌,没有气体外泻 遇有故障和误差,可立即停止操作,报警,打印并记录 所有信息 内容积大于 200 升,请说明内舱尺寸
环氧乙烷灭菌器技术参数
1 2 3* 4 5 6. 6.1 6.1.1 6.1.2
产品名称 制造商名称 产品原产地 产品型号 用途 技术规格环氧乙烷浓度 6.1.5 灭菌和排气时间
6.2* 安全要求
6.3
故障和误差处理
6.4
容积要求
环氧乙烷气体灭菌器 请说明 要求原装进口 请说明 用于对无法进行蒸汽灭菌的所有物品进行低温灭菌
脉冲送风方式 符合国家标准 可在 1-99 小时的范围内设定 大气排放,非地漏排放
内置式 能记录和打印运转中的温度、压力、湿度数据和运行 曲线 停电后可以记忆灭菌信息,待恢复供电后自动继续工 作,无需重新启动 要求国内装机量超过 300 台 要求生产厂家和经销商均在湖北省有办事处或派驻 人员,便于售后维修 要求配置装卸车辆
医疗器械环氧乙烷灭菌知识全解

医疗器械环氧乙烷灭菌知识全解以下为正文:环氧乙烷灭菌是一种广谱、高效、穿透力强、对消毒物品损害轻微的灭菌方法。
环氧乙烷分子式C2H4O,分子量44.05。
它的蒸气压比较大,可以穿透微孔而达到物品的深部。
其液体和气体均有较强的杀微生物作用,气体的杀微生物作用更强。
环氧乙烷可以杀灭各种微生物,包括细菌繁殖体、芽孢、真菌、病毒等,是一种广谱消毒剂。
其作用原理是环氧乙烷能与微生物的蛋白质、DNA和RNA发生非特异性烷基化作用,使蛋白质上的羧基、氨基、硫氨基和羟基被烷基化,使蛋白质失去了在基本代谢中需要的反应基,阻碍了细菌蛋白质正常的化学反应和新陈代谢,从而导致微生物的死亡。
环氧乙烷的消毒作用受多种因素的影响,如消毒剂的浓度、环境温度和相对湿度、消毒处理的时间、消毒物品的质量和厚度,微生物的菌龄和含水量等。
环氧乙烷对多数消毒物品无损害,但可以破坏食物的某些成分,也不可用作血液灭菌。
环氧乙烷对人及动物也是有毒性的,工作环境环氧乙烷的允许浓度应低于1mg/kg。
据文献记载,公元1859年,Wurtz首先发现了环氧乙烷(ethyleneoxide,简称EO)又名氧化乙烯或氧丙烷。
但将其作为消毒与灭菌剂应用是在1936年。
1936年,Schrader与Bossert发现EO与CO2相混合,用于杀灭各种害虫和细菌。
1937年Gross与Dixon发现EO对试验的48种微生物都有杀灭作用。
1940~1943年间,Griffith和Hull共同出版了多本书籍并申请专利。
1949年,Phillips和Kaye对EO进行了系统而较全面的研究。
此后Ernst和Shull,Ernst和DoyleKereluk和Lloyd等对EO的灭菌机理、影响因素、急、慢性毒性、灭菌效果、腐蚀性及其在环境中的变迁等进行了广泛深入地研究。
20世纪50年代起EO开始用于医院灭菌,据调查20世纪90年代中期,美国几乎所有的医疗机构都具备EO灭菌设备。
环氧乙烷灭菌验证方案计划

环氧乙烷灭菌验证方案XXXXX医疗科技有限公司年月,.环氧乙烷灭菌验证方案目录1. 概述2. 验证目的3. 相关文件4. 验证组织职责5. 验证实施时间6. 验证内容与方法7. 漏项、偏差的处理程序8. 验证周期9. 验证结果评定与结论10.附表附表1:环氧乙烷灭菌人员资格确认表附表2:产品灭菌适用性验证确认表附表3:生物指示剂检验记录表附表4:初始微生物负载检验记录表附表5:环氧乙烷残留量检验记录表附表6:漏项、偏差处理表1.概述XXXXX医疗科技有限公司生产的XXXXXXXXXX将会直接与患者的器官和组织接触,器械以无菌的形式提供给医院。
XXXXXXXXXXX的包装总体分3层,从内向外依次是无菌包装、彩盒包装、瓦楞纸箱包装。
每一个无菌包装中放置一把器械,每一个无菌包装将放置于一个彩盒包装中,瓦楞纸箱包装也是最终的运输包装。
其中无菌包装是由两部分组成的,PETG材质的泡壳和Tyvek材质的盖材。
然后用专用的热封机将两者热封合到一起,形成完整的阻菌屏障。
由于Tyvek具有一定的通气性,故EO 混合气体可以穿过盖材进入包装内,从而实现杀灭的目地。
2.验证目的通过本次测试,验证吻合器系列产品采用的热封工艺和EO灭菌工艺,产品能够达到以下标准:a)热封工艺有稳定可重复的输出结果,满足厂内标准;b)在合适的EO灭菌工艺参数下能确保足够的无菌保证水平;c)能可靠的在有效期内处于无菌状态;灭菌工艺对产品的使用性能不产生影响;3.相关文件3.1 环氧乙烷灭菌器作业指导书3.2 《医疗器械生产质量管理规范》及无菌医疗器械附录4.验证组织职责4.1验证人员职责管理者代表:负责验证方案、验证报告的批准;负责签发验证证书。
组长:审核验证方案、验证报告,制定验证计划;负责验证实施全过程的组织协调工作;对验证过程的技术、质量负责;组员:负责验证过程中的具体工作,并做好记录工作。
4.2验证过程中各相关部门职责4.2.1质量管理部:负责组织验证方案、报告与结果的会审会签;负责对验证全过程实施监控;负责验证过程的取样、检验及结果报告;负责核查、汇总验证数据;负责建立验证档案,及时将批准实施的验证资料收存归档。
环氧乙烷灭菌系统技术参数

环氧乙烷灭菌系统技术参数环氧乙烷灭菌器用途:用于对湿热敏感的医疗器械和物品进行低温灭菌,对医疗器械的结构复杂度无要求产品认证: CFDA医疗器械注册证性能参数:腔体容积:舱体大于220 L灭菌温度:38℃和55℃湿度控制方式:动态湿度直接测量,加湿和保湿两种算法,进一步保证湿度控制的精确性参数测量:压力、温度和湿度传感器均为双配置灭菌时间:38℃灭菌时间为4.5小时,55℃灭菌时间为1小时通风时间:可根据被灭菌物品的特性自由设定通风解析时间控制主机:嵌入式电脑控制系统,遇有故障和误差,可立即停止操作,报警,打印并记录故障信息控制方式:高分辨率彩色触摸屏,具有中文操作界面。
灭菌循环实时显示主要参数,包括温度、湿度、真空度和时间*参数打印:内置打印机,可以选择三种打印方式,能记录和打印运行中的温度、时间、压力、湿度曲线和关键时间点参数以及相关辅助警报信息,可以通过USB 导出灭菌循环参数或连接灭菌质量控制系统参数存储:可自动存储最近的100次灭菌循环参数安全设置:负压灭菌:全过程负压灭菌,保证灭菌全过程舱内处于负压状态,确保灭菌气体不向舱外泄漏。
电脑自动检测,如有泄露,自动中断灭菌过程并开始自动排气,报警提醒用户*腔体真空:具有内置式的文氏真空泵,利用流体力学原理通过外置压缩空气进行抽真空,其内部不具有产生任何电火花的部件,保证机器运行安全*EO气罐罐装:小剂量罐装100%环氧乙烷气体,气罐自带二维码集成批号效期等信息,在灭菌开始前会读取气罐信息,在确保气罐为正品并有效后,才可以开始灭菌循环EO气罐安装:自带气罐锁紧配置,可以将气罐安全固定在灭菌器中,降低因为人为操作不当造成气罐安装不到位的几率,避免灭菌器报警EO气罐刺破:EO气罐自动被刺破,EO气体通过特定管路进入灭菌腔体中。
全部过程须自动进行,无需人工操作舱门控制:无把手舱门设计,灭菌时嵌入式系统自动锁定舱门,防止灭菌过程中因为误操作打开舱门。
医疗器械灭菌环氧乙烷灭菌过程参数放行指南

医疗器械灭菌环氧乙烷灭菌过程参数放行指南一、前言医疗器械灭菌是防止交叉感染的关键步骤之一,环氧乙烷灭菌被广泛应用于医疗器械的消毒过程中。
为了保证灭菌的效果和安全性,正确设置灭菌过程参数非常重要。
本文将针对环氧乙烷灭菌过程参数放行给出相关指南,以帮助医疗机构和相关人员更好地进行操作。
二、灭菌过程参数的选择1. 温度:环氧乙烷灭菌需要在特定的温度下进行。
温度的选择应根据医疗器械的特性、适应性和灭菌目的来确定。
一般情况下,温度范围为50℃-60℃。
2. 湿度:环氧乙烷灭菌需要在一定的湿度条件下进行。
湿度的调节可以通过设备的加湿功能来实现。
在灭菌过程中,湿度应保持在30%-80%之间,以保证灭菌效果。
3. 压力:灭菌过程中的压力控制对于保持环氧乙烷的气相浓度和渗透性至关重要。
一般情况下,压力范围为300-500mbar。
4. 气体浓度:环氧乙烷的浓度是影响灭菌效果的重要因素之一。
过高的气体浓度可能对医疗器械造成损害,而过低的气体浓度则无法有效灭菌。
一般来说,环氧乙烷的浓度应控制在300mg/L-1200mg/L之间。
5. 时间:灭菌的时间是保证灭菌效果的关键因素。
时间的选择应根据医疗器械的复杂程度、灭菌目的和设备性能来确定。
一般情况下,灭菌时间为4-12小时。
三、灭菌参数放行流程1. 设备验证:在灭菌过程开始之前,应对设备进行验证,包括温度、湿度、压力、气体浓度等参数。
设备验证的目的是确保设备运行正常,并且能够满足灭菌过程的要求。
2. 灭菌参数设置:根据医疗器械的特性和要求,设置合适的灭菌参数,包括温度、湿度、压力、气体浓度和时间等。
参数设置应符合相关标准和规范的要求。
3. 参数监测与控制:在灭菌过程中,应进行参数监测和控制。
通过实时监测温度、湿度、压力和气体浓度等参数,及时调整设备工作状态,确保参数的稳定和一致。
4. 灭菌效果验证:灭菌过程结束后,应进行灭菌效果验证。
通过采集灭菌器械样品,进行微生物检测和生物指示器等方法,评估灭菌效果的合格与否。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
灭菌器和通风解读器为二合一
第三方《灭菌后物品残留量检测报告》
负压灭菌,无环氧乙烷气体无外泄
和认证
售后
*整机保修,不少于年
保修期内,提供生物监测
提供每年,每季度设备维护保养,并提供保养报告
提供设备维修资料(中英文操作手册,中英文故障代码提示)
提供维修工程师院内培训、操作人员培训
每年提供一次灭菌间的环氧乙烷环境浓度检测(第三方检测报告)
网络
报价含与院内所有网络连接费用
环氧乙烷灭菌器技术参数
序号
项目
要求
功能
医疗器械低温灭菌
配置
环氧乙烷灭菌器台
有害气体浓度检测仪(环氧乙烷)台
同品牌自动阅读仪(快速)台
旋涡空压机台
提供产品配置清单
性能
灭菌温度:低温℃±,高温℃±
灭菌湿度范围:不小于、不大于
舱体容积:≥
灭菌剂浓度:不小于;不大于
最大灭菌时间:不大于
最大通风解读时间:不大于小时
高分辨率液晶彩色显示屏
电脑自动控制功能(舱门开启)
双温度、湿度、压力传感器
环氧乙烷废气分解器通讯及控制
环氧乙烷气罐扫描功能,自动识别正品气罐和保质期
自动故障诊断
泄露监控系统
水箱水位可视
设备断电后,自动锁死,自动供电
自动保存不少于组最近循环参数
立式、单门
保温材料覆盖不少于腔体总面积
硅胶材料门封条
耐腐蚀金属内舱
