物理化学 8章表面化学与胶体化学
第八章 土壤胶体化学和表面反应

(三)土壤胶体双电层结构和表面电位
胶体微粒
胶核 双电层
决定电位离子层(内) 非活性离子层
补偿离子层(外) 扩散层
当静电引力与热扩散相平衡时,在带电胶体表 面与溶液的界面上,形成了由一层固相表面电荷和 一层溶液中相反符号离子所组成的电荷非均匀分布 的空间结构,称为双电层***(图8-2)。
们都称为盐基离子。
(2)盐基饱和度(base saturation percentage)BSP
在土壤胶体所吸附的阳离子中,盐基离子的数量
占所有吸附的阳离子的百分比,叫盐基饱和度***。
盐基饱和的土壤具有中性或碱性反应; 而盐基不饱和的土壤则具有酸性反应,为酸性土壤;
盐基饱和交阳度换离性子盐交基换总量当量量(/量1/1( 0毫 0克0克0毫克土土克当))100%
中
高
***影响土壤阳离子交换量的因素有:
(1)质地 质地越粘重,含粘粒越多的土壤, 其阳离子交换量也越大。
质地
砂土 砂壤土 壤土
粘土
CEC
1~5
7~8
(2)有机质 OM % CEC
15~18
25~30
(3)胶体的性质及构造
蒙脱石 > 高岭石
(4)pH值 在一般情况下,随着pH的升高,土壤 的可变电荷增加,土壤的阳离子交换量也增加。
表8-3 不同类型土壤胶体的阳离子交换量
土壤胶体
CEC[cmol(+).kg-1]
腐殖质 蛭石 蒙脱石 伊利石 高岭石 倍半氧化物
200 100-150 70-95 10-40
3-15 2-4
4.影响阳离子交换能力的因素**
(1)电荷的影响;
表面与胶体化学表面吸附.pptx

第22页/共43页
第Ⅳ和Ⅴ型等温线属于有毛细管凝聚作用的吸附,因此BET两常数或三常数公式均不能说明这两种类型 等温变化的规律。
BET理论没考虑到表面的不均匀和分子之间的相互作用。这就决定了它的局限性,有一定的适用范围。 许多结果表明,低压时实验吸附量较理论值偏高,而高压时又偏低。
一.物理吸附与化学吸附
按吸附作用力的不同,可将吸附区分 为物理吸附和化学吸附。
物理吸附的作用力是分子间力,如 范德华力和氢键。
化学吸附的作用力是化学键力。
第3页/共43页
物理吸附和化学吸附的基本区别
物理吸附
吸附热 吸附力
近似液化热 ( <40kJ·mol-1)
范德华力,弱
吸附层数 单分子层或多分子层
这种发生于毛细孔中凹液面上的蒸汽凝结称为毛细凝结。
第25页/共43页
吸附滞后
Zigmondy对吸附滞后的解释是吸附时液态吸附质润湿孔壁的过程,接触角是前进角;脱附是液体从 一润湿的表面上退出的过程,接触角是后退角。而前进角一般总是大于后退角。因而脱附时平衡相对压力 小于吸附时的。
第26页/共43页
由Vm可算出呈单层饱和吸附时所需吸 附质的分子数,这时如果再知道每个吸附分 子的截面积,则可算出吸附剂的比表面。
第21页/共43页
C exp( E1 EL ) RT
当n=1时,BET公式可用单分子层吸附等温式。 当n>1时,根据不同的C值BET可用来说明第Ⅱ和第Ⅲ 等温线。
C>1时,E1>EL,即吸附剂与吸附质分子之间的 吸引力大于吸附质为液体时分子之间的引力,这时低 压下曲线是凸的,于是等温线呈S型,即第Ⅱ型。
物理化学(第三版)第8章 界面现象与胶体化学

F
2l
只适用于液体
三、影响表面张力的因素
1.物质的本性 表面张力是分子间相互作用的结果,一般来讲,物质分子 间相互作用力愈大,表面张力也愈大。
金属键 离子键 极性共价键 非极性共价键
2.接触相的性质
3.温度
L
液体分子受力情况示意图
表面层的分子恒受到指向液体内部的拉力
在恒温、恒压、系统的组成不变条件下,可逆地扩展系统表面 积所需的功,与系统表面积的增量dA成正比:
W dA
恒温恒压下,系统的表面功应等于系统吉布斯函数的增量
dG W
dG dA
G A
T
,
p
,nB
-----比表面吉布斯函数, 单位为J·m-2
解:(1) 球体体积 V 4 r3
3
大水滴半径 r 3 3V 6.2 103 m
4
分散后的液滴总数
n
4 r 3
3
4 3
r13
r r1
3
6.2 10 109
3
3
2.4 1020
(2)半径为r的球形液滴:
A 4 r2 4 (6.2103)2 4.8104 m2
AV
A V
4 4
r2 r3
r1 r2
为什么两块玻璃板之间有水时不易拉开? 由于表面张力和附加压力的作用。
二、弯曲液面的饱和蒸气压
弯曲液面的饱和蒸气压不仅与物质的本性和温度有关, 而且还与液面曲率半径有关。
物理化学
第8章 界面现象与胶体化学
(张坤玲)
多相系统中,相与相之间密切接触的交界部分称为界面 物质的存在状态: 界面类型气—液界面固—气界面源自气液—液界面液
物理化学课后习题解答

第8章 表面和胶体化学习题解答1. 若一球形液膜的直径为2×10-3m ,比表面自由能为0.7 J ·m -2,则其所受的附加压力是多少? 解:球形液膜 3440.7 kPa 2.8 kPa 210/2p r γ-⨯∆===⨯ 2. 若水在293 K 时的表面力为72.75×10-3N ·m -1,则当把水分散成半径为10-5m 的小液滴时,曲面下的附加压力为多少?解:3452272.7510 Pa 1.4510 Pa 10p r γ--⨯⨯∆===⨯ 3. 在293 K 时把半径1 mm 的水滴分散成半径为1 µm 的小水滴,问比表面增加了多少倍?表面吉布斯函数增加了多少?完成该变化时,环境至少需做多少功?已知水的表面力为72.75×10-3 N ·m -1。
解:设半径1 mm 水滴的表面积为A 1,体积为:V 1,半径为:R 1;半径1 µm 水滴的表面积为A 2,体积为:V 2,半径为:R 2;N 为小水滴的个数。
33121244 , 33V NV R N R ππ== 33912 1 mm 101 μm R N R ⎛⎫⎛⎫=== ⎪ ⎪⎝⎭⎝⎭ 229222114 1 μm 1010004 1 mm A N R A R ππ⨯⎛⎫=== ⎪⎝⎭ 12221440.07288 N m 4()=9.14510 N m 9.14510 JA G dA NR R γπ---∆==⋅⨯-⨯⋅=⨯49.14510 J A W G -=-∆=-⨯4. 在298 K ,101.325 kPa 下,将直径为1 µm 的毛细管插入水中,问管需加多大压力才能防止水面上升?若不加额外压力,让水面上升达平衡后,管液面上升多高?已知:该温度下水的表面力为0.072 N ·m -1,水的密度为1000 kg ·m -3,设接触角为0o ,重力加速度为9.8 m ·s -2。
物理化学中的表面现象与胶体化学

物理化学中的表面现象与胶体化学物理化学是一门探讨物质性质变化及相关规律的学科。
与之相关的表面现象和胶体化学则是物理化学领域中一项重要的分支。
本文将从表面现象和胶体化学两个方面入手,探讨它们的基本概念、相关应用和研究意义。
一、表面现象观察一个物体,我们会发现它的表面是与外界直接接触的部分。
因此,表面现象是物质研究中一种极其普遍和重要的现象。
表面现象是指两种或两种以上介质相接触时,有特殊性质的现象出现。
在物理化学中,表面现象主要包括表面张力、毛细现象和润湿现象。
表面张力是液体表面处由于分子间作用力而表现出来的一种现象。
表面张力较大的液体在容器中形成凸面或水滴状,这种现象称为毛细现象。
液体与固体相接触时,液体能否在固体表面上均匀分布并附着称为润湿现象。
表面现象在自然界和人类生活中都有广泛应用。
例如,水平稳定的大船只是因为水面的表面张力;高楼大厦的毛细管水系统则利用了毛细现象;润滑油、乳液、涂料等都运用了润湿性质。
二、胶体化学胶体化学是涉及无色透明的小粒子(胶体)和它所处的环境之间的相互作用的学科。
胶体是介于小分子和宏观物体之间的一种存在形式,其中粒子的平均大小在1至1000纳米之间。
胶体物理包括多种胶体类型,例如溶胶、凝胶和气溶胶等。
胶体学科研究中的主要问题是如何制备胶体,以及在胶体中所表现出的各种特殊性质。
胶体的制备方法包括溶胶法、凝胶法和胶体化合物分解法等。
在胶体中存在的各种特殊现象包括布朗运动、泡沫现象和重力分选等。
胶体的应用十分广泛,例如在涂料、油墨、胶水、陶瓷、橡胶等方面都得到了广泛的应用。
另外,人类生命活动中的一些基础物质,例如蛋白质、肌肉等,都是以胶体形式存在的。
三、物理化学中的表面现象与胶体化学的关联表面现象与胶体化学之间有着密不可分的联系。
在液态物质中,固液接触面所呈现的动态变化与胶体的形成和演化密切相关。
例如,胶体粒子表面的物理化学特征决定了胶体粒子的成长和聚集行为。
此外,表面现象和胶体化学之间也有着一些实际应用。
表面与胶体化学复习
3、微小液滴的饱和蒸汽压---开尔文公式
凸液面 RTln Pr P 2γM ρ r 2γVm r
凹液面 RTln P Pr 2γM ρ r 2γVm r
即:Pr(凸液面)>P(平液面)>Pr(凹液面)。
8.某水溶液发生负吸附后,在干净的毛吸管中的上升高度比 纯水在该毛吸管中上升的高度低。 ( )
8. 答: ×
9.通常物理吸附的速率较小,而化学吸附的速率较大。( ) 9. 答: ×
10.兰缪尔定温吸附理论只适用于单分子层吸附。( ) 10. 答:
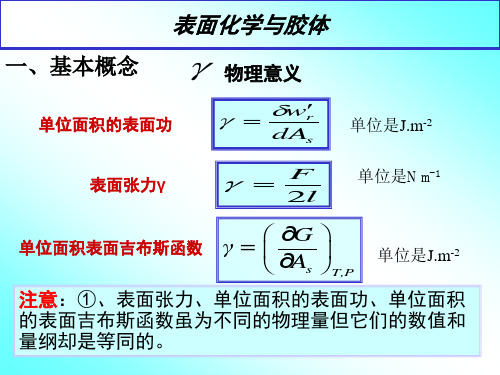
表面化学与胶体
一、分散系统的分类
1、分散系统,分散相,分散介质
斯特恩电势 ——Stern面 与溶液本体间的电势差 ;
电动电势称为 电势。带电
的固体或胶粒在移动时,滑 动面与液体本体之间的电位 差称为电动电势。(概念)
+ +++++++ +
固体表面
+ +
斯特恩面
滑动面
+ + +
--
-
-
-
-
-
-
-
-
+ +
+ +
--
-
-
-
-
-
扩散层 斯特恩层(紧密层)
表面化学与胶体
5.水在干净的玻璃毛细管中呈凹液面,因附加压力 p >0,
所以表面张力 0 是不可能的。( )
5. 答:
6.在相同温度下,纯汞在玻璃毛吸管中呈凸液面,所以与之 平衡的饱和蒸气压必大于其平液面的蒸气压。( )
表面及胶体化学知识点归纳

胶体: 指具有高度分散的分散体系(亦是研究对象),分散相可以是一相和多相,粒子大小通常为10-7~10-9m之间.胶体的研究内容:表面现象、分散体系、高分子溶液。
表面能δ:恒温恒压下,可逆地增加单位表面积,环境对体系所做的功,单位J·m-2。
表面张力δ:单位长度液体表面的收缩力,单位N·m-1(或mN·m-1)l aplace方程:球面,则R1=R2=R,ΔP=2σR 柱面,则R1=R,R2=∞,ΔP=σ/R 球形气泡,且R1=R2=RΔP=4σ/R表面过剩:界面相与体相的浓度差。
接触角:固液气三相交点处作气液界面的切线,此切线与固液交界线之间的夹角θ。
Gibbs吸附公式:(双组分体系)固体表面张力:新产生的两个固体表面的表面应力之和的一半。
固体表面能:指产生一平方厘米新表面所消耗的等温可逆功。
Laugmuir理论:假设被吸附分子间无作用力,因而分子脱附不受周围分子的影响。
只有碰撞在空间表面的分子才有可能被吸附(单分子层吸附)。
固体表面是均匀的,各处吸附能相同。
BET理论的基本假设:①固体表面是均匀的,同层分子(横向)间没有相互作用,分子在吸附和脱附时不受周围同层分子的影响。
②物理吸附中,固体表面与吸附质之间有范德华力,被吸附分子间也有范德华力,即吸附是多分子层的。
影响溶液中吸附的因素:吸附剂:溶质、溶剂三者极性的影响;温度:溶液吸附也是放热过程,一般T上升,吸附下降;溶解度:吸附与溶解相反,溶解度越小,越易被吸附;同系物的吸附规律一般随C-H链的增长吸附有规律的增加和减少。
Trube规则;吸附剂的孔隙大小;吸附剂的表面化学性质,同一类吸附剂由于制备条件不同,表面活性相差很大,吸附性能也会有很大差异;混合溶剂的影响,色谱法中使用混合溶剂,洗提效果比单纯溶剂好,若自极性相同的混合溶剂中吸附第三组份,等温线界于两单等温线之间;若自极性不相同的混合溶剂中吸附第三组份,吸附量比任何单一溶剂中少,混合溶剂极性一致或不一致情况不同;多种溶质的混合溶液;9、盐的影响,盐的存在通过影响溶质的活度系数、溶解度、溶质的电离平衡而影响吸附。
物理化学表面现象及胶体化学总结

1.压缩因子任何温度下第七章表面现象1.在相界面上所发生的物理化学现象陈称为表面现象。
产生表面现象的主要原因是处在表面层中的物质分子与系统内部的分子存在着力场上的差异。
2.通常用比表面来表示物质的分散度。
其定义为:每单位体积物质所具有的表面积。
3.任意两相间的接触面,通常称为界面(界面层)。
物质与(另一相为气体)真空、与本身的饱和蒸气或与被其蒸汽饱和了的空气相接触的面,称为表面。
4.表面张力:在与液面相切的方向上,垂直作用于单位长度线段上的紧缩力。
5.在恒温恒压下,可逆过程的非体积功等于此过程系统的吉布斯函数变。
6.影响表面及界面张力的因素:表面张力与物质的本性有关、与接触相的性质有关(分子间作用力)、温度的影响、压力的影响。
7.润湿现象:润湿是固体(或液体)表面上的气体被液体取代的过程。
铺展:液滴在固体表面上迅速展开,形成液膜平铺在固体表面上的现象。
8.亚稳状态与新相生成:a.过饱和蒸汽:按通常相平衡条件应当凝结而未凝结的蒸汽。
过热液体:按通常相平衡条件应当沸腾而仍不沸腾的液体。
过冷液体:按相平衡条件应当凝固而未凝固的液体。
过饱和溶液:按相平衡条件应当有晶体析出而未能析出的溶液。
上述各种过饱和系统都不是真正的平衡系统,都是不稳定的状态,故称为亚稳(或介安)状态。
亚稳态所以能长期存在,是因为在指定条件下新相种子难以生成。
9.固体表面的吸附作用:吸附:在一定条件下一种物质的分子、原子或离子能自动地粘附在固体表面的现象。
或者说,在任意两相之间的界面层中,某种物质的浓度可自动发生变化的现象。
吸附分为物理吸附(范德华力)和化学吸附(化学键力)。
具有吸附能力的物质称为吸附剂或基质,被吸附的物质称为吸附质。
吸附的逆过程,即被吸附的物质脱离吸附层返回到介质中的过程,称为脱附(或解吸)。
10.吸附平衡:对于一个指定的吸附系统,当吸附速率等于脱附速率时所对应的状态。
当吸附达到平衡时的吸附量,称为吸附量。
气体在固体表面的吸附量与气体的平衡压力及系统的温度有关。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附加压强ps:由表面张力的合力产生,指向“球心”的压 强
其大小与表面的弯曲程度、表面张力的大小相关 p 4 3 2 p p0 ps As 4r V r
3
p dp
δW ' ps dV 2 ps r
dAs 8rdr
dV 4r 2dr
δW ' dAs
l σ m2 f m1
2018/10/25
物理化学
表面张力:垂直作用于单位长度相界面上,与表
面平行(平面)或相切(曲面)的收 缩力。 力的方向:与液面相切,与单位线段垂直。 力的类型:表面收缩力。 力的单位量纲:N· m-1 表面层分子受力不均匀 内压力 表面张力 体系的一种强度性质,受到多种因素的影响。
σ
相等
σ
量纲
单位 J.m-2
相通
N.m-1
标量
强度性质
2018/10/25 物理化学
矢量
要点: 1) 表面分子所受到不对称力场 ——表面张力 2) 一切减小 σ,As 的过程为自动过程
提问:表面Gibbs自由能、比表面Gibbs自由能、 表面张力三者的概念、单位是否相同? 如何表示? 固体表面有过剩的Gibbs自由能吗?它与 液体的有何不同?
§1
引
言
一、几个概念 表面化学:研究物质相界面上发生的现象的规律。 1. 界面和表面 界面(interface):密切接触的两相间的过渡区, 约10-9—10 -8 m, 有几个分子层厚。 五类界面:气(g)-液(l) ,气(g)- 固(s), 液(l)- 固(s) ,液(l1)-液(l2) ,固(s1)- 固(s2) 表面(surface): 若其中的一相为气相(习惯)。如l-g,s-g。
s
σ= 58.85×10-3N.m-1, ps= 2 /r =11.77×103kPa
2018/10/25 物理化学
h = 0.02m,ρ=958.1kg· m-3
p静=gh = 958.1×9.8×0.02=0.1878kPa p大气=100kPa
p =100 + 0.1878 + 11.77×103 = 11.87×103kPa pr 2M 1 007127 根据开尔文公式 ln 得: p0 RT r
2018/10/25 物理化学
注意:表面自由能与表面张力的代表符相同,均 为σ,量纲相通,但两者的概念不同!! 表面自由能是单位表面积的能量,标量;
表面张力是单位长度上的力,矢量。 讨论:dU =TdS – pdV +σdAs+Σidni dH =TdS + Vdp +σdAs+Σidni
dA =-SdT –pdV +σdAs+Σidni
r1
s s r2
l
r2= 8×10-5 m 1 1 ps ( ) 2730 Pa r 1 r2
2018/10/25
物理化学
毛细现象:毛细管插入液相中,毛细管内液体 上升或下降的现象。 p大气 原因:附加压强 ps=p静压时, rm 在液面处达力平衡 r ps= 2σ/r p静压=ρgh cosθ=rm/r p大气 pS h ∵2σ/r =ρgh ∴2σcosθ/rm=ρgh h = 2σcosθ/rmρg rm:毛细管半径 r:凹液面曲率半径 rm ↘, ρ↘, h↗ θ<90o,h>0; θ>90o ,h<0;rm→∞,h →0
将开尔文公式与亨利定律结合,推导得: c2 2M 1 1 cr 2M 1 ln ( ) 和 ln c1 RT r2 r1 c0 RT r
若r2<r1,则c2 > c1,
即:物质颗粒越小,其溶解度越大;
因为固体颗粒的r>0,所以微小物质的溶解度 (c r)大于正常条件下物质的溶解度(c 0)
2018/10/25 物理化学
2. 界面现象和表面现象: 在相的界面上发生的行为 。 如: 露珠为球形 微小液滴易蒸发 水在毛细管中会自动上升 3. 比表面A0
A 或 Ao 单位(量纲):面积· 质量-1 m 6l2 6 例如:有边长为 l 的立方体, A0 3 l l 60 l 分割成边长为 的小立方体,A0 ' 10 A0 l 10
微小物质化学势
r,B RT ln
pr,B
r,B B(l) 微物熔融应满足:
只有降低熔点,才能使 r,B减小,故有: Tf(微小)< Tf(大块)
2018/10/25 物理化学
▲ 微小固体物质的溶解度大 溶解度:恒T﹑p下,溶质在溶剂中达到溶解 平衡时的(饱和)浓度。
2018/10/25 物理化学
公式应用:测表面张力 —— 最大气泡压力法
p大气
p控
pS
ps+p控=p大气 减小p控 :气泡长大,最终逸出 气泡半径r 变化: 大→小→大 ps变化:小→大→小 ps,max= 2σ/r (r曲率=r毛细管) ps,max = p大气 - p控
2018/10/25
物理化学
dG =-SdT +Vdp +σdAs+Σidni
G A s U A T , p ,ni s H A S ,V ,ni s
物理化学
A A S , p ,ni s
2018/10/25 物理化学
2. 影响表面张力的因素 ★ 与物质本性有关 分子间的作用力越大,σ越大: σ金属键>σ离子键>σ极性键>σ非极性键, ★ 与温度有关 一般:温度升高,σ↓;教材P544 式(11-3) 温度升高到临界温度Tc时,σ→0 ★ 与接触相的性质有关(见教材P543表11-2) 接触相相同, σ固体 > σ液体 ★ 与压强有关 一般:压强升高,σ↓;见教材P544图11-5 ★ 其它:分散度 ,运动情况等
表 面 层 粒 子 受 力 分 析
1.
表面张力 表面层粒子受力不均匀,产生内压力。 表面有自动缩小的趋势,产生表面收缩力。
2018/10/25 物理化学
例:记 f g (m1 m2 ),金属丝移动 到一定位置时,可以保持不再滑动 δW ' ∝ dAs 2ldx f δW ' dAs fdx 2l ——表面张力
★ 微小物质的饱和蒸气压 pr 增大,
其化学势增高
2018/10/25 物理化学
▲ 微小物质的熔点低(凸面) 微小物质的饱和蒸气压>大块物质饱和蒸气压
p pB B RT ln 大块物质化学势 p r,B> B ,熔融时, B B(l) 则: r,B>B(l)
表面能达到 220J,是原有表面能的6.3×106倍。 恒T、P、恒组成、可逆过程,生成dAs新表面 需环境作功:dGT,p=δWr’=σdAs
2018/10/25 物理化学
积分:
GT ,P ,ni
0
dGT , P,ni dAs Wr '
0
As
得: Wr ' GT , p,ni As Gs 则:σ= Gs/As= W ’ / A r s σ:(比)表面Gibbs自由能,表面自由能。 也表示恒T,p,ni下,增加单位面积所必须 对体系作的非体积功,又称比表面功。 单位量纲:J· m-2 J· m-2 = N· m· m-2 = N· m-1
物理化学
Kelvin公式化为:
pr 2M 1 ln p0 p凹< p0,
且|r|越小,p凹越小;
★ 凸液面,r>0,则:pr= p凸> p0,
r/m
pr / p0
10-6
10-7
10-8
10-9
1.001 1.011 1.114 2.95
★ 物质要小到一定程度,表面效应才显著
1 1 ps ( ) r 1 r2
球面 任意曲面 Young-Laplace公式
2018/10/25 物理化学
r
ps p0
适用范围: 1)适用毛细管直径<0.5mm情形 2)适用于r为定值的小液滴或液体中小气泡。 注意: 1) r 的符号: 凸液面,r>0,ps>0, r 指向液相(固相)内部 凹液面,r <0,ps<0, r 指向气相 气 平液面,r→∞,ps→0, 气 2)气泡的附加压强: ps,1 r1 肥皂泡两个l-g界面,r1≈r2 r2 p s,2 ps=ps,1+ ps,2= 4σ/r
二、微小物质的特性 微小物质:比表面积大,Gs=σAs大 1.弯曲液面的饱和蒸气压与表面曲率半径的关系
p2 2M 1 1 ln ( ) p1 RT r2 r1
Kelvin公式
★ r1> r2,p2 > p1; ★ r1→∞, p1 → p0, r2取为r, p2= pr
Kelvin 公式化为: 2018/10/25
2018/10/25 物理化学
A 单位(量纲):长度-1 A0 V
可见:体系的分散程度越高,比表面积越大。
二、表面化学和胶体化学的关系 胶体: 粒子粒径在1nm—100nm间的高度分散的多 相体系。 胶体粒子的比表面积极大,表面效应极为显著。
2018/10/25 物理化学
§2 表 面 热 力 学 性 质 一、表面张力及其影响
2018/10/25 物理化学
◆ 过饱和蒸气
降温过程:
p
微小
pB
A:不能凝出微小液滴 pA B:凝出微小液滴 AB:过饱和蒸气 pB> pA
l
B 大块
A
g TA T
消除:如人工降雨,加AgI颗粒
◆ 过冷液体
原因:凝固点下降。如纯净水可到-40℃不结冰。
2018/10/25
物理化学
◆过热液体 液体在正常沸腾温度不沸腾,要温度超过正 常沸腾温度才沸腾。 原因:液体表面气化,液体内部的极微小气泡 (新相)不能长大逸出(气泡内为凹液面)。 小气泡受到的压力为: p大气 p = p大气+ ps+ p静 p静=ρgh ps = 2σ/r h 如 r =-10-8m,T = 373.15K时, p
