高一化学(下)学期 第一次段考测试卷及解析
高一化学第二学期第一次质量检测测试卷及解析

高一化学第二学期第一次质量检测测试卷及解析一、选择题1.下列说法不正确的是A .氯水、氨水、漂白粉都是混合物B .C 60、金刚石、石墨都是碳元素的同素异形体 C .HClO 、H 2SO 4(浓)、HNO 3都是强氧化性酸D .Na 2O 2、Cl 2、SO 2都能使紫色石蕊溶液褪色 【答案】D 【详解】A .氯水是氯气的水溶液,氨水是氨气的水溶液,漂白粉是氯化钙和次氯酸钙的混合物,都属于混合物,选项A 正确;B .C 60、石墨和金刚石都是碳元素形成的不同单质,属于同素异形体,选项B 正确; C .HClO 、H 2SO 4(浓)、HNO 3都具有强氧化性,是强氧化性酸,选项C 正确;D .Na 2O 2、Cl 2都能使紫色石蕊溶液褪色,SO 2只能使紫色石蕊溶液变红而不能褪色,选项D 不正确; 答案选D 。
2.一定量的SO 2与NaOH 溶液反应,所得产物中含有Na 2SO 3和NaHSO 3,物质的量之比为2∶3,则参加反应的SO 2与NaOH 的物质的量之比为( ) A .1∶2 B .3∶5C .5∶7D .8∶11【答案】C 【详解】假设Na 2SO 3和NaHSO 3的物质的量分别为x 、y ,由原子守恒可知,则SO 2的物质的量为x+y ,NaOH 的物质的量为2x+y ;由于x :y=2:3,则参加反应的SO 2与与NaOH 的物质的量之比为2x y x y++=23223x x x x++=5:7,故答案选C 。
3.下列操作或叙述正确的是( )A .向无色溶液中加入BaCl 2溶液有白色沉淀出现,再加盐酸沉淀不消失,该溶液中一定含有SO 42-B .向某溶液中加入浓氢氧化钠溶液并加热,用湿润的红色石蕊试纸进行如图所示操作来检验溶液中是否存在NH 4+C .将某固体试样完全溶于盐酸,再滴加KSCN 溶液,没有出现血红色,该固体试样中也可能存在Fe 3+D.向无色溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体,则该溶液中一定含有CO32-【答案】C【详解】A、向无色溶液中加入BaCl2溶液有白色沉淀出现,再加盐酸沉淀不消失,该沉淀不一定是BaSO4,也有可能是AgCl,该现象说明该溶液中可能含SO42-,也可能含Cl-;检验SO42-的方法是向无色溶液中先加入HCl,若无明显现象,再加入BaCl2溶液,出现白色沉淀说明无色溶液中含有SO42-,A错误;B、应将用镊子夹住试纸放在试管口,B错误;C、固体样品中可能含有Fe和Fe2O3,加入盐酸后,Fe可以和Fe3+反应,使得溶液中没有Fe3+,再加入KSCN溶液,溶液不变红,C正确;D、能使澄清石灰水变浑浊的气体不一定是CO2,也可能是SO2;此外,和盐酸反应生成CO2、SO2的离子有CO32-、HCO3-或SO32-、HSO3-,D错误;故选C。
高一化学第二学期 第一次 质量检测测试卷含解析

高一化学第二学期第一次质量检测测试卷含解析一、选择题1.有一瓶可能部分被氧化的Na2SO3溶液,某同学取少量此溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。
下述有关此实验的结论正确的是()A.Na2SO3已部分被空气中的氧气氧化B.加入 Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4C.加足量硝酸后的白色沉淀一定是BaSO4D.此实验能确定Na2SO3是否部分被氧化【答案】C【分析】根据题意可知,本题考查物质的检验和鉴别,运用硫酸根的鉴别方法分析。
【详解】A. 取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀,硝酸根离子在酸溶液中具有氧化性,原溶液中可以是硫酸根离子或亚硫酸根离子,故A错误;B.原溶液中可以是硫酸根离子或亚硫酸根离子,加入Ba(NO3)2溶液后,生成的沉淀中不一定含有BaSO4,可能是BaSO3,故B错误;C. 取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀,硝酸根离子在酸溶液中具有氧化性,生成的BaSO3也会被氧化为BaSO4,所以加硝酸后生成沉淀一定是BaSO4,故C正确;D. 硝酸根离子在酸溶液中具有氧化性,原溶液中可以是硫酸根离子或亚硫酸根离子,此实验不能确定Na2SO3是否部分被氧化,故D错误;答案选C。
2.下列有关物质检验方法不合理的是( )A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显血红色,该溶液中一定含有Fe2+B.用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2C.检验亚硫酸盐是否已氧化变质,可滴入硝酸酸化的BaCl2溶液,再观察溶液是否有沉淀生成。
D.向某溶液中加入NaOH溶液产生红褐色沉淀,说明溶液中含有Fe3+【答案】C【详解】A.滴加KSCN溶液,溶液不变色,则不含铁离子,滴加氯水后溶液显血红色,可知亚铁离子被氧化为铁离子,则原溶液中一定含Fe2+,故A正确;B.KMnO4溶液与FeCl3溶液不发生反应,但与亚铁离子发生氧化还原反应,则用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2,故B正确;C.酸性条件下亚硫酸根离子被硝酸根离子氧化生成硫酸根离子,不能检验,应该滴入盐酸酸化的BaCl2溶液,再观察溶液是否有沉淀生成,故C错误;D.加NaOH溶液产生红褐色沉淀氢氧化铁,则说明溶液中含有Fe3+,故D正确;故选C。
人教版高一第二学期 第一次段考化学试卷及答案

人教版高一第二学期 第一次段考化学试卷及答案一、选择题1.不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是( )A .①②③④B .②③④⑤C .①③④D .②③④【答案】A 【解析】 【详解】①由于石灰水过量,因此必有3CaCO 和3CaSO 沉淀生成,故①正确;②同样由于石灰水过量,因此必有3CaCO 沉淀生成,故②正确;2CO ③气体与32Ba(NO )不反应,2SO 气体通入32Ba(NO )溶液后,由于溶液酸性增强,2SO 将被3NO -氧化生成24SO -,因此有4BaSO 沉淀生成,故③正确;2NO ④和2SO 混合后,2SO 将被2NO 氧化成3SO ,通入2BaCl 溶液后有4BaSO 沉淀生成,故④正确;⑤当3NH 过量时溶液中3CaCO 沉淀生成,发生反应的化学方程式为:3222342NH CO CaCl H O CaCO 2NH Cl +++=↓+;当3NH 不足时,最终无沉淀生成,发生反应的化学方程式为:32223242NH 2CO CaCl 2H O Ca(HCO )2NH Cl +++=+,故⑤错误。
故选A 。
【点睛】本题考查元素化合物知识,注意丙过量,对相应物质的化学性质要掌握到位。
解题时要认真审题、一一排查,同时要掌握2NO 的氧化性,2SO 具有还原性,2SO 具有酸性氧化物的性质、2SO 气体通入32Ba(NO )溶液后,由于溶液酸性增强,2SO 将被3NO -氧化生成24SO -,此时有4BaSO 沉淀生成。
2.下图是一检验气体性质的实验装置。
向装置中缓慢通入气体X ,若关闭活塞K ,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞K ,则品红溶液褪色。
据此判断气体X 和洗气瓶内液体Y(足量)可能是( )选项 A B C D X CO SO 2CO 2 Cl 2Y浓H 2SO 4NaHCO 3饱和溶液Na 2SO 3溶液NaHSO 3饱和溶液A .AB .BC .CD .D【答案】B 【详解】A .CO 不能使品红褪色,A 错误;B .若关闭活塞K ,SO 2与NaHCO 3溶液反应生成CO 2气体,品红溶液无变化,澄清石灰水变浑浊;若打开活塞K ,SO 2使品红褪色,B 正确;C .CO 2与Na 2SO 3溶液不反应,且不能是品红褪色,C 错误;D .Cl 2与饱和NaHSO 3溶液发生氧化还原反应,Cl 2不能使澄清石灰水变浑浊,D 错误。
高一化学第二学期 第一次 质量检测测试卷及解析

高一化学第二学期第一次质量检测测试卷及解析一、选择题1.下列“实验结论”与“实验操作及现象”相符的一组是()A.A B.B C.C D.D【答案】D【详解】A. 向某溶液中加入AgNO3溶液,有白色沉淀生成,则原溶液中可能含Cl−或SO42-等,A错误;B. 向某溶液中加入稀盐酸,有无色气体产生,则原溶液中可能含CO32−或SO32−,或HCO3−等,B错误;C. 向某溶液中加入BaCl2溶液,有白色沉淀生成,则溶液中可能含有SO42−或Ag+,但二者不能同时存在,C错误;D. 向某溶液中加入NaOH溶液,立即产生红褐色沉淀,则沉淀为氢氧化铁,该溶液中一定含有Fe3+,D正确;故答案为:D。
2.下列“解释或结论”与“实验操作及现象”不相符的一组是A.A B.B C.C D.D【答案】C【详解】A、浓硫酸具有强脱水性,遇到有机物后,“强行”以H2O的形式脱去有机物中的H、O元素,从而使有机物碳化变黑,A正确;B、氯水中含有HCl和HClO,HCl使石蕊变红,HClO再氧化石蕊成无色物质,氯水的酸性主要靠HCl体现,漂白性靠HClO体现,B正确;C、能使澄清石灰水变浑浊的气体不一定是CO2,还可能是SO2,故该溶液中的离子可能是CO32-、HCO3-、SO32-、HSO3-中的一种或者几种,C错误;D、能使湿润的红色石蕊试纸变蓝的气体是NH3,NH4+和强碱溶液在加热的条件下,可以反应产生NH3,D正确;故选C。
【点睛】能使澄清石灰水变浑浊的气体,一般认为是CO2,和酸反应产生CO2的离子有CO32-、HCO3-,在分析时,这两种离子都要考虑到;此外,SO2也能使澄清石灰水变浑浊,故若题中没有说明,也要考虑到SO2,相应的,和酸反应产生SO2的离子有SO32-、HSO3-。
3.下列关于金属的说法正确的是()A.金属单质在氧化还原反应中常作还原剂B.金属在加热条件下都易与氧气反应C.加热条件下铜与硫蒸气反应生成硫化铜D.铁丝能在氯气中燃烧生成氯化亚铁【答案】A【详解】A、金属元素的最低价为0价,金属单质在氧化还原反应中化合价升高,作还原剂,故A 正确;B、金、铂等不活泼金属在加热条件不易与氧气反应,故B错误;C、硫的氧化性弱,加热条件下铜与硫蒸气反应生成硫化亚铜,故C错误;D、氯气的氧化性强,铁丝能在氯气中燃烧生成氯化铁,故D错误。
高一化学(下)学期 第一次质量检测测试卷及答案

高一化学(下)学期第一次质量检测测试卷及答案一、选择题1.有一瓶可能部分被氧化的Na2SO3溶液,某同学取少量此溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。
下述有关此实验的结论正确的是()A.Na2SO3已部分被空气中的氧气氧化B.加入 Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4C.加足量硝酸后的白色沉淀一定是BaSO4D.此实验能确定Na2SO3是否部分被氧化【答案】C【分析】根据题意可知,本题考查物质的检验和鉴别,运用硫酸根的鉴别方法分析。
【详解】A. 取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀,硝酸根离子在酸溶液中具有氧化性,原溶液中可以是硫酸根离子或亚硫酸根离子,故A错误;B.原溶液中可以是硫酸根离子或亚硫酸根离子,加入Ba(NO3)2溶液后,生成的沉淀中不一定含有BaSO4,可能是BaSO3,故B错误;C. 取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀,硝酸根离子在酸溶液中具有氧化性,生成的BaSO3也会被氧化为BaSO4,所以加硝酸后生成沉淀一定是BaSO4,故C正确;D. 硝酸根离子在酸溶液中具有氧化性,原溶液中可以是硫酸根离子或亚硫酸根离子,此实验不能确定Na2SO3是否部分被氧化,故D错误;答案选C。
2.下列有关物质检验方法不合理的是( )A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显血红色,该溶液中一定含有Fe2+B.用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2C.检验亚硫酸盐是否已氧化变质,可滴入硝酸酸化的BaCl2溶液,再观察溶液是否有沉淀生成。
D.向某溶液中加入NaOH溶液产生红褐色沉淀,说明溶液中含有Fe3+【答案】C【详解】A.滴加KSCN溶液,溶液不变色,则不含铁离子,滴加氯水后溶液显血红色,可知亚铁离子被氧化为铁离子,则原溶液中一定含Fe2+,故A正确;B.KMnO4溶液与FeCl3溶液不发生反应,但与亚铁离子发生氧化还原反应,则用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2,故B正确;C.酸性条件下亚硫酸根离子被硝酸根离子氧化生成硫酸根离子,不能检验,应该滴入盐酸酸化的BaCl 2溶液,再观察溶液是否有沉淀生成,故C 错误;D .加NaOH 溶液产生红褐色沉淀氢氧化铁,则说明溶液中含有Fe 3+,故D 正确; 故选C 。
人教版高一第二学期 第一次段考化学试卷及解析
人教版高一第二学期第一次段考化学试卷及解析一、选择题1.下列有关实验操作、现象和解释或结论都正确的是选项实验操作现象解释或结论A将水蒸气通过灼热的铁粉粉末变红铁与水在高温下发生反应B将Na投入到CuSO4溶液中生成气体,并有固体产生气体是H2,固体是CuC将SO2通入滴有酚酞的氨水中溶液红色褪去SO2是酸性氧化物D 向某溶液中先加入少量BaCl2溶液,再加入足量盐酸产生白色沉淀原溶液是硫酸溶液A.A B.B C.C D.D【答案】C【详解】A.将水蒸气通过灼热的铁粉,反应生成黑色的四氧化三铁固体,说明铁在高温下和水反应,故A错误;B.将Na投入到CuSO4溶液中,钠先与水反应生成氢氧化钠和氢气,氢氧化钠与硫酸铜反应生成硫酸钠和氢氧化铜沉淀,故B错误C.二氧化硫是酸性氧化物,能与氢氧化钠反应生成亚硫酸钠或亚硫酸氢钠,碱性减弱,红色褪去,与漂白性无关,体现二氧化硫是酸性氧化物,故正确;D.先加氯化钡溶液,后加稀盐酸有白色沉淀生成,原溶液中可能存在Ag+,故D错误;故选:C。
【点睛】检验硫酸根离子,先滴加盐酸没有现象,再滴加氯化钡溶液,出现白色沉淀,滴加的顺序不能颠倒。
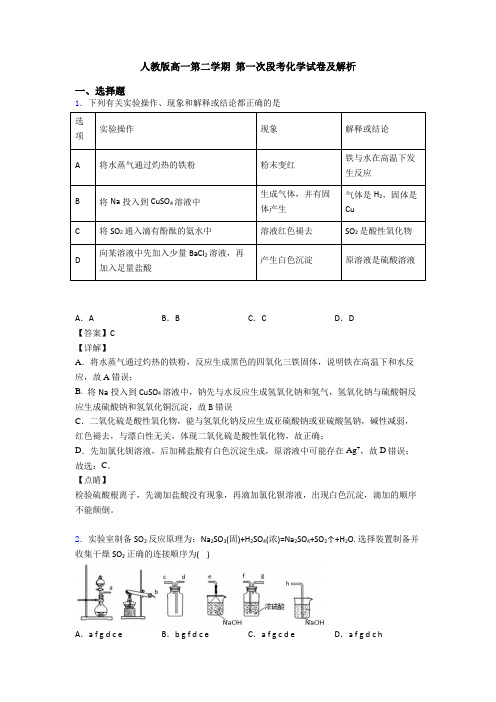
2.实验室制备SO2反应原理为:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O. 选择装置制备并收集干燥SO2正确的连接顺序为( )A.a f g d c e B.b g f d c e C.a f g c d e D.a f g d c h【答案】A【详解】该实验的目的是制备并收集干燥SO2,根据题中的方程式可知,该反应的发生装置是固液不加热型(可选A装置),然后将气体经过E装置来干燥SO2,用C装置收集SO2,D装置作尾气处理装置;由于SO2的密度比空气大,需要用向上排气法收集,SO2应从d口进入C 装置;D装置和F装置相比,D装置可以防止倒吸,更为安全;综上所述,正确的连接顺序为a f g d c e,故选A。
高一(下)学期 第一次 质量检测化学试卷及解析
高一(下)学期第一次质量检测化学试卷及解析一、选择题1.有一瓶可能部分被氧化的Na2SO3溶液,某同学取少量此溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。
下述有关此实验的结论正确的是()A.Na2SO3已部分被空气中的氧气氧化B.加入 Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4C.加足量硝酸后的白色沉淀一定是BaSO4D.此实验能确定Na2SO3是否部分被氧化【答案】C【分析】根据题意可知,本题考查物质的检验和鉴别,运用硫酸根的鉴别方法分析。
【详解】A. 取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀,硝酸根离子在酸溶液中具有氧化性,原溶液中可以是硫酸根离子或亚硫酸根离子,故A错误;B.原溶液中可以是硫酸根离子或亚硫酸根离子,加入Ba(NO3)2溶液后,生成的沉淀中不一定含有BaSO4,可能是BaSO3,故B错误;C. 取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀,硝酸根离子在酸溶液中具有氧化性,生成的BaSO3也会被氧化为BaSO4,所以加硝酸后生成沉淀一定是BaSO4,故C正确;D. 硝酸根离子在酸溶液中具有氧化性,原溶液中可以是硫酸根离子或亚硫酸根离子,此实验不能确定Na2SO3是否部分被氧化,故D错误;答案选C。
2.下列有关物质检验方法不合理的是( )A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显血红色,该溶液中一定含有Fe2+B.用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2C.检验亚硫酸盐是否已氧化变质,可滴入硝酸酸化的BaCl2溶液,再观察溶液是否有沉淀生成。
D.向某溶液中加入NaOH溶液产生红褐色沉淀,说明溶液中含有Fe3+【答案】C【详解】A.滴加KSCN溶液,溶液不变色,则不含铁离子,滴加氯水后溶液显血红色,可知亚铁离子被氧化为铁离子,则原溶液中一定含Fe2+,故A正确;B.KMnO4溶液与FeCl3溶液不发生反应,但与亚铁离子发生氧化还原反应,则用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2,故B正确;C.酸性条件下亚硫酸根离子被硝酸根离子氧化生成硫酸根离子,不能检验,应该滴入盐酸酸化的BaCl2溶液,再观察溶液是否有沉淀生成,故C错误;D.加NaOH溶液产生红褐色沉淀氢氧化铁,则说明溶液中含有Fe3+,故D正确;故选C。
人教版高一(下)学期 第一次质量检测化学试卷含解析
人教版高一(下)学期第一次质量检测化学试卷含解析一、选择题1.以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下,下列说法不正确...的是( )A.焙烧时产生的SO2气体可以用NaOH溶液吸收B.滤液中的铝元素主要以AlO2-存在,可以往滤液中通入过量二氧化碳,经过滤、灼烧生产氧化铝C.可以将少量Fe3O4产品溶于稀硫酸中,再滴入酸性高锰酸钾溶液,若溶液褪色则证明产品中含有FeOD. Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16【答案】C【分析】高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)粉碎后通入空气、加入氧化钙焙烧,其中氧化钙和二氧化硫反应生成亚硫酸钙,和二氧化硅反应生成硅酸钙,得到产物加入氢氧化钠溶液碱浸其中氧化铝溶解生成偏铝酸钠溶液,经操作Ⅰ得到的固体中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,以此解答该题。
【详解】A.二氧化硫可与氢氧化钠溶液反应而被吸收,避免污染环境,A正确;B.向“过滤”得到的滤液中通入过量CO2,可以将AlO2-转化为Al(OH)3,灼烧可生成氧化铝,B正确;C.Fe3O4产品溶于稀硫酸中,可生成硫酸亚铁,可与酸性高锰酸钾溶液反应,不能证明产品中含有FeO,C错误;D.“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,设有x mol Fe2O3和y mol FeS2完全参加反应,根据电子得失守恒:2x×(3-8 3)=2y×5+y×(83-2),解得xy=16,所以理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16,D正确;故合理选项是C。
人教版高一第二学期 第一次段考化学试卷含答案
人教版高一第二学期第一次段考化学试卷含答案一、选择题1.以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下,下列说法不正确...的是( )A.焙烧时产生的SO2气体可以用NaOH溶液吸收B.滤液中的铝元素主要以AlO2-存在,可以往滤液中通入过量二氧化碳,经过滤、灼烧生产氧化铝C.可以将少量Fe3O4产品溶于稀硫酸中,再滴入酸性高锰酸钾溶液,若溶液褪色则证明产品中含有FeOD. Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16【答案】C【分析】高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)粉碎后通入空气、加入氧化钙焙烧,其中氧化钙和二氧化硫反应生成亚硫酸钙,和二氧化硅反应生成硅酸钙,得到产物加入氢氧化钠溶液碱浸其中氧化铝溶解生成偏铝酸钠溶液,经操作Ⅰ得到的固体中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,以此解答该题。
【详解】A.二氧化硫可与氢氧化钠溶液反应而被吸收,避免污染环境,A正确;B.向“过滤”得到的滤液中通入过量CO2,可以将AlO2-转化为Al(OH)3,灼烧可生成氧化铝,B正确;C.Fe3O4产品溶于稀硫酸中,可生成硫酸亚铁,可与酸性高锰酸钾溶液反应,不能证明产品中含有FeO,C错误;D.“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,设有x mol Fe2O3和y mol FeS2完全参加反应,根据电子得失守恒:2x×(3-8 3)=2y×5+y×(83-2),解得xy=16,所以理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16,D正确;故合理选项是C。
高一化学第二学期第一次质量检测测试卷及解析
高一化学第二学期第一次质量检测测试卷及解析一、选择题1.下列有关化学反应的叙述正确酌是A .常温下铜在浓硝酸中发生钝化B .氯气和烧碱反应可制取漂白粉C .碳酸氢钠固体受热分解可得到纯碱D .铁和高温水蒸气反应生成铁红【答案】C【详解】A. 常温下铁和铝在浓硝酸中发生钝化,铜不发生钝化,故A 错误;B. 氯气和石灰乳反应可制取漂白粉,故B 错误;C. 碳酸氢钠固体受热分解323222NaHCO Na CO +CO +H O =∆↑可得到纯碱,故C 正确; D. 铁和高温水蒸气反应生成四氧化三铁,故D 错误;故答案选:C 。
2.下列有关说法正确的是( )A .因为硫单质具有氧化性,故铁粉与硫粉共热可以生成Fe 2S 3B .硫在空气中燃烧的产物是SO 2,在纯氧中燃烧的产物是SO 3C .SO 2的水溶液能导电,所以SO 2是电解质D .二氧化硫可用于抑制酒类中细菌的生长,可在葡萄酒中微量添加【答案】D【详解】A. 因为硫单质具有氧化性,但氧化性不强,铁粉与硫粉共热生成FeS ,A 错误;B. 硫在空气中燃烧的产物是SO 2,在纯氧中燃烧的产物也是SO 2,B 错误;C. SO 2的水溶液能导电,因为二氧化硫与水反应生成亚硫酸,亚硫酸是电解质,二氧化硫不是电解质,C 错误;D. 二氧化硫可用于抑制酒类中细菌的生长,可在葡萄酒中微量添加,D 正确; 答案为D 。
【点睛】S 具有弱氧化性,与Fe 反应生成FeS 。
3.下列四种有色溶液与SO 2气体作用,其实质相同的是( )①酸性高锰酸钾溶液;②品红溶液;③溴水;④滴有酚酞的氢氧化钠溶液;A .②③B .①③C .①④D .②④【答案】B【详解】①酸性高锰酸钾溶液与二氧化硫反应发生氧化还原反应,体现二氧化硫的还原性; ②品红溶液与二氧化硫发生非氧化还原反应生成无色的物质,体现二氧化硫的漂白性; ③溴水与二氧化硫反应发生氧化还原反应,体现二氧化硫的还原性;④滴有酚酞的氢氧化钠溶液与二氧化硫反应生成亚硫酸钠和水,体现二氧化硫的酸性;综上所述,①③反应原理相同,答案为B。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高一化学(下)学期第一次段考测试卷及解析一、选择题1.下图是物质间发生化学反应的颜色变化,下表选项物质对应正确的是选项M N P QA NH3·H2O Ba(OH)2铜KSCNB Na BaCl2FeO KSCNC NaOH Ba(NO3)2铁粉KSCND Na2O2MgCl2锌粉KSCNA.A B.B C.C D.D【答案】C【分析】硫酸铁与M发生反应生成红褐色沉淀,红褐色沉淀为Fe(OH)3沉淀,M为碱或与水反应能生成碱的物质。
硫酸铁与N反应生成白色沉淀,可以为BaSO4沉淀,N可能含有Ba2+。
P 与硫酸铁反应生成浅绿色溶液,浅绿色微粒为Fe2+,P起到还原剂的作用;硫酸铁与Q作用溶液变为红色,则Q为硫氰化钾。
【详解】A. N不能是氢氧化钡,因为它与硫酸铁反应除了生成硫酸钡,还会生成氢氧化铁,二者的混合物为红褐色,不是白色沉淀,A错误;B. P不能为氧化亚铁,因为FeO不能与硫酸铁反应生成Fe2+,B错误C. M若为NaOH,与硫酸铁反应生成Fe(OH)3红褐色沉淀;N若为硝酸钡,与硫酸铁反应生成BaSO4白色沉淀;P若为铁粉,还原+3价的Fe3+为+2价的Fe2+,C正确;D. N不能为氯化镁,它不能与硫酸铁反应生成白色沉淀,D错误;故合理选项是C。
【点睛】本题考查了有关铁元素的化学反应,注意各种物质之间的化学反应及常见物质的颜色及溶解性。
2.下图是一检验气体性质的实验装置。
向装置中缓慢通入气体X,若关闭活塞K,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色。
据此判断气体X和洗气瓶内液体Y(足量)可能是()选项A B C DX CO SO2CO2Cl2Y浓H2SO4NaHCO3饱和溶液Na2SO3溶液NaHSO3饱和溶液A.A B.B C.C D.D【答案】B【详解】A.CO不能使品红褪色,A错误;B.若关闭活塞K,SO2与NaHCO3溶液反应生成CO2气体,品红溶液无变化,澄清石灰水变浑浊;若打开活塞K,SO2使品红褪色,B正确;C.CO2与Na2SO3溶液不反应,且不能是品红褪色,C错误;D.Cl2与饱和NaHSO3溶液发生氧化还原反应,Cl2不能使澄清石灰水变浑浊,D错误。
3.下列关于物质的检验说法不正确的是( )SO-A.加入氯化钡溶液有白色沉淀生成,再加稀硝酸沉淀不消失,一定含有24B.观察钾元素焰色反应的操作是:将铂丝用稀盐酸洗涤后灼烧至火焰为无色,然后再用铂丝蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察C.待检液加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液NH+中一定含有4D.待检液加入氯化钡溶液有白色沉淀生成,再加入足量盐酸沉淀消失且产生无色无味的CO-气体,则待检液中一定含有23【答案】A【详解】SO-,还可能含A. 加入氯化钡溶液有白色沉淀生成,再加稀硝酸沉淀不消失,可能含有24SO-,所以A错误;有SO32-被硝酸氧化成24B. 观察钾元素焰色反应的操作是:将铂丝用稀盐酸洗涤后灼烧至火焰为无色,然后再用铂丝蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察,如果火焰呈紫色,说明含有钾元素,故正确;C.加入NaOH 溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,说明有NH 3产生,则原溶液中一定含有4NH +,故C 正确;D. 待检液加入氯化钡溶液有白色沉淀生成,再加入足量盐酸沉淀消失且产生无色无味的CO 2气体,则待检液中一定含有23CO -,故D 正确; 答案:A 。
【点睛】根据离子鉴别方法进行分析。
要鉴别24SO -先加入稀盐酸排除干扰离子;要鉴别4NH +选择强碱和湿润的红色石蕊试纸;要鉴别23CO -需加入氯化钡溶液有白色沉淀生成,再加入足量盐酸沉淀消失且产生无色无味的气体。
4.下列四种有色溶液与SO 2气体作用,其实质相同的是( )①酸性高锰酸钾溶液;②品红溶液;③溴水;④滴有酚酞的氢氧化钠溶液; A .②③ B .①③C .①④D .②④【答案】B 【详解】①酸性高锰酸钾溶液与二氧化硫反应发生氧化还原反应,体现二氧化硫的还原性; ②品红溶液与二氧化硫发生非氧化还原反应生成无色的物质,体现二氧化硫的漂白性; ③溴水与二氧化硫反应发生氧化还原反应,体现二氧化硫的还原性;④滴有酚酞的氢氧化钠溶液与二氧化硫反应生成亚硫酸钠和水,体现二氧化硫的酸性; 综上所述,①③反应原理相同,答案为B 。
5.为了确定某物质是否变质,所选试剂(括号内物质)达不到实验要求的是( ) A .K 2SO 3是否被氧化(BaCl 2溶液) B .新制氯水已经完全变质(紫色石蕊试液) C .KI 是否被氧化(淀粉溶液) D .FeSO 4是否被氧化(KSCN 溶液)【答案】A 【详解】A 、K 2SO 3在空气中会被氧化为K 2SO 4,K 2SO 3、K 2SO 4和BaCl 2反应都会生成白色沉淀,故BaCl 2溶液不能达到实验要求,A 错误;B 、新制氯水中存在Cl 2+H 2OHClO+HCl ,HClO 不稳定、易分解,随着HClO 的分解,平衡不断右移,最终新制氯水会变质为盐酸溶液,失去漂白性,故使用紫色石蕊试液,若溶液变红后,不褪色,可以说明氯水完全变质,即紫色石蕊试液能达到实验要求,B 正确; C 、KI 会被空气氧化生成I 2,I 2遇到淀粉溶液,溶液会显蓝色,故淀粉溶液能达到实验要求,C 正确;D 、FeSO 4会被空气氧化为Fe 2(SO 4)3,加入KSCN 溶液,若溶液变红,则说明FeSO 4已被氧化,故KSCN 溶液能达到实验要求,D 正确; 故选A 。
6.由下列实验及现象,推出的相应结论正确的是实验现象结论A.用铂丝蘸取某金属的盐溶液,火焰呈黄色此盐溶液中含有 Na+,不含 K+在酒精灯火焰上灼烧B.向饱和NaHCO3溶液中加入足量有无色气体产生氯水中含HClO氯水C.将足量SO2气体通入石蕊试液中石蕊试液变红色SO2水溶液显酸性D.向酸性KMnO4溶液中通入SO2溶液紫色褪去SO2具有漂白性A.A B.B C.C D.D【答案】C【详解】A.钾的焰色是浅紫色,容易被钠的黄色火焰所掩盖,因此要在蓝色钴玻璃下进行观察才能确定有没有钾元素,A项错误;CO,B.酸性:盐酸大于碳酸,碳酸大于次氯酸;因此次氯酸不可能与碳酸氢钠反应得到2应该考虑是盐酸的影响,B项错误;SO的水溶液显酸性,C项正确;C.石蕊变红则证明溶液显酸性,因此说明2SO和高锰酸钾之间发生的是氧化还原反应导致褪色,与漂白性无关,D项错误;D.2答案选C。
【点睛】二氧化硫能够漂白一些有机色质,如品红溶液,属于非氧化性漂白;而二氧化硫在与酸性高锰酸钾溶液、溴水、氯化铁等溶液反应时,体现了二氧化硫的强的还原性,导致了溶液的颜色发生了变化,而非漂白性。
7.如图是产生和收集气体的实验装置,该装置最适合于A.用 H2O2溶液和 MnO2反应制取O2B.用浓盐酸和 MnO2反应制取C12C.用浓硝酸与 Cu反应制取 NO2D.用Na2SO3和浓H2SO4反应制取SO2【答案】A【详解】A. 用 H2O2溶液和 MnO2反应制取O2,固体不加热,故A符合;B. 用浓盐酸和 MnO2反应制取C12,是固体加热,故B不符;C. 用浓硝酸与 Cu反应制取 NO2,不能用排水法收集,故C不符;D. 用Na2SO3和浓H2SO4反应制取SO2,SO2在水中溶解度大,不用排水法收集,故D错误;故选A。
8.下列关于金属的说法正确的是()A.金属单质在氧化还原反应中常作还原剂B.金属在加热条件下都易与氧气反应C.加热条件下铜与硫蒸气反应生成硫化铜D.铁丝能在氯气中燃烧生成氯化亚铁【答案】A【详解】A、金属元素的最低价为0价,金属单质在氧化还原反应中化合价升高,作还原剂,故A 正确;B、金、铂等不活泼金属在加热条件不易与氧气反应,故B错误;C、硫的氧化性弱,加热条件下铜与硫蒸气反应生成硫化亚铜,故C错误;D、氯气的氧化性强,铁丝能在氯气中燃烧生成氯化铁,故D错误。
9.把70 mL硫化氢和90 mL氧气(标准状况)混合,在一定条件下点燃,使之反应。
当反应完全后恢复到原来状况时,可得到SO2的体积是(不考虑二氧化硫在水中溶解)() A.50 mL B.55 mL C.60 mL D.70 mL【答案】B【详解】H2S完全燃烧的化学方程式为:2H2S+3O22SO2+2H2O,根据方程式可知90mLO2完全反应消耗60mLH2S,同时产生60mLSO2,剩余10mL H2S,剩余H2S与反应产生的SO2会进一步发生反应:SO2+2H2S=3S+2H2O,10mLH2S反应消耗5mL SO2,因此充分反应后,剩余SO2气体的体积是60mL-5mL=55mL,故合理选项是B。
10.下列关于单质硫的叙述中正确的是()A.硫的活泼性不如氯气B.硫在过量纯氧中的燃烧产物是三氧化硫C.硫与金属单质或非金属单质反应均做氧化剂D.硫与铁反应产物为Fe2S3【答案】A【详解】A.硫元素和氯元素在同一周期,氯元素的非金属性比硫元素强,硫的活泼性不如氯气,故A正确;B.硫燃烧时只能生成SO2,SO3可由SO2催化氧化制取,故B错误;C.硫与非金属单质反应时可以做氧化剂也可以做还原剂,如硫与O2反应时做还原剂,硫与H2反应时做氧化剂,故C错误;D.硫与变价金属反应的产物为金属的低价态硫化物,故D错误;故选:A。
11.CuSO4•5H2O在不同温度下分解情况不同,取5.00g该晶体在密闭容器中进行实验,测得分解后剩余固体质量与温度关系如图,下列说法不正确...的是( )A.113℃分解得到的固体产物为CuSO4•H2OB.温度低于650℃时的分解反应,均不属于氧化还原反应C.650℃时的气态产物冷却至室温,可得组成为n(H2SO4):n(H2O)=1:4的硫酸溶液D.1000℃分解得到的固体产物为CuO【答案】D【分析】n(CuSO4•5H2O)=5.00g250g/mol=0.02mol,CuSO4•5H2O完全失去结晶水时,所得CuSO4的质量为0.02mol×160g/mol=3.20g,由图中可知,刚好位于温度在258~650℃之间,说明在此之前,胆矾受热分解,只失去结晶水;650~1000℃之间,固体质量为1.60g,其中Cu元素的质量为0.02mol×64g/mol=1.28g,则氧元素质量为1.60g-1.28g=0.32g,物质的量为0.32g16g/mol=0.02mol,此固体为CuO;1000℃之后,固体质量为1.44g,其中Cu元素质量为1.28g,则氧元素质量为1.44g-1.28g=0.16g,物质的量为0.16g16g/mol=0.01mol,此固体为Cu2O。
