饲料中粗蛋白测定方法审批稿
饲料中粗蛋白测定方法

饲料中粗蛋白测定方法 Document serial number【KKGB-LBS98YT-BS8CB-BSUT-BST108】饲料中粗蛋白测定方法1、原理凯氏法测定试样中的含氮量,即在催化剂作用下,用硫酸破坏有机物,使含氮物转化成硫酸铵。
加入强碱进行蒸馏使氨逸出,用硼酸吸收后,再用酸滴定,测出氮含量,将结果乘以换算系数6.25,计算出粗蛋白含量。
2、试剂2.1硫酸(GB625):化学纯,含量为98%,无氮。
2.2混合催化剂:0.4g硫酸铜,5个结晶水(GB665),6g硫酸钾(HG3—920)或硫酸钠(HG3—908),均为化学纯,磨碎混匀。
2.3氢氧化钠(GB629):化学纯,40%水溶液(m/V)。
2.4硼酸(GB628):化学纯,2%水溶液(m/V)。
2.5混合指示剂:甲基红(HG3—958)0.1%乙醇溶液,溴甲酚绿(HG3—1220)0.5%乙醇溶液,两溶液等体积混合,在阴凉处保存期为三个月。
2.6盐酸标准溶液:邻苯二甲酸氢钾法标定,按GB601制备。
2.6.1盐酸标准溶液:c(HCl)=0.1mol/L。
8.3mL盐酸(GB622,分析纯),注入1000mL蒸馏水中。
2.6.2盐酸标准溶液:c(HCl)=0.02mol/L。
1.67mL盐酸(GB622,分析纯),注入1000mL蒸馏水中。
2.7蔗糖(HG3—1001):分析纯。
2.8硫酸铵(GB1396):分析纯,干燥。
2.9硼酸吸收液:1%硼酸水溶液1000mL,加入0.1%溴甲酚绿乙醇溶液10mL,0.1%甲基红乙醇溶液7mL,4%氢氧化钠水溶液0.5mL,混合,置阴凉处保存期为一个月(全自动程序用)。
3、仪器设备3.1实验室用样品粉碎机或研钵。
3.2分样筛:孔径0.45mm(40目)。
3.3分析天平:感量0.0001g。
3.4消煮炉或电炉。
3.5滴定管:酸式,10、25mL。
3.6凯氏烧瓶:250mL。
3.7凯氏蒸馏装置:半微量水蒸气蒸馏式。
饲料中粗蛋白的测定度-不确定度评估
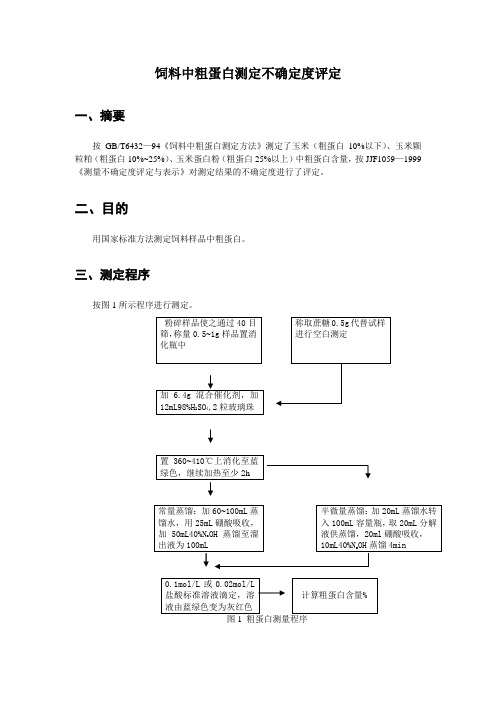
饲料中粗蛋白测定不确定度评定一、摘要按GB/T6432—94《饲料中粗蛋白测定方法》测定了玉米(粗蛋白10%以下)、玉米颗粒粕(粗蛋白10%~25%)、玉米蛋白粉(粗蛋白25%以上)中粗蛋白含量,按JJF1059—1999《测量不确定度评定与表示》对测定结果的不确定度进行了评定。
二、目的用国家标准方法测定饲料样品中粗蛋白。
三、测定程序按图1所示程序进行测定。
图1 粗蛋白测量程序四、被测量粗蛋白含量以占样品质量的百分比表示式中:V 1—滴定试样时所需酸标准溶液体积,mL ; V 2—滴定空白时所需酸标准溶液体积,mL ; C — 酸标准溶液浓度,mol/L ; m — 试样质量,g ;V — 试样分解液总体积,mL ; V 3—试样分解液蒸馏用体积,mL ; 0.0140— 每毫摩尔质量氮的克数;6.25— 氮换算成蛋白质的平均系数。
五、不确定度来源分析不确定度来源见图2— 因果关系图图2 因果关系图10025.60140.0)(321⨯⨯⨯⨯⨯-=Vm C V V P称样m滴定试样(空白)用标液体积V 1、V 2重复性(r)摩尔质量M(N)六、不确定度分量的量化1、 标准溶液浓度标准溶液浓度不确定度是测量不确定度的主要分量之一,同时,标准溶液浓度不确定度也是由多个分量合成所得,按GB601—88《化学试剂 标准溶液制备方法》,使用的盐酸标准溶液是采用标定法配制而成,下面详细描述配制过程。
1.1目的以无水碳酸钠(Na 2CO 3)基准标定0.1mol/L (或0.02mol/L )盐酸溶液。
1.2标定程序见图3,按GB601—88标准有标定程序框图图3 标定程序框图 1.3被测量按下式计算盐酸标准溶液的浓度(GB601-88)05299.0)V V (m C 21⨯=-式中:m —无水碳酸钠质量,g;V 1—滴定用盐酸溶液体积,mL;量取9mL 盐酸注入1000mL 水中V 2—空白试验用盐酸溶液体积,mL;0.05299—每1/2毫摩尔质量碳酸钠的克数。
饲料中粗蛋白测定方法

饲料中粗蛋白测定方法1、原理凯氏法测定试样中的含氮量,即在催化剂作用下,用硫酸破坏有机物,使含氮物转化成硫酸铵.加入强碱进行蒸馏使氨逸出,用硼酸吸收后,再用酸滴定,测出氮含量,将结果乘以换算系数,计算出粗蛋白含量.2、试剂硫酸GB625:化学纯,含量为98%,无氮.混合催化剂:硫酸铜,5个结晶水GB665,6g硫酸钾HG3—920或硫酸钠HG3—908,均为化学纯,磨碎混匀.氢氧化钠GB629:化学纯,40%水溶液m/V.硼酸GB628:化学纯,2%水溶液m/V.混合指示剂:甲基红HG3—958%乙醇溶液,溴甲酚绿HG3—1220%乙醇溶液,两溶液等体积混合,在阴凉处保存期为三个月.盐酸标准溶液:邻苯二甲酸氢钾法标定,按GB601制备. 2.6.1盐酸标准溶液:cHCl=L.盐酸GB622,分析纯,注入1000mL蒸馏水中.盐酸标准溶液:cHCl=L.盐酸GB622,分析纯,注入1000mL蒸馏水中.蔗糖HG3—1001:分析纯.硫酸铵GB6:分析纯,干燥.硼酸吸收液:1%硼酸水溶液1000mL,加入%溴甲酚绿乙醇溶液10mL,%甲基红乙醇溶液7mL,4%氢氧化钠水溶液,混合,置阴凉处保存期为一个月全自动程序用.3、仪器设备实验室用样品粉碎机或研钵.分样筛:孔径40目.分析天平:感量.消煮炉或电炉.滴定管:酸式,10、25mL.凯氏烧瓶:250mL.凯氏蒸馏装置:半微量水蒸气蒸馏式.锥形瓶:150、250mL.容量瓶:100mL.消煮管:250mL.定氮仪:以凯氏原理制造的各类型半自动.4、试样的选取和制备选取具有代表性的试样用四分法缩减至200g,粉碎后全部通过40目筛,装于密封容器中,防止试样成分的变化.5分析步骤试样的消煮称取试样~1g含氮量5~80mg准确至,放入凯氏烧瓶中,加入混合催化剂,与试样混合均匀,再加入12mL硫酸和2粒玻璃珠,将凯氏烧瓶置于电炉上加热,开始小火,待样品焦化,泡沫消失后,再加强火力360~410℃直至呈透明的蓝绿色,然后再继续加热,至少2h.氨的蒸馏:将试样消煮液冷却,加入20mL蒸馏水,转入100mL容量瓶中,冷却后用水稀释至刻度,摇匀,做为试样分解液.将半微量蒸馏装置的冷凝管末端浸入装有20mL硼酸吸收液和2滴混合指示剂的锥形瓶内.蒸汽发生器的水中应加入甲基红指示剂数滴,硫酸数滴,在蒸馏过程中保持此液为橙红色,否则需补加硫酸.准确移取试样分解液10~20mL注入蒸馏装置的反应室中,用少量蒸馏水冲洗进样入口,塞好入口玻璃塞,再加10mL氢氧化钠溶液,小心提起玻璃塞使之流入反应室,将玻璃塞塞好,且在入口处加水密封,防止漏气.蒸馏4min降下锥形瓶使冷凝管末端离开吸收液面,再蒸馏1min,用蒸馏水冲洗冷凝管末端,洗液均流入锥形瓶内,然后停止蒸馏.5.1.2.3蒸馏步骤的检验精确称取硫酸铵,代替试样,按步骤进行操作,测得硫酸铵含氮量为±%,否则应检查加碱、蒸馏和滴定各步骤是否正确.滴定用或法蒸馏后的吸收液立即用L或L盐酸标准溶液滴定,溶液由蓝绿色变成灰红色为终点.6、空白测定称取蔗糖,代替试样,按第5章进行空白测定,消耗L 盐酸标准溶液的体积不得超过.消耗L盐酸标准溶液体积不得超过.7、分析结果的表述计算见下式:粗蛋白质%=V2-V1·c××m×V'/V×100式中:V2──滴定试样时所需标准酸溶液体积,mL;V1──滴定空白时所需标准酸溶液体积,mL;c──盐酸标准溶液浓度,mol/L;m──试样质量,g;V──试样分解液总体积,mL;V──试样分解液蒸馏用体积,mL;──与盐酸标准溶液〔cHCl=L〕相当的、以克表示的氮的质量.──氮换算成蛋白质的平均系数.重复性每个试样取两个平行样进行测定,以其算术平均值为结果.当粗蛋白质含量在25%以上时,允许相对偏差为1%.当粗蛋白含量在10%~25%之间时,允许相对偏差为2%.当粗蛋白质含量在10%以下时,允许相对偏差为3%.。
饲料分析与检测实验:饲料中粗蛋白质的测定

实验三、饲料中粗蛋白质的测定【学习目标】掌握饲料中粗蛋白质的测定方法,并能用此方法测定饲料中粗蛋白质的含量。
一、原理饲料中纯蛋白质和非蛋白氮总称粗蛋白质。
凯氏法的基本原理是用浓H2SO4在催化剂(CuSO4、K2SO4、Na2SO4等)的催化作用下消化饲料样本,使其中的蛋白质和非蛋白氮都转变为 (NH4)2SO4,(NH4)2SO4在浓碱作用下放出NH3,通过蒸馏,氨气随水蒸汽沿冷凝管流入硼酸吸收液被硼酸吸收并与之结合成为四硼酸铵,然后以甲基红、溴甲酚绿作指示剂,用标准HCL溶液滴定,求出氮含量,根据氮含量再乘以系数(通常为 6.25),即为粗蛋白质的含量。
上述原理的主要化学反应如下:催化剂1.2CH3CHNH2COOH+13H2SO (NH4)2SO4+6CO2↑+12SO2↑+16H2O加热2.(NH4)2SO4+2NaOH 2NH3↑+2H2O+Na2SO43.4H3BO3+NH3 NH4HB4O7+5H2O4.NH4HB4O7+5H2O+HCL NH4CL+4H3BO3系数6.25是根据饲料蛋白质平均含氮量为16.0%而来的,而实际上,各种样本的蛋白质种类不同,含氮量有差异,变动为14.7~19.5%之间,故一般饲料换算系数用6.25,已确定的最好用实际系数。
为方便使用,将已知几种饲料的系数介绍如下:肉类6.25,玉米6.00,小麦、燕麦、黑麦、大豆、箭舌豌豆、蚕豆5.70,牛奶及制品6.28,坚果及油饼类5.30。
二、仪器设备1.样品粉碎机 40目分样筛;2.分析天平感量0.0001g;3.电子天平感量0.0001g;4.工业天平感量0.01g;5.六联电炉 6×800-1000W;6.半微量凯氏定氮仪或改良式半微量凯氏定氮仪(图1、图2);7.酸式滴定管 25.0ml或50.0ml;8.凯氏烧瓶 100.0ml;9.烧杯 250.0ml;10.三角瓶 150.0ml;11.容量瓶 100.0ml;12.移液管 10.0ml;13.量筒 10.0ml、25.0ml。
饲料粗蛋白实验报告

一、实验目的1. 掌握饲料粗蛋白测定的原理和方法;2. 熟悉实验操作步骤,提高实验技能;3. 了解饲料粗蛋白含量的重要性及其对动物营养的影响。
二、实验原理饲料粗蛋白是指饲料样品中含氮物质的总量,包括蛋白质和非蛋白质含氮化合物。
测定饲料粗蛋白含量,可以了解饲料的营养价值,为动物饲料配方提供依据。
凯氏定氮法是测定饲料粗蛋白的常用方法,其原理如下:1. 将饲料样品与浓硫酸、无水碳酸钠混合,加热消化,使蛋白质和氨态氮转化为硫酸铵;2. 消化液在浓碱的作用下进行蒸馏,释放出的氨随汽水顺着冷凝管流入硼酸吸收液中,并与其结合成硼酸铵;3. 用盐酸标准溶液滴定,求出氨的含量,再乘以一定的换算系数(6.25),即得出试样中粗蛋白的含量。
三、实验材料1. 饲料样品:玉米粉、豆粕、鱼粉等;2. 试剂:浓硫酸、无水碳酸钠、氢氧化钠、硼酸、盐酸标准溶液、甲基红-溴甲酚绿指示剂等;3. 仪器:凯氏瓶、消化炉、冷凝管、滴定管、分析天平等。
四、实验步骤1. 样品消化(1)称取0.5-1g饲料样品,置于凯氏瓶中;(2)加入0.4g无水硫酸铜、6g无水碳酸钠,与试样混合均匀;(3)加入10ml浓硫酸,摇匀;(4)将凯氏瓶置于消化炉上,加热消化,直至溶液呈透明蓝绿色。
2. 滴定(1)将消化液转移至500ml容量瓶中,用蒸馏水定容;(2)取25ml消化液于锥形瓶中,加入5ml氢氧化钠溶液、5ml硼酸溶液、1滴甲基红-溴甲酚绿指示剂;(3)用盐酸标准溶液滴定至溶液由蓝绿色变为灰绿色;(4)记录盐酸标准溶液的消耗体积。
3. 计算(1)根据滴定结果,计算氨的物质的量;(2)乘以换算系数(6.25),得出饲料样品中粗蛋白的含量。
五、实验结果与分析1. 实验数据样品名称 | 样品质量(g) | 盐酸标准溶液消耗体积(ml) | 粗蛋白含量(%)------- | -------- | ------------------- | --------玉米粉 | 0.5 | 25.00 | 9.20豆粕 | 0.5 | 30.00 | 38.40鱼粉 | 0.5 | 35.00 | 58.002. 结果分析通过实验,我们得到了玉米粉、豆粕、鱼粉的粗蛋白含量分别为9.20%、38.40%、58.00%。
饲料中粗蛋白的测定方法

• 蒸馏:样液中的硫酸铵在碱性条件下释放出氨
(NH4)2SO4+2NaOH→2NH3↑+Na2SO4+2H2O
• 滴定:用硼酸溶液吸收氨后,再用标准盐酸溶液滴定
2NH3+4H3BO3 =(NH4)2B4O7+5H2O (NH4)2B4O7+HCL +5H2O =2NH4CL+4H3BO3
三、消化过程
1:消化过程: 样品中的有机物和含N有机化合物,经浓H2SO4加 热消化, H2SO4使有机物脱水,炭化为碳、氢、氮; 碳将H2SO4还原为SO2,而本身则变为CO2; SO2 使N还原为NH3,而本身则氧化为SO3,消化过程中 所产生的新生态氢,加速了氨的行成。在反应中生 成物CO2、H2O和SO2、 SO3逸出,而NH3与H2SO4 结合生成(NH4)2SO4留在消化液中。 蛋白质+ H2SO4 C C+ H2SO4 SO2+ CO2 SO2+[N] NH3+ SO3 NH3+ H2SO4 (NH4)2SO4
混合指示剂
标准盐酸溶液滴定吸收液中的氨的PH值突跃 范围为6.3-4.3
指示剂名称 溴甲酚绿
甲基红 甲基红+溴甲酚绿
PH<5.1 黄色
红色 酒红色
PH=5.1 绿色
橙色 灰色
PH>5.1 蓝色
黄色 蓝绿色
甲基红-溴甲酚绿混合指示剂:pH 5.0 以下为酒 红色,pH 5.1 为灰色,pH 5.2 以上为蓝绿色。 变色域很窄
消化过程注意点
1:加入的催化剂要适量,硫酸钾加入量不能太大,否则温
饲料中粗蛋白的测定(精)
饲料中粗蛋白的测定一、实验目的通过饲料样品中粗蛋白的测定,掌握饲料粗蛋白质含量的测定方法。
二、适用范围本方法适用于配合饲料、浓缩饲料和单一饲料。
三、实验原理凯氏法测定试样中的含氮量,即在催化剂作用下,用浓硫酸破坏有机物,使含氮物转化成硫酸铵。
加入强碱进行蒸馏使氨逸出,用硼酸吸收后,再用酸滴定,测出氮含量,将结果乘以换算系数,计算出粗蛋白含量。
四、试剂(1)硫酸:化学纯,含量为98%,无氮。
(2)混合催化剂:0.4g硫酸铜,5个结晶水;6g硫酸钾或硫酸钠,均为化学纯,磨碎混匀。
(3)氢氧化钠:化学纯,40%水溶液(m/V)。
(4)硼酸:化学纯,2%水溶液(m/V)。
(5)混合指标剂:甲基红%乙醇溶液,溴甲酚绿%乙醇溶液,两溶液等体积混合,在阴凉处保存期为3个月。
(6)盐酸标准溶液:基准无水碳酸钠法标定;① L盐酸标准溶液:盐酸注入1000ml蒸馏水中。
② L盐酸标准溶液:盐酸注入1000ml蒸馏水中。
(7)蔗糖:分析纯。
(8)硫酸铵:分析纯,干燥。
(9)硼酸吸收液:1%硼酸水溶液1000mL,加入%溴甲酚绿乙醇溶液10mL,%甲基红乙醇溶液7mL,4%氢氧化钠水溶液,混合,置阴凉处保存期为1个月(全自动程序用)。
五、仪器设备(1)实验室用样品粉碎机或研钵。
(2)分样筛:孔径0.45mm(40目)。
(3)分析天平:感量0.0001g。
(4)消煮炉或电炉。
(5)滴定管:酸式,10、25mL。
(6)凯氏烧瓶:250mL。
(7)凯氏蒸馏装置:常量直接蒸馏式或半微量水蒸汽蒸馏式。
(8)锥形瓶:150、250mL。
(9)容量瓶:100mL。
(10)消煮管:250mL。
(11)定氮仪:以凯氏原理制造的各类型半自动、全自动蛋白质测定仪。
六、分析步骤试样的选取和制备: 选取具有代表性的试样用四分法缩减至200g,粉碎后全部通过40目筛,装于密封容器中,防止试样成分的变化。
(1)仲裁法①试样的消煮称取试样~1g(含氮量5~80mg)准确至0.0002g,放入凯氏烧瓶中,加入6.4g混合催化剂,与试样混合均匀,再加入12mL硫酸和2粒玻璃珠,将凯氏烧瓶置于电炉上加热,开始小火,待样品焦化,泡沫消失后,再加强火力(360~410℃)直至呈透明的蓝绿色,然后再继续加热,至少2h。
饲料中粗蛋白的测定
饲料中粗蛋白的测定-定氮仪法参照GB/T 6432-941 适用范围本方法适用于配合饲料、浓缩饲料及单一饲料。
2 测定原理在催化剂(如硫酸铜、硫酸钾、硫酸钠或硒粉)作用下,试样中有机物质被浓硫酸消化分解,使含氮物质(蛋白质,氨态氮等)转化为硫酸铵,而非含氮物质则以二氧化碳、水蒸气、二氧化硫等气态逸出。
消化液在强碱作用下蒸馏,释放出氨气,氨气冷凝后被硼酸吸收,并与其结合成硼酸铵,然后以甲基红-溴甲酚绿作混合指示剂,用盐酸标准滴定溶液滴定,求出氮的含量,再乘以一定的换算系数(通常用6.25计算),即得出试样中粗蛋白质的含量。
3 试剂和材料未特殊标注的试剂均为分析纯。
水至少应为GB/T 6682-1992规定的3级3.1 浓硫酸:化学纯。
3.2 400g/L氢氧化钠溶液:400 g氢氧化钠(化学纯),溶于1000 mL水中。
3.3 混合催化剂:取质量比为1:9的五水合硫酸铜(预处理:研磨至粉末状)和无水硫酸钾混合并研磨混匀,装入试剂瓶中密封备用。
3.4 1 g/L甲基红乙醇溶液:称取0.10g甲基红溶于100 mL乙醇中,棕色瓶中保存3个月。
3.5 1 g/L溴甲酚绿乙醇溶液:称取0.10g溴甲酚绿溶于100 mL乙醇中,棕色瓶中保存3个月。
3.6 硼酸吸收液:称取40 g硼酸溶于1 L水中,缓慢加热搅拌溶解,注意加热时不能将溶液加热沸腾,加入溴甲酚绿乙醇溶液(1 g/L)10 ml和甲基红乙醇溶液(1 g/L)6.8 mL,充分混匀。
向其中加入2%的氢氧化钠溶液,直到达到以下要求:取30mL上液于锥形瓶中,加入100 mL水,观察溶液颜色,应为接近盐酸滴定终点的暗灰绿色,以利于蛋白测定中空白的滴定(每10升硼酸溶液约加2%的氢氧化钠溶液3.8mL)。
混合均匀后置阴凉处保存,保存期为1个月。
3.7 0.1 mol/L或0.05mol/L盐酸标准滴定溶液:8.3 ml(或4.15ml)盐酸注入1000 mL水中,用无水碳酸钠法标定。
饲料中粗蛋白含量的测定方法_李晴媛
饲料及饲料添加剂中国畜牧兽医文摘 2013年 29卷 第2期粗蛋白含量是饲料产品质量检测的重要控制指标。
饲料样品中粗蛋白质含量的高低,是评定饲料营养价值的重要因素,决定着配合饲料及饲料原料的成本和价值。
近年来,我国饲料工业发展迅速,饲料产量也随之增长,市场上出售的饲料种类繁多,质量良莠不齐。
国标法测定饲料中的粗蛋白采用的是凯氏定氮法,由于操作的过程比较复杂,如果操作不当,往往会导致检测结果不准确。
1 样品制备一般的饲料样品都是经过一定的采集过程后送检的。
采集方法是否规范,是粗蛋白测定准确与否的基础。
采样方法随不同的物品而有所不同,一般来说,可根据物品均匀性质分为下列两种[1]。
1.1 均匀性质物品对于均匀性质的物品,每一小部分的成分与全部的成分相同,可以采取其任何一部分作为分析样本。
在通常情况下,粉末或研碎后的样品可用“四分法”来采样。
1.2 不均匀性质物品不均匀的物品,须采取多量样本,然后在取出的样本中重复取样多次,得出一连串逐渐减少的样本,叫做初级、次级、三级……样本。
分析用的样本可以在最末一级样本中制备,使样本能代表全部物品。
所采用的取样方法称为“几何法”。
经过采集的样品部分基本代表全部样品的成分,但是,由于饲料在生产过程中的工艺限制,样品颗粒并不均匀,所以在实验前要通过样品粉碎来实现称量样品的均匀性。
根据饲料工业标准标定,样品要求粉碎后全部通过40目(0.45 mm)分样筛,然后混合均匀放入密封容器[2]。
一般饲料样品颗粒较大,成分复杂,检测时称量样品量较少,如果细度不够,必然造成称样时样品不均匀,这是造成结果误差的重要原因。
2 称样用分析天平称取试样0.5~1 g(精确到0.000 1),标准要求做平行样以保证测量结果的准确性,所以需要称样2份。
称样时的称样量要合适,不能太少也不能太多。
一般粗蛋白含量在10%以上的饲料称样量为0.500 0 g即可;若饲料样品中粗蛋白含量较低,如含量为3%~5%的,称样量就应高于0.5000 g,一般称取1.000 g 样品,否则,测定结果的误差就会偏大。
饲料粗蛋白检测方法
饲料粗蛋白的检测方法(凯氏半微量定氮法)1 原理凯氏法测定试样含氮量,即在催化剂存在下,用浓硫酸破坏有机物,使含氮物转化成硫酸铵,加入强碱(NaOH)并蒸馏使氨逸出,用硼酸吸收后,用标准盐酸溶液滴定测出含氮量,将结果乘以换算系数6.25,计算出粗蛋白质含量。
2 仪器设备2.1实验室用样品粉碎机或研钵2.2分样筛:孔径0.45mm(40目)2.3分析天平:感量0.0001g2.4消煮炉或电炉2.5滴定管:酸式25mL2.6凯氏烧瓶:100mL2.7凯氏蒸馏装置:半微量水蒸汽蒸馏式2.8锥形瓶:150mL2.9容量瓶:100mL3 试剂3.1硫酸:分析纯3.2硫酸铜:分析纯3.3硫酸鉀:分析纯3.4硒粉:分析纯3.5氢氧化钠:分析纯40g溶于100mL蒸馏水配成40%水溶液。
3.6硼酸:分析纯2g溶于100mL蒸馏水配成2%水溶液。
3.7混合指示剂:甲基红分析纯0.1%乙醇溶液,溴甲酚绿分析纯0.5%乙醇溶液,两溶液等体积混合,阴凉处保存期三个月以内。
3.8 0.02N盐酸标准溶液:1.67mL盐酸分析纯溶于1000mL 蒸馏水中。
3.8.1 0.02N盐酸标准溶液的标定(碳酸钠法)精确称取0.04g于270—300°C灼烧至恒重的基准级无水碳酸钠,准确至蒸馏水(新做蒸馏水或蒸0.0001g,无损失地转入100 mL三角瓶中,加入无CO2馏水煮沸数分钟放凉后使用)50mL溶解,并加入混合指示剂10滴,用盐酸标准溶液滴定至溶液由绿色变为暗红色,煮沸2分钟,冷却后继续滴定至溶液呈暗红色,同时做空白试验。
3.8.2盐酸标准溶液当量浓度的计算GN =(V1-V2)×0.05299式中:G——无水碳酸钠的重量,g;V1——盐酸标准溶液消耗的体积,mL;V2——空白试验所消耗盐酸标准溶液的体积,mL;0.05299——每毫克当量碳酸钠的克数;注:标定各浓度间的相对偏差不大于0.2%。
3.9蔗糖:分析纯3.10硫酸铵:分析纯,干燥。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
饲料中粗蛋白测定方法 YKK standardization office【 YKK5AB- YKK08- YKK2C- YKK18】
饲料中粗蛋白测定方法
1、原理
凯氏法测定试样中的含氮量,即在催化剂作用下,用硫酸破坏有机物,使含氮物转化成硫酸铵。
加入强碱进行蒸馏使氨逸出,用硼酸吸收后,再用酸滴定,测出氮含量,将结果乘以换算系数,计算出粗蛋白含量。
2、试剂
硫酸(GB625):化学纯,含量为98%,无氮。
混合催化剂:硫酸铜,5个结晶水(GB665),6g硫酸钾(HG3—920)或硫酸钠(HG3—908),均为化学纯,磨碎混匀。
氢氧化钠(GB629):化学纯,40%水溶液(m/V)。
硼酸(GB628):化学纯,2%水溶液(m/V)。
混合指示剂:甲基红(HG3—958)%乙醇溶液,溴甲酚绿(HG3—1220)%乙醇溶液,两溶液等体积混合,在阴凉处保存期为三个月。
盐酸标准溶液:邻苯二甲酸氢钾法标定,按GB601制备。
2.6.1盐酸标准溶液:c(HCl)=L。
盐酸(GB622,分析纯),注入1000mL蒸馏水中。
盐酸标准溶液:c(HCl)=L。
盐酸(GB622,分析纯),注入1000mL蒸馏水中。
蔗糖(HG3—1001):分析纯。
硫酸铵(GB1396):分析纯,干燥。
硼酸吸收液:1%硼酸水溶液1000mL,加入%溴甲酚绿乙醇溶液10mL,%甲基红乙醇溶液7mL,4%氢氧化钠水溶液,混合,置阴凉处保存期为一个月(全自动程序用)。
3、仪器设备
实验室用样品粉碎机或研钵。
分样筛:孔径(40目)。
分析天平:感量。
消煮炉或电炉。
滴定管:酸式,10、25mL。
凯氏烧瓶:250mL。
凯氏蒸馏装置:半微量水蒸气蒸馏式。
锥形瓶:150、250mL。
容量瓶:100mL。
消煮管:250mL。
定氮仪:以凯氏原理制造的各类型半自动。
4、试样的选取和制备
选取具有代表性的试样用四分法缩减至200g,粉碎后全部通过40目筛,装于密封容器中,防止试样成分的变化。
5分析步骤
试样的消煮
称取试样~1g(含氮量5~80mg)准确至,放入凯氏烧瓶中,加入混合催化剂,与试样混合均匀,再加入12mL硫酸和2粒玻璃
珠,将凯氏烧瓶置于电炉上加热,开始小火,待样品焦化,泡沫消失后,再加强火力(360~410℃)直至呈透明的蓝绿色,然后再继续加热,至少2h。
氨的蒸馏:
将试样消煮液冷却,加入20mL蒸馏水,转入100mL容量瓶中,冷却后用水稀释至刻度,摇匀,做为试样分解液。
将半微量蒸馏装置的冷凝管末端浸入装有20mL硼酸吸收液和2滴混合指示剂的锥形瓶内。
蒸汽发生器的水中应加入甲基红指示剂数滴,硫酸数滴,在蒸馏过程中保持此液为橙红色,否则需补加硫酸。
准确移取试样分解液10~20mL注入蒸馏装置的反应室中,用少量蒸馏水冲洗进样入口,塞好入口玻璃塞,再加10mL氢氧化钠溶液,小心提起玻璃塞使之流入反应室,将玻璃塞塞好,且在入口处加水密封,防止漏气。
蒸馏4min降下锥形瓶使冷凝管末端离开吸收液面,再蒸馏1min,用蒸馏水冲洗冷凝管末端,洗液均流入锥形瓶内,然后停止蒸馏。
5.1.2.3蒸馏步骤的检验
精确称取硫酸铵,代替试样,按步骤进行操作,测得硫酸铵含氮量为±%,否则应检查加碱、蒸馏和滴定各步骤是否正确。
滴定
用或法蒸馏后的吸收液立即用L或L()盐酸标准溶液滴定,溶液由蓝绿色变成灰红色为终点。
6、空白测定
称取蔗糖,代替试样,按第5章进行空白测定,消耗L盐酸标准溶液的体积不得超过。
消耗L盐酸标准溶液体积不得超过。
7、分析结果的表述
计算见下式:
粗蛋白质(%)=(V2-V1)·c××(m×V'/V)×100
式中:V2──?滴定试样时所需标准酸溶液体积,mL;
V1──?滴定空白时所需标准酸溶液体积,mL;
c──?盐酸标准溶液浓度,mol/L;
m──?试样质量,g;
V──?试样分解液总体积,mL;
V──?试样分解液蒸馏用体积,mL;
──?与盐酸标准溶液〔c(HCl)=L〕相当的、以克表示的氮的质量。
──?氮换算成蛋白质的平均系数。
重复性
每个试样取两个平行样进行测定,以其算术平均值为结果。
当粗蛋白质含量在25%以上时,允许相对偏差为1%。
当粗蛋白含量在10%~25%之间时,允许相对偏差为2%。
当粗蛋白质含量在10%以下时,允许相对偏差为3%。
