烃的含氧衍生物
烃的含氧衍生物燃烧通式

烃的含氧衍生物燃烧通式1. 烃和它的含氧衍生物说到烃,大家一定不会陌生。
这玩意儿就是我们日常生活中最常见的化合物之一,像是汽油、蜡烛、甚至某些油炸食品里的油,都是烃的身影。
不过,今天咱们不光说烃本身,还要聊聊它的“亲戚”——含氧衍生物。
这些小家伙可厉害了,它们一旦燃烧起来,产生的能量可不是闹着玩的。
1.1 含氧衍生物的类型含氧衍生物其实就是在烃的基础上,增加了氧元素的化合物,像是醇、醚、酸等等。
别小看它们,这些东西可广泛应用于各种领域,比如燃料、溶剂,甚至药物。
就像是家里的调料一样,少了可不行,有了才香。
1.2 它们的燃烧反应这些含氧衍生物在燃烧时,通常会和氧气反应,释放出二氧化碳和水。
简单来说,就是把它们丢到火里,呼啦一下,热量就蹭蹭地上来了。
你要是看过露营的时候把木材扔进篝火,那种熊熊燃烧的景象,你就能理解这燃烧过程有多壮观。
2. 燃烧的化学反应燃烧其实是个化学反应,简单点说,就是物质和氧气反应,释放能量。
在这个过程中,含氧衍生物的分子结构会被打乱,重新组合成二氧化碳和水。
想象一下,这就像是一个人参加了聚会,原本穿着的衣服(分子结构)在狂欢中被撕扯(反应),最后变成了一件崭新的T恤(产物)。
不过,这个过程可不是一蹴而就的,还得有合适的条件,比如温度、压力等等。
2.1 燃烧的热量说到热量,那可真是一个有趣的东西。
我们常常用卡路里来衡量食物的热量,其实燃烧反应中释放的热量也是可以量化的。
不同的含氧衍生物,燃烧时产生的热量也是不同的,就像每道菜都有自己的特色,烹饪出来的味道自然也不一样。
比如,酒精燃烧时就能释放出不少热量,用来当燃料再合适不过了。
2.2 燃烧的副产物不过,燃烧可不只是好看,它还有副作用。
尤其是当氧气不足时,燃烧产生的一氧化碳可是个“大麻烦”,它可是无色无味,杀伤力十足的家伙,长期吸入可就危险了。
所以在使用这些含氧衍生物的时候,安全可得放在第一位。
就像是开车出门,一定要系好安全带,确保自己和他人的安全。
烃含氧衍生物

CH3CH2OH 氧化 CH3CHO 氧化 CH3COOH
乙醇
乙醛
乙酸
反应
与金属反应 催化氧化 消去反应
分子间脱水 与HX反应
⑤
H H② ①
H―C―C―O―H
③ ④H H
断键位置
①
①③
②④
①②
②
练习:对于司机酒后驾车者,可对其呼出
的气体进行检验而查出,所利用的化学反 应如下:
2CrO3(红色)+3C2H5OH+ 3H2SO4→Cr2(SO4)3(绿色)+3 CH3CHO +6H2O,被检测的气体成分是: ,上 述反应中氧化剂是: ,还原剂是:
CH2OH CH2OH
乙二醇
选含—OH的最长碳链为主链
从离—OH最近的一端起编号
取代基位置— 取代基名称 — 羟基位置— 母 体名称(羟基位置用阿拉伯数字表示;羟基 的个数用“二”、“三”等表示。)
CH2OH
CH2OH
CHOH
苯甲醇
CH2OH 1,2,3—丙三醇 (或甘油、丙三醇)
[练习] 写出下列醇的名称
学与问
乙二醇的沸点高于乙醇,1,2,3—丙三醇的 沸点高于1,2—丙二醇, 1,2—丙二醇的沸点高 于1—丙醇,其原因是:由于羟基数目增多,使得 分子间形成的氢键增多增强。
思考与交流
处理反应釜中金属钠的最安全、合理的方法是 第(3)种方案,向反应釜中慢慢加入乙醇,由于 乙醇与金属钠的反应比水与钠的反应缓和,热效应 小,因此是比较安全,可行的处理方法。
第七章 烃的含氧衍生物
第一节 醇 酚
据我国《周礼》记载,早在周朝就有酿酒 和制醋作坊,可见人类制造和使用有机物有很 长的历史。
从结构上看,酒、醋、苹果酸、柠檬酸等 有机物,可以看作是烃分子里的氢原子被含有 氧原子的原子团取代而衍生成的,它们被称为 烃的含氧衍生物。
人教化学选修5第3章《烃的含氧衍生物》归纳提升
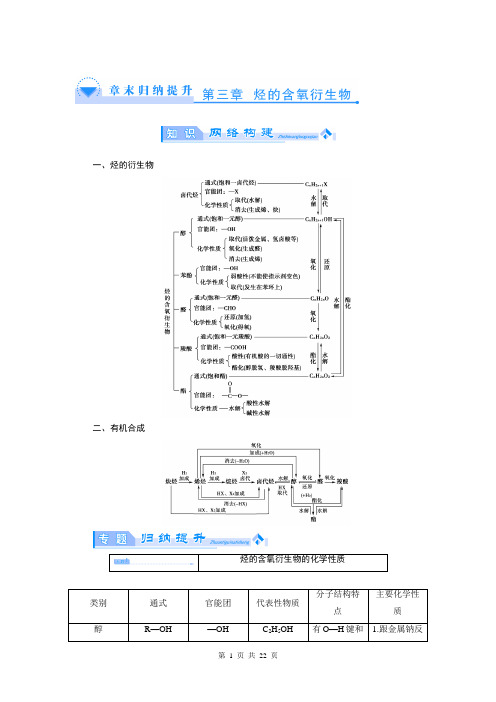
一、烃的衍生物二、有机合成(2013·长安一中高二期末)2011年西安世园会期间对大量盆栽鲜花施用了诱抗素剂,以保持鲜花盛开。
诱抗素的分子结构如图,下列关于该分子说法正确的是( )A .含有碳碳双键、羧基、酯基三种官能团B .1 mol 该物质在催化剂加热条件下最多可与4 mol H 2发生加成反应C .1 mol 该有机物与足量的溴水反应能消耗4 mol Br 2D .该分子中所有碳原子可能位于同一平面上【解析】 该分子含有碳碳双键、羧基和羰基三种官能团,A 项错误;1 mol 该有机物最多消耗3 mol Br 2,C 项错误;分子内部有饱和碳原子,D 项不正确;分子中三个碳碳双键和羰基能够与H2发生加成反应,—COOH中的碳氧双键不能与H2反应,B项正确。
【答案】 B醇、由于与—OH相连的基团不同,—OH受相连基团的影响也不同,这些羟基上的氢原子活性也就不同,表现在性质上也就有较大差异。
如下表:2332 ROH。
(2012·上海高考)过量的下列溶液与水杨酸(COOHOH)反应能得到化学式为C7H5O3Na的是()A.NaHCO3溶液B.Na2CO3溶液C.NaOH溶液D.NaCl溶液【解析】由于酸性:COOH>H2CO3>OH,可知水杨酸与NaHCO3溶液反应时只是—COOH作用转化为—COONa,产物的分子式为C7H5O3Na,A项正确;水杨酸与Na2CO3溶液反应时—COOH、—OH均反应,生成产物的分子式为C7H4O3Na2,B项错误;水杨酸与NaOH溶液反应时—COOH、—OH均反应,生成产物的分子式为C7H4O3Na2,C项错误;与NaCl溶液不反应,D项错误。
【答案】 A现有4种液态有机物A、B、C、D,分子式均为C3H6O2,请根据下表所给出的实验结果,判断这4种物质为何物质(写出结构简式)。
A________;B________;C________;D________。
烃的含氧衍生物 (1)

烃的含氧衍生物【要点精讲】要点1:各类含氧衍生物的结构及性质有极要点2:重要的有机反应类型、等要点3:烃的羟基衍生物比较【典例精讲】典例1:烃的衍生物及其官能团的性质(08广东化学卷25)某些高分子催化剂可用于有机合成。
下面是一种高分子催化剂(Ⅶ)合成路线的一部分(Ⅲ和Ⅵ都是Ⅶ的单体;反应均在一定条件下进行;化合物Ⅰ-Ⅲ和Ⅶ中含N 杂环的性质类似于苯环):回答下列问题:(1)写出由化合物Ⅰ合成化合物Ⅱ的反应方程式 (不要求标出反应条件)。
(2)下列关于化合物Ⅰ、Ⅱ和Ⅲ的说法中,正确的是 (填字母)。
A .化合物Ⅰ可以发生氧化反应B .化合物Ⅰ与金属钠反应不生成...氢气 C .化合物Ⅱ可以发生水解反应 D .化合物Ⅲ不可以...使溴的四氯化碳深液褪色 E .化合物Ⅲ属于烯烃类化合物(3)化合物Ⅵ是 (填字母)类化合物。
A .醇B .烷烃C .烯烃D .酸 E.酯 (4)写出两种可鉴别V 和VI 的化学试剂(5)在上述合成路线中,化合物Ⅳ和V 在催化剂的作用下与氧气反应生成Ⅵ和水,写出反应方程式 (不要求标出反应条件) 解析:(1)由II的结构可以看出和I的区别在于侧链中多了一个乙酰基,也就是说I中侧链上的羟基与乙酸发生了酯化反应,生成了酯类物质。
(2)化合物I 官能团有羟基,碳碳双键,故可发生氧化反应,也可以与金属钠发生反应生成氢气,故A 正确,B 错误。
化合物II 官能团有酯基,可以发生水解发生,生成相应的酸和醇,故C 正确。
化合物III 的官能团有碳碳双键,可以使溴的四氯化碳溶液褪色,属于以乙烯为母体的烯烃类衍生物,故D 错误,E 正确。
(3)VI的结构可以从VII的结构来判断,VII中有两种单体,一种是由III提供,另一种是由VI提供,将III的结构单元去掉即为VI的结构单元,可以看出应是一种酯的结构。
(4)2008年诺贝尔化学奖授予美籍华裔钱永键等三位科学家,以表彰他们在发现和研究绿色荧光蛋白方面做出的杰出贡献。
烃的含氧衍生物小专题

芳香醇与芳香醛的应用
芳香醇的应用
芳香醇在化学工业中有着广泛的应用,如可用于制备 香料、染料、药物等。此外,某些芳香醇还具有生物 活性,如具有抗菌、抗炎、抗肿瘤等作用。
芳香醛的应用
芳香醛在化学工业中也有着广泛的应用,如可用于制 备香料、农药、医药等。此外,某些芳香醛还具有特 殊的功能,如可作为香味剂、除臭剂、防腐剂等。
08
酚类化合物
酚的合成
酚通常通过苯环上的羟基取代反 应来合成,例如卤代苯与碱反应,
或芳香胺的磺化后水解。
酚也可以通过氧化反应来制备, 例如苯环上其他取代基的氧化。
酚类化合物还可以通过酯的水解 和脱羧反应来合成。
酚的性质
01
酚具有酸性,可以与碱反应生成盐。
02
酚羟基可以发生取代反应,例如酯化、醚化、烷基 化等。
烯烃的水合
烯烃与水在催化剂的作用下发生水合反应, 可以得到醇。
酯的水解
酯在酸性或碱性条件下水解,可以得到相应 的醇和羧酸。
醇的性质
醇的氧化
在一定条件下,醇可以 被氧化生成酮或羧酸。
醇的酯化
醇与羧酸在一定条件下 发生酯化反应,生成酯 和水。
醇的脱水
在一定条件下,醇可以 发生脱水反应生成烯烃。
醇的应用
酰胺可以用于合成聚酰胺等高分子材料,广泛应用于工程塑料、
纤维等领域。
药物合成
02
酰胺在药物合成中具有重要应用,如青霉素、头孢菌素等药物
的合成。
化学反应中间体
03
酰胺在许多有机化学反应中作为中间体,用于合成其他有机化
合物。
05
胺类化合物
胺的合成
硝化反应
通过硝基化合物的还原得到胺 ,常用的是用铁粉和盐酸还原
烃的含氧衍生物小专题

OH
+3Br2
OH
Br
Br
+3HBr
Br
思考三:实验室如何制乙 烯,如何检验生产的产物 中有乙烯?
氢氧化钠除去酸性气体 (SO2、CO2)
思考四:写出以下醇类在铜催化下与
氧气反应的方程式。(若不能则不写
)
①
②
③
思考五:只用一种试剂鉴别甲酸,乙醛和乙 酸,解释现象及发生的反应类型。
➢ 新制氢氧化铜悬浊液 甲酸:常温得到蓝色溶液,加热有红色沉淀产生
烃的含氧衍生物
据我国《周礼》记载,早在周朝就有酿酒和制 醋作坊,可见人类制造和使用有机物有很长的历史。
从结构上看,酒、醋、苹果酸、柠檬酸等有机物, 可以看作是烃分子里的氢原子被含有氧原子的原子团 取代而衍生成的,它们被称为烃的含氧衍生物。
烃的含氧衍生物种类很多,可分为醇、酚、醛、 羧酸和酯等。
思考一:如何鉴别以下两种物质? 思考二:如何除去苯中混有的苯酚?
已知: ①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢; ②化合物B为单氯代烃;化合物C的分子式为C5H8; ③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
写出B与新制的Cu(OH)2悬浊液反应的化学方程式:_________________。
(4)写出E与足量NaOH溶液共热反应的化学方程式:____________________。
聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材 枓的生物相存性方面有很好的应用前景。 PPG的一种合成路线如下:
②
小试牛刀
1. 2015年10月5日,我国科学家屠呦呦因在抗疟疾药青 蒿素研究中的突出贡献而获得诺贝尔奖,成为第一位获得 诺贝尔科学奖项的本土中国科学家、第一位获得诺贝尔生 理学及医学奖的华人科学家。青蒿素结构如图所示。有关 青蒿素的叙述正确的是
烃的含氧衍生物 文档

第十章 烃的含氧衍生物10.1 醇、酚高考考点:醇、酚的性质与结构是高考的重点和热点,在有机合成与推断中处于中心枢纽位置。
一.烃的含氧衍生物1. 定义:从结构上说,可以看作是烃分子里的氢原子被含氧原子的原子团取代而衍生二.乙醇1.分子结构:结构式:电子式:分子式:C 2H 6O 结构简式:CH 3CH 2OH 官能团:-OH(羟基)2.物性:无色透明有特殊香味的液体,ρ(CH 3CH 2OH )>ρ(H 2O )易挥发,沸点78.5℃ 熔点:-117.3℃ 能与水以任意比互溶,能溶解多种有机物和无机物,工业酒精含乙醇96%,用工业酒精与生石灰混合蒸馏可制取无水酒精 3.化学性质:(1)与活泼金属反应2CH 3CH 2OH+2Na 3CH 2ONa+H 2↑ (2)氧化反应: CH 3CH 2OH+O 2 2+3H 2O 2CH 3CH 2OH+O 2 3CHO+2H 2O乙醇可以使酸性KMnO 4溶液褪色,能与酸性重铬酸钾(K 2Cr 2O 7)溶液反应,被直接氧化成乙酸。
(3)消去反应: ↑+H 2OCH 3CH 2OH(4)取代反应: CH 3CH 2 2Br +H 2O (浓氢溴酸)CH 3CH 2OH+CH 3COOH CH 3COOCH 2CH 3+H 2O2CH 3CH 23CH 2OCH 2CH 3 +H 2O4.工业制法:CH 2=CH 2 CH 3CH 2OH发酵法:淀粉 3CH 2OH+2CO 2 三.醇类1. 2. 分类※ 乙二醇、丙三醇都是无色粘稠、有甜味的液体,易溶于水和乙醇3. 物理性质:饱和一元醇(C n H 2n+2O )随着碳原子数的递增沸点逐渐升高4. 化学性质:与乙醇相似能与活泼金属反应、氢卤酸反应、能发生氧化反应和消去反应。
※ 催化氧化:-OH 在端上氧化成醛、在链中氧化成酮、与-OH 相连的C 上无氢则不能被催化氧化。
消去反应:CH 3-CH=CH-CH 3 +H 2O (查依采夫规则)10.1‘酚一.苯酚(石炭酸)1.分子结构分子式:C6H6O 结构简式:或C6H5OH2.物理性质:纯净的苯酚是无色的晶体,但放置时间较长的苯酚往往是粉红色,这是由于部分苯酚被空气中氧气氧化所致。
备战2021年高考化学考点 烃的含氧衍生物

考点烃的含氧衍生物一、醇类1.醇类(1)定义:羟基与烃基或苯环侧链上的碳原子相连形成的化合物称为醇。
(2)醇的分类注意啦:饱和一元醇的通式是C n H2n+1OH,饱和一元醚的通式为C n H2n+2O,所以碳原子数相同的饱和一元醇和饱和一元醚互为同分异构体,如丁醇和乙醚互为同分异构体。
碳原子数相同的芳香醇及酚互为同分异构体。
(3)醇的物理性质和化学性质物理性质递变规律密度一元脂肪醇的密度一般小于1g·cm-3直链饱和一元醇的沸点随着分子中碳原子数的递增而升高沸点醇分子间存在氢键,所以相对分子质量相近的醇和烷烃相比,醇的沸点高于烷烃水溶性低级脂肪醇易溶于水,饱和一元醇的溶解度随着分子中碳原子数的递增而逐渐减小化学性质由于醇类都以羟基为官能团,所以醇类的化学性质与乙醇相似,即能与活泼金属反应,能发生酯化反应、消去反应、取代反应、氧化反应等。
注意啦:在二元醇或多元醇的分子中,两个或两个以上的羟基结合在同一个碳原子上时,物质不能稳定存在(如:→)。
在写二元醇或多元醇的同分异构体时,要避免这种情况。
(4)重要的醇的用途①甲醇:有毒,饮用约10 mL就能使人双目失明。
工业酒精中含甲醇,甲醇是重要的化工原料和车用燃料。
②乙二醇和丙三醇:都是无色、黏稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。
乙二醇还用作汽车防冻液,丙三醇用于配制化妆品。
2.脂肪醇、芳香醇、酚和芳香醚的比较类别脂肪醇芳香醇酚芳香醚实例CH3CH2OH C6H5CH2OH C6H5OH C6H5OCH3官能团—OH—OH—OH—O—结构特点—OH与链烃基相连—OH与芳香烃侧链相连—OH与苯环直接相连氧原子连接2个烃基主要化学性质①与钠反应②取代反应③脱水反应④氧化反应⑤酯化反应等①弱酸性②取代反应③显色反应④加成反应等______特性红热铜丝插入醇中有刺激性气味(生成醛或酮)与FeCl3溶液反应显紫色______二、酚1.酚的概念和结构特征羟基与苯环直接相连而形成的化合物称为酚。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
PPT文档演模板
2020/11/21
烃的含氧衍生物
教学目标:
1.掌握乙醇的主要化学性质
2.掌握乙醇 的工业制法和用 途
3.了解醇的分类和命名
4.了解醇类的一般通性和典型 醇的用途
重点: 乙醇的化学性质
PPT文档演模板
烃的含氧衍生物
• 1.什么叫烃的衍生物? 如果烃分子中的
氢原子被-OH取代产物是什么?
•一元醇
•饱和一元醇:•CnH2n+1OH •不饱和一元醇
•多元醇•:如乙二醇、丙三醇等
2、同系物的物理性质比较:P.49思考交流
•表3-1图 •沸点/℃
•表3-2图 •沸点/℃
•●
•10 0•5 0•0
•氢键 •醇•●
•30
•● •●
•40 •50 •●•6 •相对分子质量
•20 •0150 •乙?醇
•2.溴乙烷在氢氧化钠水溶液中加热生成?
•C2H5-Br+NaOH
•水 •△
C2H5-OH+NaBr
• 烃分子中的氢原子被含有氧的原子团
取代得到的化合物称为烃的含氧衍生物。
•醇•链烃基与羟基相连而成 •羟基化合物
•酚•苯环与羟基直接相连而成
•可分为一元羟基化合物和多元羟基化合
一、醇
1、醇的分类:
•醇
•2CH3CH2-OH +2Na →2CH3CH2ONa +H2↑ •产物乙醇钠在水中强烈水解
•CH3CH2-ONa +H2O→CH3CH2OH +NaOH
•练习:写出乙醇•②与•K①、Ca分别反应的化学方程
式
•④
•P.49思考与交流
•③
•实验装置及
•2)乙醇的消去反应•实验3-1 注意事项
•注意事项:•1)反应温度:170℃ 2)加•碎②瓷•①片
•3)V乙醇:V浓硫酸=1:3 4•)④检查气密
•可能产生性的现象分析 •③ •题外话:分子间脱水 •2CH3CH2-OH••浓14H02℃SO4 CH3CH2-OC•3H)2C乙H醇3+与H2氢O卤酸的取代反应 •2CH3CH2-OH+HBr •△ CH3CH2Br+H2O •4)乙醇的氧化反应
PPT文•档演乙模板 醇能不能被其他氧化剂氧化烃?的含•氧实衍生物验3-2
•100 •●
•氢键
•● •●
数目增
•丙?醇 多
•-50 •-
•烷•●
100 PPT文档演模板
•●
0
•醇的沸点
•50
远高于烷烃。 •0
•● •醇羟基越 多沸点越高。
烃•1的含氧衍•生2物 •3 •羟基数
•3、乙醇
•1)乙醇的物理性质和分子结构
•a.乙醇的物理性质
• 乙醇(酒精)是无色透明、具有特殊香味
•怎样制备 无水乙醇
•5、醇的化学性质——与乙醇相似
PPT文档演模板
烃的含氧衍生物
3rew
演讲完毕,谢谢听讲!
再见21
烃的含氧衍生物
•乙醇的化学性•乙质醇小的结氧化反应
•CH3CH2-O-CH2CH3
•浓H2SO4
•O •CH3C-O-CH2CH3
• 140℃
•[O]
•[O]
•CH3CH2-OH •CH3CHO •CH3COOH
•浓H2SO4 • 170℃
•CH3CH2-ONa
•CH2=CH2 •CH3CH2-Br •4、乙醇的工业制法?
的液体,密度比水小,沸点比水低,易挥发,
任意比溶于水,能溶解多种无机物和有机物。
•b.乙醇的分子结构
• 化学式:C2H6O
•结构式:
•结 构 简 式 :
CH3CH2OH
••乙醇是极性或分C子2H5OH
PPT文档演模板
烃的含氧衍生物
• 2、乙醇的化学性质 •现象:缓慢产生气
•1) 乙醇与钠反应
泡,金属钠沉于底 部或上下浮动。
