分光光度法快速测定蔬菜水果中维生素C的含量_于晓萍
紫外可见分光光度法测定果蔬中的维生素C

第 32 卷第 1 期 2009 年 01 月
t/min 图 1 VC 在偏磷酸和醋酸中的稳定性
2. 2 最大吸收峰的选择 准确吸取 2.0 mL 的 VC 标准溶液于 50 mL 容量
瓶中用蒸馏水定容,然后以蒸馏水作空白,在 190~ 400 nm 的波长范围内多次进行光谱的连续扫描,确 定 VC 最大吸收峰在 246.0 nm。 2. 3 维生素 C破坏剂的选择
Vol.32 No.1 Jan . 2009
紫外可见分光光度法测定果蔬中的维生素 C
张立科 1,田水泉 1,谢太平 1,张洪浩 1,范顺利 2
(1.河南许昌学院化学化工学院,河南 许昌 461000;2.河南师范大学化学与环境科学学院,河南省环境污染控制重点实 验室,河南 新乡 453007)
[ 摘 要] 在 0~450 μg/mL 线性范围内,以 Cu2+ 作催化剂,以溶解氧将还原型维生素 C(VC)氧化为 246.0 nm 处无吸收的氧
完全破坏,测出的仅是 Cu2+ 的吸光度值。本文提出了
反应中 Cu2+ 不作氧化剂而作为催化剂来催化溶液中
的溶解氧去氧化还原型 VC,使之在 2462)。Cu2+ 的量不影响
VC 在 246.0 nm 处的吸光度,Cu2+ 本身本底吸收小。确
定 Cu2+ 用量为 30 μg。
ZHANG Li-ke1,TIAN Shui-quan1,XIE Tai-ping1,ZHANG Hong-hao1,FAN Shun-li2
紫外分光光度计法测定果蔬中维生素c的含量

紫外分光光度计法测定果蔬中维生素c的含量紫外分光光度计法是一种常用的测定果蔬中维生素C含量的方法。
维生素C具有强的紫外吸收性质,在265nm处有最大吸收峰。
通过测定样品溶液与标准溶液在相同条件下的吸光度,可以比较它们的维生素C含量。
以下是该方法的详细步骤:一、目的本实验的目的是通过紫外分光光度计法测定果蔬中维生素C的含量,了解其含量变化情况,为科学饮食提供参考。
二、原理维生素C具有强的紫外吸收性质,在265nm处有最大吸收峰。
在实验条件下,一定浓度的维生素C溶液与其吸光度呈线性关系。
通过比较样品溶液与标准溶液在相同条件下的吸光度,可以求出样品中维生素C的含量。
三、实验步骤1.标准曲线的制作(1)配制不同浓度的维生素C标准溶液。
分别称取0.05g、0.1g、0.2g、0.3g、0.4g的维生素C,用蒸馏水定容至100mL,得到浓度分别为5mg/mL、10mg/mL、20mg/mL、30mg/mL、40mg/mL的溶液。
(2)用1cm石英比色皿分别在紫外分光光度计上测定各标准溶液在265nm处的吸光度。
(3)以维生素C浓度为横坐标,吸光度为纵坐标绘制标准曲线。
2.样品处理(1)将果蔬样品洗净,晾干表面水分。
(2)将样品切成小块,放入榨汁机中榨汁,收集榨出的汁液。
(3)用纱布过滤,去除汁液中的杂质和果肉颗粒。
(4)将滤液倒入50mL容量瓶中,用蒸馏水定容至刻度线。
3.测定样品吸光度(1)用移液管准确移取5mL样品溶液于1cm石英比色皿中。
(2)在紫外分光光度计上测定样品溶液在265nm处的吸光度。
4.计算样品中维生素C的含量(1)从标准曲线上查得相应的维生素C浓度(mg/mL)。
(2)计算样品中维生素C的含量(mg/100g),公式如下:维生素C含量 = 查得浓度× 溶液体积× 稀释倍数 / 样品质量其中,溶液体积为50mL,稀释倍数为100(即5mL样品溶液稀释成50mL),样品质量为榨出的果蔬质量。
分光光度法测定果蔬中Vc的含量

Divide all Luminosity Law and Determine the Content of Vitamin C in the Fruits and Vegetables
CAO Shu—jie
(Department of Chemistry,Nanyang Normal University,Nanyang 473061,China)
作者: 作者单位: 刊名:
英文刊名: 年,卷(期): 被引用次数:
曹书杰, CAO Shu-jie 南阳师范学院,化学系,河南,南阳,473061
河南教育学院学报(自然科学版) JOURNAL OF HENAN INSTITUTE OF EDUCATION(NATURAL SCIENCE) 2005,14(3) 1次
O.18 O.16 O.14 O.12 0.10 《O.08 O.06 0.04 0.02
phenhnl图2显色源自用■对吸光度的影响pH图3酸度对吸光度的影响
图4反应时问对吸光度的影响
Vc/(1 0。‘mol/1) 图5标准曲线 2.3.6果蔬中vc的测定 取去皮橙子、苹果、梨、白萝卜各509,在榨汁机中分别榨 汁,将其定容至250ml容量瓶中,再各取2ml于50ml容量瓶 中,加4 mlFe(Ⅲ)标准液,6mlphell,用Imol/LHAc定容,于暗 处放置20分钟后,以空白试剂作参比,分别测其吸光度. 每种样品各测三次,求平均值.最后得样品中含Vc的量为: 橙子:0.141 609/lOOg,苹果:0.011 589/lOOg,梨:0.012 1is/lOOg,白萝卜:O.025 659/lOOg 2.4干扰物质 果蔬中含有的铁是以有机物形式存在,不与phen直接 络合.故不影响测定结果.
紫外分光光度法测定水果或蔬菜中的维生素C含量

2. 标准曲线的
绘制
1
2
3
4
5
6
7
8
标准抗坏血酸溶液加入体
积/mL
0.1 0.2 0.3 0.4 0.5 0.6 0.8 1.0
9.9 9.8 9.7 9.6 9.5 9.4 9.2 9.0
总体积/mL
抗坏血酸溶液浓度 /(μg·mL-1)
10.0 10.0 10.0 10.0 10.0 10.0 10.0 10.0 1.0 2.0 3.0 4.0 5.0 6.0 8.0 10.0
3.消光值的测定:以蒸馏水为空白,在243 nm处 测定标准系列抗坏血酸溶液的消光值,以抗坏血酸的含 量(μg)为横坐标,以相应的消光值为纵坐标作标准 曲线。
(二)样品的测定
1.样品的提取:将果蔬样品洗净、擦 干、切碎、混匀。称取5.00 g于研体中, 加入2~5 mL 1% HCl,匀浆,转移到25 mL 容量瓶中,稀释至刻度。若提取液澄清透明, 则可直接取样测定,若有浑浊现象,可通过 离心(10000 g, 10 min)来消除。
样品液与碱处理样品液两者消光值之差,通过查标准
曲线,即可计算样品中维生素标准曲线的制作 1.抗坏血酸标准溶液的配制:用分析 天平准确称取抗坏血酸10 mg,加2 mL 10%盐酸,加蒸馏水定容至100 mL,混匀。 此抗坏血酸溶液的浓度为100 μg·mL-1。
93.4 计算
μ×V总
分光光度法测定水果中Vc的含量(精)

综合性、设计性实验报告(本科学生姓名:杨道林王丽萍杨文英张崇斌学号:2011021157201102114320110211442011021160专业:化学班级:2011级实验课程名称:分光光度法测定水果中Vc的含量指导教师及职称:郭老师高级实验师开课学期:2012 至 2013 学年下学期上课时间:2013 年 6 月 9 日一、实验设计方案实验序号及名称:分光光度法测定水果中Vc的含量实验时间:2013.6.18-2013.6.19小组合作:是〇否〇小组号: 4号成员:杨道林、杨丽萍、杨文英、张崇斌一、实验目的:1.了解柠檬、荔枝中Vc的含量2. 学习如何选择吸光度分析的实验条件3.巩固分光光度法的应用二、实验设备及仪器组成:1、实验试剂:a、Vc溶液(称取0.1gVc)配成500ml的储备液,移取25.00ml(储备液稀释至250ml b、铁标准溶液(100ug/ml)(准确称取0.04317gNH4Fe(SO42.12H2O,置于烧杯中,加入10ml,6mol/L的盐酸和适量蒸馏水,转至500ml 容量瓶中,稀释至刻度 c、邻二氮菲:1.5g/L.d、HAc溶液.e、NaOH溶液,0.1mol/L仪器:分光光度计、50ml比色管、500ml,250ml容量瓶、吸量管、移液管三、理论依据及实验原理:Vc分子中有烯二醇基能还原三价铁为二价铁,二价铁与phen 生成橙红色络合物反应如下:2Fe3++C6H8O6=2Fe2++C6H6O6+2H+二价铁与phen生成的橙红色络合物,此物在510nm处有最大吸收,其颜色的深浅在一定范围内与Vc含量成正比。
查阅资料知酸度控制在PH4.3至6.2 ,反应时间控制在15min 为宜。
4、实验内容、步骤(用流程图表示及注意事项:1.吸收曲线的绘制:两支比色管,①0.00mlvc标液②2.00ml标液分别加入2.00ml phen和4mlFe3+标液,1mol/LHAc定容暗处放置15min 440-560nm间每隔10nm测一次②号的吸光度A2. 显色剂容量的确定:7支50ml比色管分别加入4mlFe3+标液、2mlVc液和0.3ml、0.5ml、0.8ml、1.0ml、1.5ml、2ml、4ml、6 ml 1.5g/Lphen液,1mol/LHAc定容,暗处放15min,测吸光度。
分光光度法快速测定鲜果刺梨Vc的含量

分光光度法快速测定鲜果刺梨Vc的含量代甜甜;陈晓靓;吴娜怡郁;李齐激;杨小生【摘要】建立简单、快速、准确的刺梨维生素C含量测定方法.以维生素C标准品为对照品,采用紫外可见分光光度法于267 nm波长处测定吸光度值,建立标准曲线方程计算刺梨鲜果中维生素C的含量.维生素C对照品溶液在0.2~1.0μg·mL-1范围内呈良好的线性关系(r=0.9984),平均加样回收率为101.2%,RSD=1.5%(n=9).本方法操作简便、准确度高,精密度、重现性、回收率良好,可用于刺梨鲜果中维生素C的含量测定.【期刊名称】《广州化工》【年(卷),期】2017(045)024【总页数】3页(P99-100,140)【关键词】刺梨果;紫外可见分光光度法;维生素C;含量测定【作者】代甜甜;陈晓靓;吴娜怡郁;李齐激;杨小生【作者单位】贵阳护理职业学院,贵州贵阳 550081;贵阳护理职业学院,贵州贵阳550081;贵阳护理职业学院,贵州贵阳 550081;贵州省中国科学院天然产物化学重点实验室,贵州贵阳 550002;贵州省中国科学院天然产物化学重点实验室,贵州贵阳 550002【正文语种】中文【中图分类】O6刺梨(Rosa roxburghii Tratt)又名文先果、送春归,系蔷薇科蔷薇属多年生落叶小灌木,主产于贵州,在川东南、滇东北、桂西北、湘西、鄂西南、陕南等地也有分布[1]。
刺梨具有很高营养价值,富含维生素C、多酚、有机酸、多糖、黄酮、微量元素等物质[2],其中维生素C的含量是苹果的800倍、香蕉的400倍、紅桔的100倍、西红柿的22倍、猕猴桃的10倍,被称为水果中的“维生素C大王[3]”。
刺梨的药理作用有抗氧化、抗癌防癌、降低重金属负荷等。
现代医学研究表明,刺梨具有调节机体免疫功能、解毒、镇静、延缓衰老、抗动脉粥样硬化、抗肿瘤等多种生物学作用。
同时大量药理实验证明刺梨具有健胃消食、防治糖尿病、增强免疫、抗突变等功效。
紫外分光光度法测定五种果蔬中维生素C的含量

紫外分光光度法测定五种果蔬中维生素C的含量一、本文概述维生素C,也被称为抗坏血酸,是一种重要的水溶性维生素,对人体健康具有多种重要作用,包括增强免疫力、促进铁的吸收和利用、参与胶原蛋白的合成等。
由于其对人体健康的重要性,了解各种食物中维生素C的含量对于合理搭配膳食、保障人体维生素C的充足摄入具有重要意义。
因此,本研究采用紫外分光光度法测定了五种常见果蔬中维生素C的含量,旨在为公众提供更为准确、科学的膳食指南。
紫外分光光度法是一种基于物质对紫外光的吸收特性进行定量分析的方法。
该方法具有操作简便、灵敏度高、重现性好等优点,因此被广泛应用于各种生物化学分析中。
在本研究中,我们通过对五种果蔬样品进行前处理,提取其中的维生素C,并利用紫外分光光度计测定其吸光度,从而计算出样品中维生素C的含量。
本研究选取的五种果蔬分别为苹果、橙子、草莓、菠菜和番茄,它们都是人们日常膳食中常见的富含维生素C的食物。
通过对这些果蔬中维生素C含量的测定,我们可以了解不同食物中维生素C含量的差异,为人们在日常饮食中合理搭配食物提供参考。
本文旨在利用紫外分光光度法测定五种常见果蔬中维生素C的含量,为公众提供更为准确、科学的膳食指南,以促进人们的健康。
二、实验材料与方法选择了五种具有代表性的果蔬样品,包括苹果、橙子、草莓、菠菜和青椒。
这些果蔬因其维生素C含量高且易得而被选中。
实验所需的主要试剂包括2,6-二氯靛酚钠、草酸、偏磷酸等。
设备方面,使用了紫外可见分光光度计、离心机、电子天平、研钵、容量瓶、移液管等。
将每种果蔬样品洗净、切碎,并去除不可食部分。
然后,将样品用偏磷酸-草酸混合液研磨,离心取上清液,用于后续的维生素C含量测定。
采用偏磷酸-草酸混合液作为提取液,通过研磨和离心,使果蔬中的维生素C充分溶解在提取液中。
准确称取一定量的2,6-二氯靛酚钠标准品,用蒸馏水溶解并定容,得到不同浓度的标准溶液。
然后,在紫外可见分光光度计上,以蒸馏水为空白对照,测定各标准溶液的吸光度,绘制标准曲线。
紫外分光光度法测定水果蔬菜中维生素C含量测定
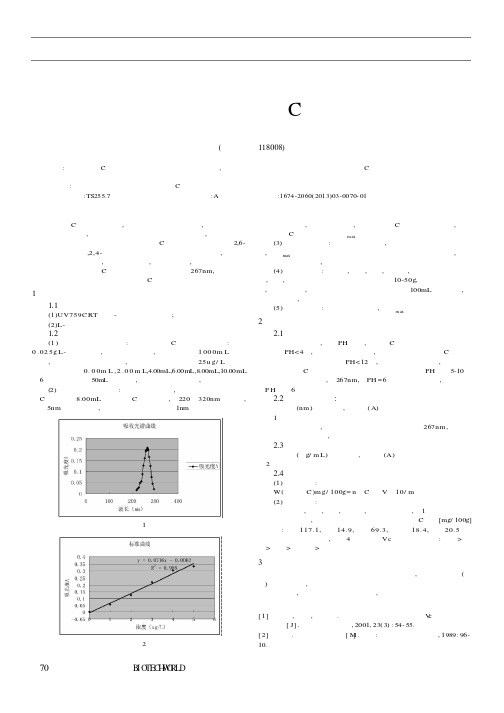
图2
3 结语
本次实验测量快速、稳定、使用试剂简单易得,有些水果略高(略 低)于标准含量,这与被测产品的产地、品种、生长环境等因素有关。 经实验分析,本方法快速、准确、简便,有利于提高工 作效率。 参考文献
[ 1] 张炳春, 聂燕, 孟立红. 水果、蔬菜有色提取液中 Vc 的测定—— 反滴定法[ J] . 食品研究与开发, 2001, 23( 3) : 54- 55. [ 2] 黄伟坤. 食品检验与分析[ M] . 北京: 中国轻工业出版社, 1989: 9610 .
1.1 仪器试剂 (1)UV759C RT紫 外-可 见分光 光度计; (2)L-抗坏 血酸等。 1.2 实验方法 (1 ) 配 制 系 列标 准 溶 液 :配 制 维 生 素 C 系列 标 准 溶 液 :称 取 0 .02 5g L- 抗 坏 血 酸 ,溶 于 蒸 馏 水 中, 定 量 转移 入 1 00 0m L容 量 瓶 中,用 蒸 馏 水稀 释 至 标线 ,摇 匀。此 溶 液 浓度 为 25u g/ L。分 别 吸 取 上 述 溶 液 0. 0 0m L ,2 .0 0 m L,4.00mL,6.00mL,8.00mL,10.00mL 于6只洁净且干燥的50mL容量瓶中,用蒸馏水稀释至标线,摇匀。 (2)绘制吸收 光谱曲线:以蒸馏水为 参比,取上述配制的 含维生 素C 标准溶液8.00mL的维生素C标 准溶液,在220∽320nm 范围内, 每隔5nm测定吸光度,在最大吸光度附近每隔1nm 测定吸光度。以吸
70 生物技术世界 BI OTECHWORLD
(5)样液的测 定:以蒸 馏水为参比, 在λm ax处测定吸 光度。
2 结果与讨论
2.1 酸度对吸收波长的影响 实验结果 表明,不 同PH 值下,维 生素C的最大吸 收波长会有所 变化。当PH< 4时,最大吸收波长紫移,这可能是由于维生素C此时 以 离子化形式存在而造成。当PH< 12时,最大吸收波长红移,很明显这 是由于维生素C在碱性环境中不稳定分解而引起的。PH 值在5-10时 的最大吸收波长不变,为267nm,但PH = 6时的吸收值最大,故选择最 佳P H值为6。 2.2 光谱吸收曲线: 以波长(nm )为横坐标,吸光度( A)为纵坐标 绘制光谱吸收曲线 如图1。 测定结 果表明,最大吸光度 对应的吸收 波长为267nm ,故 选此 波长为测定条件波 长,作为 定量依据。 2.3 标准曲线 以浓度( g/ m L)为横坐标,吸光度(A)为纵坐标作标 准曲线如 图2。 2.4 实验结果 (1) 计算 公式: W(维生素C )m g/ 100g= n×C 样×V×10/ m (2) 样品 分析: 称取青椒,苹 果,橙子,西红柿,黄瓜五种果蔬,按 1中样品溶液的 制备和测定方法,分别测定上述五种果蔬中维生素C含量[mg/ 100g] 分别为:青 椒117.1,苹果14.9,橙子 69.3,西 红柿18.4,黄瓜20.5。 由以 上数据 可见,市售4中果 蔬中Vc的 含量顺 序是:青椒 > 橙 子> 黄瓜> 西红柿> 苹果
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2009年11月第6卷第2期Nov. 2009 No.2 vol.6- 16 -工程技术与应用分光光度法快速测定蔬菜水果中维生素C的含量于晓萍扬州工业职业技术学院 江苏 扬州 225127摘要:维生素C在食品中能起抗氧化剂作用,即它在一定时间内能防止油脂变酪。
维生素C是水溶性的,为此,笔者首先通过吸收光谱曲线法确定维生素C的水溶液的最大吸收波长为267nm,进而通过工作曲线法快速测定蔬菜水果中维生素C的含量,本方法与常规方法比较,具有快速、准确、简便、试剂易得等优点。
方法的RSD为0.75%~0.84%,回收率为99.7%~100.1%。
关键词:蔬菜;水果;维生素C;快速测定中图分类号:D65 文献标识码:A 文章编号:(2009)-02-016-03Quick Determination of Vitamin C Content inVegetables and Fruits by SpectrophotometryYu XiaopingYangzhou Polytechnic Institute, Yangzhou 225127, JiangsuAbstract: Vitamin C plays an antioxidant role in food, namely in a certain period of time it can prevent fats and oils from changing into cheese. Given the reason that vitamin C is water-soluble, the author first determine that Vitamin C water-soluble fluid biggest absorption wave length is 267nm through the absorption spectrum curve method, then with the working curve method, the vitamin C content in vegetables and fruits can be tested quickly. The results of testing indicate that the method has the merits of being quick, simple, accurate and facile reagent etc in comparison to conventional ones. RSD of the method is 0.75%~0.84% and the recovery is 99.7%~100.1%.Key word: vegetable; fruit; Vitamin C; quick determination引言维生素C(Vc)广泛存在于新鲜水果中,它具有保持肌肤润滑、防止衰老、抗坏血酸等作用,是人体必需的主要维生素之一[1][2]。
Vc在水果中主要以还原型(ASA)存在。
维生素C又名抗坏血酸,能溶于水、乙醇和甲醇,而不溶于其他有机溶剂,具有酸味和还原性,有4 种异构体,即L-抗坏血酸,D-抗坏血酸,L-异抗坏血酸,D-异抗坏血酸。
天然抗坏血酸主要以L-抗坏血酸为主,其效力最高,也是通常所指的抗坏血酸。
抗坏血酸在合适的条件下,可氧化成脱氢抗坏血酸,脱氢后的L-脱氢抗坏血酸在生物体内可还原为L-抗坏血酸,且这种变化是可逆的,故仍有生物活性。
脱氢抗坏血酸可进一步被氧化,生成二酮古洛糖酸,而这一过程是不可逆的。
在许多水果和蔬菜中,维生素C主要以还原型抗坏血酸存在。
维生素C的固体较稳定,水溶液最容易受氧化,所以测定维生素C的准确性很大程度上取决于分析技术。
蔬菜中维生素C含量的测定一般采用2,6-二氯靛酚滴定法、碘量法、2,4-二硝基苯肼法和萤光分光光度法等[3],这些方法都有所用试剂不稳、操作程序复杂、费时等缺点,为此,笔者首先通过吸收光谱曲线法确定维生素C的水溶液的最大吸收波长为267nm,进而通过工作曲线法快速测定蔬菜水果中维生素C的含量,本方法与常规方法比较,具有准确、快速、稳定、试剂易得等优点。
收稿日期:2009-9-25作者简介:于晓萍(1970-),女,江苏扬州人,扬州工业职业技术学院,副教授,研究方向:仪器分析。
2009年11月第6卷第2期Nov. 2009No.2 vol.6- 17 -一、试验部分1.仪器试剂(1)主要仪器。
756型紫外-可见分光光度计;石英吸收池一对;榨汁机;50mL 容量瓶;1000mL 容量瓶;10mL 吸量管。
(2)试剂。
维生素C 标准溶液:25.00μg/mL。
称取0.2500g 维生素C,溶于蒸馏水中,定量转移至100mL 容量瓶中,稀释至标线,摇匀。
用吸量管吸取10.00mL 定量转移入1000mL 容量瓶中,用蒸馏水稀释至刻线,摇匀,因为维生素C 水溶液最容易受氧化,要求现配现用。
2.实验方法(1)标准系列溶液的配制。
分别吸取上述溶液0.00、2.00、4.00、6.00、8.00、10.00mL 于6个洁净且干燥的50mL 容量瓶中,用蒸馏水稀释至标线,摇匀。
(2)吸光度的测定。
1)绘制吸收光谱曲线。
以蒸馏水为参比,取上述配制的含维生素C 标准溶液6.00mL 的溶液,在220-320nm 范围绘制维生素C 的吸收光谱曲线,并确定入射光波长λmax。
2)绘制工作曲线。
以蒸馏水为参比,取上述配制的系列标准溶液,于λmax 波长处测吸光度,作标准曲线。
(3)样品分析。
样品用榨汁机获得蔬菜汁或加适量水匀浆,于1000r/min 下,离心10min,取上层清液,视Vc 含量及样液颜色确定稀释倍数(西红柿汁需要稀释100倍,黄瓜汁需要稀释100倍,苹果汁需要稀释100倍,西瓜汁需要稀释50倍),以使吸光度在合适的范围。
二、结果与讨论1.吸收曲线按上述实验方法所得数据绘制吸收光谱曲线(图1),由图1可见,最大吸收波长在267nm 处,可作定量依据。
图1 吸收光谱曲线2.酸度对吸收波长的影响实验结果表明,不同pH 值下,维生素C 的最大吸收波长会有所变化。
当pH<4时,最大吸收波长紫移,这可能是由于维生素C 此时以离子化形式存在而造成的。
当pH>12时,最大吸收波长红移,很明显这是由于维生素C 在碱性环境中不稳定分解而引起的。
pH 值在5~10时的最大吸收波长不变,为267nm,但pH=6时的吸收值最大,故选择最佳pH 值为6。
3.标准曲线按上述实验方法绘制A-m(50mL 容量瓶中所含维生素C 的质量)标准曲线(图2),由图2上查得稀释一定倍数后的蔬菜水果中的维生素C 的含量,(式中ρ为某蔬菜或水果中维生素C的含量,m x 为从标准曲线图上查得的稀释一定倍数后的蔬菜水果中的维生素C 的含量相当于50mL 容量瓶中所含维生素C 的质量),将实验所测定的西红柿、黄瓜、苹果、西瓜的测定计算结果列于表1中。
图2 标准曲线于晓萍:分光光度法快速测定蔬菜水果中维生素C 的含量表1 Vc 含量的计算结果蔬菜或水果名称西红柿黄瓜苹果西瓜榨汁中Vc 含量(μg/mL)38118028298.22009年11月第6卷第2期Nov. 2009 No.2 vol.6- 18 -工程技术与应用由以上数据可见,市售4 种蔬菜水果中Vc 的含量顺序是:西红柿>苹果>黄瓜>西瓜4.回收实验准确吸取上述实验方法中稀释100倍后西红柿汁和稀释100倍后的黄瓜汁25.00ml于50mL容量瓶中,加2.00ml 25.00μg/mL维生素C标准溶液,用蒸馏水稀释至标线,摇匀。
测定该溶液的吸光度并从标准曲线上查找出所测定的50mL容量瓶中所含有维生素C(Vc)的含量。
结果见表2。
表2 回收试验结果(μg)样品名称及批号本底值(μg)加入量(μg)测定值平均值回收率西红柿稀释液(20070506号)95.350.0144.0;145.0;146.5;147.0;145.0145.5100.1黄瓜稀释液(20070508号)45.050.094.5;94.0;95.5;95.3;94.094.799.7注:实验数据为维生素C(Vc)的含量。
三、结论本次试验测量快速、稳定、使用试剂简单易得,有些水果略高(或略低) 于标准含量,这与被测产品的产地、品种、生长环境等因素有关。
经实验分析,本方法快速、准确、简便,有利于提高工作效率。
参考文献:[1] 张丙春,聂燕,孟立红等.水果、蔬菜有色提取液中Vc的测定——反滴定法[J].食品研究与开发,2001,23(3):54-55.[2] 阎树刚,韩涛.果蔬及其制品中维生素C测定方法的评价[J].中国农学通报,2002,18(4):110-112.[3] 黄伟坤.食品检验与分析[M].北京:中国轻工业出版社,1989:96-104.[责任编校:刘凤云]高等职业教育的管理人员与教师,我们应该对高等职业教育的发展多做研究与分析,以期高等职业教育获得更大、更好、更科学的发展,更好地适应行业的需求,服务于地方经济的发展。
参考文献:[1] 周三多,陈传明,鲁明泓.管理学原理与方法[M].上海:复旦大学出版社,2002.[2] (美)斯蒂芬·P·罗宾斯,玛丽·库尔特.Management[M].9thEdition.Prentice Hal.,2005.[3] 苏东水,彭贺.中国管理学[M].上海:复旦大学出版社,2009.[4] (美)詹姆斯·斯通纳(James A.F.Stoner).Management[M].北京:华夏出版社,2001.[5] 胡象明.行政管理学[M].北京:高等教育出版社,2005.[责任编校:徐国方](上接第15页)。
