酸碱中和滴定、滴定曲线的分析方法共33页
《酸碱中和滴定曲线
酸碱中和反应与中和滴定方法

滴定曲线的分析
滴定曲线的概念:表示溶液pH值与滴定过程中加入滴定剂体积关系的曲线。
滴定曲线的绘制方法:通过实验测定不同体积下溶液的pH值,并记录数据,绘制出滴定 曲线。
滴定曲线的分析:根据滴定曲线可以判断反应的定量关系:通过滴定曲线可以确定酸碱中和反应的定量关系,如反应计量 数、反应常数等。
酸碱指示剂的变色原理
酸碱指示剂的种类:酚酞、甲基橙、溴酚蓝等
酸碱指示剂的变色范围:不同的指示剂有不同的变色范围 酸碱指示剂的变色原理:指示剂分子在不同酸碱环境下结构发生变化,从 而呈现不同颜色 酸碱指示剂在中和滴定中的应用:用于判断滴定终点,计算滴定结果
酸碱指示剂的选择原则
酸碱指示剂的变色范围应尽可能小,且颜色变化应明显易于观察。 指示剂的变色点应尽量接近于滴定分析所要求的终点pH值。 指示剂应具有适当的酸碱性和稳定性,不易受溶液的酸碱性影响。 指示剂应无毒、无害,对人体和环境无害。
单击此处添加副标题
酸碱中和反应与中和滴定
方法
汇报人:XX
目录
01 02 03 04 05 06
添加目录项标题
酸碱中和反应
中和滴定方法
酸碱指示剂
酸碱滴定曲线 酸碱中和反应的实验操作与注意事
项
01
添加目录项标题
02
酸碱中和反应
酸碱中和反应的定义
酸碱中和反应:酸和碱反应生成盐和水的反应 反应特点:中和反应是放热反应,且反应速率快 反应实质:酸中的氢离子与碱中的氢氧根离子结合生成水 酸碱中和反应的应用:在化学实验、工业生产、医疗等领域有广泛应用
中和反应的原理
中和反应的定义:酸和碱反应生成盐和水的反应。 中和反应的实质:氢离子与氢氧根离子结合生成水。 中和反应的化学方程式:$H^{+} + OH^{-} = H_{2}O$ 中和反应的应用:中和滴定法测定溶液中酸或碱的浓度。
酸碱中和滴定 新高考化学 考点详细分析 深入讲解 提升解题能力 化学高考必看 最新版

3.容量瓶 容量瓶定容时,视线应与容量瓶上的刻度线在同一条直线上,且
与凹液面最低处相切。若仰视定容,则加水过多,结果偏低;若俯视定容,则加
水过少,结果偏高,如图丙所示。
必备知识通关
必备知识通关
步骤 洗涤
操作 酸式滴定管未用标准溶液润洗 碱式滴定管未用待测溶液润洗
锥形瓶用待测溶液润洗 锥形瓶洗净后还留有蒸馏水
c(I-),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液 a.准确称取AgNO3基准物4.246 8 g(0.025 0 mol)后,配制成250 mL标准 溶液,放在棕色试剂瓶中避光保存,备用。 b.配制并标定100 mL 0.100 0 mol·L-1 NH4SCN标准溶液,备用。
解题能力提升
VA 偏大 偏小 偏大 不变
cB 偏高 偏低 偏高 无影响
必备知识通关
必备知识通关
高考链接 [2015广东,12]准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.100 0
mol·L-1 NaOH溶液滴定。下列说法正确的是
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定 B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大 C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定 D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小 答案 B
解题能力提升
解题能力提升
解题能力提升
命题角度2 导电能力与酸碱中和滴定图像 以中和滴定为载体,考查指示剂的选择、滴定过程中溶液酸碱性的变化、 导电能力的变化等知识。 示例5 [2019全国卷Ⅰ,11,6分]NaOH溶液滴定邻苯二甲酸氢钾(邻苯二
甲酸H2A的Ka1=1.1×10-3,Ka2=3.9×10-6)溶液,混合溶液的相对导电能力
酸碱中和滴定和曲线培训课件

酸碱中和滴定和曲线
1
2/5/2021
3、原理:中和反应中 H++OH-=H2O 当n(H+)=n(OH-),完全中和
对于一元酸与碱反应时: C酸V酸=C碱V碱
4、关键:
①准确测出参加反应的两种溶液的体积。
②准确判断中和反应是否恰好进行完全。
酸碱中和滴定和曲线
⑶指示剂 变化确定终点 ——选灵—择—敏—原,——则变终—色点————明与——显变——、色—范——围—一—致
酸碱中和滴定和曲线
5
2/5/2021
2.仪器
2 酸式滴定管
.
酸
碱 碱式滴定管
中 和 锥形瓶
滴 定
铁架台
所 滴定管夹
需
的 仪
容量瓶
器
酸碱中和滴定和曲线
6
2/5/2021
中和滴定——主要实验仪器
2/5/2021
酸式滴定管使用
酸碱中和滴定和曲线
15
2、滴定过程: ⑴用 ——碱—式——滴——定—管—量取一定体积的待测液 (NaOH)于锥形瓶中,滴入2~3滴指示剂 (酚酞试液),待测液变成——红—色——
⑵振用荡锥—左—形—手—瓶握,活眼塞睛旋注转视开锥关形,瓶—右中——手——不—溶—断—液—旋—颜转— —色——变—化和滴定管————液—流—,速至度————红变色成——— —,无且色半分钟不褪色为止,记下滴定管刻度
4.3 突跃范围 9.7
酚酞
甲基橙
强碱滴定强酸
无→粉红
橙→黄
强酸滴定强碱
粉红→无
黄→橙
石蕊的变2/5色/2021不明显,所酸以碱中不和滴能定和做曲线中和滴定的指示剂。13
酸碱中和滴定曲线分析

酸碱中和滴定曲线分析常温下,用0.1000mol·L-1NaOH溶液滴定20.00 mL 0.1000mol·L-1HA 溶液,溶液pH随NaOH溶液体积( V )的改变而变化的滴定曲线如图所示:【认识酸碱中和滴定曲线的相同点和不同点】高。
②突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与弱酸反应(或强酸与弱碱反应) .③滴定终点的酸碱性不同,pH不同:室温下,当等体积、等浓度的一元强碱和一元强酸反应时,pH=7;但当等体积、等浓度的一元强碱和一元弱酸(或一元强酸和一元弱碱)反应时,pH>7(或pH<7) .④指示剂的选择不同:强酸滴定弱碱用甲基橙,强碱滴定弱酸用酚酞;强酸与强碱的滴定,用甲基橙和酚酞即学即用1.(2016·全国卷Ⅰ,12)298 K时,在20.0 mL 0.10 mol·L-1氨水中滴入0.10 mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。
已知0.10 mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是()A.该滴定过程应该选择酚酞作为指示剂B.M点对应的盐酸体积为20.0 mLC.M点处的溶液中c(NH+4)=c(Cl-)=c(H+)=c(OH-)D.N点处的溶液中pH<122.室温时,向20 mL 0.100 0 mol·L-1H2C2O4溶液中滴加0.100 0 mol·L-1NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化关系如图所示。
下列有关叙述错误的是()A.忽略H2C2O4的第二步电离,由题给信息,可以计算出常温下H2C2O4的电离常数B.A、B、C三点所对应的溶液中,水的电离程度最小的是A点C.A、B、C三点所对应的溶液中,均有c(Na+)<c(OH-)+c(HC2O-4)+2c(C2O2-4)D.在B点溶液中,生成的含钠化合物有两种,且c(HC2O-4)+2c(C2O2-4)=0.100 0 mol·L-13.下列滴定中,指示剂的选择或滴定终点颜色变化有错误的是()提示:2KMnO4+5K2SO3+3H2SO4===6K2SO4+2MnSO4+3H2O、I2+Na2S===2NaI+S↓选项滴定管中的溶液锥形瓶中的溶液指示剂滴定终点颜色变化A NaOH溶液CH3COOH溶液酚酞无色→浅红色【其他滴定】1.(2017·全国卷Ⅱ)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为MnO-4+H++H2C2O4―→Mn2++CO2↑+H2O。
酸碱中和滴定曲线图像考点分析

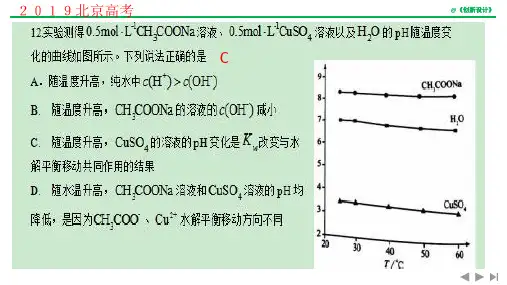
D. 滴定 过程 中可 能 出现 : c( CH。 CO OH ) > f( CH 。 COO一)> C( H )> C( Na )>
c(o H 一 )
解析 : 由图像 中 和 百 分 之 百 时 的 p H 突
跃 可 知 酸 性 最 强 的 是 HA, 最 弱 的 是 HD , 故
一 ( H +) 知 A 项 错
。
因 醋 酸 钠 能 水 解 导 致
HB 两 种 溶 质 , 且 其浓 度 相 等 , 又 因 P 点 时 溶
液呈 酸 性 , 故 可 知 H B 的 电 离 程 度 大 于 Na B
溶液 呈碱 性 , 在点 ② 时 p H 一 7推 知 溶 液 中 含
有 醋 酸
相结 合 思想 的功 能 。
一
= .考 查 溶液 中粒 子浓 度大 小 关系
考 查 电解 质的 强弱 判断
1 1 厂
倒 2 常温下 , 用0 . 1 0 0 0 o t o 1 . L N a O H
溶 液 滴 定 2 0 . 0 0 m L 一
0 . 1 0 0 0 mo l ・L
f( Na 。 。 ) > C( H B) > C( H ) > c( OH )
C ( CH 3 COO H ) +C ( H ) B .点 ② 所 示 溶 液 中 :C ( Na ) 一
c( CH 3 CO O H ) + C( C H 3 CO O 一)
C. p H 一 7时 , 三 种 溶 液 中 : f( A
) 。
器 数 o %
‘ 州日
A. 点 ① 所 示 溶
。
¨ … 川 “
化学实验中的溶液的酸碱中和滴定
化学实验中的溶液的酸碱中和滴定在化学实验中,溶液的酸碱中和滴定是一种常用的分析方法。
它通过滴加已知浓度的酸或碱溶液到待测溶液中,利用酸碱反应的中和反应完成对待测物质浓度的测定。
本文将介绍溶液的酸碱中和滴定的原理、操作步骤以及注意事项。
一、原理溶液的酸碱中和滴定是基于酸碱中和反应的理论基础进行的。
在酸碱反应中,酸和碱发生化学反应,产生相应的盐和水。
滴定过程中,通过逐滴加入酸或碱溶液,使待测溶液中的反应物与滴加溶液中的反应物按化学计量比例进行反应,从而达到酸碱中和的状态。
当酸或碱溶液滴加到与待测溶液中的反应物完全反应时,可以根据滴加的酸碱溶液的体积计算出待测溶液中的物质浓度。
二、操作步骤1.准备工作首先,需要准备好实验所需的仪器和试剂,包括滴定管、容量瓶、酸或碱溶液、指示剂等。
同时,要确保实验操作区域的清洁和安全,避免交叉污染和意外事故的发生。
2.样品制备将待测溶液准备好,并计量出适量的待测溶液放入容量瓶中。
3.滴定过程a) 将滴定管插入滴定瓶中,吸取适量的滴定液。
b) 将滴定管中的滴定液滴加到容量瓶中的待测溶液中。
c) 同时加入一滴指示剂,用以指示中和点的变化。
d) 持续滴加滴定液,直到待测溶液的颜色变化示意达到中和点。
e) 记录滴定液的滴定体积。
4.计算结果根据已知滴定液的浓度和滴定液的滴定体积,可以计算出待测溶液中的物质浓度。
三、注意事项1.实验过程中应注意操作的准确性和仪器的清洁,避免误差的发生。
2.选用适当的指示剂,以获得准确的中和点。
3.滴定液和待测溶液应有明显的颜色区分,便于观察颜色变化。
4.滴定液应以适量滴加,避免一次加入过多导致误差。
5.实验过程中,要注意安全操作,避免对皮肤和眼睛的直接接触。
总结:溶液的酸碱中和滴定是一种常用的分析方法,通过对待测溶液中的物质浓度进行测定。
在操作过程中,我们需要掌握滴定的原理和操作步骤,并注意实验的准确性和安全性。
只有在滴定液与待测溶液中的物质按化学计量比例完全反应时,才能得到准确的测定结果。
第32讲中和滴定曲线的分析与应用(精讲课件)-2023届高考二轮精准复习45讲(全国通用)
c(Na+)+ c(H+)=c(A-)+ c(OH-),溶液呈中性时 c(H+)=c(OH-),
c(A-)=c(Na+)= 0.1x mol·L-1;根据物料守恒,c(HA)=0.1×20 mol·L-1- 0.1x mol·L-1
20+x
20+x
20+x
2-0.1x =
20+x
10-7× 0.1x
回答下列问题: (1)向二元弱酸 H2Y 中滴加 NaOH 溶液,依次反应的离子方程式为 _______________。 (2)随着 NaOH 溶液的滴加,lgccHHY2Y-________(填“增大”或“减小”, 下同),lgccHYY2--________。 (3)Ka2(H2Y)=________。 (4)在交叉点“e”,c(H2Y)________(填“>”“<”或“=”)c(Y2-)。
①滴定曲线特点
氢氧化钠滴定等浓度等体积的盐 盐酸滴定等浓度等体积的氢氧
酸、醋酸的滴定曲线
化钠、氨水的滴定曲线
CH3COONa呈碱性:酚酞作指示剂 NH4Cl呈酸性:甲基橙作指示剂
②读懂滴定曲线
曲线起点不同:碱滴酸,起点在下;酸滴碱,起点在上 突变范围不同:强与强,突变大;强与弱,突变小 终点pH值不同:强与强,终点pH=7;
数、δ1 为 HC2O4- 分 布系数、δ2 为 C2O24-
δ1 为 H2PO- 4 δ2 为 HPO24-
分布系数、 分布系数、
分布系数
δ3 为 PO34- 分布系数
当 pH<pKa 时,主要存 当溶液的 pH=1.2 时 当溶液的 pH=2 时,δ0=
在形式是 CH3COOH; δ0=δ1,pH=4.2 时 δ1 δ1,pH=7.1 时 δ1=δ2,pH
酸碱中和滴定曲线的绘制
在化学反应中的应用
酸碱中和反应
酸碱中和反应是酸和碱之间的反应, 通过滴定实验可以确定反应的终点, 从而计算出酸或碱的浓度。
酸碱滴定法
酸碱滴定法是一种常用的化学分析方 法,通过滴定实验可以测定溶液中酸 或碱的含量,绘制酸碱滴定曲线可以 确定滴定的终点。
在化学分析中的应用
物质鉴定
通过绘制酸碱滴定曲线,可以对未知物质进行鉴定,判断其是酸性还是碱性物 质。
果的准确性。
02
在滴定过程中,应控制好滴定速度,避免过快或过慢
,影响实验结果。
03
在绘制酸碱中和滴定曲线时,应选择合适的指示剂,
并控制好滴定终点,确保实验结果的准确性。
实验结果处理注意事项
01
在处理实验数据时,应进行误差分析和数据筛选, 排除异常值和误差较大的数据。
02
在绘制酸碱中和滴定曲线时,应选择合适的数学模 型和图表类型,以便更好地展示实验结果。
到中和点。记录下每滴定体积对应的pH值,绘制出滴定曲线。
THANKS FOR WATCHING
感谢您的观看
化学反应速率
酸碱中和反应的速率可以通过滴定实验进行测定,绘制酸碱滴定曲线可以研究 化学反应速率的影响因素。
在化学工业中的应用
产品质量控制
在化学工业中,绘制酸碱滴定曲线可以用于产品质量控制,确保生产过程中的原 料、中间产物和最终产品的质量符合要求。
生产过程优化
通过绘制酸碱滴定曲线,可以对化学工业中的生产过程进行优化,提高生产效率 和产品质量。
滴定管、容量瓶、烧杯、移液管、电 子天平等。
确保台面干净整洁,准备好实验记录 本和笔。
试剂
待测酸或碱溶液、标准碱或酸溶液、 指示剂等。
实验步骤
酸碱滴定法—酸碱滴定曲线及应用(分析化学课件)
02
一元弱酸(碱)的滴定
0.10mol·L-1 NaOH滴定20.00mL 0.10mol·L-1 HAC
(Ka(HAc)=10-4.76, Ka(HA)=10-7.00)
用0.1 mol/LNaOH滴定相同浓度的 HAc:
pHsp为8.72 突 跃:pH7.74~9.70之间。 指示剂:酚酞
-0.1%时:
pH=4.30
3. sp时: [H+]=[OH-] pH=7.00
4. sp后:[OH-]=c(NaOH)(过量)
+0.1%时:
[H+]=2.0×10-10mol·L-1 pH=9.70
0.1000mol·L-1 NaOH滴定20.00mL 0.1000mol·L-1 HCl
NaOH mL
V2
NaCl+ H2O NaHCO3 V2
V1 第一计量点
V2
CO2 + H2O 第二计量点
小结
1. 酸碱指示剂: 了解作用原理, 影响因素, 掌握常用指示剂(MO, MR, PP)的 变色区间和变色点. 理论变色范围 pH=PKa±1
2. 酸碱滴定曲线和指示剂的选择: 强酸(碱)滴定、 一 元弱 酸(碱)滴定过程中pH计算, 重点是
Ka值对突跃范围的影响: 酸愈弱,Ka越小,突跃范围越小。
强酸滴定一元弱碱
用0.1 mol/LHCl滴定 相同浓度的NH3。
pHsp:5.28 突 跃:pH4.30~6.25之间。 指示剂:甲基红
03
多元酸和混合酸的滴定
多元酸的滴定
多元酸的滴定: 用等浓度NaOH滴定0.10 mol/L
H3PO4 pHsp1=4.70 甲基橙 pHsp2=9.66 酚酞 * CKa1≥10-8 准确的滴定, * 相邻两级Ka比值≥ 104, 分步滴定。
