高中化学第六章 化学反应与能量单元测试及答案(1)
新高考化学第六章 化学反应与能量 单元测试及答案(1)

新高考化学第六章化学反应与能量单元测试及答案一、选择题1.某同学为探究FeCl3与KI反应是否存在反应限度,设计了如下实验方案(FeCl3溶液、KI 溶液浓度均为0.1mo1・L-1),最合理的方案是A.方案1 B.方案2 C.方案3 D.方案4【答案】D【详解】KI溶液和FeCl3溶液发生氧化还原反应生成Fe2+和I2,反应的离子方程式为2Fe3++2I-═2Fe2++I2,反应后的溶液中加入CCl4,如有机层呈紫红色,则说明生成碘;向含Fe3+的溶液中滴加几滴KSCN溶液呈血红色,这是Fe3+的特殊反应,所以可滴加KSCN溶液,溶液显血红色,发生Fe3++3SCN-═Fe(SCN)3,就说明Fe3+没有反应完,故D正确。
2.Mg-H2O2电池可用于驱动无人驾驶的潜航器。
该电池以海水为电解质溶液,示意图如图。
该电池工作时,下列说法正确的是()A.Mg电极是该电池的正极B.H2O2在石墨电极上发生氧化反应C.石墨电极附近溶液的碱性增强D.溶液中Cl-向正极移动【答案】C【分析】镁、过氧化氢和海水形成原电池,镁做负极发生氧化反应,过氧化氢在正极上发生还原反应,过氧化氢做氧化剂被还原为OH-,溶液pH增大,原电池中阴离子移向负极。
【详解】A.组成的原电池的负极被氧化,镁为负极,不是正极,故A错误;B.双氧水作为氧化剂,在石墨上被还原变为氢氧根离子,发生还原反应,故B错误;C.双氧水作为氧化剂,在石墨上被还原变为氢氧根离子,电极反应为,H2O2+2e-=2OH-,故溶液pH值增大,故C正确;D.溶液中Cl-移动方向与同外电路电子移动方向一致,应向负极方向移动,故D错误;答案选C。
3.下列反应属于放热反应的是A.氢氧化钡晶体和氯化铵晶体的反应B.能量变化如图所示的反应C.化学键断裂吸收的热量比化学键生成放出的热量多的反应D.燃烧反应和中和反应【答案】D【分析】反应物总能量大于生成物总能量,或反应物断键吸收的能量小于生成物成键放出的热量,该反应为放热反应,据此进行分析。
2021年高中化学必修二第六章《化学反应与能量》经典复习题(答案解析)(1)

一、选择题1.Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+ Mg =Mg2++ 2Ag+2Cl-。
有关该电池的说法正确的是A.Mg为电池的正极B.负极反应为AgCl+e-=Ag+Cl-C.Cl-移向负极D.电流由镁电极经外电路流向正极2.一定温度下,向容积为4L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,下列对反应的推断合理的是A.该反应的化学方程式为3B+4C⇌6A+3DB.反应进行到1s时,υ(A)=υ(D)C.反应进行到6s时,各物质的反应速率相等D.反应进行到6s时,B的平均反应速率为0.025mol⋅(L⋅s)−13.三元电池成为2019年我国电动汽车的新能源,其充电时总反应为:LiNi x Co y Mn z O2+6C(石墨)=Li1-a Ni x Co y Mn z O2+Li a C6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。
下列说法正确的是A.允许离子X通过的隔膜属于阴离子交换膜B.充电时,A为阴极,Li+被氧化C.可从无法充电的废旧电池的石墨电极中回收金属锂D.放电时,正极反应式为Li1-a Ni x Co y Mn z O2+aLi++ae-=LiNi x Co y Mn z O24.两电极用导线连接插入电解质溶液中(不考虑溶液中溶解的氧气的影响),你认为不能构成原电池的是()选项A B C D 电极材料Zn Fe Cu Al电极材料Cu Zn Ag Sn电解质溶液CuCl2溶液H2SO4溶液CuSO4溶液NaOH溶液A.A B.B C.C D.D5.运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生H2的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。
下列说法不正确的是A.HCOOH吸附在催化剂表面是一个吸热过程B.HCOO*+H*═CO2+2H*是该历程的决速步骤C.该反应过程中存在C-H键的断裂和C=O键的生成D.Pd和Rh作催化剂时HCOOH分解产生H2的反应热相同6.向某密闭容器中加入0.3 mol A、0.1 molC、和一定量的B三种气体。
黄冈市高中化学必修二第六章《化学反应与能量》经典测试卷(含答案)(1)
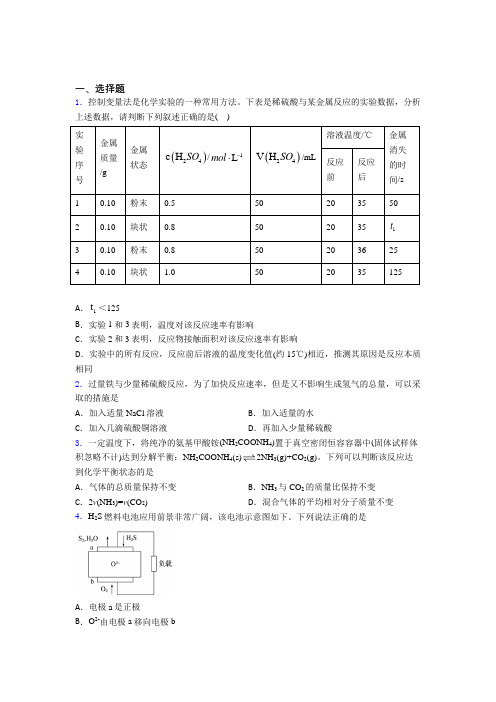
一、选择题1.控制变量法是化学实验的一种常用方法。
下表是稀硫酸与某金属反应的实验数据,分析上述数据,请判断下列叙述正确的是( )实验序号金属质量/g金属状态()24c H SO/1Lmol-⋅()24V H SO/mL溶液温度/℃金属消失的时间/s反应前反应后10.10粉末0.550203550 20.10块状0.85020351t30.10粉末0.85020362540.10块状 1.0502035125A.1t<125B.实验1和3表明,温度对该反应速率有影响C.实验2和3表明,反应物接触面积对该反应速率有影响D.实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因是反应本质相同2.过量铁与少量稀硫酸反应,为了加快反应速率,但是又不影响生成氢气的总量,可以采取的措施是A.加入适量NaCl溶液B.加入适量的水C.加入几滴硫酸铜溶液D.再加入少量稀硫酸3.一定温度下,将纯净的氨基甲酸铵(NH2COONH4)置于真空密闭恒容容器中(固体试样体积忽略不计)达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g)。
下列可以判断该反应达到化学平衡状态的是A.气体的总质量保持不变B.NH3与CO2的质量比保持不变C.2v(NH3)=v(CO2)D.混合气体的平均相对分子质量不变4.H2S燃料电池应用前景非常广阔,该电池示意图如下。
下列说法正确的是A.电极a是正极B.O2-由电极a移向电极bC.电极 a 的反应式为:2H2S+2O2--4e-=S2+2H2OD.当通入11.2 L O2,转移电子数2N A5.某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构如图,电池总反应可表示为2H2+O2=H2O,下列有关说法正确的是A.电流通过外电路从a极流向b极B.b极上的电极反应式为O2+2H2O+4e-=4OH-C.H+由a极通过固体酸电解质传递到b极D.每转移0.2 mol电子,在负极上消耗标况下1.12 L的O26.在一定条件下,A气体与B气体反应生成C气体。
高一化学必修二第六章 化学反应与能量知识点及练习题及答案(1)

高一化学必修二第六章化学反应与能量知识点及练习题及答案(1)一、选择题1.1mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应:X(g) + aY(g)bZ(g),反应达到平衡后,测得X的转化率为50% 。
而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是A.a=l,b=2 B.a=2,b=1 C.a=2,b=2 D.a=3,b=2【答案】D【分析】1mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应:X(g)+a Y(g)⇌b Z (g)。
反应达到平衡后,测得X的转化率为50%.而且,在同温同压下反应前后混合气体的密度之比和气体体积成反比即和气体物质的量成反比,讨论分析判断得到a、b的取值。
【详解】X(g)+a Y(g)⇌b Z(g)。
起始量(mol) 1 a 0变化量(mol) 0.5 0.5a 0.5b平衡量(mol) 0.5 0.5a 0.5b依据在同温同压下反应前后混合气体的密度之比和气体体积成反比即和气体物质的量成反比,在同温同压下测得反应前混合气体的密度是反应后混合气体密度的34,即反应后气体物质的量是反应前气体物质的量34,则得到;(0.5+0.5a+0.5b):(1+a)=3:4,计算得到:2b=a+1,依据选项中的取值分析判断,a=3,b=2符合计算关系。
故选D。
2.下列过程中ΔH小于零的是( )A.Ba(OH)2与 NH4Cl 固体混合B.氯化铵分解得氨气C.碳酸钙分解得二氧化碳D.实验室制备氢气【答案】D【分析】根据常见的放热反应有:所有的物质燃烧、金属与酸或水反应、中和反应、铝热反应、绝大多数化合反应等;常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),Ba(OH)2•8H2O与氯化铵的反应。
【详解】ΔH小于零的反应为放热反应。
A.Ba(OH)2•8H2O晶体和NH4Cl混合反应,是吸热反应,选项A不符合;B.氯化铵受热分解得氨气和氯化氢,属于吸热反应,选项B不符合;C.碳酸钙高温受热分解得二氧化碳和碳酸钙,属于吸热反应,选项C不符合;D .实验室制备氢气是利用金属锌与稀硫酸反应生成硫酸锌和氢气,属于放热反应,选项D 符合; 答案选D 。
高一化学第六章 化学反应与能量单元测试含答案解析(1)

高一化学第六章 化学反应与能量单元测试含答案解析一、选择题1.反应2NO(g)+2H 2(g)═N 2(g)+2H 2O(g)中,每生成7gN 2放出166kJ 的热量,该反应的速率表达式为v=k•c m (NO)•c n (H 2)(k 、m 、n 待测),其反应包含下列两步: ①2NO+H 2═N 2+H 2O 2(慢) ②H 2O 2+H 2═2H 2O(快) T ℃时测得有关实验数据如下:下列说法错误的是A .整个反应速度由第①步反应决定B .正反应的活化能一定是①<②C .该反应速率表达式:v=5000c 2(NO)•c(H 2)D .该反应的热化学方程式为2NO(g)+2H 2(g)═N 2(g)+2H 2O(g)△H=-664kJ•mol -1 【答案】B 【解析】 【详解】A .①2NO+H 2═N 2+H 2O 2(慢),②H 2O 2+H 2═2H 2O(快),反应历程中反应慢的决定反应速率,整个反应速度由第①步反应决定,故A 正确;B .反应①难以进行,说明反应的活化能高,正反应的活化能一定是①>②,故B 错误;C .比较图表Ⅰ、Ⅱ数据可知NO 浓度不变,氢气浓度增大一倍,反应速率增大一倍,Ⅲ、Ⅳ数据分析,H 2浓度不变,NO 浓度增大一倍,反应速率增大到4倍,据此得到速率方程,v=Kc 2(NO)•c(H 2),依据Ⅰ中数据计算K=5000,则速率方程v=5000c 2(NO)•c(H 2),故C 正确;D .反应2NO(g)+2H 2(g)═N 2(g)+2H 2O(g)中,每生成7gN 2放出166kJ 的热量,生成28gN 2放热664KJ ,热化学方程式为:2NO(g)+2H 2(g)═N 2(g)+2H 2O(g)△H=-664kJ•mol -1,故D 正确; 故选B 。
2.下列反应属于氧化还原反应,而且△H >0的是( ) A .铝片与稀H 2SO 4的反应 B .22Ba(OH)8H O 与4NH Cl 的反应 C .灼热的木炭与CO 2的反应D .甲烷在O 2中的燃烧反应【答案】C 【详解】A .铝片与稀H 2SO 4的反应中有元素化合价的变化,反应属于氧化还原反应;反应发生放出热量,反应属于放热反应,故△H <0,A 不符合题意;B .22Ba(OH)8H O 与4NH Cl 反应吸收热量,属于吸热反应;反应过程中元素化合价没有发生变化,故反应属于非氧化还原反应,B 不符合题意;C .灼热的木炭与CO 2反应产生CO ,反应发生吸收热量;反应过程中有元素化合价的变化,反应属于氧化还原反应,C 符合题意;D .甲烷在O 2中的燃烧,放出热量,属于放热反应;反应过程中有元素化合价的变化,因此反应属于氧化还原反应,D 不符合题意; 故合理选项是C 。
2021——2022学年高中化学人教版(新版本)必修第二册第六章《化学反应与能量》单元测试卷有答案

第六章《化学反应与能量》单元测试卷一、单选题(共15小题)1.已知氢气与溴蒸汽化合生成1 mol溴化氢时放出的能量51 kJ,1 mol H—H、Br—Br和H—Br键断裂时需要吸收的能量分别是436 kJ、a kJ和369 kJ则a为()A. 404B. 260C. 230D. 2002.关于化学反应的下列说法中正确的是()A.分子的种类和数目一定发生改变B.原子的种类和数目一定发生改变C.能量变化主要是由化学键变化引起的D.能量变化的大小与反应物的质量多少无关3.如图是以稀硫酸为电解质溶液的原电池装置,下列叙述正确的是()A.锌片上有气泡产生B.锌片为负极,铜片发生氧化反应C.电解质溶液中的H+向铜极移动D.电子流动方向:锌极→导线→铜极→电解质溶液→锌极4.一定温度下,恒容密闭容器中发生反应2NO2(g)2NO(g)+O2(g),达到平衡的标志是()①相同时间内,氧气的生成速率为n mol·L-1·s-1,二氧化氮的生成速率为2n mol·L-1·s-1①单位时间内生成n mol 氧气的同时生成2n mol的一氧化氮①混合气体的颜色不再变化①混合气体的密度保持不变①混合气体的平均相对分子质量不再改变①压强不再随时间变化而变化A. ①①①①B. ①①①C. ①①①D.全部5.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为2Ag+Zn(OH)2Ag2O+Zn+H2O,其放电过程是原电池反应,在此电池放电时,负极上发生反应的物质是() A. AgB. Zn(OH)2C. Ag2OD. Zn6.鱼雷采用Al—Ag2O动力电池,以溶有氢氧化钾的流动海水为电解液,电池反应为2Al+3Ag2O +2KOH===6Ag+2KAlO2+H2O,下列说法错误的是()A. Ag2O为电池的正极B. Al在电池反应中被氧化C.电子由Ag2O极经外电路流向Al极D.溶液中的OH-向Al极迁移7.下列说法不正确的是()A.化学反应可分为吸热反应和放热反应B.化学反应中的能量变化都是以热能的形式表现出来C.化学反应的实质是旧键的断裂与新键的生成D.化学反应能量变化的实质是旧键断裂吸收的能量与新键形成释放的能量大小不同8.酒精燃烧的过程中,发生了能量的转化。
盘锦市高中化学必修二第六章《化学反应与能量》测试卷(含答案)(1)
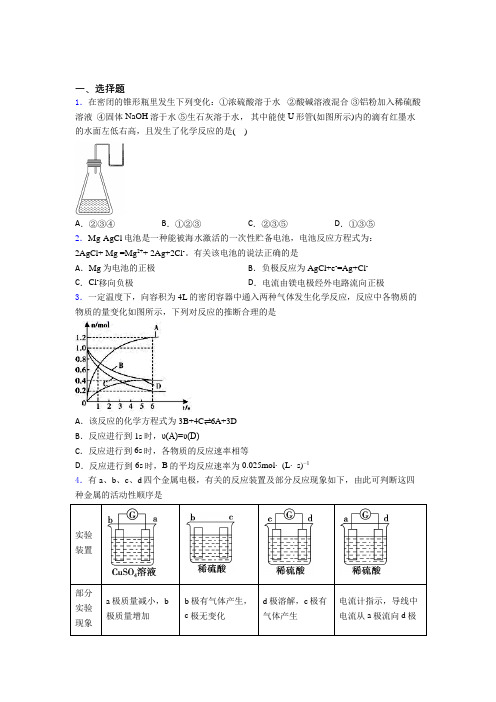
一、选择题1.在密闭的锥形瓶里发生下列变化:①浓硫酸溶于水②酸碱溶液混合③铝粉加入稀硫酸溶液④固体NaOH溶于水⑤生石灰溶于水,其中能使U形管(如图所示)内的滴有红墨水的水面左低右高,且发生了化学反应的是( )A.②③④B.①②③C.②③⑤D.①③⑤2.Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+ Mg =Mg2++ 2Ag+2Cl-。
有关该电池的说法正确的是A.Mg为电池的正极B.负极反应为AgCl+e-=Ag+Cl-C.Cl-移向负极D.电流由镁电极经外电路流向正极3.一定温度下,向容积为4L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,下列对反应的推断合理的是A.该反应的化学方程式为3B+4C⇌6A+3DB.反应进行到1s时,υ(A)=υ(D)C.反应进行到6s时,各物质的反应速率相等D.反应进行到6s时,B的平均反应速率为0.025mol⋅(L⋅s)−14.有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下,由此可判断这四种金属的活动性顺序是实验装置部分实验现象a极质量减小,b极质量增加b极有气体产生,c极无变化d极溶解,c极有气体产生电流计指示,导线中电流从a极流向d极A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c 5.一种以联氨(N2H4)为燃料的环保电池工作原理如图所示,电解质溶液显弱酸性,电池工作时产生稳定无污染的物质。
下列说法正确的是()A.在电极M充入N2H4,每消耗1molN2H4,会有4molH+通过质子交换膜B.该燃料电池工作时,化学能只能转化为电能C.N极的电极反应式为O2+2H2O+4e-=4OH-D.电极总反应式为N2H4+O2=N2+2H2O,电解质溶液的pH始终不变6.根据一定条件下NH4Cl有关转化过程的能量变化,判断下列说法不正确的是NH4Cl(s)=N(g)+4H(g)+Cl(g) △H1 NH4Cl(s)=NH3(g)+H(g)+Cl(g) △H2NH (g)+Cl-(g)=NH4Cl(s) △H3 Cl(g)+e-=Cl- (g) △H44A.△H4<△H1B.△H3<0C.△H1<△H2D.相同条件下,NH4Br和NH4I也进行类似转化,NH4Br的△H2比NH4I的大7.下列物质间的反应,其能量变化符合图示的是A.由Zn和稀H2SO4制氢气B.甲烷的燃烧C.Ba(OH)2·8H2O晶体和NH4Cl晶体混合搅拌D.氧化钙和水反应8.向某密闭容器中加入0.3 mol A、0.1 molC、和一定量的B三种气体。
人教高一化学第六章 化学反应与能量 练习题及答案

人教高一化学第六章 化学反应与能量 练习题及答案一、选择题1.关于碳和碳的氧化物知识网络图(图中“→”表示转化关系,“…”表示相互能反应)说法正确的是( )A .“C…CO 2”的反应是放热反应B .“CO→CO 2”的反应类型为置换反应C .“CO 2→CaCO 3”的反应可用于检验二氧化碳D .“CO 2 ⇌ H 2CO 3”的反应可用酚酞试剂验证 【答案】C 【详解】A . C 和CO 2的反应是吸热反应,故A 错误;B . “CO→CO 2”的反应可以是222CO O 2CO 点燃,是化合反应,也可以是2CO+CuOCu+CO 高温,也不属于置换反应,故B 错误;C . 检验二氧化碳使用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故C 正确;D . 二氧化碳与水反应生成碳酸,碳酸不能使酚酞溶液变色,故“CO 2 ⇌ H 2CO 3”的反应不可用酚酞试剂验证,故D 错误; 故选C 。
2.下列反应既属于氧化还原反应,又是吸热反应的是 A .铝片与盐酸的反应B .灼热的碳与CO 2的反应C .Ba(OH)2·8H 2O 与NH 4Cl 的反应D .甲烷在氧气中的燃烧反应【答案】B 【详解】A .金属与酸的反应属于放热反应,故A 错误;B .灼热的碳与CO 2的反应为吸热反应,且C 元素的化合价变化,属于氧化还原反应,故B 正确;C .Ba(OH)2•8H 2O 与NH 4Cl 的反应为放热反应,但没有元素的化合价变化,不属于氧化还原反应,故C 错误;D.甲烷在氧气中燃烧属于放热反应,故D错误;故选B。
【点睛】本题考查氧化还原反应和吸热反应,为高考高频考点,侧重反应类型判断的考查。
常见的吸热反应有:Ba(OH)2•8H2O与NH4Cl反应、大多数的分解反应、C(或氢气)参加的氧化还原反应等。
3.下列过程中ΔH小于零的是( )A.Ba(OH)2与 NH4Cl 固体混合B.氯化铵分解得氨气C.碳酸钙分解得二氧化碳D.实验室制备氢气【答案】D【分析】根据常见的放热反应有:所有的物质燃烧、金属与酸或水反应、中和反应、铝热反应、绝大多数化合反应等;常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),Ba(OH)2•8H2O与氯化铵的反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学第六章化学反应与能量单元测试及答案一、选择题1.全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2S x(2≤x≤8)。
下列说法错误的是A.电池工作时,正极可发生反应:2Li2S6+2Li++2e−=3Li2S4B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 gC.石墨烯的作用主要是提高电极a的导电性D.电池充电时间越长,电池中Li2S2的量越多【答案】D【详解】A.原电池工作时,Li+向正极移动,则a为正极,正极上发生还原反应,随放电的多少可能发生多种反应,其中可能为2Li2S6+2Li++2e-=3Li2S4,故A正确;B.原电池工作时,转移0.02mol电子时,氧化Li的物质的量为0.02mol,质量为0.14g,故B正确;C.石墨能导电,利用石墨烯作电极,可提高电极a的导电性,故C正确;D.电池充电时间越长,转移电子数越多,生成的Li和S8越多,即电池中Li2S2的量越少,故D错误;答案为D。
2.反应3A(g)+B(g)═2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为:①v A═1mol/(L•min),②v C═0.5 mol/(L•min),③v B═0.5mol/(L•min),三种情况下该反应速率大小的关系正确的是( )A.②>③>①B.①>②>③C.③>①>②D.②>①>③【答案】C【详解】都转化为A表示的反应速率来比较反应速率的快慢。
①v A=1 mol/(L•min);②v C=0.5 mol/(L•min),由3A(g)+B(g)═2C(g),则转化为A表示的反应速率v A=0.5mol/(L•mi n)×32=0.75 mol/(L•min);③v B=0.5 mol/(L•min),由3A(g)+B(g)═2C(g),则转化为A表示的反应速率v A=0.5 mol/(L•min)×3=1.5 mol/(L•min);显然③>①>②,故选C。
3.运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是A.铝的金属活动性比铁强,则铝制品比铁制品更易锈蚀B.水和过氧化氢的组成元素相同,则二者的化学性质相同C.Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8D.同温下分解氯酸钾,加催化剂的反应速率更快,说明催化剂可以改变反应速率【答案】D【详解】A.铝的金属活动性比铁强,但铝制品比铁制品更耐腐蚀,因为在铝制品表明能形成一层致密的氧化膜,A错误;B.水和过氧化氢的组成元素相同,二者的化学性质不相同,B错误;C.Na+、Mg2+、Cl-的最外层电子数均为8,但离子的最外层电子数不一定均为8,例如铁离子等,C错误;D.同温下分解氯酸钾,加催化剂的反应速率更快,说明催化剂可以改变反应速率,D正确;答案选D。
4.在密闭容器中进行反应:X 2(g)+3Y2(g)2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是()。
A.c(Z)=0.5 mol·L-1B.c(Y2)=0.5 mol·L-1C.c(X2)=0.2 mol·L-1D.c(Y2)=0.6 mol·L-1【答案】B【详解】若反应向正反应进行,假定完全反应,则:X 2(g)+3Y2(g)2Z(g)起始量(mol/L) 0.1 0.3 0.2变化量(mol/L) 0.1 0.3 0.2平衡量(mol/L) 0 0 0.4若反应逆反应进行,假定完全反应,则:X 2(g)+3Y2(g)2Z(g)起始量(mol/L) 0.1 0.3 0.2变化量(mol/L) 0.1 0.3 0.2平衡量(mol/L) 0.2 0.6 0由于为可逆反应,物质不能完全转化,所以平衡时浓度范围为0<c(X2)<0.2,0<c(Y2)<0.6,0<c(Z)<0.4,B正确、ACD错误;答案选B。
【点晴】化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,计算出相应物质的浓度变化量,实际变化量小于极限值,解答的关键是利用可逆反应的不完全性,运用极限假设法解答。
5.下列反应中属于氧化还原反应又是吸热反应的是 A .镁与盐酸反应放出氢气 B .氢氧化钠与盐酸的反应 C .硫在空气或氧气中燃烧 D .灼热的炭与二氧化碳反应【答案】D 【详解】A .镁与盐酸反应放出氢气,属于放热反应,A 不合题意;B .氢氧化钠与盐酸的反应,属于非氧化还原反应,B 不合题意;C .硫在空气或氧气中燃烧,属于放热反应,C 不合题意;D .灼热的炭与二氧化碳反应,既属于氧化还原反应,又属于吸热反应,D 符合题意; 故选D 。
6.航天飞船可用肼(N 2H 4)做动力源,已知液态肼与液态 H 2O 2 反应时放出大量的热量, 下列说法错误的是A .1mol 肼(N 2H 4)分子中含有4molN-H 键B .该反应中的热量变化如图所示C .该反应的反应物总键能小于生成物总键能D .该反应的化学方程式为:N 2H 4(l)+2H 2O 2(l)=N 2(g)+4H 2O(g),其产物对环境无污染 【答案】B 【详解】 A .肼结构式为,1个肼分子中含有4个N-H 键,则1mol 肼中含有4molN-H 键,故A 正确;B .如果反应物总能量大于生成物总能量,则该反应为放热反应,否则为吸热反应,液态肼和液态过氧化氢反应时放出大量热量,则该反应为放热反应,图中为吸热反应,不符合,故B 错误;C .液态肼和液态过氧化氢反应时放出大量热量,则该反应为放热反应,断键吸收能量、成键放出能量,该反应为放热反应,则反应的反应物总键能小于生成物总键能,故C 正确;D .氮气和水都无毒,所以其产物无污染,故D 正确; 故答案为B 。
7.一定条件下,在容积固定的某密闭容器中发生反应N 2(g )+3H 2(g )Δ催化剂2NH 3(g ),在10s 内N 2的浓度由5 mol/L 降至4mol/L ,下列说法正确的是( ) A .用NH 3表示的化学反应速率为0.1 mol/(L•s )B.升高温度,可以加快反应的反应速率C.增加H2的浓度或降低温度都会加快该反应的速率D.反应足够长时间,N2浓度降为零【答案】B【详解】A.反应计量数之比为1:3:2,设容器的体积为VL,2N的浓度由5mol/L降至4mol/L,变化了1Vmol,所以3NH变化了2Vmol,V(3NH)=2V10V(mol/L.s)=0.2mol/(L·s),选项A错误;B.升高温度,活化分子的百分数增大,有效碰撞的几率增大,化学反应速率增大,选项B 正确;C.该反应是在高温高压条件下进行,降低温度虽然平衡可以向右移动,但会降低反应速率,选项C错误;D.反应是可逆反应,不可能反应物全部转化为生成物,即N2浓度不可能降为零,选项D 错误;答案选B。
8.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液。
下列说法正确的是A.电子由Zn电极流出,经KOH溶液流向正极B.正极反应式为2Fe24O-+=Fe2O3+5H2OC.该电池放电过程中电解质溶液浓度不变D.电池工作时OH-向负极迁移【答案】D【解析】【详解】A.电子由电源的负极经导线流向正极,所以电子从锌极经导线流向K2FeO4极,A错误;B.KOH溶液为电解溶质溶液,则正极电极反应式为:2Fe24O-+8H2O+6e-=Fe(OH)3+10OH-,B 错误;C.该电池放电过程中电解质溶液浓度减小,C错误;D.电池工作时阴离子向负极移动,所以OH-向负极迁移,D正确;答案选D。
9.下列关于化学能与其他能量相互转化的说法正确的是()A.图1所示的装置能将化学能转变为电能B.图2所示的反应为吸热反应C.中和反应中,反应物的总能量比生成物的总能量低D.化学反应中能量变化的根本原因是化学键的断裂与生成【答案】D【详解】A.图1所示的装置没形成闭合回路,不能形成原电池,没有电流通过,所以不能把化学能转变为电能,选项A错误;B.图2所示的反应,反应物的总能量大于生成物的总能量,所以该反应为放热反应,选项B错误;C.中和反应是放热反应,所以反应物总能量大于生成物总能量,选项C错误;D.化学反应总是伴随着能量变化,断键需要吸收能量,成键放出能量,所以化学反应中能量变化的主要原因是化学键的断裂与生成,选项D正确;答案选D。
10.电化学在日常生活中用途广泛,图甲是镁-次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理。
下列说法正确的是A.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓B.图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合,转化成Cr(OH)3除去C.图乙电解池中,若有0.84 g阳极材料参与反应,则阴极会有168 mL(标准状况)的气体产生D.若图甲燃料电池消耗0.36 g镁产生的电量用以图乙废水处理,理论上可产生1.07g氢氧化铁沉淀【答案】A【详解】A.该原电池中,镁作负极,负极上镁失电子发生氧化反应,负极反应为Mg-2e-=Mg2+,电池反应式为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,正极上次氯酸根离子得电子发生还原反应,则总反应减去负极反应可得正极还原反应为Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓,A正确;B.图乙中惰性电极为阴极,Fe电极为阳极,则Cr2O72-离子向金属铁电极移动,与亚铁离子发生氧化还原反应生成的金属阳离子与惰性电极附近的OH-结合转化成Cr(OH)3除去,B 错误;C.图乙的电解池中,阳极反应式是Fe-2e-=Fe2+,阴极反应式是2H++2e-=H2↑,则n(Fe)=0.8456/gg mol=0.015mol,阴极气体在标况下的体积为0.015mol×22.4L/mol=0.336L,C错误;D.由电子守恒可知,Mg~2e-~Fe2+,由原子守恒可知Fe2+~Fe(OH)3↓,则n(Mg)=0.3624/gg mol=0.015mol,理论可产生氢氧化铁沉淀的质量为0.015mol×107g/mol=1.605g,D错误;答案选A。
11.目前科学家已开发出一种新型燃料电池——固体氧化物电池,该电池用辛烷(C8H18)作燃料,电池中间部分的固体氧化物陶瓷可传递氧离子,下列说法正确的是A.电池工作时,氧气发生氧化反应B.电池负极的电极反应:O2+2H2O+4e-=4OH-C.电池负极的电极反应:C8H18+25O2--50e-=8CO2↑+9H2OD.若消耗的O2为11.2 L(标准状况),则电池中有1 mol电子发生转移【答案】C【分析】该燃料电池中,辛烷失电子发生氧化反应,电极反应式为C8H18+25O2--50e-=8CO2+9H2O,正极上氧气得电子发生还原反应,电极反应式为O2+4e-=2O2-,再结合物质之间的反应来分析解答。
