实验《探究光的反射定律》
年中考物理重点实验复习《探究光的反射规律》

探究光的反射定律【考点梳理】(1)实验器材:平面镜、可折转的纸板、激光手电筒、量角器。
(2)纸板与平面镜的关系:垂直。
(3)(粗糙)纸板的作用:显示光路。
(4)折转纸板的目的:探究反射光线、入射光线、法线是否在同一平面内。
(5)让入射光线沿着FO入射,则反射光线沿着OE射出,说明在反射现象中,光路是可逆的。
(6)结论:反射定律。
【典例引领】(2023年齐齐哈尔中考题)24.小明利用如图装置探究光反射时的规律。
(1)如图1所示,实验时,把一个平面镜放在水平桌面上,再把白色纸板ENF(右侧可绕ON翻折)竖直地立在平面镜上,纸板上的直线ON应_________于镜面。
使一束光贴着纸板沿某一角度射到O点,光在纸板上发生________(选填“镜面”或“漫”)反射,呈现径迹。
光经平面镜反射,沿另一个方向射出;(2)改变光束入射的角度,多做几次,换用不同颜色的笔记录每次光的径迹。
取下纸板,用量角器测量ON两侧的∠i和∠r,是为了_________________________________________;根据实验结论可知:当入射光EO与平面镜夹角为50°时,反射角为__________;(3)让光沿图1中FO方向照射到镜面,它会沿着OE方向射出。
这表明:在光的反射现象中,光路是_________的。
(4)如图2所示,把纸板ENF右侧绕ON向前折或向后折,在右侧纸板上看不到反射光。
这表明:在反射现象中,反射光线、入射光线和法线都在___________内。
解析:(1)①法线与镜面垂直,纸板上的直线ON相当于法线,所以ON应垂直于镜面。
②我们能在纸板上看到入射光线和发射光线的路径,是由于光线在粗糙的纸板上发生了漫反射。
(2)③用量角器测量ON两侧的∠i和∠r,∠i是入射角,∠r是反射角,可以探究反射角与入射角的大小关系。
④当入射光EO与平面镜夹角为50°时,反射角90°-50°=40°(3)⑤若将一束光贴着纸板沿FO方向射到O点,光将沿图中的OE方向射出,即光线沿着原来反射光线的路径入射,反射光线会沿着原来入射光线的路径反射,说明在反射现象中,光路是可逆的。
《探究:光的反射定律》 学习任务单

《探究:光的反射定律》学习任务单一、学习目标1、理解光的反射现象,能够准确描述光的反射过程。
2、掌握光的反射定律,包括反射光线、入射光线和法线的位置关系,反射角与入射角的大小关系。
3、学会运用光的反射定律解释生活中的相关现象。
4、通过实验探究,培养观察能力、动手能力和逻辑思维能力。
二、学习重难点1、重点(1)光的反射定律的内容及理解。
(2)利用光的反射定律作图。
2、难点(1)探究光的反射定律的实验设计与操作。
(2)理解光路的可逆性。
三、学习方法1、理论学习:通过阅读教材、观看教学视频等方式,了解光的反射的基本概念和定律。
2、实验探究:亲自动手进行光的反射实验,观察现象,记录数据,分析得出结论。
3、实例分析:结合生活中的实际例子,如镜子反射、湖面反光等,加深对光的反射定律的理解和应用。
四、学习过程(一)知识回顾1、光在同种均匀介质中沿_____传播。
2、我们能够看到本身不发光的物体,是因为物体_____的光进入了我们的眼睛。
(二)新课导入思考:当光照到平面镜上时,会发生什么现象?为什么我们能在镜子中看到自己的像?(三)光的反射现象1、观察下面的图片,描述光的反射现象。
插入相关图片,如镜子反射、水面反光等2、定义:光射到物体表面时,有一部分光会被物体表面_____,这种现象叫做光的反射。
(四)光的反射定律1、实验探究:探究光的反射规律实验器材:激光笔、平面镜、白色硬纸板、量角器等。
实验步骤:(1)将平面镜平放在水平桌面上,把白色硬纸板竖直地立在平面镜上,纸板上的直线 ON 与镜面垂直。
(2)使一束光贴着纸板沿某一角度射到 O 点,经平面镜反射,在纸板上描出入射光线和反射光线的径迹。
(3)改变入射光线的方向,重做两次,换用另一种颜色的笔,记录光的径迹。
(4)取下纸板,用量角器测量入射角和反射角的大小,并记录在表格中。
实验记录表格:|实验次数|入射角|反射角||::|::|::|| 1 |||| 2 |||| 3 |||2、分析实验数据,得出光的反射定律:(1)反射光线、入射光线和法线在_____平面内。
物理实验探究光的反射定律
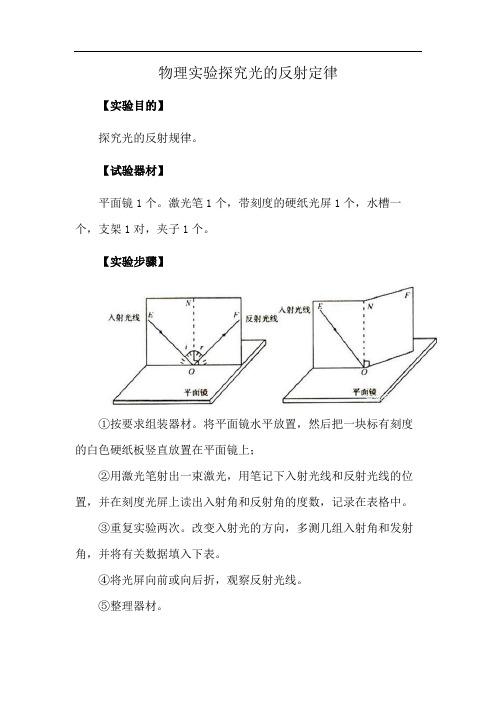
物理实验探究光的反射定律
【实验目的】
探究光的反射规律。
【试验器材】
平面镜1个。
激光笔1个,带刻度的硬纸光屏1个,水槽一个,支架1对,夹子1个。
【实验步骤】
①按要求组装器材。
将平面镜水平放置,然后把一块标有刻度的白色硬纸板竖直放置在平面镜上;
②用激光笔射出一束激光,用笔记下入射光线和反射光线的位置,并在刻度光屏上读出入射角和反射角的度数,记录在表格中。
③重复实验两次。
改变入射光的方向,多测几组入射角和发射角,并将有关数据填入下表。
④将光屏向前或向后折,观察反射光线。
⑤整理器材。
【实验结论】
1、在反射现象中,入射光线、反射光线、法线在同一平面内;
2、入射光线和反射光线分居法线两侧;
3、反射角等于入射角。
4、反射过程中光路是可逆的。
【实验补充】
1、以法线ON为轴,将硬纸板的B面向后旋转,这时在B面上观察不到反射光线,证明三线共面;通
过比较入射角和反射角的大小关系可以证明反射角等于入射角;反射光线和入射光线对称,并且对称还意味着分居法线两侧。
2、反射定律是用来确定反射光线位置的,对应每一条确定的入射光线而言,反射光线是唯一的。
3、如果光线垂直射向平面镜,入射角为EO,反射角为OF,入射光线、反射光线、法线重合。
实验1 探究光的反射定律 (解析版)

实验1 探究光的反射定律知识点一、光的反射现象1.光的反射:光从一种介质射向另一种介质的表面时,会有一部分光在介质表面反射回原介质中,这种传播现象叫光的反射。
2.一点、三线、两角(1)“一点”:投射到两种介质表面上的光线与表面的交点叫入射点;(2)“三线”:入射到介质表面的光线叫入射光线;经入射点做垂直于两种介质表面的辅助线叫法线;经介质表面,反射回原来介质的光线叫反射光线。
(3)“两角”:入射光线与法线的夹角叫入射角;反射光线与法线的夹角叫反射角。
3.人们能看见不是光源的物体的原因:我们能看到本身不发光的物体,是因为这些物体反射的光进入了我们的眼睛,产生视觉。
4.光的反射规律(定律):在反射现象中,反射光线、入射光线和法线都在同一平面内;反射光线、入射光线分别位于法线两侧;反射角等于入射角。
5.光的反射光路可逆:在探究光的反射规律实验中,如果让光逆着反射光的方向射到平面镜上,它被反射后就会逆着原来的入射光的方向射出。
这表明,在反射现象中,光路是可逆的。
如图所示。
知识点二、探究光反射时的规律1.纸板在实验中的三个作用(1)显示光的传播路径;(2)验证反射光线、入射光线和法线在同一平面内,具体操作是将纸板NOF向前或向后折转,使其和纸板EON不在同一平面内,观察有无反射光的径迹;(3)记录光路。
具体操作是在纸板上画出入射光和反射光的径迹,以分析反射角随入射角的变化而变化情况。
2.实验注意事项(1)应在光线较暗的室内进行实验,以便于观察实验现象;(2)实验时,纸板必须与平面镜垂直,否则在纸板上看不到反射光;(3)实验过程中严禁将激光对着人眼,以防灼伤眼睛;(4)通过镜面对入射光的反射作用,可以看出镜子有改变光路的作用;(5)本实验是一个归纳性实验,改变入射光的方向多次实验的目的是为了得到多组实验数据,从而得出普遍规律,避免实验结论的偶然性。
3.考向点拨(1)验证三线共面:沿折版中轴折转光屏是否还能看见反射光线;(2)验证分居:观察反射光线、入射光线是否在中轴两侧;(3)验证等角:通过量角器测量或带有刻度的折板光屏测量;(4)观察光路是否可逆:沿原反射光线路径改变入射光线,观察反射光线;(5)漫反射:能看见光线的传播方向说明折板发生了漫反射;(6)改变入射角(改变入射光线方向),进行多次实验的目的:寻找实验结论的普遍性;(7)光线的理想化模型:观察激光笔射出的光线即可构建用带箭头的直线表示光的传播方向和路径;(8)折转光屏用白色的目的:显示光线的路径;(9)实验应选较暗的环境目的是:便于观察实验现象;(10)实验时,折板应与平面镜垂直的目的:否则折板上看不到反射光;(11)当光垂直镜面入射时,入射角为零,为什么看不到反射光线:有反射光线,但反射角也为零,反射光线与入射光线在一条直线上。
中考物理实验专题《实验:探究光的反射定律》(解析版)
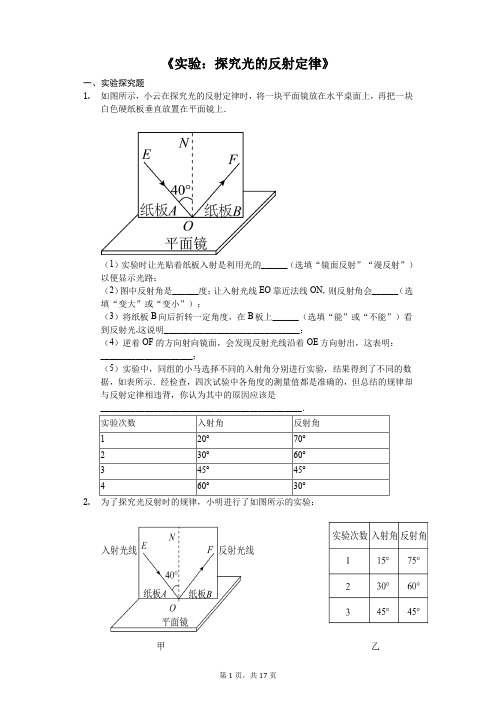
《实验:探究光的反射定律》一、实验探究题1.如图所示,小云在探究光的反射定律时,将一块平面镜放在水平桌面上,再把一块白色硬纸板垂直放置在平面镜上.(1)实验时让光贴着纸板入射是利用光的______(选填“镜面反射”“漫反射”)以便显示光路;(2)图中反射角是______度;让入射光线EO靠近法线ON,则反射角会______(选填“变大”或“变小”);(3)将纸板B向后折转一定角度,在B板上______(选填“能”或“不能”)看到反射光,这说明_______________________________;(4)逆着OF的方向射向镜面,会发现反射光线沿着OE方向射出,这表明:_____________________;(5)实验中,同组的小马选择不同的入射角分别进行实验,结果得到了不同的数据,如表所示.经检查,四次试验中各角度的测量值都是准确的,但总结的规律却与反射定律相违背,你认为其中的原因应该是2.(1)如图甲所示,如果入射角为40°,则根据光的反射定律,反射角的大小是___________.(2)图甲中的光屏是一个可折转的硬纸板,此光屏在实验中的作用是:①______________;② ______________(3)小明在实验时,选择入射角分别为15°、30°、45°的三条光线进行实验,结果得到了不同的数据(见表格乙).经检查,三次实验中各角度的测量值都是准确的,但总结的规律却与反射定律相违背.你认为其中的原因应该是 _______________________ ,反射定律中两角的关系表达为_______________________。
(4)如果让光线逆着OF的方向射向镜面,会发现反射光线沿着OE方向射出,这表明:_________________________3.如图所示,小云在探究光的反射定律时,将一块平面镜放在水平桌面上,再把一块白色硬纸板垂直放置在平面镜上.实验时让光贴着纸板入射是利用光的______选填“镜面反射”“漫反射”以便显示光路;图中反射角是_____度;让入射光线EO靠近法线ON,则反射角会______选填“变大”或“变小”;将纸板B向后折转一定角度,在B板上______选填“能”或“不能”看到反射光,这说明_____;逆着OF的方向射向镜面,会发现反射光线沿着OE方向射出,这表明:_________;实验中,同组的小马选择不同的入射角分别进行实验,结果得到了不同的数据,如表所示经检查,四次试验中各角度的测量值都是准确的,但总结的规律却与反射定律相违背,你认为其中的原因应该是______________________________________________4.桌面上,白色硬纸板垂直立在平镜面上。
实验3 探究光的反射定律(解析版)

实验3 探究光的反射定律基础考点梳理1. 实验装置图2.实验器材:平面镜、激光笔、可折转的硬纸板、笔、量角器等.(1)可折转的硬纸板的作用:①显示光路;①探究反射光线、入射光线和法线是否在同一平面内(2)量角器的作用:测量反射角和入射角的大小(3)平面镜的作用:使入射光线在其表面发生镜面反射3.实验环境:在较暗环境中进行实验的目的:减小其他光线对实验的影响,使实验现象更明显4. 实验过程(1)让光贴着硬纸板入射的目的:在硬纸板上显示光路(2)纸板与平面镜应该垂直放置的原因:若不垂直,则反射光线不能(选填“能”或“不能”)在纸板上呈现(3)记录光线的方法:用笔在纸板上沿着光路将其描画下来(4)多次改变入射角的大小进行实验的目的:可以探究反射角与入射角的大小关系,使实验结论更具普遍性(5)“三线共面”的判断方法将图中纸板右侧沿ON向后折,观察到右侧纸板上看不到反射光线,说明反射光线、入射光线和法线在(6)光路可逆的验证:将激光沿着FO方向射入,观察到反射光线沿着OE方向射出,说明光路具有可逆性5.实验结论反射光线、入射光线和法线在同一平面内;反射光线、入射光线分别位于法线两侧;反射角等于入射角.6.实验评价(1)使光路明显的方法:①向纸板上喷烟或雾;①选用表面粗糙的纸板(2)记录反射角和入射角互余的原因:将入射光线(或反射光线)与平面镜的夹角当成入射角(或反射角)(3)实验时从不同方向都能观察到光线的原因:光在粗糙纸板上发生了漫反射典型例题赏析实验结论:(1)反射现象中,反射光线、入射光线和法线在同一平面内;(2)反射光线、入射光线分别位于法线两侧;(3)反射角等于入射角.1.在探究光的反射规律的实验中,小明设计了如图所示的装置,平面镜放在水平桌面上,纸板E、F分别可绕ON转动,入射光AO始终紧贴纸板E射向平面镜的O点.(1)除图甲器材外,实验中还需要用到的测量仪器是量角器,为了使光线更明显,应在较暗(选填“亮”或“暗”)的环境下进行实验,为了能在光屏上清晰地显示出光的传播路径,光屏表面应粗糙(选填:“光滑”或“粗糙”)些.(2)实验中需要使轴ON始终与平面镜垂直,入射光AO紧贴纸板是为了在纸板E上呈现光路.(3)入射光AO紧贴纸板E射向平面镜的O点,在纸板F上可以看到反射光OB,小明想把光的径迹保留在纸板上,可以进行的操作是在入射光线AO上取点A,在反射光线OB上取点B,去掉光源,直线连接AO和OB即可.(4)(人教八上素材改编)实验中需要多次改变入射光的入射角度,最后纸板上留下多条光路,为了避免出错,应进行的操作是将每一组对应的光路进行标记编号.(5)改变入射光AO的入射角度,多次实验后,记录的数据如下:实验次数 1 2 3 4入射角20°30°45°60°反射角20°30°45°60°①由表中数据可知,在光的反射过程中,反射角等于入射角,反射角随入射角的增大而增大.①观察实验中多组光的径迹可知,在反射现象中,反射光线与入射光线分居法线两侧.(6)在上问的实验中,光屏上总能同时呈现出反射光线和入射光线,于是得出结论:光反射时,反射光线、入射光线和法线在同一平面内。
物理实验:探究光的反射定律

实验器材:平面镜、激光笔、量角器等。
实验步骤:将平面镜固定在量角器上,调整激光笔的角度,使光线射到平面镜上并反射到墙上, 观察入射角和反射角的关系。
反射光线的特性
反射光线与入射光线具有相 同的入射角和反射角
反射光线与入射值
实验器材
平面镜
定义:平面镜是一种反射面为平面的光学仪器
特点:具有成像清晰、真实的特点,常用于日常生活和科学实验中 用途:在光的反射定律实验中,平面镜常用来呈现清晰的像,便于观 察和测量 注意事项:使用时应注意保护镜面,避免刮伤或污染
激光笔
介绍激光笔在光的反射定律实 验中的作用
激光笔的特点和优势
激光笔的种类和选择
激光笔的使用注意事项
量角器
定义:量角器是一种测量角度的仪器
用途:在光的反射定律实验中,量角器用于测量入射角和反射角的角度
重要性:确保实验数据的准确性和可靠性,从而验证光的反射定律
使用方法:将量角器放置在反射面上,使量角器的中心与入射光或反射光的交点重合,然后读取 角度值
白纸
用途:作为实验背景,展示光反射现象 特点:平滑、白色,能够有效地反射光线 实验中的作用:提供光反射的界面,便于观察和记录实验结果 注意事项:保持白纸的干净整洁,避免污渍或划痕影响实验效果
总结实验结论
实验结果:通过实验验证了光的 反射定律
实验意义:通过实验加深了对光 的反射定律的理解
添加标题
添加标题
添加标题
添加标题
结论分析:光的反射定律在实验 中得到了验证,证明了反射角等 于入射角
实验不足:实验中存在一些误差, 需要进一步改进和完善
提出改进意见
实验操作流程需要进一步规范
《探究光的反射定律》光和眼睛PPT课件2

CONTENTS
光的反射 现象
光的反射 规律
镜面反射 和漫反射
光反射的 作图
01
反射现象
当光在同一种均匀介质中传播时是沿直线行进的, 那么光碰到障碍物时又会怎样传播呢?和我们生活中 那种物质碰到障碍物一样呢?请你猜想一下。
我们为什么能够看见发光的物体?
因为从物体发出的光进入我们的眼睛
我们为什么能看见平面镜、书等不发光的物体?
因为光射到黑板和粉笔字上都要发生光的反射。黑板“反光” 部分发生镜面反射,字上发生漫反射,两部分反射光同时射入眼 睛时,由于镜面反射反射光比漫反射的光强,对眼睛的刺激强烈。 所以黑板“反光”时粉笔字反而变得看不清楚。
入射角和反射角的大小分别为 ( D )
A.40°40°
B.40°50°
C.50°40°
D.50°50°
7.坐在教室各个位置的同学,眼睛能清楚地看到黑板上 面的字,这是由于:( D )
A.粉笔字发出的光射入眼内 B.眼睛发出的光觉察到黑板上粉笔字 C.粉笔字对光产生了镜面反射 D.粉笔字对光产生了漫反射
【练习5】(2014•德阳)在如图中,根据给出的反射光线 OB画出入射光线AO,并标出入射角及其度数.
.
C ห้องสมุดไป่ตู้ B
D C
.
漫 沿直线传播
0o 60o
65o
探究光的反射定律
波光粼粼
夏日的夜晚暑气难消,然而当你来到 美丽的滨河路,看到月光下,微风吹 拂的河面,波光粼粼,顿时心旷神怡 酷热全忘,你知道这波光粼粼是如何 形成的吗?它包含了光学的哪些知识 呢?
漫反射
平行光线射到凹凸不平的表面上,反射光线 射向各个方向
能
舒从
服 极
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验《探究光的反射定律》
1(09绵阳)右图是探究“光反射时的规律”的实验装置图。
把平面镜放在水平桌面上,再把一张可以沿ON向前或向后折的纸板竖直地立在平面镜上,纸板上的ON垂直于镜面。
一束红光贴着纸板沿EO射到f)点,光将沿OF方向射出,如果把纸板ON的右半边向后折,反射光线将_存在__(选填“存在”或“不存在”);如果一束蓝光沿原FO
方向射到0点,它反射后沿_ OE__方向射出。
2(09义乌)课堂上,老师用一套科学器材进行“研究光的反射定律”的实验演示,得出了正确的结论。
(1)根据光的反射定律,如果入射角为20o,则反射角的大小是20°(2)课后,某同学利用同一套实验器材,选择入射角分别为15o、30o、45o的三条光线进行实验,结果得到了不同的数据,如图所示。
经检查,三次试验中各角度的测量值都是准确的,但总结的规律却与反射定律相违背。
你认为其中的原因应该是将反射光线与反射面(或镜面)的夹角作为反射角(填“反射角判断错误可得分”;只表达出“反射角测量错误”的不得分)
3(09潍坊)(4分)小明同学用如图所示的装置,研究光的反射规律,其中有一个可折转的光屏,光屏在实验中的作用是:(写出两条)
①显示光的传播路径;
②探究入射光线、反射光线、法线是否共面。
3 (09安徽)如图,探究光的反射规律时,在平面镜的上方垂直放置一块光屏,光屏由可以绕ON折转的E、F两块板组成。
让一束光贴着光屏左侧的E板沿AO方向射到O点,在右侧F板上能看到反射光线OB。
实验时从光屏前不同的方向都能看到光的传播路径,这是因为光在光屏上发生了(填“镜面”或“漫”)反射。
若将F板向后折转一定的角度,则在F板上(填“能”或“不能”)看到反射光,此时反射光线和入射光线(填“在”或“不在”)同一平面内。
答案镜面不能在
4(09玉林)为了探究光反射的规律,小李进行如图12所示的实验。
(1)小李想探究反射光线与人射光线是否在同一平面内,他将如何操作?
(2)如果让光线逆着OF的方向射向镜面,会发现反射光线沿着OF方向射出,这表明:。
(1)将纸板B向前(后)折,观察在纸板B上是否有反射光线。
(2分)
(2)在反射现象中,光路是可逆的。
(2分) (本题满分4分)
5(09湘西)右图是研究光的反射规律的实验装置图,实验表明
A.反射角总是大于入射角
B.入射角总是大于反射角
C.反射角总是等于入射角
D.在反射现象中,光路是不可逆的
1 (2010滨州)在探究“平面镜成像特点”的试验中
(1)如图所示,在玻璃板前面放置一支点燃的蜡烛,再拿一支没有点燃的相同的蜡烛,在玻璃板后面移动,直到跟前面那支蜡烛的像。
若用光屏替换玻璃板后面的蜡烛,在玻璃板后面观察光屏,将(选填“能”或“不能”)观察到玻璃板前面点燃蜡烛的像。
(2)实验数据如下表:
实验表明:平面镜所成像是虚像,像与物的大小,像到平面镜的距离物体到平面镜的距离。
答案:(1)重合不能(2)相等等于
2(2010广安12.(5分)石林中学的张江同学自备器材,主动探究“平面镜成像的规律”,其情形如图7所示,他先把一块平板玻璃垂直立在水平桌面上,再准备A、B两支大小、外形完全一样的蜡烛,然后把点燃的蜡烛A立在玻璃板前,又把蜡烛B放在玻璃板后面,并移动蜡烛B的位置,使它与蜡烛A的像完全重合。
(1)张江同学在做探究实验时用透明玻璃板代替平面镜是为了_____________。
)看清镜后的情况
(2)他选择的蜡烛B与蜡烛A的大小、外形完全一样是为了_______________。
比较像与物的大小
(3)如果把蜡烛A向镜面移动一段距离,又移动蜡烛B去与蜡烛A的像比较,会发现蜡烛A像的大小_______________(选项“变大”、“变小”或“不变”)。
(4)如果在蜡烛A像的位置放一个光屏,光屏上___________承接到像(选项“会”或“不会”),这说明平面镜所成的像是________像(选填“虚”或“实”)。
3(2010北京)30.小明利用如图16所示的实验器材探究平面镜成像的特点。
请你解答以下问题:
(1)该实验采用薄透明平板玻璃作为平面镜,是为了能确定,能比较。
蜡烛A的像的位置蜡烛A的像与蜡烛B的大小(2)该实验选择两个相同的蜡烛A和B,是为了观察蜡烛B是否与蜡烛A所成的像。
重合
1(11舟山)9.如图是研究光的反射定律的实验装置,为了研究反射角与入射角之间的关系,实验时应进行的操作是
A.沿ON前后转动板E
B.沿ON前后转动板F
C.改变光线OB与ON的夹角
D.改变光线AO与ON的夹角
答案:D
2(11丹东市)40.(4分)在探究“光反射时的规律”实验中,某小组实验步骤如下:
A.把一个平面镜放在水平桌面上,再把一张硬纸板竖直地立在平面镜上,纸板上的直线
ON垂直于镜面,如图甲所示。
B.让一束红光贴着硬纸板沿着某一角度射到O点,经平面镜反射,沿着另一方向射出,在纸板上用笔描出入射光线EO和反射光线OF的径迹。
改变入射光线的方向,重做两次,换用另一种颜色
的笔,记录光的径迹(如甲图)。
C.取下硬纸板,用量角器测量NO两侧的角i 和角r。
D.纸板ENF是用两块纸板连接起来的,把纸板NOF向前折或向后折,观察反射光线。
(如乙图)根据上述实验步骤,回答下列问题:
(1)该实验中硬纸板显示出:反射光线与入射光线两侧。
(2)该实验中硬纸板NOF向前折或向后折是为了确定反射光线、入射光线、法线是否。
(3)由实验步骤C可以得到的规律是。
(4)在甲图中,如果将光线沿着FO射向平面镜时,你还会发现的规律
是。
答案:(1)分居法线(2)在同一平面内(3)反射角等于入射角(4)在反射时光路可逆
3(11铁岭)27.(5分)小义看到教学楼对面的玻璃幕墙把太阳光反射到教室里,他想:光在反射时会遵循怎样的规律?于是他利用平面镜、白纸板、量角器和激光笔进行如图甲和乙所示的实验。
(l)由图甲可以得出结论:反射角入射角。
(2)如图乙将纸板NOF 向后折,纸板上(填“能”或“不能”)看到反射光线,这说明。
(3)小义又找来了两支完全相同的蜡烛继续探究平面镜成像特点,他将白纸板和平面镜互换位置,做了如图丙所示的实验,但是他无法确定像的位置,他应该用
代替平面镜,就可以解决问题。
请你写出平面镜成像特点
(写出一条即可)。
答案:(1)等于(2)不能反射光线、入射光线和法线在同一平面内
(3)玻璃板:平面镜所成的像与物体大小相同(或平面镜所成的像是虚像或像与物体到平面镜的距离相等或像与物体的连线与平面镜垂直)
4(11长沙)34.为了研究光的反射规律,小明进行了如图所示的实验。
(1)请在图中画出反射光线,并标出反射角的大小。
(2)若将纸板B向后折转一定的角度,则在纸板B上不能看到反射光,此现象表明。
答案:(1)图略角度光线各占一分(2)反射光线、入射光线和法线都在同一平面内
(注:文档可能无法思考全面,请浏览后下载,供参考。
可复制、编制,期待你的好评与关注)。
