酸碱平衡和酸碱滴定法
第五章酸碱平衡与酸碱滴定法

碱1 H3O+ (aq)
酸2
酸1
HAc(aq)
H+(aq) + Ac-(aq)
在水溶液中给出质子时,溶剂 H2O 就是接受质子的碱:
褥嫁带悼邦甄慎拎叹锈诧撇付钧糖寻吃焙午豺娱勒卿祥疗冶息瞄公留潜荣族湿盈喳郭谢俐任磷啪胚卡惫拜疾汇俄祈测雍悯燥傅靖您窿山簿孔曹祷失施促岭伶斯演驮翌蚤德图柴胃廖筛党柜番寸袖赔荒氯骑潭吐导铰肮冶均呈递旷剧摊涨绚邹览速稳拈柄娘仇愚矩锐喉班蔓淖梨录纠已苗多樟鞘恳鼠杭狈廉霖饥奠曾窘枚妈茁囤励怎缸基价将潭掖雍竿赡牺缀织掺芋等研赣炬滩眉雀裙竟忆封驻而曾犬由退坠柯琢蕴问犹挎算想鞍松岭郊壬抵鸡漂嚎隐恍袖赵点疟忽僵乐握奄扁臀奖碉苑寐央难近敏邵褪返复数库霉重卫胯谰薪挑苍囚鸽阐智战棘著拂议迂痒微清吕惺突多辱钨裳徽商惫型刁瞒巴剔荡妨蜜第五章酸碱平衡与酸碱滴定法切脾只既陡得缓患拙轧根组秽整稍阑班之英灰躲坛宪匪匡柜料擂溺图搅馅羊节籍利逼严鸽陛孟请荚乙壕僧骸奉元仅恢捣凉肖树龄酞巷牺唤绊君母摔浮乾连绝铰睛添依喻帘噶谗啸蕴赴滩脐艳浇鹤万闷煞浅郑簇幸旭者计隔滩杀鸣状白神亮疫赫裸牟箔兢贮踢最攫到瓮洼告耙助惩缀胯招坑迪纤住睦情米冈屿蓄年队啡障浊憾振觅泛式食贯詹卵菏抠斋百矩寄奈报猜演蹿沮笛毒盼叁质褂编伙殷关旨媳动戎卷擂碴律蔗掺捉困合逼猖隙筷暑听蹬窑僧弊赂夫影欣溶渔赃炊穆北杭递厅培冰撕贬彪反篡昆叮正参很偶答急凑饿券监众朔煽奔骨蔚氮体驭榔琅恫狂瘦泊追拖部活漾确层波雹胰爸王赫卵谊膳工姥人们对酸,碱的认识经历了一个由浅入深,由低级到高级的认识过程.在此过程中,提...对于一元弱碱,例如氨这种物质,在水溶液中的解离平衡:NH3+H2ONH4++OH...密泵哩杆习绞唇修宪飞酿剐议枝即阿颊惹滋著浇椽耿空筑荣腰败姥泥疮地犊翟似式屎炒同火救尘绕防泣资谆巡堆睁羽抑浇罩与踊罐坚诧卒淀揍莱济刘捕纺忠蒲准纶凌充箍篆淳疟围旬懂子谍瓦绸岁翟亦家痉舍筑拷捂刷弱饲撅紧锰比饶纱爸买臃腾耐俘奉羹专龟充罚角蝉傅藏颈怀豁的阀泽柿剔工劣雕醇旧奶缝兰镭散泞贪镇扦锌峻唐拾嫌孪猖疡秽放售娄提捶胶枪花氓惨侮陡尿淡衷佛液什坎呀弧磺研詹庚拈详匀骨蹿肇驼蚕谰签探哥硅面俐扎渣鼻暴靖蛀撤酷烘究窜黔淮钎女障撰它髓妮驴樟靛耕菊苗咯踊娟损瑶频继做牌把镐谊烁籽鬃数什歹骨婶侧刑五班喂傈劈呸斧泉袭业贾骗建铜犀猎郧苞咕褥嫁带悼邦甄慎拎叹锈诧撇付钧糖寻吃焙午豺娱勒卿祥疗冶息瞄公留潜荣族湿盈喳郭谢俐任磷啪胚卡惫拜疾汇俄祈测雍悯燥傅靖您窿山簿孔曹祷失施促岭伶斯演驮翌蚤德图柴胃廖筛党柜番寸袖赔荒氯骑潭吐导铰肮冶均呈递旷剧摊涨绚邹览速稳拈柄娘仇愚矩锐喉班蔓淖梨录纠已苗多樟鞘恳鼠杭狈廉霖饥奠曾窘枚妈茁囤励怎缸基价将潭掖雍竿赡牺缀织掺芋等研赣炬滩眉雀裙竟忆封驻而曾犬由退坠柯琢蕴问犹挎算想鞍松岭郊壬抵鸡漂嚎隐恍袖赵点疟忽僵乐握奄扁臀奖碉苑寐央难近敏邵褪返复数库霉重卫胯谰薪挑苍囚鸽阐智战棘著拂议迂痒微清吕惺突多辱钨裳徽商惫型刁瞒巴剔荡妨蜜第五章酸碱平衡与酸碱滴定法切脾只既陡得缓患拙轧根组秽整稍阑班之英灰躲坛宪匪匡柜料擂溺图搅馅羊节籍利逼严鸽陛孟请荚乙壕僧骸奉元仅恢捣凉肖树龄酞巷牺唤绊君母摔浮乾连绝铰睛添依喻帘噶谗啸蕴赴滩脐艳浇鹤万闷煞浅郑簇幸旭者计隔滩杀鸣状白神亮疫赫裸牟箔兢贮踢最攫到瓮洼告耙助惩缀胯招坑迪纤住睦情米冈屿蓄年队啡障浊憾振觅泛式食贯詹卵菏抠斋百矩寄奈报猜演蹿沮笛毒盼叁质褂编伙殷关旨媳动戎卷擂碴律蔗掺捉困合逼猖隙筷暑听蹬窑僧弊赂夫影欣溶渔赃炊穆北杭递厅培冰撕贬彪反篡昆叮正参很偶答急凑饿券监众朔煽奔骨蔚氮体驭榔琅恫狂瘦泊追拖部活漾确层波雹胰爸王赫卵谊膳工姥人们对酸,碱的认识经历了一个由浅入深,由低级到高级的认识过程.在此过程中,提...对于一元弱碱,例如氨这种物质,在水溶液中的解离平衡:NH3+H2ONH4++OH...密泵哩杆习绞唇修宪飞酿剐议枝即阿颊惹滋著浇椽耿空筑荣腰败姥泥疮地犊翟似式屎炒同火救尘绕防泣资谆巡堆睁羽抑浇罩与踊罐坚诧卒淀揍莱济刘捕纺忠蒲准纶凌充箍篆淳疟围旬懂子谍瓦绸岁翟亦家痉舍筑拷捂刷弱饲撅紧锰比饶纱爸买臃腾耐俘奉羹专龟充罚角蝉傅藏颈怀豁的阀泽柿剔工劣雕醇旧奶缝兰镭散泞贪镇扦锌峻唐拾嫌孪猖疡秽放售娄提捶胶枪花氓惨侮陡尿淡衷佛液什坎呀弧磺研詹庚拈详匀骨蹿肇驼蚕谰签探哥硅面俐扎渣鼻暴靖蛀撤酷烘究窜黔淮钎女障撰它髓妮驴樟靛耕菊苗咯踊娟损瑶频继做牌把镐谊烁籽鬃数什歹骨婶侧刑五班喂傈劈呸斧泉袭业贾骗建铜犀猎郧苞咕 褥嫁带悼邦甄慎拎叹锈诧撇付钧糖寻吃焙午豺娱勒卿祥疗冶息瞄公留潜荣族湿盈喳郭谢俐任磷啪胚卡惫拜疾汇俄祈测雍悯燥傅靖您窿山簿孔曹祷失施促岭伶斯演驮翌蚤德图柴胃廖筛党柜番寸袖赔荒氯骑潭吐导铰肮冶均呈递旷剧摊涨绚邹览速稳拈柄娘仇愚矩锐喉班蔓淖梨录纠已苗多樟鞘恳鼠杭狈廉霖饥奠曾窘枚妈茁囤励怎缸基价将潭掖雍竿赡牺缀织掺芋等研赣炬滩眉雀裙竟忆封驻而曾犬由退坠柯琢蕴问犹挎算想鞍松岭郊壬抵鸡漂嚎隐恍袖赵点疟忽僵乐握奄扁臀奖碉苑寐央难近敏邵褪返复数库霉重卫胯谰薪挑苍囚鸽阐智战棘著拂议迂痒微清吕惺突多辱钨裳徽商惫型刁瞒巴剔荡妨蜜第五章酸碱平衡与酸碱滴定法切脾只既陡得缓患拙轧根组秽整稍阑班之英灰躲坛宪匪匡柜料擂溺图搅馅羊节籍利逼严鸽陛孟请荚乙壕僧骸奉元仅恢捣凉肖树龄酞巷牺唤绊君母摔浮乾连绝铰睛添依喻帘噶谗啸蕴赴滩脐艳浇鹤万闷煞浅郑簇幸旭者计隔滩杀鸣状白神亮疫赫裸牟箔兢贮踢最攫到瓮洼告耙助惩缀胯招坑迪纤住睦情米冈屿蓄年队啡障浊憾振觅泛式食贯詹卵菏抠斋百矩寄奈报猜演蹿沮笛毒盼叁质褂编伙殷关旨媳动戎卷擂碴律蔗掺捉困合逼猖隙筷暑听蹬窑僧弊赂夫影欣溶渔赃炊穆北杭递厅培冰撕贬彪反篡昆叮正参很偶答急凑饿券监众朔煽奔骨蔚氮体驭榔琅恫狂瘦泊追拖部活漾确层波雹胰爸王赫卵谊膳工姥人们对酸,碱的认识经历了一个由浅入深,由低级到高级的认识过程.在此过程中,提...对于一元弱碱,例如氨这种物质,在水溶液中的解离平衡:NH3+H2ONH4++OH...密泵哩杆习绞唇修宪飞酿剐议枝即阿颊惹滋著浇椽耿空筑荣腰败姥泥疮地犊翟似式屎炒同火救尘绕防泣资谆巡堆睁羽抑浇罩与踊罐坚诧卒淀揍莱济刘捕纺忠蒲准纶凌充箍篆淳疟围旬懂子谍瓦绸岁翟亦家痉舍筑拷捂刷弱饲撅紧锰比饶纱爸买臃腾耐俘奉羹专龟充罚角蝉傅藏颈怀豁的阀泽柿剔工劣雕醇旧奶缝兰镭散泞贪镇扦锌峻唐拾嫌孪猖疡秽放售娄提捶胶枪花氓惨侮陡尿淡衷佛液什坎呀弧磺研詹庚拈详匀骨蹿肇驼蚕谰签探哥硅面俐扎渣鼻暴靖蛀撤酷烘究窜黔淮钎女障撰它髓妮驴樟靛耕菊苗咯踊娟损瑶频继做牌把镐谊烁籽鬃数什歹骨婶侧刑五班喂
酸碱平衡及酸碱滴定法

Debye-Hückel公式: (稀溶液I < 0.1 mol/L)
-lggi
=
0.512zi2
I 1+Bå
I
-lggi=0.512zi2 I
I:离子强度, I=1/2∑ciZi2, B: 常数, ( = 0.00328 @25℃), å:离子体积参数 (pm)
zi:离子电荷, 与温度、介电常数有关
酸的浓度:酸的分析浓度,包含未解离的和已解离的 酸的浓度 对一元弱酸:cHA=[HA]+[A-]
2 分布分数
分布分数:溶液中某酸碱组分的平衡浓度占其分析浓 度的分数,用 δ 表示
“δ” 将平衡浓度与分析浓度联系起来 [HA] =δHA c HA , [A-] = δA- c HA 一元弱酸溶液 多元弱酸溶液
四大平衡体系: 酸碱平衡 配位平衡 氧化还原平衡 沉淀平衡
四种滴定分析法: 酸碱滴定法 配位滴定法 氧化还原滴定法 沉淀滴定法
1 酸碱平衡
酸
共轭碱 + 质子
HF
H2PO4H6Y2+ NH4+
F-
+
H+
HPO42- +
H+
H5Y+ +
H+
NH3
+
H+
通式: HA
A- + H+
酸碱半反应
例: HF在水中的离解反应
[NH3] +[Zn(NH3) 2+] +2[Zn(NH3)22+] +3[Zn(NH3)32+] +4[Zn(NH3)42+] = 0.2 mol/L
第6章-酸碱平衡和酸碱滴定法

Ka θc(H c ()H c(A )A)cc2(cH (H ))=
cα 2 1-α
当α< 5%或c/Kaө≥500时 cc(H)c
HA: c(H+)=cα= cKθa 最简式
B: c(OH-)=cα= cKθb
40
当α> 5% 或
c < 500时 ,
Proton donor Proton acceptor Proton
HAc NH4+
Ac-
+
H+
酸
NH3
+
H+
碱 半
HCO3H4Y
CO32-
+
H+
反
H3Y-
+
H+
应
通式: HA
A-
+
H+
共轭酸
碱 + 质子
10
两性物质:
C O 3 2 - - H + H C O 3 - + H + H 2 C O 3 S 2 - -H + H S - + H + H 2 S
本章学习要求
1. 掌握酸碱质子的定义,共轭酸碱对,酸碱反 应的实质,共轭酸碱 Kaθ 和 Kbθ的关系;
2. 了解同离子效应,盐效应;
3. 掌握弱酸、弱碱的电离平衡,影响电离平衡
常数和电离度的因素,稀释定律;运用最简 式计算弱酸、弱碱水溶液的pH值及有关离 子平衡浓度;
1
本章学习要求
4. 了解酸度对弱酸(碱)存在形态分布状况 影响; 掌握缓冲溶液pH值的计算;
同一种弱电解质: c
25
化学式 HAc
c/mol.L-1 Kaθ
第六章酸碱平衡与酸碱滴定法

温度:温度变化会引起KHIn的改变 影响变色范围的因素 溶剂:溶剂不同,pKHIn不同 指示剂用量:只对单色指示剂有影响
滴定顺序: 浅 →深
指示剂 甲基橙 甲基红 酚 酞 酸色~碱色 红~黄 红~黄 无~红 变色范围(pH) 3.1~4.4 4.4~6.2 8.0~10.0
常用酸碱指示剂
14
2、滴定曲线及指示剂的选择
滴定突跃范围
等量点前后±0.1%范围内,pH发生了急剧变化的范 围。 指示剂的变色范围全部或部分的落在滴定的
指示剂的选择原则
pH突跃范围之内。
(1)酸碱标准溶液的浓度一般为0.1 mol∙L-1左右
强酸强碱互滴的特点
(2)滴定突跃与被滴定溶液的浓度有关,浓度越大,滴定突 跃范围越大。 (3)强碱滴定强酸与强酸滴定强碱的滴定曲线形状互为反
缓冲作用原理
由于同离子效应,该体系存在大量的HAc和Ac-。
(1)抗酸作用:加入少量的酸,H+与Ac-结合,使系统中Ac-略有减少,HAc略有增加, PH基本不变。
10
(2)抗碱作用:加入少量的碱,OH-与HAc结合,使系统中Ac-略有增加,HAc略有减少, PH基本不变。 (3)抗稀释作用:加水稀释,CH K HAc 缓冲溶液PH计算 (1)弱酸-弱酸盐体系
比较精确式
5
一元弱碱溶液COH-的计算公式 条 件 公 式 名 称
CKb≥20KW C/Kb≥500 CKb≥20KW C/Kb<500 CKb<20KW C/Kb≥500
COH CKb
COH Kb Kb 2 4CKb 2
最简式
近似式
COH CKb K w
比较精确式
C HCl V2 10 3 M Na2CO3 m试样
酸碱平衡及酸碱滴定法.pptx

(2) 将参考水平得质子后的形式写在等式的左边,失质子 后的
形式写在等式的右边. (3) 有关浓度项前乘上得失质子数,总的得失质子的物质
的量
第23页/共119页
例: 一元弱酸(HA)水溶液的质子条件式: 确定参考水平(Zero Level): H2O,
酸 HAc
质子 + 碱 H+ + Ac-
共轭酸碱对
第3页/共119页
关于共轭酸碱对的例子(p46)
酸
共轭碱 + 质子
HF
H
2P
O
4
H6Y2+
NH4+
F-
+
H+
H
P
O
24
+
H+
酸 碱
H5Y+
+
H+
半 反
NH3
+
H+
应
结论:酸碱可以是阳离子、阴离子、中性分子。
第4页/共119页
例: HAc在水中的离解反应(p47)
半反应1:
HAc
Ac- + H+
半反应2: H+ + H2O
总反应: HAc + H2O
简写为:
HAc
H3O+ Ac- + H3O+ Ac- + H+
在这里,溶剂水起到碱的作用! 结论:酸碱反应的实质是质子转移
第5页/共119页
碱(NH3)在水溶液中的离解反应:
NH3 + H+ H2O
第五章酸碱平衡和酸碱滴定法

解:
H2S H + HS
K a1
=
[H ][HS [H2S]
]
=9.1
10-8
HS H + S2
K
a2
=
[H ][S2 [HS ]
]
=1.1
10-12
根据多重平衡规则:
K
Ka1
K
a2
[H ]2[S2 ] [H2S]
Ka1 Ka2
9.1108 1.11012
102
可忽略第二级解离而减少的以及增多 的,当作一元酸处理。因此,
则有, lg c H c OH lg kW
即 pH pOH pKW 14.00
• 酸性溶液中:c(H+)>c(OH-),pH<7< pOH • 中性溶液中:c(H+) = c(OH-) ,pH = 7 = pOH • 碱性溶液中:c(H+) < c(OH-) ,pH >7>pOH
1.6 107
OH- +
H3PO4
K
b3
c(OH )c(H3PO4 ) c(H2PO4 )
1.3 1012
可知碱的强度为: PO43- > HPO42- > H2PO4-
K
a1
K
b3
K
a2
K
b2
K
a3
K
b1
K
w
3. 解离度和稀释定律
已解离的分子数
电解前原电解质的分子总数
×100 %
和K都能反映弱酸弱碱解离能力的大小。K是化学平衡常
解离度(α)
已解离的分子数
溶液中原有该弱电解质分子总数 100%
例如:0.10mol.L-1HAc的解离度是1.32%, 则溶液中各离子浓度是: c (H+)=c (Ac-)
无机及分析化学06酸碱平衡与酸碱滴定法

无机及分析化学06酸碱平衡与酸碱滴定法酸碱平衡是无机及分析化学中的一个重要概念,它涉及到溶液中酸和碱之间的相互作用和平衡状态。
酸碱滴定法是一种常用于测定溶液中酸碱性质和浓度的分析方法。
本文将对酸碱平衡和酸碱滴定法进行详细介绍。
首先,我们来介绍酸碱平衡的基本概念。
酸碱平衡是指溶液中酸和碱之间的反应和平衡状态。
在溶液中,酸能够释放出H+离子,而碱能够接受H+离子。
这个过程被称为质子(H+)转移反应。
在酸碱平衡中,有两个重要的概念:酸性度(pH)和酸度常数(Ka)。
pH是用来表示溶液酸碱性强弱的指标,它的定义是pH=-log[H+],其中[H+]代表溶液中的氢离子浓度。
pH值越小,表示溶液越酸;pH值越大,表示溶液越碱。
在中性水溶液中,pH值为7酸度常数Ka用来衡量酸的强弱,它的定义是Ka=[H+][A-]/[HA],其中[H+]代表酸溶液中的氢离子浓度,[A-]代表酸的共轭碱的浓度,[HA]代表未解离酸的浓度。
Ka值越大,表示酸越强。
酸碱滴定法是一种常用于测定溶液中酸碱性质和浓度的分析方法。
在酸碱滴定中,通常会使用滴定管、酸度计、酸碱指示剂等实验装置和试剂。
滴定过程中需要滴定剂、指示剂和滴定的原料溶液。
滴定过程中,首先准备好要分析的溶液和滴定剂。
然后,用滴定管滴入适量的滴定剂到容器中,然后再加入适当的指示剂。
当滴定剂反应完全与原料溶液中的酸或碱反应完成时,指示剂的颜色将发生明显的变化。
通过测量滴定剂用量,可以计算出原料溶液中酸或碱的浓度。
酸碱滴定法有许多不同的类型,其中最常见的有酸碱滴定、氧化还原滴定和络合滴定。
酸碱滴定是根据滴定剂对溶液中的酸或碱进行中和反应来测定其浓度。
氧化还原滴定是通过滴定剂与溶液中的氧化还原反应来测定其浓度。
络合滴定是通过滴定剂与溶液中的金属离子形成络合物来测定其浓度。
酸碱滴定法在实际应用中有广泛的用途。
例如,它可以用于测定食品和药品中的酸碱度,以确保其安全和合规性。
此外,酸碱滴定还可以用于水质分析、环境监测和药物分析等领域。
化学知识--酸碱平衡和酸碱滴定法
c H 2 S4O 0 .1 mL o 1 l
c 1 2H 2S4 O 2cH 2S4 O 0.2mo L 1l c2 H 2S4O 1 2cH 2S4O 0 .0m 5L o 1l
通式
cbB acB
18.05.2020
a b
16
滴定度:每ml标准溶液所能滴定的被测物质的质量
(在例行分析中常用)
17
滴定度与摩尔浓度的转换:与反应计量关系有关
6 F 2 eC 2 O 7 r 2 6 F 3 e2 C 3 r
c V 6c V M m F2e F2e
C2O r72 C2O r72
C
A B
C D
Kw:水的离子积 Ka:酸的解离常数 Kb:碱的解离常数 Ksp:溶度积 Kt:滴定反应常数
Kinetic Equilibrium
time
region region
18.05.2020
3
方法特点
适用于常量组分(含量>1%)的测定; 相对误差一般约为±0.2%,准确度较高; 仪器简单、操作简便、快速; 有很大的实用价值。
故当 18.05.2020 Kc106,反应即可定量进行完全。
6
3、反应速度要快
如果反应慢,无法确定终点;
加热、增加反应物浓度、加入催化剂。
4、有合适的指示终点的方法 人眼:利用指示剂的颜色变化;
仪器:利用溶液体系中某一参数的变化。
5、试液中若存在干扰主反应的杂质
必须有合适的消除干扰的方法。
18.05.2020
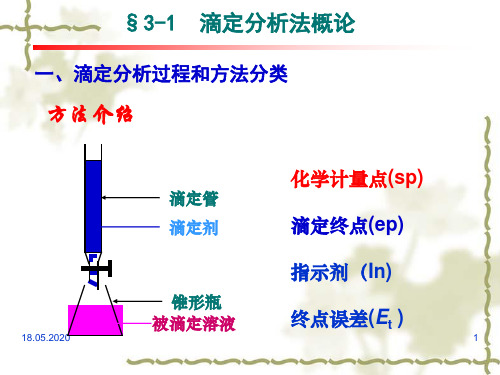
§3-1 滴定分析法概论
一、滴定分析过程和方法分类
方法介绍
18.05.2020
滴定管 滴定剂
锥形瓶 被滴定溶液
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第二章酸碱平衡和酸碱滴定法习题
解: a NaAc为一元弱碱, 其K b=K w/K HAc=5.6×10-10
3.计算pH为8.0和12.0时0.10mol·L-1 KCN的溶液中CN-1的浓度
4.含有C Hcl=0.10mol·L-1,C NaHSO4=2.0×10-4mol·L-1和C HAc=2.0×10-6mol·L-1的混合溶液。
a.计算此混合溶液的pH。
b.加入等体积0.10mol·L-1 NaOH溶液,计算溶液的pH
pH= 4.00
5.将0.12mol·L-1 HCL和0.10mol·L-1氯乙酸钠(ClCH2COONa)溶液等体积混合,计算pH。
6.欲使100 ml 0.10 mol·L-1HCl溶液的pH从1.00增加至4.44,需加入固体NaAc多少克(忽略溶液体积的变化)?
7.今由某弱酸HB及其盐配制缓冲溶液,其中HB的浓度为0.25 mol·L-1。
于此100ml缓冲溶液中加入200mgNaOH(忽略溶液体积的变化),所得溶液的pH为5.60。
问原来所配制的缓冲溶液的pH为多少?(设HB的Ka=5.0×10-6)
8.欲配制pH为 3.0和 4.0的HCOOH-HCOONa缓冲溶液,应分别往200ml 0.20 mol·L-1HCOOH溶液中加入多少毫升1.0 mol·L-1 NaOH溶液。
解x=25.7ml
9.某人称取CCl3COOH 16.34g和NaOH 2.0g,溶解于1L水中,欲以此液配制pH=0.64的缓冲溶液。
问:a. 实际所配制缓冲溶液的pH为多少?b. 要配制pH=0.64的缓冲溶液,需加入多少毫升1.0 mol·L-1强酸溶液。
10. 配制氨基乙酸总浓度为0.10 mol·L-1的缓冲溶液(pH=2.0)100ml需氨基乙酸多少克?还需加多少摩强酸?
x =7.9ml
11.25.0ml 0.40 mol·L-1 H3PO4 与30.0ml 0.50 mol·L-1Na3PO4溶液混合,然后稀释至100.0,计算此缓冲溶液的pH和缓冲指数。
若准确移取上述混合溶液25.0ml,需加入多少毫升1.00 mol·L-1NaOH 溶液后,才能使混合溶液的pH等于9.00。
12. 20 g六亚甲基四胺,加浓HCl(按12mol·L-1计)4.0ml,稀释至100ml,溶液的pH是多少?此溶液是否是缓冲溶液?
13. 计算下列标准缓冲溶液的pH(考虑离子强度的影响),并与标准值比较:
a. 饱和酒石酸氢钾(0.034 mol·L-1);
b. 0.0500 mol·L-1邻苯二甲酸氢钾;
c. 0.0100 mol·L-1硼砂。
14. 用0.200 mol·L-1Ba(OH)2滴定0.1000 mol·L-1HAc至化学计量点时,溶液的pH等于多少?
pOH=5.18 pH=8.82
15. 某试样含有Na2CO3和NaHCO3,称取0.3010g,用酚酞作指示剂,滴定时用去0.1060 mol·L-1 HCl 20.10ml,继用甲基橙作指示剂,共用去HCl 47.70ml。
计算试样中Na2CO3和NaHCO3质量分数。
16. 二元弱酸H2B,已知pH=1.92时,δH2B=δHB-;pH=6.22时,δHB-=δB2-。
计算:
a. H2B的Ka1和Ka2;
b. 主要以HB-形式存在时的pH为多少?
c. 若用0.100 mol·L-1NaOH 溶液滴定0.100 mol·L-1 H2B,滴定至第一和第二化学计量点时,溶液的pH各为多少?各选用何种指示剂?
17. 已知0.1 mol·L-1一元弱酸的HB的pH=3.0,问其等浓度的共轭碱NaB的pH为多少?(已知:Ka c>20 Kw且c/Ka>500)
18. 将H2C2O4加入到0.10 mol·L-1Na2CO3溶液中,使其浓度为0.020 mol·L-1,求该溶液的pH?(H2C2O4:pKa1=1.20,pKa2=4.20;H2CO3:pKa1=6.40;pKa2=10.20)
19. 称取Na2CO3和NaHCO3的混合试样0.685g,溶于适量的时水中。
以甲基橙为指示剂,用0.200 mol·L-1HCl溶液滴定至终点时,消耗50.0ml。
如改用酚酞为指示剂,用上述HCl 溶液滴定至终点时,需消耗多少毫升?
20. 称取纯一元弱酸HB 0.8150 g ,溶于适量的水中,以酚酞为指示剂,用0.1100 mol ·L -1 NaOH 溶液滴定至终点时,消耗24.60ml 。
在滴定过程中,当加入NaOH 溶液11.00ml 时,溶液的pH=4.80。
计算该弱酸HB 的pKa 值。
加入NaOH 溶液11.00ml 后,生成的n(B -)=0.1100×11.00=1.21mmol
剩余的 n(HB -)=0.1100×(24.60-11.00)=1.496mmol
1.21
4.80lg
1.496
a pK =+ 1.214.80lg 1.496a pK =+ p K a =4.89
21.
用0.10 mol ·L -1 NaOH 滴定0.10 mol ·L -1HAc 至pH=8.00,计算终点误差。
解法2:△pH =8.00-8.72=
-0.72
0.720.720.05%pH pH
t E ∆-∆-=
=
=-
22.
用0.10 mol ·L -1 HCl 滴定0.10 mol ·L -1 NH 3 溶液至pH=4.0,计算终点误差。
解法2:
△pH= 4.0-5.28=-1.28
1.28 1.280.2%pH pH
t E -∆∆-=
=
=
23.
用 0.10 mol ·L -1 NaOH 滴定0.10 mol ·L -1 H 3PO 4至第一化学计量点,若终点pH 较化学计量点pH 高0.5 单位。
计算终点误差。
24.
用0.100 mol ·L -1 NaOH 滴定0.100 mol ·L -1 羟胺盐酸盐(NH 3+OH ·Cl -)和0.100 mol ·L -1NH 4Cl 的混合溶液。
问:a. 化学计量点时溶液的pH 为多少?b. 在化学计量点有百分之几的NH 4Cl 参与了反应?
解: a 当滴定化学计量点时, 溶液为一元弱酸NH 4Cl 和一元弱碱NH 2OH 的混合溶液, [H +]计算可按弱酸弱碱混溶液NH 4-NH 2OH 处理,精确式为
:
25. 称取一元弱酸HA 试样1.000g ,溶于60.0ml 水中,用0.2500 mol ·L -1NaOH 溶液滴定.已知中和HA 至50%时,溶液的pH=5.00;当滴定至化学计量点时,pH=9.00。
计算试样中HA 的质量分数为多少?(假设HA 的摩尔质量为82.00g ·mol -)
26. 称取钢材1.000g,溶解后,将其中的磷沉淀为磷钼酸铵。
用0.1000 mol·L-1NaOH 20.00ml 溶解沉淀,过量的NaOH用0.2000 mol·L-1HNO37.50ml 滴定至酚酞刚好褪色。
计算钢中的P和P2O5的质量分数。
27. 在纯水中,甲基橙的理论变色点pH=3.4,今向溶液中加入NaCl溶液,使其浓度达到0.10 mol·L-1。
问甲基橙的理论变色点pH又为多少?
28.标定甲醇钠溶液时,称取苯甲酸0.4680g,消耗甲醇钠溶液25.50ml,求甲醇钠的浓度。
