玻璃2-玻璃的熔制试验
高温熔融法制备ZnO-B2O3-SiO2玻璃

玻璃具有均匀、 透明、 稳定性好 , 可以掺杂较高浓度的稀土等激活离子等优点。其信息读 出的空间分辨 率 也 比晶体材料 高 引 , 因而在 电子俘获 型光存 储材 料 的应 用 中有着 良好 的前 景 。
Z OB O 一i 玻璃 即为一 种性 能优 良的宿 主玻 璃 , 结构 均 匀且 各 向 同性 , n — SO 其 不存 在 双折 射 及 光散 射 现
第3 2卷
第 3期
河北理工大学学报 ( 自然 科 学 版 )
V 13 N . o. 2 o3
21 00年 8月
Jun l f bi o t h i iesy N t a Si c dtn o ra e P l e ncUnvri ( a rl ce eE io ) o He y c t u n i
中图分 类 号 : Q 1 1 6 2 文献标 志码 : T 7 . 1 A
0 引 言
电子 俘获 光存储 的本质是 材料 的光激 励发 光特 性 。 自从 上 世纪 4 O年 代 出现 关 于光 激 励 发光 材 料 的报 道 以来 , 材料 在光 存储 、 该 红外 探测 、 辐射 剂量测 定 、 光信 息处理 等许 多领 域展 现 了其应 用潜力 ¨ 。 引
象, 因此能得到更高的空间分辨率性质稳定 , 易于存放和加工 , 以此为基质 , 又可克服以往 电子俘获材料稳定 性不好 的缺 点 。在发 光材 料 领域 的研 究 已得 到关 注 【 。本 实 验 以氧化 锌 ( n 、 J Z O) 氧化 硼 ( , 、 化 硅 BO ) 氧
( i 为主要 原料 采用 高温 熔融 法制备 Z O B O 一 i: 系玻璃 。并 利用 X D和傅里 叶红外 光谱 ( R) SO ) n — SO 体 R r m
玻璃的熔制过程

玻璃的熔制过程玻璃是一种广泛应用于制造建筑材料、器皿、光学仪器、电子仪器等工业领域的无机非金属材料。
玻璃的基础原料主要是硅酸盐类物质,包括石英砂、长石、白云石等。
玻璃的制造涉及到多种工艺步骤,其中最主要的过程是熔制。
玻璃的熔制过程,一般分为两个阶段:玻璃原料熔融和玻璃成形。
1. 玻璃原料熔融玻璃原料熔融是制造玻璃的第一步。
首先要将玻璃原料送到炉中,然后在炉内进行高温熔化。
玻璃熔化的温度通常在1300-1600℃之间。
炉内的高温条件有助于熔化原料,并促进原料之间的充分混合。
玻璃熔化过程中,炉内的温度、炉膛的结构、炉膛的加热方式、气氛以及熔化时间等因素都对玻璃性质有很大的影响。
其中,炉温的控制是其中最为关键的一个因素。
炉温过低时,原料无法充分熔化,熔击出来的玻璃比较粗糙;而炉温过高时,虽然玻璃可以很快熔化,但却会使得玻璃成分中的气体难以释放,造成玻璃内部气泡增多,影响玻璃的质量。
同时,熔制过程中原料的混合也是影响玻璃质量的重要因素之一。
原料混合过程中必须注意保持物料配比的稳定,以确保每份原料的比例都是正确的,否则会影响玻璃性能的均匀性和稳定性。
2. 玻璃成形玻璃原料熔融后,需要将其通过成形工艺,将其变成需要的形状。
玻璃成形技术大致可以分为两大类,即自由成形技术和模压成形技术。
自由成形技术包括吹制、拉伸、浸涂等;模压成形技术包括平板压制、吹瓶、挤出等。
自由成形技术中的吹制是最常用的一种方法。
吹制工艺是先将玻璃熔液通过玻璃管或小片,吹成一个球体,然后在模具上加工形状,最后风冷固化。
玻璃吹制的工艺简单,成本低,成品形态多,应用非常广泛。
而模压成形技术,如平板压制、吹瓶、挤出等,则需要利用模具或挤压机来对玻璃进行成形。
这类制品比较规整且饱满,常常用于制备工艺精密的玻璃器具、仪器件等。
总之,玻璃熔制过程经历了玻璃原料熔融和玻璃成形两个阶段。
通过高温下的熔融,使玻璃原料混合均匀,在成型过程中呈现出所需的形态,从而制备成建筑材料、器皿、光学仪器、电子仪器等多种应用领域中的产品。
综合设计性材料试验报告(配制融融温度范围在700—900℃的玻璃试样)

综合设计性材料实验报告实验名称:配置熔融温度范围在700~900℃的玻璃试样学生姓名:谢万熠学号: 201130451108 指导老师:罗婷时间: 2014年3月18日景德镇陶瓷学院科技艺术学院2014年3 月18 日一、实验目的和要求1.按照确定的原料配方和所用的化学成分进行配合料的计算。
2.了解玻璃熔制温度和温度制度对材料性能的影响。
3.掌握实验室常用高温仪器、设备的使用方法。
4.通过实验学会分析材料的熔制缺陷,制定合理的烧成制度。
二、实验仪器设备研钵,电子称,小瓷舟,箱式实验炉,小勺子,塑料杯三、实验原理玻璃是由熔融物冷却硬化而得到的非晶态固体,其内能和构形熵高于相应的晶体,结构为短程有序、长程无序。
由熔融状态转变为固态的温度称为玻璃转变温度Tg。
玻璃具有四个通性:各向同性、介稳性、固态和熔融态间转变的渐变性和可逆性、性质随成分变化的连续性和渐变性。
玻璃按组成可分为元素玻璃(如硫玻璃和硒玻璃)、氧化物玻璃(如硅酸盐玻璃、硼酸盐玻璃、磷酸盐玻璃)和非氧化物玻璃(如卤化物玻璃和硫族化合物玻璃)。
玻璃是在熔体急速冷却时形成的。
具有相应的热力学和动力学条件。
热力学上,同组成晶体和玻璃态内能差别越小,越容易生成玻璃。
动力学上,生成玻璃的关键在于熔体在凝固点附近具有较大的粘度。
由于急速冷却时,由于粘度迅速增大,内部质点来不及进行规则排列从而形成玻璃。
本实验采用熔融淬冷法制备玻璃。
先由所给组分计算、称取、混合得到混合料。
由配合料熔制成玻璃液、淬冷得到玻璃可以分为以下几个阶段:(1)硅酸盐形成。
在此阶段中粉末混合料在高温下进行固相反应,并逸出大量气体,最后变成各种硅酸盐和未起反应的石英颗粒所组成的烧结物。
此阶段随成分的不同约在800-900℃结束。
(2)玻璃液的形成。
此阶段包括烧结物的熔融和石英颗粒的溶解,变成了含有大量气泡、条纹、成分不均匀的玻璃液。
这一阶段约在900℃结束。
(3)玻璃液的澄清。
此阶段温度较高,目的是使玻璃液在较小的粘度下释放出可见气泡,并建立起炉气、气泡中气体、玻璃液中溶解气体平衡。
PbBr_2_PbCl_2_PbF_2_PbO_P_2O_5系统玻璃成分分析

2 2 2 2 5朱冬梅 , 周万城 , 赵宏生(西北工业大学凝固技术国家重点实验室 ,陕西 西安 710072)率 45570 ,线色散率 (一级) 0 . 8nm/ mm 。
摘 要 : 研究了 Pb Br 2 - PbC l 2 - Pb F 2 - PbO - P 2 O 5 系统的玻 璃在熔融过程中的变化 。
发现在玻璃的熔制过程中 ,元素 P 、Pb 和 Br 的损失量最大 。
化学分析和理论计算表明 ,这些元素是以 PbC l 2 、PbBr 2 和 P 2 O 5 的形式挥发的 。
而且 ,随着配料成分中含 量的增加 , P bC l 2 、PbBr 2 和 P 2 O 5 的挥发量也随之增加 。
关键词 : 成分变化 ;化合物形式 ;挥发 结果和讨论3 3 . 1 玻璃的光谱半定量分析在试样的熔制过程中 ,所用容器为陶瓷坩埚 。
为了讨论使用陶瓷坩埚是否会引入侵蚀产物 ,我们采用光谱半定量分析法 对试样 1 的成分进行了分析 ,结果表明 ,试样中元素 S i 和 Al 的 含量总和仅为 7 ×10 - 5 左右 ,这说明在玻璃的熔制过程中 ,使用 陶瓷坩埚对玻璃成分的影响不大 。
3 . 2 玻璃成分的化学分析为了探索玻璃成分的变化 ,我们对玻璃的实际成分进行了 分析 。
表 1 列出了一些玻璃的设计成分与分析成分的对比 。
从 表中可以看出 ,玻璃中元素的实际含量与设计含量有很大差别 , 其中 P 、Pb 和 Br 的含量变化相对较大 。
同时 ,由于 P 、Pb 和 Br 的损失 ,使得其它元素的相对含量升高 ,因此 ,无法说明它们是 否损失 。
表 1 一些玻璃由配料成分换算得的组元成分和化学分析成分 Tab le 1 C alcu lat ed element al batch co m po sitio n and chemical analy 2sis of g lasses中图分类号 : TQ171 文献标识码 :A1 引 言具有低的熔融温度 、好的化学稳定性的玻璃 ,在许多领域都 有应用 。
玻璃制备实验

1. 实验目的:玻璃的结构和性质1、掌握玻璃组成的设计方法和配方的计算方法;2、了解玻璃熔制的原理和过程以及影响玻璃熔制的各种因素;3、熟悉高温炉和退火炉的使用方法和玻璃熔制的操作技能。
2。
实验试剂:玻璃的原料及其作用注:原料混合需要加水,防止原料反应的粉尘污染而且可以增大物料之间的反应表面积。
但含水率太高,在批料加热熔融时,水分蒸发要多消耗热能,延长融融时间。
所以含水率要控制在5%以下.着色剂的投放应循序渐进,不要一下子投放太多,否则玻璃会出现偏色时会很难纠正.(1)玻璃设计配方:此方被称为768 号玻璃,其组成成分(%)如下:SiO2 75 ,B2O3 0. 54 ,CaO 3.7 ,MgO 1。
08 ,PbO 0. 48 ,ZnO 0。
74 ,K2O 0。
91 ,Na2O 17. 3。
组成中除含有17. 3 %的Na2O 外,还有B2O3 、PbO等,硬化速度较慢,属于“长”(慢凝)玻璃,由于轻瓶壁厚减薄,冷却速度加快,采用“长”玻璃,可使玻璃液在模型中合理分布,壁厚均匀,有利于提高强度和热稳定性.熔制温度为1480~1500 ℃,成型温度为1200 ℃,退火温度为540 ℃,退火质量对强度影响较大,可使强度变化20 %或更多。
(3)玻璃原料的作用SiO2 ;玻璃的主要成分,占玻璃65~75%以上.Al2O3;提高玻璃的化学稳定性,热稳定性,机械强度、硬度和折射率,减轻玻璃对耐火材料的侵蚀。
Fe2O3;与Cr2O3共用,可制得绿色玻璃。
Ca O :作稳定剂,但含量大于12.5%时,能使玻璃结晶化增大,发脆.MgO : 作稳定剂。
BaO :作助溶剂,防辐射。
Na2O :降低玻璃粘度,使之易于熔融和成型.Cuso:使物质对光线产生选择性吸收,显出蓝绿色。
Na2SO4 :作澄清剂,在玻璃熔制过程中能分解产生气体,或能降低玻璃的粘度,促进排除玻璃液中气泡.3.实验原理:根据玻璃制品的性能要求,设计玻璃的化学成分组成,并为此为主要依据进行配料,制备好的配合料在高温下加热,将进行一系列的物理的、化学的、物理化学的变化,变化的结果使各种原料的机械混合物变成复杂的熔融物,即没有气泡、结石、均匀的玻璃液,然后均匀地降温以供成型需要。
玻璃熔制及熔窑---玻璃熔制过程剖析

玻璃的形成
2.石英颗粒的尺寸: τ---形成玻璃的时间
k1r03
石英颗粒越小,反应时间越短。注:过小,结团而成为大颗 粒,反而不宜熔化。 3.熔体温度: τ---形成玻璃的时间
aebt
b、t与玻璃成分、原料颗粒度等相关的常数
玻璃的形成
4.配合料及投料质量 a.原料的颗粒级配 难熔的小一些、易熔的大一些;密度小的 粗一些,密度大的细一些。 b.配合料质量 均匀性与水分含量 c.投料方式 薄层投料、均匀投料 d、碎玻璃
玻璃形成的动力学: 1.玻璃成分:τ---熔化速度常数,表示玻璃相对难熔的特征。
τ是一经验常数, 要综合各种因
一般工业玻璃:
SiO2
Al 2 O3
素后确定熔化 温度。
Na2O K 2O
硼酸盐玻璃:
SiO2 Al2O3
Na2O
K2O
1 2
B2O3
铅酸盐玻璃:
SiO2 Al2O3
Na2O K 2O 0.125 PbO
O2与N2:一般情况下以物理溶解为主,溶解度很小
玻璃液的澄清
(4)几种气体在玻璃液中的性质
CO2:物理溶解度随着T升高,过饱和程度的增加而降低;玻璃液 的吸收能力随碱性氧化物浓度增加而增加。化学溶解为主 SO2:低于1200℃时玻璃液的吸收能力随着T升高而增大,超1200℃ 时,溶解量迅速减少。化学溶解为主
500℃左右开始分解;白云石700 ℃左右MgCO3(先)分解 完全,CaCO3(后)分解很少;硝酸钠350 ℃左右开始分解。
c.脱水:结晶水、结构水、化学结合水
d.熔融:固态转变为液态
硅酸盐的形成阶段
3.各组分之间(多组分)的加热反应
a.固相反应:
玻璃熔制过程的五个阶段

玻璃的熔制过程通常分为以下五个主要阶段,每个阶段对最终玻璃质量起着至关重要的作用:
1. 原料准备
•玻璃熔制的原料主要包括硅砂(SiO2)、碱金属氧化物(如Na2O)和助熔剂(如CaO)。
原料需要经过筛分、混合、干燥等处理,确保原料均
匀并去除杂质。
通常还会加入碎玻璃(废玻璃),帮助提高熔化效率。
2. 熔化
•在熔窑中,混合好的原料在高温(1300-1500℃)下加热熔化,形成均匀的液态玻璃。
熔化过程需要较长时间,以确保所有成分充分反应,减少
气泡和夹杂物。
这一阶段至关重要,决定了玻璃的基本性质。
3. 澄清
•在熔化完成后,玻璃液需要经过澄清阶段。
此时,熔融玻璃中的气泡和未完全溶解的固体颗粒会逐渐上升并排出。
通常会通过提高温度或使用
澄清剂(如硝酸钾或硝酸钠)来加速气泡的消除。
4. 均化
•在气泡排除后,玻璃液需要均化,即通过搅拌或控制温度,使玻璃液中的各成分分布更加均匀,确保不同区域的化学成分和物理性质一致。
这
一过程能够防止玻璃内部出现成分不均或结构缺陷。
5. 成形与退火
•成形:玻璃液冷却至适当温度后,会进行成形,常见的成形方法包括浮法(用于生产平板玻璃)、吹制法(用于生产瓶子、玻璃器皿)等。
•退火:成形后的玻璃需要经过退火炉进行缓慢冷却。
退火过程可以缓解玻璃内部的应力,防止玻璃在冷却过程中因热应力而开裂。
这五个阶段共同作用,确保玻璃的结构完整性、透明度和机械性能。
玻璃实验讲义:玻璃高温熔制、玻璃内应力与透射比的测定
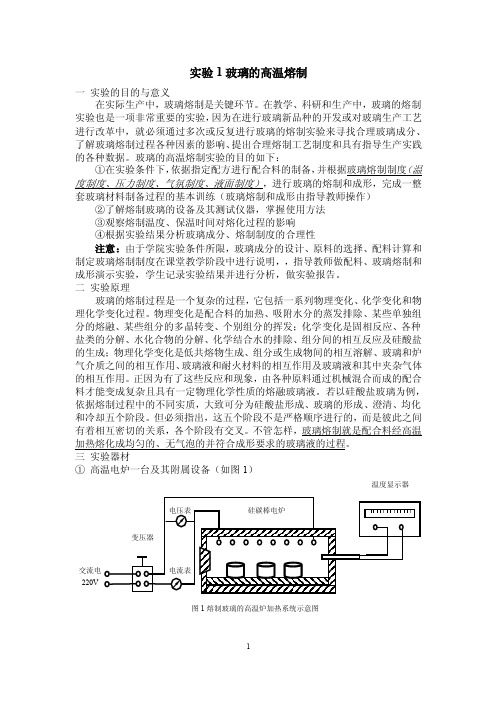
实验1玻璃的高温熔制一实验的目的与意义在实际生产中,玻璃熔制是关键环节。
在教学、科研和生产中,玻璃的熔制实验也是一项非常重要的实验,因为在进行玻璃新品种的开发或对玻璃生产工艺进行改革中,就必须通过多次或反复进行玻璃的熔制实验来寻找合理玻璃成分、了解玻璃熔制过程各种因素的影响、提出合理熔制工艺制度和具有指导生产实践的各种数据。
玻璃的高温熔制实验的目的如下:①在实验条件下,依据指定配方进行配合料的制备,并根据玻璃熔制制度(温度制度、压力制度、气氛制度、液面制度),进行玻璃的熔制和成形,完成一整套玻璃材料制备过程的基本训练(玻璃熔制和成形由指导教师操作)②了解熔制玻璃的设备及其测试仪器,掌握使用方法③观察熔制温度、保温时间对熔化过程的影响④根据实验结果分析玻璃成分、熔制制度的合理性注意:由于学院实验条件所限,玻璃成分的设计、原料的选择、配料计算和制定玻璃熔制制度在课堂教学阶段中进行说明,,指导教师做配料、玻璃熔制和成形演示实验,学生记录实验结果并进行分析,做实验报告。
二实验原理玻璃的熔制过程是一个复杂的过程,它包括一系列物理变化、化学变化和物理化学变化过程。
物理变化是配合料的加热、吸附水分的蒸发排除、某些单独组分的熔融、某些组分的多晶转变、个别组分的挥发;化学变化是固相反应、各种盐类的分解、水化合物的分解、化学结合水的排除、组分间的相互反应及硅酸盐的生成;物理化学变化是低共熔物生成、组分或生成物间的相互溶解、玻璃和炉气介质之间的相互作用、玻璃液和耐火材料的相互作用及玻璃液和其中夹杂气体的相互作用。
正因为有了这些反应和现象,由各种原料通过机械混合而成的配合料才能变成复杂且具有一定物理化学性质的熔融玻璃液。
若以硅酸盐玻璃为例,依据熔制过程中的不同实质,大致可分为硅酸盐形成、玻璃的形成、澄清、均化和冷却五个阶段。
但必须指出,这五个阶段不是严格顺序进行的,而是彼此之间有着相互密切的关系,各个阶段有交叉。
不管怎样,玻璃熔制就是配合料经高温加热熔化成均匀的、无气泡的并符合成形要求的玻璃液的过程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
在硅酸盐形成阶段,配合料变成由硅酸盐 和二氧化硅组成的不透明烧结物。经过进一步 加热,不透明烧结物,变成透明玻璃体,此时, 配合料全部反应完毕,但玻璃液含有大量可见 气泡和条纹。澄清和均化过程就是为了消除玻 璃液中的可见气泡和条纹。玻璃的冷却阶段, 是指把澄清均化后无气泡的、均匀玻璃液降低 200-300C,以满足成型时的粘度要求。 玻璃熔制的各个阶段,各有其特点,同 时又彼此关联,在实际过程中。常常是同时进 行或交错进行的,这主要取决于熔制的工艺条 件和玻璃熔窑的结构类型。
③让电炉继续升温,当温度达到预定的熔制 温度时,在该温度下保温,保温时间根据玻 璃熔化程度而定、在此期间,根据需要可搅 拌并挑料观察,同时记录实验现象。
④当玻璃熔制好后,关闭电炉、从炉内取出 坩埚,倒出玻璃液,并按性能测试的试样要 求成型。将成型好的样品放入事先已升温的 退火炉中退火。在退火温度下保温 0.5至 1小 时,然后让其随炉冷却至室温取出,供进一 步实验用。
①检查熔制设备是否正常,若无误,接通电 源,让电炉按一定升温速率升温,升温之前, 在电炉内应事先放置好坩埚,并在炉膛底铺一 层氧化铝粉,以防坩埚破裂时漏料损坏炉体耐 火材料。
②当温度升到加料温度时,打开炉门,将配 的合格配合料迅速加入炉内坩埚中,若一次加 不完,分多次加料,每次加料完毕后,炉温会 有不同程度下降,待重新升至加料温度且停留 一段时间后再行加料、按此方法直至加完为止。
一、实验目的
1 .通过玻璃的熔制试验,使同学们掌握在 实验室条件下熔制玻璃的方法,为以后从 事玻璃工业生产和科研工作打下一定基础。 2.熟悉常用玻璃原料的颜色、性状。 3.掌握配方计算及配合料的制备
二、实验原理
配合料在高温作用下,经过一系列复杂的 物理化学反应,变成均匀、无气泡且符 合成型要求的玻璃液,此即玻璃的熔制 过程。它可分为几个阶段? 它可分为烧结体(硅酸盐)形成 过程、玻璃液形成过程、澄清、均化和 冷却五个阶段。为何要澄清和均化?
实验二 玻璃的熔制试验
概 述
将配合料经过高温加热熔化成为均匀、无 气泡且符合成型要求的玻璃液的过程称为玻璃 的熔制。 工厂生产,玻璃的熔制是在池炉或坩埚炉 中进行。但在新产品投入生产之前都必须先在 实验室进行熔制试验,通过反复的熔制试验和 性能测试,掌握影响熔制的各种因素,最后摸 索出最佳的玻璃组成和工艺条件,使设计的组 成满足使用要求。因此,玻璃的熔制试验在科 研和生产过程中都是一个很重要的环节。
四、实验步骤
1.组成设计 根据要求,选择合适的玻璃组成系统,并 参考相图及有关文献进行组成设计,计算其 熔化温度,并交由指导教师审核后,方可据 此配料、进行熔制。 2.配方计算与配合料制备 根据实验室提供的原料,进行配方计算, 经仔细审核后,按配方进行称量、混合,要 求配合料过40目/寸筛。
3.熔制
三、实验设备
1.高温炉 1台; 2.退火炉 1台; 3.台式(或架盘)天平 1台,感量1g; 4.40目、80目筛各1个; 5.研钵 2个; 6.料盆 4个; 7.坩埚钳 1把; 8.手钳 1把; 9.模具 1套; 10.坩埚300m1 2个; 11.烘箱 1台; 12.石棉手套 1付; 实验主要设备为高温炉。按发热材料不同,可分 为硅碳棒炉和硅钼棒炉;按炉型结构不同可分为箱 式炉和立式炉。一般硅碳棒炉的使用温度为 13001350℃,硅钼棒炉的使用温度在 1500-1600℃。在 实际使用时,根据具体需要选用。
五、熔制结果
通过目测或其它测试手段、对新制得的玻 璃样品进行评价,如玻璃液对坩埚的侵蚀, 熔化的程度、玻璃的透明度、玻璃中的缺 陷等。
高温电炉
