实验8 二氧化碳的溶解性 初中化学实验报告
九 年 级 化 学 分 组 实 验 一 览 表
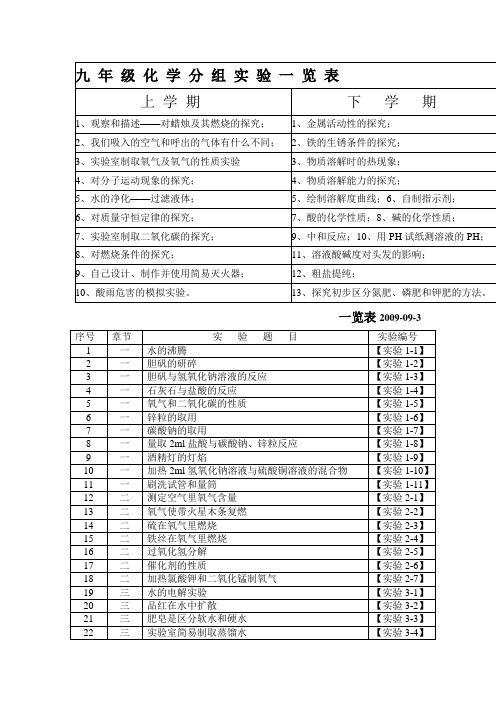
一览表2009-09-3附3:人教版九年级化学实验目录九年级上册:一、演示实验1、水加热沸腾;2、研碎胆矾观察发生的变化;3、胆矾溶解于水并和NaOH反应;4、石灰石和盐酸反应把产生的气体通入Ca(OH)2;5、闻气体气味的方法;6、固体的取用(锌粒);7、固体的取用(Na2CO3粉末);8、液体的取用;9、Na2CO3和盐酸反应;10、酒精灯的使用;11、加热NaOH和CuSO4的混合溶液;12、洗涤玻璃仪器;13、测定空气中氧气的含量;14、带火星的木条伸入氧气中的现象;15、硫在空气和氧气中燃烧;16、细铁丝在氧气中燃烧;17、加热过氧化氢溶液制取氧气;18、加热KClO3和MnO2混合物制取氧气;19、电解水;20、向盛水的烧杯中加入品红;21、用盐酸和碳酸钠反应验证质量守恒定律;22、镁条在空气中燃烧验证质量守恒定律;23、木炭还原氧化铜;24、活性炭的吸附性;25、收集CO2并验满;26、灯火实验;27、CO2溶于水的验证;28、CO2和水的反应;29、燃烧的条件的实验;30、灭火的原理;31、粉尘爆炸;32、用Mg和盐酸反应验证化学反应中的能量变化;33、点燃甲烷;二、化学活动与探究实验1、观察和描述——对蜡烛及其燃烧的探究;2、我们吸入的空气和呼出的气体有什么不同;3、实验室制取O2,O2的性质实验;4、对分子运动现象的探究;5、水的净化——过滤液体;6、对质量守恒定律的探究;7、实验室制取二氧化碳的探究;8、对燃烧条件的探究;9、自己设计、制作并使用简易灭火器;10、酸雨危害的模拟实验;九年级下册:一、演示实验1、比较黄铜片和铜片、焊锡和锡;2、CO还原Fe2O3;3、铁与稀盐酸和稀硫酸的反应;4、蔗糖溶解;5、I2和KMnO4在水和汽油中的溶解性;6、水和乙醇能否互溶;7、洗涤剂的乳化功能;8、三种不同组成的硫酸铜溶液;9、配制NaCl溶液;10、配制质量分数一定的溶液;11、向溶液中加入酸碱指示剂;12、观察的颜色和状态;13、闻盐酸和硫酸的气味;14、浓硫酸的腐蚀性实验;15、浓H2SO4稀释;16、把水慢慢注入浓H2SO4;17、NaOH的物理性质观察;18、生石灰和水反应;19、溶液的导电性;20、Na2CO3和HCl反应;21、Na2CO3溶液和澄清的石灰水反应;22、聚乙烯塑料的热塑性;二、化学活动与探究实验1、金属活动性的探究;2、铁的生锈条件的探究;3、物质溶解时的热现象;4、物质溶解能力的探究;5、绘制溶解度曲线;6、自制指示剂;7、酸的化学性质;8、碱的化学性质;9、中和反应;10、用pH试纸测溶液的pH;11、溶液酸碱度对头发的影响;12、粗盐提纯;13、探究初步区分氮肥、磷肥和钾肥的方法。
化学法吸收二氧化碳的实验研究共3篇

化学法吸收二氧化碳的实验研究共3篇化学法吸收二氧化碳的实验研究1化学法吸收二氧化碳的实验研究二氧化碳是一种温室气体,能够导致气候变化和海平面上升等环境问题。
作为人类社会的一部分,我们需要找到解决和减缓其影响的方法。
其中,一种方法是通过吸收和固定二氧化碳来达到目的。
在这方面,化学法吸收二氧化碳是一个非常有前途的选择。
化学法吸收二氧化碳的原理是在一定的条件下,将二氧化碳与化学物质反应,形成固体或液体物质。
这些物质往往是碱性物质,如氢氧化钠、氢氧化钾、氨水等。
它们与二氧化碳反应后,产生碳酸盐、碳酸氢盐等物质。
在实验研究中,我们采用了氢氧化钠作为吸收剂,通过反应形成碳酸钠等物质。
首先,准备好实验所需的材料和器材,包括氢氧化钠、二氧化碳气罐、反应装置、分析天平、草图本等。
然后,将反应装置中的氢氧化钠加入到蒸馏水中进行稀释,得到1mol/L浓度的氢氧化钠溶液。
在这个浓度下,氢氧化钠具有较好的二氧化碳吸收效果。
接下来,将二氧化碳气罐与反应装置连接起来,打开气罐阀门,将二氧化碳气体流入反应装置中。
同时,将氢氧化钠溶液一点一点滴入,反应开始。
观察反应瓶内的现象,可以看到氢氧化钠与二氧化碳反应后,溶液从透明变为混浊,并放出了大量的气体。
此时,反应已经基本完成。
最后,我们用分析天平称量出反应后的固体产物的质量,确定吸收二氧化碳的量。
根据反应方程式,可以计算出吸收的二氧化碳量。
在实验中,我们发现当氢氧化钠浓度达到1mol/L时,每克氢氧化钠可以吸收0.44克二氧化碳。
通过本次实验研究,我们发现化学法吸收二氧化碳是一种有效的方法。
这种方法具有较高的吸收速度和反应完整性,可以达到固定二氧化碳的效果。
同时,它也有一定的经济适用性和可操作性,可以被广泛地应用在各个领域。
但是,在应用中还需要考虑到吸收剂的成本、处理固体和液体废物的问题等。
这些问题需要进一步地研究和解决通过本次实验研究,我们了解到化学法吸收二氧化碳是一种高效的固定二氧化碳方法,具有较高的吸收速度和反应完整性。
二氧化碳用途实验报告

二氧化碳用途实验报告实验目的:探究二氧化碳的一些常见用途及其实验方法。
实验材料:1. 二氧化碳气体源(例如干冰)2. 盛装试管3. 镊子或塑料袋4. 针或细管5. 火柴或打火机6. 钢绒或细纱布7. PH试纸8. 温度计实验步骤:一、二氧化碳灭火实验:1. 将试管放置在稳定的平面上,放入一块干冰。
2. 移开试管外侧的水分,以防止水受热产生蒸汽。
3. 使用针或细管轻轻地引燃火柴或打火机,并将其靠近试管口部。
4. 观察火焰的变化。
可观察到火焰熄灭,因为二氧化碳的密度比空气高,可以抑制火焰所需的氧气。
二、二氧化碳溶解实验:1. 将一小块干冰放入试管中,并用钢绒或细纱布封住试管口。
2. 在试管口部撕开一小孔,在试管上方装水。
3. 观察试管中的干冰逐渐融化,并产生大量的二氧化碳气体。
4. 观察二氧化碳气体通过水的反应。
可进行PH试纸测试,观察水的酸碱性变化。
三、二氧化碳的冷却实验:1. 取一小块干冰放在一张纸上。
2. 用手触摸干冰,观察温度的变化。
3. 用温度计测量纸的温度,比较纸与干冰的温度差。
实验结果及讨论:- 在二氧化碳灭火实验中,观察到火焰因氧气不足而熄灭,验证了二氧化碳的灭火性质。
- 在二氧化碳溶解实验中,观察到二氧化碳气体通过水的反应,使水呈现酸性,说明二氧化碳溶于水产生碳酸。
- 在二氧化碳的冷却实验中,观察到干冰接触纸的区域温度显著下降,说明二氧化碳能够吸收热量,导致周围物体温度降低。
结论:二氧化碳具有灭火、溶解和冷却的作用。
在实验中,我们观察到二氧化碳可以灭火、溶解于水并产生碳酸,以及通过吸热冷却物体。
这些实验结果说明了二氧化碳的一些常见用途及其相关的实验方法。
二氧化碳吸收与解吸实验

二氧化碳吸收与解吸实验一、实验目的1.了解填料吸收塔的结构、性能和特点,练习并掌握填料塔操作方法;通过实验测定数据的处理分析,加深对填料塔流体力学性能基本理论的理解,加深对填料塔传质性能理论的理解。
2.掌握填料吸收塔传质能力和传质效率的测定方法,练习实验数据的处理分析。
二、实验内容1. 测定填料层压强降与操作气速的关系,确定在一定液体喷淋量下的液泛气速。
2. 固定液相流量和入塔混合气二氧化碳的浓度,在液泛速度下,取两个相差较大的气相流量,分别测量塔的传质能力(传质单元数和回收率)和传质效率(传质单元高度和体积吸收总系数)。
3. 进行纯水吸收二氧化碳、空气解吸水中二氧化碳的操作练习,同时测定填料塔液侧传质膜系数和总传质系数。
三、实验原理:气体通过填料层的压强降:压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。
压强降与气、液流量均有关,不同液体喷淋量下填料层的压强降P ∆与气速u 的关系如图一所示:123L 3L 2L 1L 0 =>>0图一 填料层的P ∆~u 关系当液体喷淋量00=L 时,干填料的P ∆~u 的关系是直线,如图中的直线0。
ΔP , k P a当有一定的喷淋量时,P ∆~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。
这两个转折点将P ∆~u 关系分为三个区段:既恒持液量区、载液区及液泛区。
传质性能:吸收系数是决定吸收过程速率高低的重要参数,实验测定可获取吸收系数。
对于相同的物系及一定的设备(填料类型与尺寸),吸收系数随着操作条件及气液接触状况的不同而变化。
1.二氧化碳吸收-解吸实验根据双膜模型的基本假设,气侧和液侧的吸收质A 的传质速率方程可分别表达为 气膜 )(Ai A g A p p A k G -= (1) 液膜 )(A Ai l A C C A k G -= (2) 式中:A G —A 组分的传质速率,1-⋅s kmoI ;A —两相接触面积,m 2;A P —气侧A 组分的平均分压,Pa ; Ai P —相界面上A 组分的平均分压,Pa ;A C —液侧A 组分的平均浓度,3-⋅m kmol Ai C —相界面上A 组分的浓度3-⋅m kmolg k —以分压表达推动力的气侧传质膜系数,112---⋅⋅⋅Pa s m kmol ;l k —以物质的量浓度表达推动力的液侧传质膜系数,1-⋅s m 。
中学实验探究实验报告: 二氧化碳的制取及性质探究

中学实验探究实验报告:二氧化碳的制取及性质探
究
1.二氧化碳的物理性质:通常状况下是一种无色、无臭、无味的气体能溶于水。
2.二氧化碳的化学性质:能与水反应生成碳酸,使紫色石蕊试液变成红色,可使澄清的石灰水变浑浊(此反应常用于检验CO2),能与碱反应生成相应的碳酸盐和水,易与碱性氧化物反应生成相应的碳酸盐。
3.实验室中二氧化碳的制备
原理:
选择试剂的注意事项:
(1)应选择稀盐酸,因为浓盐酸易挥发,容易使制取的二氧化碳不纯。
(2)制取CO2不能用稀硫酸与大理石(或石灰石)反应,容易生成微溶的硫酸钙,阻止反应的继续。
(3)收集的方法:向上排空气法,因为二氧化碳是易溶于水的。
(4)实验室的装置;
制取二氧化碳的装置属于固液型,与过氧化氢制取氧气有相似之处。
(5)二氧化碳的验满:用燃着的小木条放在瓶口,若木条熄灭证明二氧化碳已满。
初中化学_二氧化碳的实验室制取和性质教学设计学情分析教材分析课后反思

《二氧化碳的实验室制取与性质》一、研究背景在新一轮的教学改革中,提出了“重视学生的发现学习、探究学习、研究学习”的观点,其中探究学习被列入了课程计划,它突破了原有的教学封闭状态,把学生置于一种动态、开放、生动、多元的学习环境中。
在教学中,教师要让学生在学习过程中去实现自主学习、合作学习和探究学习。
教师充当的角色是:引导学生检视和反思自我,使之明白要学什么和获得什么;指导学生设计恰当的学习活动;协助学生寻找、搜集和利用学习资源;帮助学生营造和维持学习过程中积极的心理氛围,从而让学生发现自己所学东西的意义;引领学生对学习的过程与结果进行评价。
可以说探究性学习不仅是课程形态,它还是一种好的学习方式。
应用探究式教学具有很好的现实意义。
二、教学过程设计【教学目标】1、知识与技能:⑴认识实验室制取二氧化碳气体的原理和装置,利用设计的装置制取二氧化碳气体。
⑵通过探究实验室制取二氧化碳气体及二氧化碳性质的实验,基本认识二氧化碳气体。
2、过程与方法:通过二氧化碳制取探究、及其过程的讨论交流,培养学生的合作态度和创新意识。
3、情感态度与价值观;通过对实验装置的设计,培养学生的探究精神。
【教学重点】⑴二氧化碳气体的性质的检验,初步的探究能力培养。
⑵一般探究方式和过程的形成。
【教学难点】在二氧化碳性质的探究过程中,提升实验装置的设计思维水平。
【复习回顾】引导学生讨论实验室制法的知识:1.装置选取及气密性检验2.实验室收集二氧化碳的方法;3.实验室制取二氧化碳的药品等。
【小结】二氧化碳的实验室制法。
【探究活动】一、二氧化碳倒入燃烧蜡烛的烧杯中:课件展示信息。
(见课件)【学生活动】分组做实验。
【小结】生分组汇报看到的实验现象及得到的实验结论【讲解】教师汇总以上结论【探究活动二】二、二氧化碳的化学性质实验1、学生做实验:把二氧化碳通入紫色石蕊溶液中,观察现象,并分析原因。
2、学生做实验:把已经变红的紫色石蕊试液加热,看到什么现象,并分析原因。
初三学实验二氧化碳的性质二氧化碳水溶液的弱酸性

初三学实验二氧化碳的性质二氧化碳水溶液的弱酸性(实用版)编制人:______审核人:______审批人:______编制单位:______编制时间:__年__月__日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如工作总结、述职报告、心得体会、工作计划、演讲稿、教案大全、作文大全、合同范文、活动方案、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!And, this store provides various types of practical materials for everyone, such as work summaries, job reports, insights, work plans, speeches, lesson plans, essays, contract samples, activity plans, and other materials. If you want to learn about different data formats and writing methods, please pay attention!第1页共2页初三学实验二氧化碳的性质二氧化碳水溶液的弱酸性实验用品洁净的玻璃导管一根(长约20厘米)小试管、紫色石蕊试液,酒精灯,试管夹.实验步骤1.小试管中注入1/3体积的蒸馏水,滴入几滴紫色石蕊试液,溶液显紫色。
CO2吸收填料塔实验

实验八 二氧化碳吸收填料塔实验一、实验目的⒈ 了解填料吸收塔的结构和流体力学性能。
⒉ 学习填料塔的液膜传质膜系数、总传质系数的测定方法,加深对传质过程原理的理解。
二、实验内容1.测定填料层压强降与操作气速的关系,确定填料塔在某液体喷淋量下的液泛气速。
2.采用水吸收二氧化碳,测定填料塔的液膜传质膜系数和总传质系数。
三、实验原理1.气体通过填料层的压强降压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。
压强降与气液流量有关,不同喷淋量下的填料层的压强降ΔP 与气速u 的关系如图8-1所示:图8-1 填料层的ΔP ~u 关系当无液体喷淋即喷淋量L 0=0时,干填料的ΔP ~u 的关系是直线,如图中的直线0。
当有一定的喷淋量时,ΔP ~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。
这两个转折点将ΔP ~u 关系分为三个区段:恒持液量区、载液区与液泛区。
2.传质系数填料塔在传质过程的有关单元操作中,应用十分广泛,实验研究传质过程的控制步骤,测定传质膜系数和总传质系数,尤为重要。
根据双膜模型的基本假设,气侧和液侧的吸收质A 的传质速率方程可分别表达为气膜 )(Ai A g A p p A k G -= (8-1) 液膜 )(A Ai l A C C A k G -= (8-2)式中:A G ——A 组分的传质速率,1-⋅s kmoI ;A ——两相接触面积,m 2;A P ——气侧A 组分的平均分压,Pa ;Ai P ——相界面上A 组分的平均分压,Pa ;A C ——液侧A 组分的平均浓度,3-⋅m kmol Ai C ——相界面上A 组分的浓度3-⋅m kmolk g ——以分压表达推动力的气侧传质膜系数,112---⋅⋅⋅Pa s m kmol ; k l ——以物质的量浓度表达推动力的液侧传质膜系数,1-⋅s m 。
P 2,F LP AP A +d PP 1A 。
