表面张力现象二表面张力和表面张力系数表面张力可以由前图a得到
表面张力

2、 表面能
从功能关系来考察表面张力系数与液 体表面能的关系。见图5-6。
12
外力所作的功为
E A S S
(J· m-2)
即增加单位液面所增加的势能。 由上式可知, α 在数值上等于增加单位液 面时外力所作的功,从能量的角度看,其大小 等于增加单位液面时所增加的表面自由能。 那么液体表面能的减小可以通过下面任 一种自动过程来实现:
2
一、 表面张力和表面能
1、 表面张力
液体具有收缩其表面,使表面积 达到最小的趋势。这说明液体表面存 在着张力,这种张力称为表面张力。 表面张力产生的原因,可以用分 子间相互作用的分子力来加以解释。
3
分子间的平衡距离r0的数量级约 为10-10m。 当两个分子间的距离 r = r0 时,分 子间的作用力为零。
当两分子间的距离大于r0而在10-10~ 10-9m时,分子间的作用力表现为引力; 而当分子间的距离大于 10-9m时, 引力很快趋于零。
4
如果以10-9m为半径作一球面, 显然则只有在这个球面内的分子才 对位于球心上的分子有作用力。
分子作用球 ——分子引力作用范围是 半径为 10-9m 的球形,球的半径称为 分子作用半径。
3、肺泡的表面张力
表面活性物质在呼吸过程中起着重要 的作用: 1、稳定肺泡;2、减少呼吸功。
36
37
人的肺泡总数约为3亿个,各个肺泡的 大小不一,而且有些肺泡是相连的。 在充满空气的肺中,既有肺组织的弹 性力,又有衬在肺泡表面液层组成的 气、液界面上的表面张力。 而对于肺充气来说,大部分压力是来 克服表面张力的。 肺泡的表面液层中分布着有一定量的、 由饱和卵磷脂和脂蛋白组成的表面活性 物质,起降低表面张力系数的作用。
表面张力现象

在高压条件下,物质内部的密度和分子间相 互作用力发生变化,导致表面张力发生变化。
在低压或真空条件下,气体分子间的距离增 大,相互作用力减弱,导致表面张力减小。
04
表面张力现象的应用
工业制造
微电子制造
表面张力在微电子制造中用于控 制液体的流动和表面形貌,例如 在晶片清洗、表面涂层和光刻过
程中。
金属加工
非极性分子
非极性分子在表面更倾向于形成无序 排列,降低表面张力。
表面活性剂
降低表面张力
表面活性剂分子具有两亲性,一端亲水,一端亲油,能够降低油水界面张力,从而降低整个系统的表面张力。
改变界面性质
表面活性剂能够改变界面上的分子排列和性质,影响表面张力的变化。
压力
高压下表面张力变化
低压下表面张力变化
在金属加工过程中,表面张力用于 控制熔融金属的流动,以制造出具 有特定形状和质量的金属部件。
化学工业
在化学工业中,表面张力用于指导 液体的流动和分离过程,例如在萃 取、蒸馏和结晶过程中。
生物医学领域
生物芯片
表面张力在生物芯片的制造中起到关键作用,它能够控制生物分 子的排列和反应,从而提高检测的灵敏度和特异性。
03
影响表面张力现象的因素
温度
温度升高,表面张力降低
随着温度的升高,分子间的平均动能增加,导致表面分子间的相互作用力减弱, 从而降低表面张力。
温度降低,表面张力增加
随着温度的降低,分子间的平均动能减小,表面分子间的相互作用力增强,导致 表面张力增加。
物质性质
极性分子
具有强极性的分子在表面更容易形成 定向排列,增加表面张力。
土壤修复
表面张力有助于控制土壤中污染物的 迁移和分布,为土壤修复提供新的思 路和方法。
大学物理学习指导 第3章 液体的表面性质

第3章 液体的表面性质3.1 内容提要(一)基本概念1. 表面张力:液体的表面犹如张紧的弹性薄膜,具有收缩的趋势,即液体表面存在着张力,称为表面张力。
它是液体表面层内分子力作用的结果。
2.表面张力系数:用于反映液体表面性质的物理量,三种定义如下:(1)表面张力系数表示在单位长度直线两旁液面的相互拉力。
由L f α=得 Lf =α (3.1) 在国际单位制中,α的单位用N ·m -1表示。
(2)表面张力系数α等于增加单位表面积时,外力所做的功。
由△A=α·△S 得SA ∆∆=α (3.2) (3)表面张力系数α在数值等于增大液体单位表面积所增加的表面能,由△E =△A =α△S 得 SE ∆∆=α (3.3) 严格说来,表面能是在温度不变的条件下可转变为机械能的那部分表面能。
3.影响表面张力系数的几个因素(1) 不同液体的表面张力系数不同,它与液体的成分有关,取决于液体分子的性质。
(2) 同一种液体的表面张力系数与温度有关。
温度越高,α就越小。
(3) 液体表面张力系数的大小还与相邻物质的化学性质有关。
(4) 液体表面张力系数还与液体中的杂质有关。
加入杂质能显著改变液体的表面张力系数。
4.表面张力的微观本质微观理论认为,液体的表面张力是由于液体表面层分子之间相互作用力的不对称性引起的。
所谓液体的表面层是指位于液体表面处,与表面平行、厚度等于液体分子有效作用半径(一般不超过6×10-7cm)的那层液体。
从能量的角度出发,分子处于液体表面层时,分子的相互作用热能要比处于液体内部的分子的相互作用热能大,而且越靠近液面,分子的相互作用热能就越大。
而液体处于稳定平衡时,分子的相互作用热能最小,因此,液体表面层中的分子都有挤进液体内部的趋势,结果液体的表面就会尽量地收缩。
从力的观点来看,就是在液体表面内存在一种使其收缩的力,这种力就称为表面张力。
所谓表面张力,无论从力或是从能量的角度来解释,都是表面层内分子相互作用的不对称性所引起的。
液体2
附着层的厚度为d和L中的 大者。d和L分别是内聚力 和附着力的有效距离 !
3、描述润湿或不润湿程度的物理量---接触角
接触角:液体和固体接触处的两表面切线在液体内部 所成的夹角叫做接触角。 实验发现,润湿和不润湿现象可由接触角来表示。 (1)当0<θ<90度时,润湿;当θ=0度时,完全润湿。
(2)当90<θ<180度时,不润湿; 当θ=180度时,
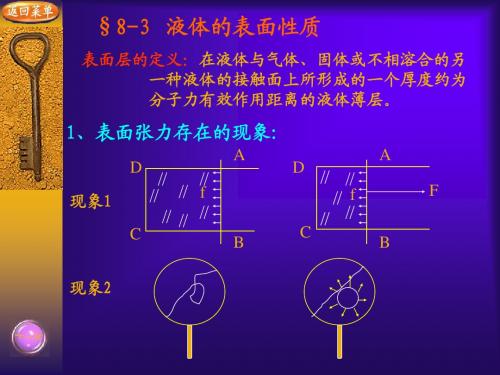
A F
AB平衡时,通过测F来确定f, 实验表明:f与F方向相反, C B F 的大小与液面的周界的 长度L成正比 ,即:f=αL 其中,α—表面张力系数,大小等于液面作用于单位长度 线段上的表面张力。
本实验中液膜有两个液面,所以,f=2αL ,即
α=f/2L
(2)从外力作功的角度给表面张力系数的定义:
4、表面张力产生的微观解释
(1)从分子力角度:
A、分子在a、b点时完 全不会受液体的作用; L B、分子在c点开始受 A N 到指向液体的引力;
液体表面层中的分子 受到的引力指向液内
a
b c e
蒸汽 f 液体
M B g O
C、分子在e点时受到引力达到最大值; D、分子在g点时受到周围分子的合引力为零。
分子作用 的半径
A N
e f O g Q
S B
导致表面层的分子分布 和液体内分子分布如右图所示!
表面层中分子的势能 (3)从能量角度: 大于液体内分子的势能!
S
将液体内部的分子移到表面层中来, 必须克服指向液内分子引力而做功。
表面层中的分子具有较液体内部的分子的更大的势能。而表 面越大,在表面层中的分子数就越多,整个表面层的势能就 越大,因为势能越小越稳定,所以液面有收缩趋势。
教科版高中物理选修3-3《液体的表面张力》参考课件

特别提醒:(1)在体积相等的各种形状的物体中,球 形物体的表面积最小,所以草叶上的露珠、小水银 滴等,都因表面张力使液面收缩而呈球形. (2)表面张力是跟液面相切的.如果液面是平面,表 面张力就在这个平面上;如果液面是曲面,表面张 力就在这个曲面的切面上.作用在任何一部分液面 上的表面张力,总是跟这部分液面的分界线垂直. (3)表面张力是根据效果命名的力,是液体的表面层 内大量分子力的宏观表现.
变式训练 下列有关表面张力的说法中,正确的是
() A.表面张力的作用是使液体表面伸张 B.表面张力的作用是使液体表面收缩 C.有些小昆虫能在水面自由行走,这是由于有表 面张力的缘故 D.用滴管滴液滴,滴的液滴总是球形,这是由于 表面张力的缘故
解析:选BCD.表面张力的作用效果是使液体表 面收缩,由于表面张力,被压弯的液面收缩,使 小昆虫浮在液面上;由于表面张力使液滴收缩成 球形.
核心要点突破
一、液体的微观结构及特性 1.液体的微观结构 液体中的分子跟固体一样是密集在一起的,液体分子 的热运动主要表现为在平衡位置附近做微小的振动, 但液体分子只在很小的区域内有规则的排列,这种区 域是暂时形成的,边界和大小随时改变,有时瓦解, 有时又重新形成.液体由大量这种暂时形成的小区域 构成,这种小区域杂乱无章地分布着.
2.液体的宏观特性 (1)各向同性:液体由大量暂时形成的杂乱无章分布 的小区域构成,所以液体表现出各向同性. (2)一定体积:液体分子的排列更接近于固体,液体 中的分子密集在一起,分子间距接近于r0,相互间 的束缚作用强,主要表现为在平衡位置附近做微小 振动,所以液体具有一定的体积.
(3)流动性:液体分子能在平衡位置附近做微小的振 动,但没有长期固定的平衡位置,液体分子可以在 液体中移动,这是液体具有流动性的原因. (4)扩散特点:液体中扩散现象是由液体分子运动产 生的,分子在液体里的移动比在固体中容易得多, 所以液体的扩散要比固体的扩散快.
表面张力课件

PPT学习交流
14
作用在小面元ΔS周界线Δl上的表面 张力为
Δf =α×Δl
Δf 可以被分解为Δf1和Δf2,由于Δf2与 半径oc垂直,对附加压强不起作用,
故不考虑。
而Δf1的方向指向液体内部,其值为
Δf1 =Δl sinφ=α×Δl sinφ
PPT学习交流
15
作用于ΔS整个周界线--即其周长上的 表面张力,指向液体内部的分力总和为
即增加单位液面所增加的势能。
由上式可知,α在数值上等于增加单位液 面时外力所作的功,从能量的角度看,其大小 等于增加单位液面时所增加的表面自由能。
那么液体表面能的减小可以通过下面任 一种自动过程来实现:
自动减小S;
自动减小α;
S和α两PPT学者习交都流 同时自动减小。
11
二、曲面下的附加压强
Hale Waihona Puke PPT学习交流PC
PA
4
R
PPT学习交流
19
一、毛细现象和气体栓塞 1、 毛细现象
(1)润湿现象 当液体和固体接触 时,液固界面之间会出现两种现象:
润湿和不润湿现象。
PPT学习交流
20
同一种液体,对不同的固体来说,
它可以是润湿的,也可以是不润湿的。 润湿和不润湿现象就是液体和固体接触 处的表面现象。其差别是由液体分子与 固体分子之间的相互作用而形成的。可 以用其分子间相互作用力的大小来解释。
PPT学习交流
4
如果以10-9m为半径作一球面, 显然则只有在这个球面内的分子才 对位于球心上的分子有作用力。
分子作用球——分子引力作用范围是 半 径 为 10-9m 的 球 形 , 球 的 半 径 称 为 分子作用半径。
表面张力和表面能 课件
表面张力在生活中的应用
01
02
03
露珠呈球形
由于表面张力,水滴在荷 叶或树叶上呈球形,不易 散开。
气泡形成
在洗衣服、洗碗时,表面 张力使气泡在水中形成并 保持。
防水表面
表面张力可以用于创造防 水表面,如荷叶的自洁效 应。
表面能在工业中的应用
涂层附着
表面能的大小影响涂层与 基材的附着力,选择合适 的涂层材料和工艺可以提 高附着力。
表面能与物质性质的关系
物质性质对表面能的影响
物质的化学性质、晶体结构、分子间作用力等都会影响其表 面能。例如,极性分子具有较大的表面能,因为它们具有更 强的分子间相互作用力。
表面能的应用
在化学、物理、工程等领域中,表面能具有广泛的应用,如 润湿现象、自组装单层膜、晶体生长等都与表面能密切相关 。
04
力等因素有关。
表面能
表面能是固体表面的能量,它是 由于固体表面原子或分子的排列 不规整而引起的。表面能的大小 与表面的粗糙度、化学组成、温
度等因素有关。
实验方法
通过测量液体在固体表面上展开 的角度或测量液体在固体表面上 的接触角,可以计算出表面张力
和表面能。
实验步骤
准备实验器材
测量液体在固体表面上的接触角
表面张力计、表面能计、待测液体和固体 样品等。
将待测液体滴在固体表面上,观察液滴的 形状,并测量接触角。
计算表面张力和表面能
分析实验结果
根据接触角的大小,利用相关公式计算出 表面张力和表面能。
分析实验结果,了解表面张力和表面能与 物质性质的关系,并得出结论。
06
相关理论介绍
杨氏方程
总结词
杨氏方程是描述表面张力和表面分子 间的相互吸引程度。
生活中的表面张力现象
流体力学课程报告课题名称: 生活中的表面张力现象学生姓名:张XX学号:2010XXXXXX班级:XXXXXXXX专业:工程力学时间:2013年6月20日生活中的表面张力现象一、表面张力的定义表面张力,是液体表面层由于分子引力不均衡而产生的沿表面作用于任一界线上的张力,在该力的作用下液体的表面总是试图获得最小的、光滑的面积达到能量最低的状态,像是一层弹性的薄膜。
表面张力产生于流体与其他物质界面处,其量纲是单位长度的力和单位面积的能。
二、表面张力产生的原因1、分子力学角度的解释液体的内聚力是形成表面张力的原因。
在液体内部,每个分子都在每个方向都受到邻近分子的吸引力(也包括排斥力)。
因此,液体内部分子受到的分子力合力为零。
然而,在液体与气体的分界面上的液体分子在各个方向受到的引力是不均衡的(如图2-1),造成表面层中的分子受到指向液体内部的吸引力,并且有一些分子被“拉”到液体内部。
因此,液体会有缩小液面面积的趋势,在宏观上的表现即为表面张力现象。
图2-1 界面及内部液体分子受力示意图2、分子势能角度的解释液体内部分子周围有大量分子,因此,内部分子的分子势能较低。
然而,表面层中的分子周围的分子明显小于液体内部分子的,所以,表面层的分子有较高的分子势能。
为了达到低能量的稳定状态,表面层中的分子有向液体内部移动的趋势,从而导致表面层中的分子数量减少,宏观表现为液体表面积减小。
如图2-2所示。
图2-2 液体界面内外分子势能示意图三、生活中的表面张力现象1、肥皂膜中的表面张力——液面收缩性如图3-1所示,将一中间系有软质棉线的铁圈在肥皂液中浸泡,在整个铁圈表面会形成一张液膜,刺破棉线左侧处液膜,在液体表面张力作用下,棉线将向另一侧拉紧;若刺破另一侧液膜,棉线将向反方向拉紧。
图3-1 肥皂膜张紧单线现象如图3-2所示,刺破棉线圈中的液膜,整个棉线圈将向四周被拉紧。
图3-3肥皂膜张紧棉圈现象如图3-4所示,将用细铁丝做的U型框架的两导轨上安置一横向铁丝,铁丝能在导轨上自由运动而不脱落。
表面张力的物理原理
表面张力的物理原理表面张力是一种特殊现象,它是液体分子间的相互作用力导致液体表面处于紧绷状态的结果。
本文将探讨表面张力的物理原理及其相关应用。
一、表面张力的概念表面张力是指液体表面处的分子受到的向内的引力,它使得液体表面呈现出一定的膜状结构,类似于一层薄膜。
表面张力是液体分子间相互作用力的结果,主要包括三种类型:分子间吸引力、分子间斥力和分子间电荷引力。
液体内部的分子间相互作用力是各向同性的,然而液体表面上的分子处在不完整的相互作用力场中,所以会出现相对较强的表面张力。
二、表面张力的原理表面张力是由于分子间力的不平衡所导致的。
对于位于液体内部的分子而言,由于与周围分子存在相互吸引的力,所以它们会受到均衡的力,使得液体内部是平衡的。
然而,位于液体表面的分子由于周围分子的减少,无法形成完整的各向同性相互作用力场,因此会受到来自液体内部的引力。
同样道理,表面上的液体分子对外部的分子也会存在一定的相互作用力,这是由于液体内部的分子施加在表面上的引力和外部分子施加在表面上的压力相抵消所导致的。
三、表面张力的性质1. 使液体表面呈现弹性形态表面张力使得液体表面呈现出类似弹性膜的形态。
当液体表面受到外部的力时,表面张力会通过液体分子的重排来恢复初始状态。
这种性质对于一些生物现象,如昆虫在水面行走、水珠在叶片上的保持等都起着重要作用。
2. 形成液滴由于表面张力的作用,液体在自由状态下会形成球状液滴。
这是因为球状液滴对于单位面积的表面积来说,具有最小的体积。
同时,在液体与其他物体接触的情况下,液滴也能够保持一定的形状和稳定性。
四、表面张力的应用1. 液体的涂布和浸润表面张力可以影响液体在固体表面的涂布和浸润行为。
对于不易润湿的固体表面,液体的接触角较大,液体无法充分润湿固体表面。
而在易润湿的固体表面,液体的接触角较小,液体能够充分润湿固体表面。
2. 水的上升和下降在细小的毛细管或细管道内,由于表面张力的作用,液体能够在内部产生一定的上升或下降效应。
表面张力
比较液体内的分子A和液面分子B的受力情况。以分子力的有效力程为半径作以分子A为中心的球面(图1), 则所有对分子A有作用的分子都在球面之内。选取一段较长的时间T(是分子两次碰撞之间的平均时间),由于对 称,在这段时间内,各个分子对A的作用力的合力等于零。以分子B为中心的球面中的一部分在液体当中,另一部 分在液面之外,这部分分子密度远小于液体部分的分子密度。如果忽略这部分分子对B的作用,则由于对称,CC' 和DD'之间所有分子作用力的合力等于零;对B有效的作用力是由球面内DD'以下的全体分子产生的向下合力。由 于处在边界内的每—个分子都受到指向液体内部的合力,所以这些分子都有向液体内部下降的趋势,同时分子与 分子之间还有侧面的吸引力,即有尽量收缩表面的趋势。这种情况使流体的表面好像蒙在一个表面积比它大的固 体外面的弹性薄膜。
如果三种介质有一种是固体(通常固体的边界面是平面),则只有平行固壁的接触线才能自由运动,由此得 到该方向的平衡方程(图3b):
或
图3三介质接触线处的平衡式中θ称为接触角。如果介质2是空气,介质3是液体,而且θ<π/2,则称固体是亲 该液体的;如果θ>π/2,则称固体是憎该液体的。θ愈小,液体对该固体的浸润程度越高。
涟波
表面张力在液体运动中有时也起很重要的作用。如微风掠过水面时产生的涟波就是表面张力起主要作用的一 种水波。
谢谢观看
影响因素
表面张力的方向与液面相切,并与液面的任何两部分分界线垂直。表面张力仅仅与液体的性质和温度有关。 一般情况下,温度越高,表面张力就越小。另外杂质也会明显地改变液体的表面张力,比如洁净的水有很大的表 面张力,而沾有肥皂液的水的表面张力就比较小,也就是说,洁净水表面具有更大的收缩趋势 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1 1 p ( ) R1 R2
这是拉普拉斯公式
2.圆柱形凹液面
2 p d
6-9、毛细现象及毛细管公式
一.润湿和不润湿 接触角
例如:水 + 玻璃
固体
水 + 涂有油脂的玻璃
接触角
θ A
液体
附着力 内聚力
附 着 层
(二)、毛细现象
2 cos h gr
R
θ θ h D A
这是拉普拉斯公式
6-9、毛细现象及毛细管公式
一.润湿和不润湿 接触角
例如:水 + 玻璃
固体
水 + 涂有油脂的玻璃
接触角
θ A
液体
附着力 内聚力
附 着 层
(二)、毛细现象
2 cos h gr
R
θ θ h D A
B
C
E S
表面能:张力系数在数值上等于在等温条件下液体表面增加单位 面积时所增加的表面能 表能自由能:表面能不同于表面内能,可以认为,它是表面内能的一 部分,是在等温条件下能够转变为机械功的那一部分,在热力学中 称为表面自由能.
两个问题的讨论: (1) 表面积问题:理论和实验表明,在等温条件下,体积一定的液体 的平衡态对于表面自由能取极小值.
能使σ 明显变小的物质称为表面活性物质 若一种物质甲能显著地降低另一种物质乙的表面 张力,就说甲对乙具有表面活性。
例6-5 长为a宽
为b.
.
m 0.88103 kg, a 3.2 102 m, b 3.0 102 m
• 求出水的表面张力系数.
三.表面能
由图6.35(a).(c)可以看出,设使AB边向右移动 距离
(2) 表面层: 从微观角度来看,液体表面并不是一个真正的几何面, 而是一个厚度为分子力有效作用距离的薄层,称为表面层
6-8、弯曲液面附加压强
一.附加压强的存在
pb pc pa
p a p0
pb p0
p p p0
由于表面张力的作用,使弯曲液面 内无限接近于液面处液面处液体 压强p与液面外的压强p0之间存 在着压强差,此压强差 p p p0 称为弯曲液面下的附加压强
f 2r 2
df2 df φ
dl r df1
o S R
φ
R
C
(3)重力mg (4)在底面S上受到下面液体的压力为PS.P为S面上的液体压强,也就 是弯曲液面下液体内部A点的压强.
2 球形液膜 p p0 R
2a P0 R
三.拉普拉斯公式
任意液面附加压强: p ( 1 1 ) R1 R2
B
C
一、表面张力现象Βιβλιοθήκη §6-7液体的表面张力
1、表面张力
二.表面张力和表面张力系数
表面张力是作用于液体表面是的使液体具有收缩倾向 的一种力。 • 表面张力可以由前图a得到.表面张力的大小与液面 的周界(或截线)长度l成正比,即 F外 2 f 2l 并由c得到外力 f l
表面张力系数与其它因素的关系
二.球形液面下附加压强的计算
(1)计算S’球冠面上的大气压的合力p0S
(2)计算半径为r的球冠 面上周边上表面张力
f df dl sin 1
sin 1 dl r 2r R
2r
2
R
(3)重力mg (4)在底面S上受到下面液体的压力为PS.P为S面上的液体压强, 也就是弯曲液面下液体内部A点的压强.
6-8、弯曲液面附加压强
一.附加压强的存在
由于表面张力的作用,使弯曲液面内无限接近于 液面处液面处液体压强p与液面外的压强p0之间 存在着压强差,此压强差 p p p0 称为弯曲液面 下的附加压强
内
外
二.球形液面下附加压强的计算
(1)计算S’球冠面上的大气压的合力p0S (2)计算半径为r的球冠面上周边上表面张力
A F外x 2 f x 2 AB x S
式中 表示AB边移动 x 时液膜的两个表面所增加的总面积, 在等温过程的条件下 ,这个功转变为液体表面能的增量 E ,所以 S 可以得出
E S
表面能:张力系数在数值上等于在等温条件下液体表面增加单位 面积时所增加的表面能 表能自由能:表面能不同于表面内能,可以认为,它是表面内能的一 部分,是在等温条件下能够转变为机械功的那一部分,在热力学中 称为表面自由能.
第六章非理想气体 固体 液体
§6-7
一、表面张力现象
液体的表面张力
二.表面张力和表面张力系数
1、表面张力
表面张力是作用于液体表面是的使液体具有收缩倾向 的一种力。此力与截线垂直并与该处液面相切. • 表面张力可以由前图a得到.表面张力的大小与液面的 周界(或截线)长度l成正比,即
f l
并由c得到外力
pS p0 S mg f
由于mg很小,可忽略不计,有:
f 2 2 p p 0 P0 f / r p 0 S R
(5)对于凹面液体
2 p p0 R
2 p p0 R
(6)对于球形气泡 内外压强差为:
4 p R
三.拉普拉斯公式
1.任意液面附加压强:
• 求出水的表面张力系数.
三.表面能
由图6.35(a).(c)可以看出,设使AB边向右移动距 离
A F外x 2 f x 2 AB x S
式中 S表示AB边移动 x 时液膜的两个表面所增加的总面积, 在等温过程的条件下,这个功转变为液体表面能的增量 E ,所以 可以得出
F外 2 f 2l
表面张力系数与其它因素的关系(温度,表面活性物质,临界 介质)
能使σ 明显变小的物质称为表面活性物质 若一种物质甲能显著地降低另一种物质乙的表面 张力,就说甲对乙具有表面活性。
例6-5 长为a宽
为b.
.
m 0.88103 kg, a 3.2 102 m, b 3.0 102 m
