高中化学 专题三高中化学知识点总结
高中化学物质结构与性质专题知识点总结

高中化学选修 3 知识点总结一、原子结构1、能层和能级(1)能层和能级的划分! 在同一个原子中,离核越近能层能量越低。
"同一个能层的电子,能量也可能不同,还可以把它们分成能级s 、p 、 d 、f ,能量由低到高依次为 s 、p 、d 、f 。
# 任一能层,能级数等于能层序数。
$ s 、p 、d 、f ⋯⋯可容纳的电子数依次是 1、3、5、7⋯⋯的两倍。
% 能层不同能级相同,所容纳的最多电子数相同。
2、构造原理(1)构造原理是电子排入轨道的顺序,构造原理揭示了原子核外电子的能级分布。
(2)构造原理是书写基态原子电子排布式的依据,也是绘制基态原子轨道表示式的主 要依据之一。
(3)不同能层的能级有交错现象,如 E (3d )>E (4s )、E (4d )> E ( 5s )、 E ( 5d )>E ( 6s )、 E ( 6d )> E ( 7s )、 E ( 4f )> E ( 5p )、 E ( 4f )> E ( 6s )等。
原子轨道的能 量关系是: ns <( n-2)f < (n-1 )d < np(4)能级组序数对应着元素周期表的周期序数,能级组原子轨道所容纳电子数目对应 着每个周期的元素数目。
根据构造原理,在多电子原子的电子排布中:各能层最多容纳的电子数为2n 2 ;最外层不超过 8 个电子;次外层不超过 18 个电子;倒数第三层不超过 32 个电子。
( 5)基态和激发态 ①基态:最低能量状态。
处于 最低能量状态 的原子称为 基态原子 。
" 激发态:较高能量状态(相对基态而言)。
基态原子的电子吸收能量后,电子跃迁至 较高能级时的状态。
处于激发态的原子称为激发态原子 。
# 原子光谱:不同元素的原子发生电子跃迁时会吸收(基态→激发态) 和放出(激发态 →&'()*(+*,-./0123456()7892:;<-=>?5&@&A5@?()2B ='C5较低激发态或基态)不同的能量(主要是光能),产生不同的光谱——原子光谱(吸收光谱和发射光谱)。
高考化学专题复习之氧化还原反应知识点总结
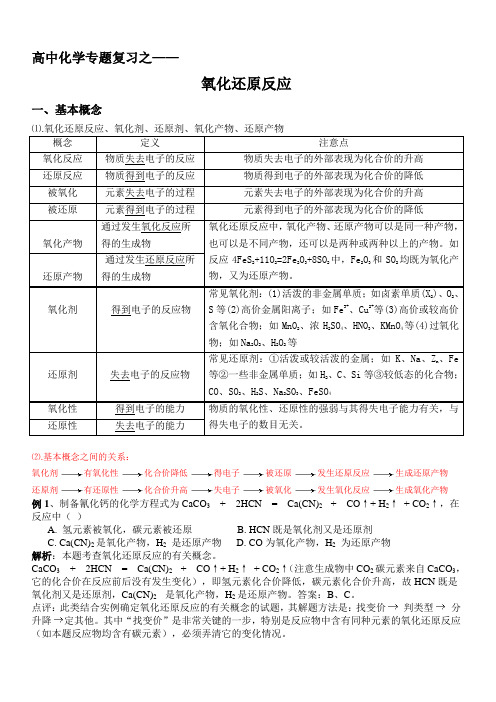
高中化学专题复习之——氧化还原反应一、基本概念⑴.氧化还原反应、氧化剂、还原剂、氧化产物、还原产物概念定义注意点氧化反应物质失去电子的反应物质失去电子的外部表现为化合价的升高还原反应物质得到电子的反应物质得到电子的外部表现为化合价的降低被氧化元素失去电子的过程元素失去电子的外部表现为化合价的升高被还原元素得到电子的过程元素得到电子的外部表现为化合价的降低氧化产物通过发生氧化反应所得的生成物氧化还原反应中,氧化产物、还原产物可以是同一种产物,也可以是不同产物,还可以是两种或两种以上的产物。
如反应4FeS2+11O2=2Fe2O3+8SO2中,Fe2O3和SO2均既为氧化产物,又为还原产物。
还原产物通过发生还原反应所得的生成物氧化剂得到电子的反应物常见氧化剂:(1)活泼的非金属单质;如卤素单质(X2)、O2、S等(2)高价金属阳离子;如Fe3+、Cu2+等(3)高价或较高价含氧化合物;如MnO2、浓H2SO4、HNO3、KMnO4等(4)过氧化物;如Na2O2、H2O2等还原剂失去电子的反应物常见还原剂:①活泼或较活泼的金属;如K、Na、Zn、Fe等②一些非金属单质;如H2、C、Si等③较低态的化合物;CO、SO2、H2S、Na2SO3、FeSO4氧化性得到电子的能力物质的氧化性、还原性的强弱与其得失电子能力有关,与得失电子的数目无关。
还原性失去电子的能力⑵.基本概念之间的关系:氧化剂有氧化性化合价降低得电子被还原发生还原反应生成还原产物还原剂有还原性化合价升高失电子被氧化发生氧化反应生成氧化产物例1、制备氰化钙的化学方程式为CaCO3+ 2HCN = Ca(CN)2 + CO↑+ H2↑+ CO2↑,在反应中()A. 氢元素被氧化,碳元素被还原B. HCN既是氧化剂又是还原剂C. Ca(CN)2是氧化产物,H2是还原产物D. CO为氧化产物,H2为还原产物解析:本题考查氧化还原反应的有关概念。
CaCO3+ 2HCN = Ca(CN)2 + CO↑+ H2↑+ CO2↑(注意生成物中CO2碳元素来自CaCO3,它的化合价在反应前后没有发生变化),即氢元素化合价降低,碳元素化合价升高,故HCN既是氧化剂又是还原剂,Ca(CN)2 是氧化产物,H2是还原产物。
高中化学知识总结氧化还原反是专题

煌敦市安放阳光实验学校氧化还原反是专题[氧化还原知识络]一、化学反的类型1.化学反基本类型(依据反物、生成物的类别和种类分类)化学反2.氧化还原反和非氧化还原反(依据反物有无电子转移或物质的相关元素在反前后有无化合价改变分类)化学反3.其它分类法a.依据反的热效分为:吸热反,放热反。
b.依据反进行的程度分为:可逆反,非可逆反。
c.依据反中有无离子参与分为:离子反,分子反。
4.氧化还原反与基本反类型的关系⑴置换反都是氧化还原反;⑵复分解反都是非氧化还原反;⑶化合反和分解反可能为氧化还原反;它们的关系可用下图表示:说明:⑴有单质参与的化合反或分解反多数为氧化还原反,但不一是氧化还原。
如:①4P(红)=P4为化合反,但为非氧化还原反;②2O3=3O2有单质生成但为非氧化还原;⑵没有单质参与的化合反或分解反也可能是氧化还原反。
如:①NH4NO3的分解,随条件不同,产物也不同,可能生成NO2、H2O为氧化还原反,但没有单质参与;②Na2O2与MnO2化合可以生成Na2MnO4也是氧化还原反,但没有单质参与。
二、氧化还原反1、特征:反前后元素的化合价发生改变。
2、实质:有电子转移(电子的得失或共用电子对的偏移)。
3、氧化还原反概念①氧化与还原(指反过程)②氧化剂与原还剂(指反物质)③氧化性与还原性(指物质能获得电子或能失去电子的性质)注:物质的氧化性(或还原性)的强弱,指的是得(或失)电子的难易,不是指得(失)电子的多少。
④氧化产物与还原产物(指生成物)4、氧化还原反概念间的关系。
5、氧化还原反中电子转移的表示方法⑴双线桥法――表明了反前后某种元素化合价的变化情况①用两条带箭头的线由反物指向生成物,且对准同种元素。
②要标明“得”“失”电子,且得失电子总数相。
③箭头不代表电子转移的方向,而是指某元素从反到产物时价态的变化。
例如:⑵单线桥法――表明了一个氧化还原反中电子的转移方向和数目①用一条箭线在反物间表示电子得失。
高中化学知识点——化学反应与能量

高中化学知识点——化学反应与能量一.反应热焓变1.定义:化学反应过程中吸收或放出的能量都属于反应热,又称为焓变(ΔH),单位kJ/mol。
解释:旧键的断裂:吸收能量;新键的形成:放出能量,某一化学反应是吸热反应还是放热反应取决于上述两个过程能量变化的相对大小。
吸热:吸收能量>放出能量;放热:吸收能量<放出能量。
2.化学反应中能量变化与反应物和生成物总能量的关系3.放热反应:放出热量的化学反应,(放热>吸热)ΔH<0;吸热反应,吸收热量的化学反应(吸热>放热)ΔH>0。
【学习反思】⑴常见的放热、吸热反应:①常见的放热反应有a燃烧反应b酸碱中和反应c活泼金属与水或酸的反应d大多数化合反应②常见的吸热反应有:a氢氧化钡晶体和氯化铵晶体混合发生反应bCO2+C=2COc大多数的分解反应⑵△H<0时反应放热;△H>0时反应吸热。
【概括总结】焓变反应热在化学反应过程中,不仅有物质的变化,同时还伴有能量变化。
1.焓和焓变焓是与物质内能有关的物理量。
单位:kJ·mol-1,符号:H。
焓变是在恒压条件下,反应的热效应。
单位:kJ·mol-1,符号:ΔH。
2.化学反应中能量变化的原因化学反应的本质是反应物分子中旧化学键断裂和生成物生成时新化学键形成的过程。
任何化学反应都有反应热,这是由于在化学反应过程中,当反应物分子间的化学键断裂时,需要克服原子间的相互作用,这需要吸收能量;当原子重新结合成生成物分子,即新化学键形成时,又要释放能量。
ΔH=反应物分子中总键能-生成物分子中总键能。
3.放热反应与吸热反应当反应完成时,生成物释放的总能量与反应物吸收的总能量的相对大小,决定化学反应是吸热反应还是放热反应。
(1)当ΔH为“-”或ΔH<0时,为放热反应,反应体系能量降低。
(2)当ΔH为“+”或ΔH>0时,为吸热反应,反应体系能量升高。
4.反应热思维模型:(1)放热反应和吸热反应(2)反应热的本质以H2(g)+Cl2(g)===2HCl(g)ΔH=-186kJ·mol-1为例E1:E(H—H)+E(Cl—Cl);E2:2E(H—Cl);ΔH=E1-E2二.热化学方程式1.概念:能表示参加反应的物质变化和能量变化的关系的化学方程式叫做热化学方程式。
2019高中化学 专题3 有机化合物的获得与应用专题小结与测评学案 苏教版必修2

2019专题3 有机化合物的获得与应用[知识网络构建]一、烃的结构和性质写出图中标号所代表的化学方程式:①___________________________________________________________。
②___________________________________________________________。
③___________________________________________________________。
④___________________________________________________________。
⑤___________________________________________________________。
⑥___________________________________________________________。
⑦___________________________________________________________。
⑧___________________________________________________________。
二、食品中的有机化合物转化关系2019写出图中标号所代表的化学方程式:⑨___________________________________________________________。
⑩___________________________________________________________。
⑪___________________________________________________________。
⑫___________________________________________________________。
2023年高三化学教学总结15篇

2023年高三化学教学总结15篇高三化学教学总结1高三化学总复习是中学化学学习的关键时期,是巩固基础、优化思维、提高能力的重要阶段,高三化学总复习的效果将直接关乎高考成绩。
为了提高高三化学总复习的效果,为此我们在开学初对高三化学教学进行了详细的计划,注重教学过程的把握,根据高三各个不同时期使用不同的教学策略和训练方式。
一、研究信息,把握方向要研究全国特别是课改区近年高考化学试题、关注新教材和新课程的变化、熟悉考试大纲和考试说明以及合理利用其他资源。
二、摆正关系,抓纲务本进入高三化学教学,很容易走进总复习的怪圈:“迷恋”复习资料,陷入“题海”。
虽然投入了大量的时间和精力,但收效甚微,效果不佳。
对此,高三化学教学过程中必须保持清醒的头脑,努力处理好教材和复习资料的关系、重视基础和培养能力的关系、化学学科和其他学科知识的关系以及练习量和复习效率的关系。
三、多思善想,提高能力首先要精读教材,字斟句酌。
系统复习,自始至终都应以教材为本,注意知识的全面性、重点性、精确性、联系性和应用性。
对中学(初、高中)化学知识和技能都要一一复习到位;对教材中的关键性知识(我们常说的考点),进行反复阅读、深刻理解,以点带面形成知识结构;对化学知识的理解、使用和描述要科学、准确和全面,如规范地使用化学用语,正确、全面地表达实验现象和操作要点等(尤其适合中等以下的学生,利用年级组统一安排的基础加强课时间);对知识点之间的相互关系及其前因后果。
如与离子反应有关的知识有离子反应方程式的书写和正误判断、离子共存问题、离子浓度大小比较、离子的检验和推断、溶液的导电性变化等。
应用性是指通过复习要学会运用知识解决实际问题的方法,如元素周期律、周期表涵盖的内容相当丰富,可以进行元素位、构、性相互推断,预测未知元素的性质,比较各种性质的强弱等。
此外,要重视对化学实验内容的复习(包括教材中的演示实验和课本后的分组实验),而且尽可能地亲自动手操作,通过这些典型实验,深入理解化学实验原理(反应原理、装置原理、操作原理)、实验方法的设计、实验结果的处理等,切实提高实验能力。
高中有机化学知识点汇总(一)

高考有机化学专题一:有机物的结构和同分异构体:(一)有机物分子式、电子式、结构式、结构简式的正确书写:1、分子式的写法:碳-氢-氧-氮(其它元素符号)顺序。
2、电子式的写法:掌握7种常见有机物和4种基团:7种常见有机物:CH4、C2H6、C2H4、C2H2、CH3CH2OH、CH3CHO、CH3COOH。
4种常见基团:-CH3、-OH、-CHO、-COOH。
3、结构式的写法:掌握8种常见有机物的结构式:甲烷、乙烷、乙烯、乙炔、乙醇、乙醛、乙酸、乙酸乙酯。
(注意键的连接要准确,不要错位。
)4、结构简式的写法:结构简式是结构式的简写,书写时要特别注意官能团的简写,烃基的合并。
要通过练习要能识别结构简式中各原子的连接顺序、方式、基团和官能团。
掌握8种常见有机物的结构简式:甲烷CH4、、乙烷C2H6、乙烯C2H4、、乙炔C2H2、乙醇CH3CH2OH、乙醛CH3CHO、乙酸CH3COOH、乙酸乙酯CH3COOCH2CH3。
(二)同分异构体:要与同位素、同素异形体、同系物等概念区别,注意这四个“同”字概念的内涵和外延。
并能熟练地作出判断。
1、同分异构体的分类:碳链异构、位置异构、官能团异构。
2、同分异构体的写法:先同类后异类,主链由长到短、支链由整到散、位置由心到边。
3、烃卤代物的同分异构体的判断:找对称轴算氢原子种类,注意从对称轴看,物与像上的碳原子等同,同一碳原子上的氢原子等同。
专题二:官能团的种类及其特征性质:(一)、烷烃:(1)通式:C n H2n+2,代表物CH4。
(2)主要性质:①、光照条件下跟卤素单质发生取代反应。
②、在空气中燃烧。
③、隔绝空气时高温分解。
(二)、烯烃:(1)通式:C n H2n(n≥2),代表物CH2=CH2,官能团:-C=C-(2)主要化学性质:①、跟卤素、氢气、卤化氢、水发生加成反应。
②、在空气中燃烧且能被酸性高锰酸钾溶液氧化。
③、加聚反应。
(三)、炔烃:(1)通式:C n H2n-2(n≥2),代表物CH≡CH,官能团-C≡C-(2)主要化学性质:①、跟卤素、氢气、卤化氢、水发生加成反应。
高中化学电子排布、第一电离能和电负性知识归纳

高中化学电子排布、第一电离能和电负性知识归纳一、原子结构1. 原子的组成: 原子核、核外电子2. 原子的特点:原子不显电性,体积小,质量小,质量主要集中在原子核上,原子核的密度非常大3. 核外电子排布规律(1 )能量最低原理(2 )每一层最多容纳电子数:2n 2 个(3 )最外层电子数不超过8 个(K 层为最外层时不超过2 个)(4 )次外层电子数不超过18 个,倒数第三层不超过32 个二、能层与能级能量最低原理: 原子的电子排布遵循能使整个原子的能量处于最低状态基态原子: 处于最低能量的原子1. 能层: 核外电子的能量是不同的, 按电子能量差异,可以将核外电子分成不同的能层——电子层同一能层的电子,能量也可能不同,还可以分成不同能级能级数2. 能级:s 、p 、d 、f····以s 、p 、d 、f···· 排序的各能级可容纳的最多电子数依次为1 、3 、5 、7 、······ 的二倍。
能级数= 能层序数(n)三、构造原理1. 电子排布式Na :1s 2 2s 2 2p 6 3s 1试书写N 、Cl 、K 、26 Fe 原子的核外电子排布式注意:24 Cr :1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 129 Cu :1s 2 2s 2 2p 6 3s 2 3p 26 3d 10 4s 1离子电子排布式书写——先失去最外层电子与能量最低原则无关1) 、能量最低原理2 )、每个原子轨道上最多能容纳__2__ 个电子,且自旋方向__ 相反____ (泡利不相容原理)3 )、当电子排布在同一能级时,总是__ 首先单独占一个轨道__ ,而且自旋方向_ 相同__。
(洪特规则)4) 、补充规则:全充满(p 6 ,d 10 ,f 14 )和半充满(p 3 ,d 5 ,f 7 )更稳定2. 简化电子排布式15P:[Ne]3s 2 3p 3 (表示内层电子与Ne 相同。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
知识点大全2013高中化学(新课标)66专题目录请在百度文库搜索“高中化学66专题”下载全部66个专题的资料1)2012化学高考真题2)高中化学方程式3)高中化学基础知识总结4)2013高中化学热点5)近年高考高频考点6)化学物质及其变化7)金属及其化合物8)非金属及其化合物9)氧化还原反应配平10)离子反应方程式和离子共存11) 反应中的能量变化12)钠及其化合物的性质13)碱金属元素14)物质的量15)气体摩尔体积16)物质的量的浓度17)物质的量_化学方程18)氯气19)卤素20)原子结构21)元素周期律22)元素周期表23)化学键_非极性分子和极性分子24)晶体的类型与性质25)氧族元素26)二氧化硫27)硫酸及其盐28)硫酸工业_环境保护29)碳族元素.碳及其化合物30)硅酸盐工业_新型无机非金属材料31) 氮和磷32)氨、铵盐33)硝酸34) 无机物的推断35) 化学反应速率36) 化学平衡37) 影响化学平衡的条件38) 合成氨条件的选择39) 电离平衡40) 水的电离和溶液的PH41) 盐类的水解42) 酸碱中和滴定43) 胶体44) 镁和铝45) 铁和铁的化合物46) 金属的冶炼47) 原电池原理及应用48) 电解原理及应用49) 甲烷烷烃50) 乙烯烯烃51) 乙炔炔烃52) 苯芳香烃53) 石油煤54)溴乙烷卤代烃55)乙醇醇类56) 有机物分子式和结构式57) 苯酚58) 乙醛醛类59)乙酸羧酸60)有机物的推断61) .糖类62) 油脂_蛋白质63) 合成材料64) 化学实验基本操作65) 物质的制备和检验66) 化学实验设计和评价高中化学全部知识点总结一、俗名无机部分:纯碱、苏打、天然碱、口碱:Na2CO3小苏打:NaHCO3大苏打:Na2S2O3石膏(生石膏):CaSO4.2H2O 熟石膏:2CaSO4·.H2O 莹石:CaF2重晶石:BaSO4(无毒)碳铵:NH4HCO3 石灰石、大理石:CaCO3生石灰:CaO 食盐:NaCl 熟石灰、消石灰:Ca(OH)2芒硝:Na2SO4·7H2O (缓泻剂) 烧碱、火碱、苛性钠:NaOH 绿矾:FaSO4·7H2O 干冰:CO2明矾:KAl (SO4)2·12H2O 漂白粉:Ca (ClO)2、CaCl2(混和物)泻盐:MgSO4·7H2O 胆矾、蓝矾:CuSO4·5H2O 双氧水:H2O2皓矾:ZnSO4·7H2O 硅石、石英:SiO2刚玉:Al2O3 水玻璃、泡花碱、矿物胶:Na2SiO3铁红、铁矿:Fe2O3磁铁矿:Fe3O4黄铁矿、硫铁矿:FeS2铜绿、孔雀石:Cu2 (OH)2CO3菱铁矿:FeCO3赤铜矿:Cu2O 波尔多液:Ca (OH)2和CuSO4石硫合剂:Ca (OH)2和S 玻璃的主要成分:Na2SiO3、CaSiO3、SiO2过磷酸钙(主要成分):Ca (H2PO4)2和CaSO4重过磷酸钙(主要成分):Ca (H2PO4)2天然气、沼气、坑气(主要成分):CH4水煤气:CO和H2硫酸亚铁铵(淡蓝绿色):Fe (NH4)2 (SO4)2溶于水后呈淡绿色光化学烟雾:NO2在光照下产生的一种有毒气体王水:浓HNO3与浓HCl按体积比1:3混合而成。
铝热剂:Al + Fe2O3或其它氧化物。
尿素:CO(NH2) 2有机部分:氯仿:CHCl3电石:CaC2电石气:C2H2 (乙炔) TNT:三硝基甲苯酒精、乙醇:C2H5OH氟氯烃:是良好的制冷剂,有毒,但破坏O3层。
醋酸:冰醋酸、食醋CH3COOH裂解气成分(石油裂化):烯烃、烷烃、炔烃、H2S、CO2、CO等。
甘油、丙三醇:C3H8O3焦炉气成分(煤干馏):H2、CH4、乙烯、CO等。
石炭酸:苯酚蚁醛:甲醛HCHO福尔马林:35%—40%的甲醛水溶液蚁酸:甲酸HCOOH葡萄糖:C6H12O6果糖:C6H12O6蔗糖:C12H22O11麦芽糖:C12H22O11淀粉:(C6H10O5)n硬脂酸:C17H35COOH 油酸:C17H33COOH 软脂酸:C15H31COOH草酸:乙二酸HOOC—COOH 使蓝墨水褪色,强酸性,受热分解成CO2和水,使KMnO4酸性溶液褪色。
二、颜色铁:铁粉是黑色的;一整块的固体铁是银白色的。
Fe2+——浅绿色Fe3O4——黑色晶体Fe(OH)2——白色沉淀Fe3+——黄色Fe (OH)3——红褐色沉淀Fe (SCN)3——血红色溶液FeO——黑色的粉末Fe (NH4)2(SO4)2——淡蓝绿色Fe2O3——红棕色粉末FeS——黑色固体铜:单质是紫红色Cu2+——蓝色CuO——黑色Cu2O——红色CuSO4(无水)—白色CuSO4·5H2O——蓝色Cu2 (OH)2CO3—绿色Cu(OH)2——蓝色[Cu(NH3)4]SO4——深蓝色溶液BaSO4、BaCO3、Ag2CO3、CaCO3、AgCl 、Mg (OH)2、三溴苯酚均是白色沉淀Al(OH)3白色絮状沉淀H4SiO4(原硅酸)白色胶状沉淀Cl2、氯水——黄绿色F2——淡黄绿色气体Br2——深红棕色液体I2——紫黑色固体HF、HCl、HBr、HI均为无色气体,在空气中均形成白雾CCl4——无色的液体,密度大于水,与水不互溶KMnO4--——紫色MnO4-——紫色Na2O2—淡黄色固体Ag3PO4—黄色沉淀S—黄色固体AgBr—浅黄色沉淀AgI—黄色沉淀O3—淡蓝色气体SO2—无色,有剌激性气味、有毒的气体SO3—无色固体(沸点44.8 0C)品红溶液——红色氢氟酸:HF——腐蚀玻璃N2O4、NO——无色气体NO2——红棕色气体NH3——无色、有剌激性气味气体三、现象:1、铝片与盐酸反应是放热的,Ba(OH)2与NH4Cl反应是吸热的;2、Na 与H 2O (放有酚酞)反应,熔化、浮于水面、转动、有气体放出;(熔、浮、游、嘶、红)3、焰色反应:Na 黄色、K 紫色(透过蓝色的钴玻璃)、Cu 绿色、Ca 砖红、Na +(黄色)、K +(紫色)。
4、Cu 丝在Cl 2中燃烧产生棕色的烟;5、H 2在Cl 2中燃烧是苍白色的火焰;6、Na 在Cl 2中燃烧产生大量的白烟;7、P 在Cl 2中燃烧产生大量的白色烟雾;8、SO 2通入品红溶液先褪色,加热后恢复原色;9、NH 3与HCl 相遇产生大量的白烟; 10、铝箔在氧气中激烈燃烧产生刺眼的白光; 11、镁条在空气中燃烧产生刺眼白光,在CO 2中燃烧生成白色粉末(MgO ),产生黑烟; 12、铁丝在Cl 2中燃烧,产生棕色的烟; 13、HF 腐蚀玻璃:4HF + SiO 2 = SiF 4 + 2H 2O 14、Fe(OH)2在空气中被氧化:由白色变为灰绿最后变为红褐色; 15、在常温下:Fe 、Al 在浓H 2SO 4和浓HNO 3中钝化;16、向盛有苯酚溶液的试管中滴入FeCl 3溶液,溶液呈紫色;苯酚遇空气呈粉红色。
17、蛋白质遇浓HNO 3变黄,被灼烧时有烧焦羽毛气味;18、在空气中燃烧:S ——微弱的淡蓝色火焰 H 2——淡蓝色火焰 H 2S ——淡蓝色火焰CO ——蓝色火焰 CH 4——明亮并呈蓝色的火焰 S 在O 2中燃烧——明亮的蓝紫色火焰。
19.特征反应现象:])([])([32OH Fe OH Fe 红褐色白色沉淀空气−−→− 20.浅黄色固体:S 或Na 2O 2或AgBr21.使品红溶液褪色的气体:SO 2(加热后又恢复红色)、Cl 2(加热后不恢复红色) 22.有色溶液:Fe 2+(浅绿色)、Fe 3+(黄色)、Cu 2+(蓝色)、MnO 4-(紫色) 有色固体:红色(Cu 、Cu 2O 、Fe 2O 3)、红褐色[Fe(OH)3] 黑色(CuO 、FeO 、FeS 、CuS 、Ag 2S 、PbS ) 蓝色[Cu(OH)2] 黄色(AgI 、Ag 3PO 4) 白色[Fe(0H)2、CaCO 3、BaSO 4、AgCl 、BaSO 3] 有色气体:Cl 2(黄绿色)、NO 2(红棕色)四、 考试中经常用到的规律:1、溶解性规律——见溶解性表;2、常用酸、碱指示剂的变色范围:指示剂 PH 的变色范围 甲基橙 <3.1红色 3.1——4.4橙色 >4.4黄色 酚酞 <8.0无色 8.0——10.0浅红色 >10.0红色 石蕊<5.1红色5.1——8.0紫色>8.0蓝色3、在惰性电极上,各种离子的放电顺序: 阴极(夺电子的能力):Au 3+ >Ag +>Hg 2+ >Cu 2+ >Pb 2+ >Fa 2+ >Zn 2+ >H + >Al 3+>Mg 2+ >Na + >Ca 2+ >K +阳极(失电子的能力):S 2- >I - >Br –>Cl - >OH - >含氧酸根注意:若用金属作阳极,电解时阳极本身发生氧化还原反应(Pt 、Au 除外) 4、双水解离子方程式的书写:(1)左边写出水解的离子,右边写出水解产物; (2)配平:在左边先配平电荷,再在右边配平其它原子;(3)H 、O 不平则在那边加水。
例:当Na 2CO 3与AlCl 3溶液混和时: 3 CO 32- + 2Al 3+ + 3H 2O = 2Al(OH)3↓ + 3CO 2↑ 5、写电解总反应方程式的方法:(1)分析:反应物、生成物是什么;(2)配平。
例:电解KCl 溶液:2KCl + 2H 2O == H 2↑+ Cl 2↑+ 2KOH 配平:2KCl + 2H 2O == H 2↑+ Cl 2↑+ 2KOH 6、将一个化学反应方程式分写成二个电极反应的方法:(1)按电子得失写出二个半反应式;(2)再考虑反应时的环境(酸性或碱性);(3)使二边的原子数、电荷数相等。
例:蓄电池内的反应为:Pb + PbO 2 + 2H 2SO 4 = 2PbSO 4 + 2H 2O 试写出作为原电池(放电)时的电极反应。
写出二个半反应: Pb –2e- → PbSO 4 PbO 2 +2e- → PbSO 4分析:在酸性环境中,补满其它原子: 应为: 负极:Pb + SO 42- -2e- = PbSO 4 正极: PbO 2 + 4H + + SO 42- +2e- = PbSO 4 + 2H 2O注意:当是充电时则是电解,电极反应则为以上电极反应的倒转:为: 阴极:PbSO 4 +2e - = Pb + SO 42- 阳极:PbSO 4 + 2H 2O -2e- = PbO 2 + 4H + + SO 42-7、在解计算题中常用到的恒等:原子恒等、离子恒等、电子恒等、电荷恒等、电量恒等,用到的方法有:质量守恒、差量法、归一法、极限法、关系法、十字交法 和估算法。
