武汉理工大学有机化学 有机化学实验1
武汉理工大学有机化学第15章习题参考答案

第15章习题参考答案15.1 (1) 谷氨酰胺(2)亮氨酸(3)赖氨酸(4)谷氨酸(5) 色氨酸(6) 组氨酸 15.2COOH CH 2COOH H H 2NCOOH 2SH H H 2NCOOHHH 2N H CH 3C 2H5RC H 2H 3NC O OH +H 3NC O OH +C H 2S H 酪氨酸半胱氨酸S-天门冬氨酸 S-半胱氨酸 (2S,3S )异亮氨酸 S-酪氨酸 15.3COO -NH 3+H OH H3COO -+H 3N HOCH 3COO -+H 3N OH HCH 3COO -NH 3+HHO3I II III VI结构式I 为L-苏氨酸,手性标记为 (2S, 3R)。
15.4(1)N a+C l-NO O HH过量H C l过量N aOHN O O -HN O O HHHPro, 色氨酸(2)C l-H OC H 2C H C O O N H 2过量N aOHH OC H 2C H C O O HN H 3+T yr, 酪氨酸N a+N a +O-C H 2C H C O O -N H 2(3) Cl-N a +H O CH 2CH CO O H N H 2过量H C l过量N aOHH O C H 2C H CO O -N H 2H O C H 2CH C O O HN H 3+Ser, 丝氨酸(4)C l -H O O C C H 2C H C O O HN H 3+过量H C l过量N aOH H O O C C H 2C H C O O H N H 2A sp, 天门冬氨酸a +N a +-OO C C H 2C H C O O -N H 215.5 加入水合茚三酮,氨基酸有显色反应15.6苯丙氨酸含一氨基一羧基,为中性氨基酸,其水溶液呈弱酸性。
因其等电点pI=5.84,故:pH=3.0时带正电荷:在pH=5.8时净电荷为零,为两性离子:在pH=10.0时带负电荷:15.7 (提示:考虑为什么杂环N 在Trp 中不是碱性的。
武汉理工大学有机化学(第二版)第1章习题及参考答案

1.3 将下列凯库勒式改写成路易斯式。
H
H
H
⑴H C O
⑵ H COC H
H
H
⑶H C N H
H
H
H
H
⑷ H C Cl
H
解:
H
⑴ H∶ C¨∶∶O¨ ¨
H
⑶ H∶ C¨∶ N¨ ∶H H¨ H¨
H
H
⑵ H∶ C¨∶O¨ ∶C¨∶H H¨ ¨ H¨
H
⑷ H∶ C¨∶C¨l∶ H¨ ¨
1.4 指出下列化合物中各个碳原子的杂化状态。
(1) CH C CH CH CH3
(2) H2C (1) CH C CH CH CH3
sp2 sp sp 2 (2) H2C C CH2
1.5 比较下列各组化合物偶极矩的大小
(1) A. C2H5Cl;B. CH2=CHCl;C. C6H5Cl;D. CCl2=CCl2
OH (1)
(2)
CH2OH
O (3)
COOH (4)
(5)
(6)
COOH
(7)
COOH (8)
O NH2
(9)
(10)
OH
NH2
解:按官能团分(1)、(2)和(10)同属醇类;(3)和(6)同属酮类;(4)、(5)和(7)同属羧酸类; (8)和(9)同属胺类。
按碳架分(1)、(3)、(4)和(9)同属脂肪族;(5)、(6)和(10)同属脂环族;(2)、(7)和(8)同属 芳香族。
第 1 章习题及参考答案
1.1 解释下列名词。 (1) 键角;(2) 官能团;(3) 构造;(4) 极性键;(5) 偶极矩;(6) 诱导效应; (7) 均裂;(8) 布莱斯特酸;(9) 路易斯碱;(10) 键能 解:(略)
2.14.4 相转移催化技术

相转移催化(Phase transfer catalysis ,简称FTC)),是20 世纪70 年代发展起来的在有机合成中应用日趋广泛的一种新的合成技术。
在有机合成中,常常遇到水溶性的无机物和不溶于水的有机物之间的非均相反应,这类反应通常速度慢、产率低,甚至很难进行。
但如果用水溶解无机盐,用极性小的有机溶剂溶解有机物,并加入催化量的季铵盐或季磷盐,此时催化剂利用自身对有机溶剂的亲和性,将水相中的反应物转移到有机相中,转化为均相反应,则反应很容易进行。
这类能提高反应速度并在两相间转移负离子的鎓盐,称为相转移催化剂。
相转移催化使许多用传统方法很难进行的反应或者不能发生的反应能顺利进行,而且具有选择性好、条件温和、产率高、操作简单、反应速度快、不要求无水操作、避免使用常规方法所需的危险试剂等优点。
相转移催化最初用于亲核取代反应,如引进一CN 和一F 的亲核取代、二氯卡宾的生成反应等。
目前,相转移催化已广泛应用于有机反应的绝大多数领域,如取代反应、氧化反应、还原反应、卡宾反应、重氮化反应、烷基化反应、酰基化反应、聚合反应,甚至高聚物修饰等,同时在医药、农药、香料、造纸、制革等行业也得到了广泛应用。
2.14.4.1 相转移催化机理相转移催化反应一般属于两相反应,主要用于液—液体系,也可用于液—固体系及液—固—液体系。
反应过程主要包括反应物从一相向另一相的转移以及被转移物质与待反应物质所发生的化学反应。
下面以季铵盐Q +X -催化RX 和NaCN 的反应为例说明相转移催化原理:R X NaCN+Q X+-(PTC)2RCN NaX +R X NaCN +Q X+-RCN+Q CN+-NaX ++Q CN+-Q X+-水相有机 相相 界面溶于水相的亲核试剂NaCN 和有机相的卤代烷RX 两者由于处于不同的相中而不能互相接近,反应很难进行。
加入季铵盐Q +X -相转移催化剂,由于季铵盐既溶于水又溶于有机溶剂,在水相中NaCN 与Q +X -相接触时,可以发生X -与CN -的交换反应生成Q +CN -离子对,这个离子对能够转移到有机相中;在有机相中Q +CN -与RX 发生亲核取代反应,生成目标产物RCN ,同时生成Q +X -,Q +X -再转移到水相,如此循环使相转移催化反应完成。
香豆素及取代香豆素的合成(1)

香豆素及取代香豆素的合成何怀国1 侍爱秋2 祁 刚3(11盐城市建湖县环境监测站,江苏建湖224000;21盐城市盐都区环境监测站,江苏盐城224000;31盐城工学院化学与生物工程学院,江苏盐城224003)摘 要 香豆素应用广泛,合成了香豆素、7-甲基香豆素、4,7-二甲基香豆素和6-甲基香豆素4个化合物,并对合成香豆素和6-甲基香豆素的后处理方法作了改进。
关键词 香豆素 7-甲基香豆素 4,7-二甲基香豆素 6-甲基香豆素合成收稿日期:2007-07-05作者简介:何怀国(1974),男,工程师,主要从事有机化合物的合成与监测工作 E -mail :qigang @ycit 1cnSynthesis of Coum arin and Substituted Coum arinHe Huaiguo 1 Shi Aiqiu 2 Qi G ang 3(11The environmental m onitoring station of Jianhu county ,Jiangsu Jianhu 224000;21The environmental m onitoring station of Y andu region ,Jiangsu Y ancheng 224000;31Department of chemistry and biology engineering ,Y ancheng Institute of T echnology ,Jiangsu Y ancheng 224003)Abstract C oumarin ,7-methylcoumarin ,4,7-dimethylcoumarin ,6-methylcoumarin were synthesized by Perkinreaction 1The preparation method of coumarin and 6-methylcoumarin were im proved 1K eyw ords coumarin 7-methylcoumarin 4,7-dimethylcoumarin 6-methylcoumarin synthesis 香豆素(C oumarin )化学名称1,2-苯并吡喃酮,广泛分布于高等植物中,尤其是芸香科和伞型科,在豆科、兰科、木樨科和菊科植物中也广泛存在,香豆素及其衍生物广泛应用于染料、医药、香料和农药中。
武汉理工大学有机化学2005-2006上A试题和答案
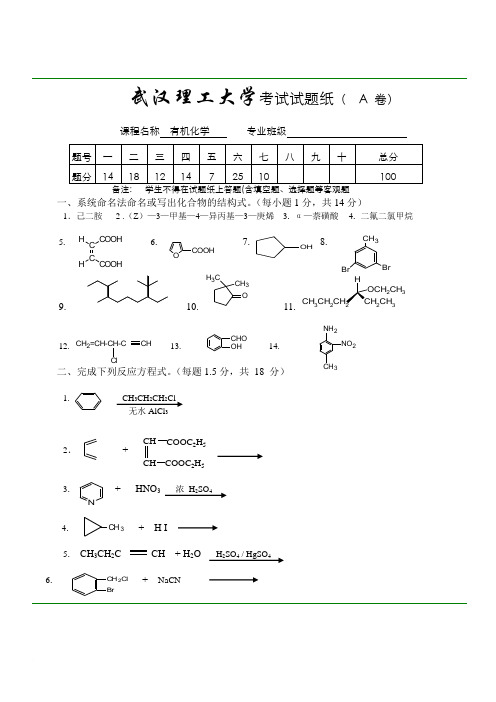
OH武汉理工大学考试试题纸( A 卷)课程名称有机化学专业班级一、系统命名法命名或写出化合物的结构式。
(每小题1分,共14分)1.己二胺 2 .(Z)—3—甲基—4—异丙基—3—庚烯3. α—萘磺酸4. 二氟二氯甲烷5. 6. 7. 8.9. 10. 11. CH3CH22CH32CH312. 13. 14.二、完成下列反应方程式。
(每题1.5分,共18 分)1. CH3CH2CH2Cl无水AlCl32.+3. + HNO3浓H2SO44. + H I5. CH3CH2C CH + H2O H2SO4 / HgSO46. + NaCNCH3BrBrCHCH2=CH-CH-CCCH COOHH COOHOH3CCH3CHOOHNH23NO2CH3CH COOC2H5COOC2H5CHCH2ClBrOCOOHN7. C 9H 12 ( ) KMnO 4 ,H + △8. C 7H 14O ( ) H +/△9. + C 2H 5MgBr (1)ether (2)H + , H 2O , △10. CH 3I + CH 3CH 2CH 2CH 2ONa 丙酮11. CH 3CH 2CH 2CH 2COOH SOCl 212. ( ) △三、用化学方法鉴别下列化合物。
(每小题4分,共12分)1. C 6H 5CH 2CH 3 ; C 6H 5CH=CH 2; C 6H 5C CH ;2. ; ; ;3. 甲酸; 乙酸 ; 丙二酸;乙二酸四、简答题。
(共14分,每小题2分)1. 排列下列化合物的碱性大小顺序: 。
A : CH 3CONH 2 B :CH 3NH 2 C :NH 32. 排列下列化合物的酸性大小顺序: 。
A : ;B : ;C :3. 排列下列化合物按S N 1机理反应时的速度顺序: 。
A: B : C:CH 3OCOOHCOOHCH 2Br OHCH 3COCH 3CH 2Br CH 2Br3CH 2Br 2OH 2OH 3OHO4. 下列化合物中不具有芳香性的是: 。
武汉理工大学有机化学参考答案

环境科学专业本科培养计划Undergraduate Program for Specialty in EnvironmentalScience一、业务培养目标ⅠEducational Objectives本专业培养具备环境科学的基本理论、基本知识和基本技能,具有较强的适应能力、实干精神和创新意识,能在科研机构、高等学校、企事业单位及行政部门等从事环境方面的科研、教学、管理等工作的高级专门人才。
The program in environmental science is designed to provide students an integrated education, which helps students to develop the basic knowledge and capabilities, and prepares them to be advanced environmental science personnel with high adaptability and creative consciousness. Students will be well-prepared for careers in academic institutions, educational institutions, and private and government agencies.二、业务培养要求ⅡEducational Requirement本专业学生主要学习环境科学方面的基本理论、基础知识和基本技能,受到基础研究和应用基础研究方面的科学思维和科学实验的训练,培养较好的科学素养,有较强的自学能力和分析解决环境问题的能力,具备一定的教学、研究、开发和管理能力。
毕业生应获得以下几方面的知识和能力:1. 掌握数学、物理、化学和微生物等方面的基本理论和基本知识;2. 掌握环境科学与管理的基本理论、基本知识和基本技能;3. 熟悉国家环境保护、自然资源合理利用、可持续发展、知识产权等有关政策和法规;4. 具有一定的实验设计能力,以及分析整理实验结果的能力;5. 具有撰写科技报告的能力;6. 掌握资料查询、文献检索及运用现代信息技术获取相关信息的基本方法。
α酮戊二酸的制备

•(3)实验步骤
•无水乙醇与金属钠在 加热回流条件下制备 乙醇钠,用甲苯除去
多余乙醇
•加乙醚溶解乙醇钠后 ,再依次加入草酸二乙 酯与丁二酸二乙酯,放
置12h
•草酰琥珀酸三乙酯 用浓盐酸酸化后,加 水回流4h,减压蒸馏
•用乙醚萃取,合并水 层后加浓盐酸酸化, 收集油层合并,用无
水硫酸钠干燥
•蒸馏至无馏分为止,趁热 将剩余物倒入蒸发皿,冷 却结晶得到产品α-酮戊二
2011.
•二、合成方法
•
目前,α-酮戊二酸的主要合成方法有微生物发
酵法[5-6]和化学合成法。合成α-酮酸的传统方法有以
下几种[7]:
➢ 酰基氰化物水解法:
➢ 草酸类乙酯水解法:
➢ 以α-叠氮苯乙酸类为起始原料的反应: ➢ N-溴-α-氰基胺类化合物为起原料的反应:
• 本次实验通过Claisen酯缩合方法合成草酰丁二 酸三乙酯。首先,丁二酸二乙酯在乙醇钠的作用下失 去α氢,生成烯醇负离子,烯醇负离子对草酸二乙酯 发生亲核加成,在消除乙氧负离子生成草酰丁二酸三 乙酯钠盐,然后再盐酸酸化作用下,得到草酰丁二酸 三乙酯。以草酰丁二酸三乙酯为原料,在酸性条件下 回流,按负离子机理,草酰丁二酸三乙酯发生脱羧反 应生成α-酮戊二酸。
•三、实验部分
•(1)实验药品 • 金属钠2.3g(0.1mol);草酸二乙酯 14.6g(13.7ml);丁二酸二乙酯17.4g(16.9ml);无水乙醇 (35.6ml);无水乙醚(65ml);无水甲苯;乙醚;浓盐酸 ;无水硫酸钠;
•(2)仪器及设备 • 设备:红外光谱仪 • 装置图:
X-4显微熔点仪
•目录
•DIRECTORY
•五、影响因素讨论…...................13
武汉理工大学有机化学 Chap.3-2

2
• Elastic deformation: as soon as the stress is removed, the structure returns to its former shape. A piece of metal will become thinner if it is stretched lengthwise.
• Tensile test reveals:
➢ the yield point, ultimate strength and strain ➢ ductility: the amount (percent) of elongation and
reduction of area at the point of failure is an indication of ductility
• Poisson’s ratio: the ratio of movement at right angles to the applied force is called ~.
3
• Plastic deformation: can take place only at a stress or load higher than the elastic limit.
9
Stress-strain diagram for a ductile steel
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
蒸馏:加热液体混合物至沸腾,收集产生 的蒸气,再冷凝为液体。此过程即为蒸馏。
目的:(1)对液体混合物进行分离提纯。液 体混合物中各组分要求在沸点附近不分解 且沸点差大于30℃;
有机化学实验的基本要求
(5)遵从指导:严格按照操作步骤进行实验, 如需改动,须由老师同意。一般情况下,不允 许重做实验,确需重做者,须经老师同意并按 有关规定办理手续;
(6)注意保持实验室的安静和整洁,不许在 实验室大声喧哗、互相窜位。废弃物应丢在指 定地点;实验完后,拆洗仪器,清理台面,值 日生应做好实验室的整理和清洁工作;
装置图:
分馏
刺形分馏柱
分馏原理:
TB
馏出液
蒸气
中A的
TC1
浓度不 温
断上升 度 最后接 近纯A
液体
TC2
TC3
TA
组成 100 % C3
C2
0%
冷凝液 浓度
C1 0% A 100% B
蒸馏液 浓度
重结晶
重结晶是分离和提纯固态有机物的 常用方法,是有机化学实验重要的基本 操作。
重结晶法适合在不同温度下溶解度 有显著不同,并和杂质的溶解度有显著 不同的固体有机物的提纯。
(玻璃仪器名称和规格、药品及用量) 五、 仪器装置图 六、 实验步骤(流程图)
1~6项属预习报告内容(进实验室前完成)
七、实验记录(包括操作步骤、试剂用量、反应温
度、反应时间、现象、产品质量、性状等)
实验操作(步骤)
现象
说明
实验过程中完成
八、产率:
产率%
实际产量 理论产量
100
九、问题讨论
十、思考题
指导教师签字
有机化学实验报告书写格式
第一部分:实验预习报告 1、实验目的、意义 2、实验原理和方法
(用反应式表示)
此处插入物理常数 包括反应物、产物、副产物
3、主要仪器设备及耗材 (仪器、药品用量)
4、实验方案与技术路线 (简要实验步骤) 此处插入装置图
有机化学实验报告
第二部分:实验记录
实验操作步骤
(2)对纯液体蒸馏测定沸点。
装置:
原理:
蒸馏
装置图: 温度计
蒸馏头 冷凝管
接液管
圆底 烧瓶
接收瓶
蒸馏原理: 组成-沸点图
蒸气
温
度
液体
冷凝液 浓度
组成
100 % C2
C1
0%
对于A:C2 > C1
蒸馏液 TB 中A的
浓度不
断下降
沸点不
TC1 断上升 最后接 近纯B
TA 的沸点
0% A 100% B
原理:
重结晶
溶解
热过滤
溶质 不溶性杂质
加热
冷却 结晶
柱色谱
原理:
有机化学实验 基本知识
有机化学实验的基本要求
(1)充分准备:按要求预习、完成预习报告;
❖预习内容:实验讲义第一章、第二章内容。 ❖预习报告:完成实验报告中1~6项内容, 其中实验步骤(流程)中的单元操作(如蒸 馏、重结晶、洗涤和萃取、回流、搅拌等) 预习讲义第二章内容。未作预习报告者,不 得做实验!
量和质量。
用、沸石的使用等
实验报告(30%):规范、正确、整洁; 问题的解答及讨论。
实验项目:(1)环己烯的制备(2)正溴 丁烷的制备(3)正丁醚的制备(4)乙 酰苯胺的制备(5)······
有机化学实验 基本操作
蒸 馏(见P51)
蒸馏是分离和提纯液态有机物的常用 方法,是有机化学实验重要的基本操作。
(3)注意安全:遵守实验室安全规则,不得 穿拖鞋背心进入实验室做实验,食品、饮料不 准带入实验室,不准在实验室吃东西;
(4)严谨求实:要如实、当时做好实验记录, 无实验记录者,老师不予以签字;
❖实验记录:实验过程中的操作步骤、试剂 用量、反应温度、时间、现象、质量、产品性 状等的记录。是科学实验中的原始数据。
蒸馏液 浓度
分馏
分馏也是分离和提纯液态有机物的常用方 法,是有机化学实验重要的基本操作。
分馏实际上就是多次蒸馏。其原理、装置 及操作与蒸馏类似,但前者分离效率高。利用 蒸馏只能将沸点差别较大(相差30℃以上)的液体 混合物分开;分馏可分离沸点比较接近(相差小 于30℃)的液体混合物,目前最精密的分馏设备 可分离沸点差仅1~2℃的混合物。
现象
说明
1、
(实验过程中完成)
2、
第三部分:结果与讨论
实验结果:产率%
实际产量 理论产量
100
问题讨论
思考题
实验成绩的考核
预习报告(20%):内容预的习完:整第二性章。蒸馏、
实 范验 性操、作熟(练程50度%);:实实验验记态录分(用度的馏分);完、 液 、洗漏干操整涤斗燥作性与的剂的;萃使的取使规产
有机化学实验的基本要求
(7)爱护公物和仪器、设备,损坏仪器、设 备按有关规章赔偿。 (8)仪器的领取和归还:领取时自己对照清 单清点仪器,归还时须经老师清点。
事故的预防和处理措施 火灾 割伤
爆炸 化学品灼伤
烫伤 中毒
参阅讲义P2。做到心中有数, 遇事不慌。
有机化学 实验报告要求
有机化学实验报告(见P104)
实验者
班级
实验日期
实验名称
一、 目的要求 (1)原理和方法
(2)相关操作技术
二、 实验原理
用反应式表示(包括副反应)
三、物理常数 查阅化学手册
名称
分子式
相对分 子质量
性状
相对 密度
d
20 4
熔沸 点 点 折光
溶解度
(℃ (℃ 率
)
)
nD20
水乙 醇ቤተ መጻሕፍቲ ባይዱ
乙 醚
包括反应物、产物、副产物(限有机物)
四、主要仪器及耗材
有机化学实验的基本要求
(2)按时到课:学生不得无故不上实验课, 无故缺课者,不得补做实验,该次实验成绩 为0分;因病因事请假,所缺的实验课按有关 规定补做;每次实验学生应提前5分钟到达 实验室,进行实验前的准备工作;实验完毕 后,应将产品及实验记录交老师检查,经老 师签字后,方可离开实验室;
有机化学实验的基本要求
