第十一章药品包装技术.pptx
8-第十一章固体制剂-4

26
解决的办法:
选用弹性小、塑性大的辅料
选用适宜的制粒方法 选用适宜压片机和操作参数等整体上提高
物料的压缩成形性。。。如,调节压力使 之适度
适当的增加粘合剂
Copyright © 2003 Fair Isaac Corporation. All rights reserved.
27
但过多易粘冲,使片剂的崩解、药物的
溶出受影响。
常用的润滑剂为疏水性物质(如硬脂酸
镁),可减弱颗粒间结合力。4 Nhomakorabea水分 适量水分有利于颗粒在压缩时相互靠近, 易于成形,但过多易粘冲。 含水分可使颗粒表面的可溶性成分溶解, 当药片失水时发生重结晶而在相邻颗粒
间架起“固体桥”,从而使片剂的硬度
增大。
通常以脆碎度<0.8%为合格。
3.弹性复原率(elastic recovery,ER)
弹性复原率是将片剂从模中推出后弹性 膨胀引起的体积增加值和片剂在最大压 力下的体积之比。 ER =(V- V0)/V0 = (H-H0)/H0
式中,V、H分别表示膨胀后片剂的体积和高 度; V0、 H0分别表示最大压力下(膨胀前)片 剂的体积和高度。
③各种调节器—压力
调节器、片重调节
器、推片调节器。
单冲压片机
压力调节器连在上冲杆上,用以调节上冲下降的 深度,下降越深,上、下冲间距越近,压力越大, 反之则小。 片重调节器连在下冲杆上,用以调节下冲下降的 深度,下降越深,从而调节模孔容积而控制片重。 推片调节器连在下冲,用以调节下冲推片时抬起 的高度,使恰好与模圈的上缘相平,由饲料器推 开。
3、粘冲
片剂的表面被冲头粘去一薄层或一小部分,造成片
医药市场营销实务 第十一章 药品终端市场营销

(1)医院集中了绝大多数的处方药品种,占处方药销售市场的50%左右。 (2)医院的西药用量较大而且是新产品上市的主要目标市场。 (3)中国的医院药品销售比重大,是大多数药品企业市场竞争的主要战场。 (4)跨国制药企业产品的主流治疗领域占绝对优势。 (5)市场细分程度高,集中度也高,基本由几家大型药品生产企业垄断。 (6)医院医生对药品需求期望值高于其他药店和诊所等其他单位。 (7)医院是新特药药品信息的集中地,也是药品相关信息的集散地。
2. 门店内客户的管理
店经理(店长)、药师、柜组、营业员、收银员、质量管 理员
四、药店终端的促销
MARKETING OF DRUGSTORE TERMINAL
指示牌促销、样品促销、礼品促销、折 价促销、咨询
店内POP
五、店员的教育培训
MARKETING OF DRUGSTORE TERMINAL
(1)基本素质:主要表现为医药职业道德不论在哪一个行业都是十分重要的;(2) 业务素质:医药代表应具备的业务素质是指掌握相关的业务知识,具备相应的实践与 操作能力。(3)身体素质:医药代表工作的性质决定了营销工作的辛苦和不稳定性, 如果没有良好的健康状况作为保障,完成工作是很困难的。如果不能保持良好的健康 和精神状况,很难让客户产生对产品的信任,也很难保证与客户的正常交往,更不可 能让客户产生良好的印象。
药店的店员教育培训是OTC代表的又一核心任务,培训的对象、内容和形式都关系到本企业药品在药店终端的 销售。药店店员的教育培训是指将药品的相关信息传递给店员,使店员熟悉药品的知识,以期在柜台销售中增加 对该药品推荐率的一种药店促销手段。
(一)
培训内容:1.公司介绍:重点在于公司的资历,质量、荣誉要说明。2.相关
《药物制剂辅料与包装材料》课标(wxy修改实验)1.28

《药物制剂辅料与包装材料》课程标准一、课程性质《药物制剂辅料与包装材料》是高职高专院校药物制剂技术专业一门专业基础课。
本课程主要内容包括药物制剂常用的辅料和包装材料等,主要讲授药用辅料的基本理论和药剂学中常用辅料的结构、物化性质、性能、用途,各种药品包装材料及包装技术等方面的内容。
本课程任务是:通过学习,使学生逐步掌握辅料的类型、基本性质、在药物制剂中的作用、各种辅料的选用原则等;掌握药物包装材料的类型、性质及对药品质量的影响及各种包装材料的选用原则能力奠定坚实基础。
二、课程目标(一)知识目标1、掌握药用辅料对药品的质量稳定性、安全性、有效性的影响;掌握常用的药物辅料的类型和具体品种及选用原则;掌握药用辅料在药剂学中的地位和作用;掌握在药物制剂中包装材料对药品质量的影响;2、熟悉我国及其他各国对药用辅料的有关法律法规;熟悉我国常用的包装材料及选用原则;3、了解我国及国外药用辅料的发展趋势;了解国外药用辅料及包装材料的发展情况。
(二)技能目标1、熟练掌握各种药用辅料在制剂中的选用方法及选用原则。
2、通过包装材料性能的学习,熟练掌握各种药品包装材料的选用方式及选用原则。
(三)职业素质和态度目标1、树立药品质量第一的观念和药品安全意识,注重理论联系实际,实事求是的工作作风和科学严谨的工作态度;2、具有良好的职业道德和行为规范。
三、学时分配及内容标准(一)学时分配本课分上下两篇:上篇介绍各类药用辅料,下篇介绍药品包装材料,共计12章。
在课时分配上,理论课时34,实践课时30,合计64课时。
(二)内容标准第一章绪论第二章表面活性剂第三章高分子材料第五章无菌制剂辅料第六章固体制剂辅料第七章膏剂基质第八章药物新剂型常用辅料第九章药品包装概述第十章药品包装材料第十一章药品包装技术第十二章辅助包装技术四、实施建议(一)教学建议1.本课应力求体现“以就业为导向,以能力为本位、以发展技能为核心”的职业教育理念,理论知识以“必需、够用”为原则适当删减和引进新的内容,实践训练着重培养药物制剂技术专业学生实际操作能力。
GMP附录1无菌药品
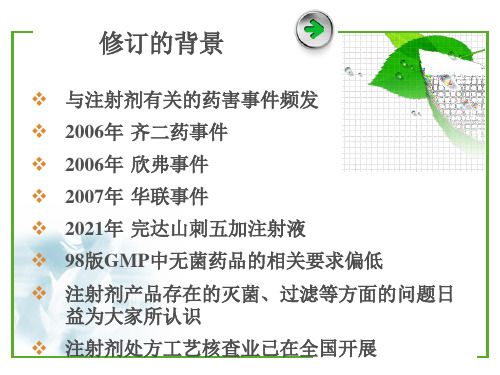
最终灭菌产品 生产操作例如
C级背景下 的局部A级
C级
D级
高污染风险(1)的产品灌装(或灌封)
1.产品灌装(或灌封); 2.高污染风险(2)产品的配制和过滤; 3.眼用制剂、无菌软膏剂、无菌混悬剂等的配
制、灌装(或灌封); 4.直接接触药品的包装材料和器具最终清洗后
直接接触的敞口包装容器的区域及无菌装配或连接操作的 区域,应当用单向流操作台〔罩〕维持该区的环境状态。 单向流系统在其工作区域必须均匀送风,风速为〔指导值 〕。应当有数据证明单向流的状态并经过验证。 在密闭的隔离操作器或手套箱内,可使用较低的风速。 B级:指无菌配制和灌装等高风险操作A级洁净区所处的背 景区域 C级和D级:指无菌药品生产过程中重要程度较低操作步骤 的洁净区。
〔六〕在A级洁净区和B级洁净区,连续或有规律地出 现少量≥5.0 µm的悬浮粒子时,应当进行调查。
规定了动态监测的本卷须知 规定了 出现异常情况时的处理
第三章 洁净度级别及监测
〔七〕生产操作全部结束、操作人员撤出生产现场并经 15~20分钟〔指导值〕自净后,洁净区的悬浮粒子应 当到达表中的“静态〞标准。
规定了A级区测试的最小采样量 规定了测试方法ISO14644-1 国标GB/T16292-2021中的测试方法同ISO14644-1
第三章 洁净度级别及监测
第九条注: 〔2〕在确认级别时,应当使用采样管较短的便携式尘埃 粒子计数器,防止≥μm悬浮粒子在远程采样系统的长采 样管中沉降。在单向流系统中,应当采用等动力学的取 样头 〔3〕动态测试可在常规操作、培养基模拟灌装过程中进 行,证明到达动态的洁净度级别,但培养基模拟灌装试 验要求在“最差状况〞下进行动态测试。
GMP实施技术 委托生产与委托检验

三、考察内容
❖ 3.额外考察
❖ (6)委托方对受托方试制生产的三批委托生产药品的质量检验 结果进行分析研究,并与委托方生产的药品质量进行对比分 析,质量标准中有溶出度或释放度检查项目的口服固体制剂 ,必须对其溶出度、释放度数据进行分析研究,尽可能使受 托方与委托方生产的产品质量保持一致,如不一致,应调查 原因,改进工作,对相关人员进行培训和指导。
三、考察内容
❖ 2.受托方的质量体系
❖ (7)质量保证体系; ❖ (8) 管理水平; ❖ (9)受托企业产品质量稳定,近三年内无产品不合格质量公
告记录和质量事故; ❖ (10) 企业信誉良好,近三年无生产销售假劣药行为处罚记
录; ❖ (11) 合作态度诚恳,积极配合改进自身缺陷,并承诺尊重
委托方知识产权包括商标权,为生产受托产品完善生产厂 房、设施、设备,并对生产工艺改进,加强管理。
❖ 生产现场检查的重点是考核受托方的生产条件、技术水平和质 量管理情况以及受托生产的药品处方、生产工艺、质量标准与 委托方的一致性。
四、委托生产首次申请、延续申请的审批流程
❖ 4.连续三批委托生产产品的检验
❖ 委托方应对受托方生产的连续三批药品进行抽样并送委托方所 在地省级药品检验机构检验,提交检验报告书原件,如在不同 省份委托生产的,则送受托方所在地省级药品检验机构检验。
三、委托生产管理的规定
❖ 麻醉药品、精神药品、药品类易制毒化学品及其复方制剂,医 疗用毒性药品,生物制品,多组分生化药品,中药注射剂和原 料药不得委托生产。
四、委托生产首次申请、延续申请的审批流程
❖ 1.提出申请
❖ 首次委托生产的,委托方应向企业所在地省级药监部门提出申 请,委托生产如在不同省份的,还须向受托方所在地省级药监 部提出申请,并提交受托方所在地省级药监部门审查意见,但 不包括药品上市许可持有人委托生产。申请报告应详述委托生 产原因,简要概述委托方、受托方、拟委托生产药品的相关情 况,委托生产时限,对受托方的考核意见,对受托方生产管理 和质量管理进行监督的方式等。
药品生产管理ppt课件

企业数量:6731家
50家西药领先企业产值只占行业总产值的39%
我国制药企业现状
医药企业缺乏自主知识产权的药品
特别是化学药,建国以来生产的3000多种西药 99%是仿制药,近几年生产的837种新药中,97.4 %是仿制的,而且其中60%还处于专利保护期
我国新药注册的现状
我国药品种类数量繁多,仅2006年我国注册的新药就达 6500多种,但是申报的新药多是仿制和对已有药品进行 剂型及给药途径的改变,而真正自主创新的药品数量很少, 去年只有19种,其中16种是中药,3种是生物制药,而注 册的化学药中没有一种是自主创新的。我国药品生产存在 着极其严重的低水平重复建设,随意申报现象较为严重。
(二)质量管理发展的4个阶段
质量检验阶段 统计质量管理阶段 全面质量管理阶段 ISO9000族国际标准
(三)质量管理原则 1.系统管理原则 2.顾客至上原则 3.预防为主原则 4.注重质量成本原则 5.以人为本的原则 6.持续改进原则
第三节
《药品生产质量管理规范》 及其认证管理
(一)我国的GMP内容介绍
结构 共十四章,87条:
第一章 总则(1-2);第二章 机构与人员(3-7): 第三章 厂房与设施(8-30); 第四章 设备(31-37);第五章 物料(38-47); 第六章 卫生(48-56);第七章 验证(57-60); 第八章 文件(61-65);第九章 生产管理(66-73); 第十章 质量管理(74-76); 第十一章 产品销售与收回(77-79); 第十二章 投诉与不良反应报告(80-82); 第十三章 自检(83-84); 第十四章 附则(85-MP 全称“GOOD MANUFACTURING PRACTICE”, 是在药品生产全过程中,保证生产出优质 药品的管理制度,是TQC的思想、理论 在药品生产过程中质量管理的具体运用和 规范化的产物。
GMP-第11章 委托生产与委托检验

第一节 委托生产与委托检验的原则
GMP对委托生产与委托检验的合同是如何规定的 ?
– 药品GMP(2010年修订)第二百七十八条规定: “为确保委托生产产品的质量和委托检验的准 确性和可靠性,委托方和受托方必须签订书面 合同,明确规定各方责任、委托生产或委托检 验的内容及相关的技术事项。”
4
– 委托生产药品的双方应当签署合同,内容应当包括 双方的权利与义务,并具体规定双方在药品委托生 产技术、质量控制等方面的权利与义务,且应当符 合国家有关药品管理的法律法规。 – 委托生产药品的质量标准应当执行国家药品质量标 准,其处方、生产工艺、包装规格、标签、使用说 明书、批准文号等应当与原批准的内容相同。在委 托生产的药品包装、标签和说明书上,应当标明委 托方企业名称和注册地址、受托方企业名称和生产 地址。 – 委托方负责委托生产药品的质量和销售。委托方应 当对受托方的生产条件、生产技术水平和质量管理 状况进行详细考察,应当向受托方提供委托生产药 品的技术和质量文件,对生产全过程进行指导和监 督。
8
第三节 受托方
GMP对受托方的条件有什么要求? – 药品GMP(2010年修订)第二百八十四条规定:“受 托方必须具备足够的厂房、设备、知识和经验以及 人员,满足委托方所委托的生产或检验工作的要求 。” GMP规定受托方的责任是什么? – 药品GMP(2010年修订)第二百八十五条规定:“受 托方应当确保所收到委托方提供的物料、中间产品 和待包装产品适用于预定用途。” – 第二百八十六条规定:“受托方不得从事对委托生 产或检验的产品质量有不利影响的活动。”
GMP规定委托方的责任是什么? – 药品GMP(2010年修订)第二百八十一条规定:“委 托方应当向受托方提供所有必要的资料,以使受托 方能够按照药品注册和其他法定要求正确实施所委 托的操作。 委托方应当使受托方充分了解与产品或操作相关 的各种问题,包括产品或操作对受托方的环境、厂 房、设备、人员及其他物料或产品可能造成的危害 。” – 第二百八十二条规定:“委托方应当对受托生产或 检验的全过程进行监督。” – 第二百八十三条规定:“委托方应当确保物料和产 品符合相应的质量标准。”
药品、食品、化妆品、器械专业知识培训PPT课件

十一、药品储存
常温储存:温度10-30℃;湿度35%-75% 常温、密封、密闭、30℃以下、0-30℃有这些字眼的,都是常温库储存
阴凉库:温度20℃以下;湿度35%-75% 阴凉、阴暗、20℃以下、0-20℃、25℃以下有这些字眼的,都是阴凉库储存
卫妆特字+(4位年份)+第××××号(例:卫妆特字(2003)第0543号) 国妆特字G+4位年度+4位编码(例:国妆特字G20121089) 国产
五、医疗器械批准文号的识别(效期5年)
一类医疗器械批文: 一类医疗器械备案编排格式为:(备案部门所在地简称)+械备+4位年份+4位流水号
医疗器械
一类医疗器械
二类医疗器械
三类医疗器械
进口第一类医疗器械为“国”字; 境内第一类医疗器械为备案部门所 在地省、自治区、直辖市简称加所 在地设区的市级行政区域的简称 (无相应设区的市级行政区域时,仅
为省、自治区、直辖市的简称)
举例说明:赣吉械备20170037 陕延械备20160010号
不需要备案或 许可即可经营
备案
举例说明:渝食药监械(准)字2013第1310130号 国食药监械(准)字2013第3241243号 国食药监械(进)字2012第3403518号 国食药监械(许)字2008第3460019号
七、标志识别
八、特殊药品
含麻黄碱类特殊复方制剂:含有麻黄碱、伪麻黄碱、盐酸麻黄碱等成分的药品 化学药品或者中成药
十五、药品说明书和标签管理规定(国家食品药品监督管理局令第24号)
2006年03月15日发布
药品说明书应当列出全部活性成份或者组方 中的全部中药药味。注射剂和非处方药还应 当列出所用的全部辅料名称。 药品说明书应当充分包含药品不良反应信息, 详细注明药品不良反应。药品生产企业未根据 药品上市后的安全性、有效性情况及时修改说 明书或者未将药品不良反应在说明书中充分说 明的,由此引起的不良后果由该生产企业承担。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十一章 药品包装技术
第一节 无菌包装技术 第二节 填充技术 第三节 防潮包装 第四节 药品防霉包装技术 第五节 热成型包装技术 第六节 防氧包装 第七节喷雾包装技术
第一节 无菌包装技术
一、概述 一)无菌包装的定义
在被包装物、包装容器或材料、包装辅助 器材无菌的情况下,在无菌的环境中进行充填 和封合的一种技术。
二)紫外线灭菌
紫外灭菌的机制主要是由于紫外线照射后微生物体内的核酸 产生化学变化,引起新陈代谢障碍,失去增殖能力,同时紫外线 在穿过空气时可以产生微量臭氧具有协同灭菌作用。
波长250-260nm的紫外线作用最强。 特点:
不残留药剂、安全性高、使用方法简单,设备昂贵、寿命短、 成本高,灭菌不彻底。
**用于不耐热物体表面和空气消毒。对人体皮肤、眼睛有损 伤作用,使用时应注意防护。
二)药品无菌包装分类
1.按药品生产工艺分类 最后灭菌:被包装药品填充到容器中后,
进行严密封口,再进行灭菌处理。 无菌加工:包装设备预先灭菌,药品在填
充之前灭菌,包装材料(或容器)灭菌和包装 环境灭菌,经过灭菌后的药品在无菌的环境下 填充到无菌的包装容器中,并进行严格密封。
二)药品无菌包装分类
2.按灭菌方法分类 物理灭菌法:主要是加热灭菌法和辐射灭菌法。 化学灭菌法:通常不能直接加入到药品中,只准
用途:一次性塑料制品消毒;食品消毒,不破坏 营养成分。
三、无菌包装系统
一系列的连续灭菌过程,从药品的输入、 包装容器或材料的输入(或直接成型),药品 的填充及最后的封合,分切等都必须在无菌的 环境中进行。
组成:容器输入部位,容器灭菌部位,无 菌填充部位,无菌封口部位,包装完成件的输 出。
一)无菌灌装系统
二)塑料袋无菌包装系统
第二节 填充技术
一、概述 填充是包装过程中间工序,将产品(待
装物品)按要求的数量放入包装容器内。 前工序:容器成型或容器准备。成型、
清洗、干燥或排列等。 后工序:密封、封口、贴签、打印。
1.填充方法
填充药品 颗粒填充、粉末填充、块状填充、液体灌装等;
计量方法 容积填充、称重填充和计算填充。
包装容器 装瓶、装罐、装袋、装盒、装箱。
பைடு நூலகம்.充填精度
装入容器内物料的实际数量和要求数量的 误差范围。
药品的充填精度要求高一些。 对贵重物料和对计量要求严格的物料,充 填精度可达±0.1%;重袋包装,精度可大些。 精度和设备
3.充填工艺选用
要求: 计量准确; 不损坏内容物; 不损坏包装容器; 生物学要求; 清洁卫生。 **结合药品品种,规模,成本一起综合选用。
(2)巴氏消毒法:一种低温消毒法,因巴斯德首创而得名。有两 种具体方法,一是低温维持法:62℃维持30分钟;二是高温瞬 时法:75℃作用15-30秒。该法适用于食品的消毒。
(3)流通蒸气灭菌法:利用常压下的流通蒸汽进行灭菌。 (4)间歇蒸汽灭菌法 。 (5)高压蒸汽灭菌法:103.4千帕蒸汽压温度达121.3℃,维持15-
20分钟。
高压蒸汽灭菌器
四)红外线辐射灭菌
通过热辐射热灭菌 温度与停留时间 280℃ 20min 320℃ 2min
其他灭菌方法
高温、微波、电离辐射 电离辐射:包括X射线和γ射线
机制:这些射线可将原子或分子放出电子变成离 子。如水分子电离可产生H+和OH-,这些离子有很 强的还原与氧化作用,能直接杀伤细菌;也可与液体 中的氧分子结合形成H2O2,从而使细菌损伤或死亡。
三)机械加压计量灌装法
安瓿、口服液的灌装等。
三、稠性药品计量填充
黏度大、流动性差,主要是软膏、流浸膏 等。
一般采用机械压力式灌装,往复式定量 泵、旋转式齿轮定量泵。
四、固体物料填充
称量填充法: 是以质量来计算充填物料的数量;
容积填充法: 是以容积来计算充填物料的数量;
计数填充法: 是计数法,块状、颗粒固体物料的数量或包装单件
紫外线辐射灭菌装置
紫外线辐射灭菌装置
三)热压蒸汽灭菌
属于湿热灭菌 由于蒸汽潜热大,穿透力强,容易使蛋白
质变性或凝固,该法的灭菌效率比干热灭菌法 高,是药物制剂生产过程中最常用的灭菌方法。
蒸汽加热灭菌,115~138℃。 主要用于玻璃制品和耐湿热包装材料。
湿热灭菌的方法
(1)煮沸灭菌法:将水煮沸至100℃,保持5-10分钟可杀死细菌繁 殖体,保持1-3小时可杀死芽胞。在水中加入百分之一至百分之 二的碳酸氢钠时沸点可达105℃,能增强杀菌作用,还可去污防 锈。此法适用于食具、刀箭、载玻片及注射器等。
许用于水质及环境的杀菌。 氯气、次氯酸盐、碘制剂、季铵盐、两性表面活
性剂、氯己定及乙醇。
二、包装容器(或材料)的灭菌
包装容器的灭菌通常有药物(化学)灭菌和紫外 线灭菌。 一)药物灭菌
要求:灭菌力强,对设备无腐蚀,不会生成有害 物质,在残留少。
过氧化氢:25%~30%,60~65℃.浸渍或喷射, 然后进行热辐射,使过氧化氢蒸发、分解。
的数量来计量的方法。
一)称量充填法
此法适用于易吸潮、易结块、粒度不均匀、密度 较大的物料的填充。 1.净重填充法
将物料先用称称量,然后充填到包装容器中的方 法。
*1 最精确的称量充填法。 *2 可采用分级进料的方法提高精度。适用于称量精 度要求高、规章及可自由流动的固体物料。速度慢, 机器价格高。
动时间控制。
2)螺旋充填机 原理:螺旋送料轴 搅拌器,螺旋轴每
二、液体药剂的填充
液体制剂:黏度小、密度稳定。 药液定量方法:称重法和容积法。
一)常压计量灌装法
定液位灌装,液体靠重力自由流下,灌 入容器中,灌入容器中液体的体积的容积决定 于容器本身的容积。
适用于黏度低、非气泡性的液体物料。
二)负压计量灌装法
减少料液与空气接触。 1.差压真空灌装 2.重力真空灌装 3.真空压差灌装 适用于黏度低、非气泡性的液体物料。
一)称量充填法
2.毛重充填法 将物料装入容器后,连同容器进行称量
的方法。
二)容积充填法
机遇容积来计量充填物料的数量,机器结构简单, 充填速率可以提高。
填充精度依赖于物料密度的稳定性,一般比称量 充填要低1%~2%。 1.控制充填物料的流量或时间来保证充填容积。
1)记时震动充填机 精度最低,结构简单,价格便宜。填充数量由震
