2019年秋九年级化学上册 第2章 空气、物质的构成 2.2 构成物质的微粒(Ⅰ)—分子习题课件(新
《第二章 空气物质的构成22 构成物质的微粒分子》初中化学科粤版九年级上册PPT课件

B.分子之间有间隔,酒精分子与水分子互相作用挤占了分 子间的空隙 C.分子之间相互作用使酒精分子和水分子都变小 D.酒精分子和水分子相互结合生成其他物质的分子
26
火眼金睛
2.下列说法错误的是( B )
A.水变成水蒸气时,只是水分子间的间隔变大了, 而水分子本身没有变化
10
11
根据下列的图形给物质分类(混 合物、纯净物):
纯净物
纯净物
混合物
混合物
12
二、分子的基本性质
1.分子在不断地运动
13
2、分子间有间隔。
14
2、分子间有间隔。
15
2、分子间有间隔。
16
2、分子间有间隔。
17
2、分子间有间隔。
18
2、分子间有间隔。
19
2、分子间有间隔。
20
实验2-7 • 压缩相同体积的水和空气哪个更容易压缩?
B.空气里的氧分子与氧气的氧分子具有不同的化学 性质
C.氨气与氯化氢发生反应时,氨分子和氯化氢分子 都发生变化,结合生成了氯化铵分子
D.蔗糖放入水中很快就不见了,这是由于蔗糖分子 不断运动,脱离了糖块而扩散到水分子中间去的 缘故
27
火眼金睛
c 3.下列有关分子的叙述正确的是( )
A.一切物质都是由分子一种粒子构成的 B.分子是保持物质物理性质的最小粒子 C.同种分子的化学性质相同 D.在化学变化中分子本身没有发生改变
8
分子是构成物质的一种微粒。
• 在物理变化中,分 • 在化学变化中分子
子本身不发生变化, 本身发生改变,生
仍保持该物质的化 成化学性质跟原物
学性质。
初中化学九年级上册 2.2 构成物质的微粒--分子 课件

H2
CO2
H2O
氧分子 O2
氢气 干冰(固态二氧化碳) 水
氧气
分子是构成物质的一种微粒
氢分子 二氧化碳分子 水分子
H2
CO2
H2O
氧分子 O2
氢气 干冰(固态二氧化碳) 水
氧气
二、分子②分子之间存在间隔
观察活动一
观察活动二
气>液/固
水 50ml
三、变化中的微观世界
化学变化
冰
水 水蒸气
物理变化
分子不变, 分子间隔改变
浓盐酸 白烟 浓氨水
分子改变
H
+ H N H
Cl
H
+ 氨气 氯化氢
NH3
HCl
H Cl HN H
H
氯化铵
NH4Cl
水的三态变化 氨气+氯化氢→氯化铵
分子是构成物质的一种微粒,也是保持 物质化学性质的一种微粒。
三、变化中的微观世界
50ml 酒 精
100ml
混合后的溶液
二、分子的特性
③分子的体积和质量很小
一滴水有 多少个水 分子呢?
如果把1个水分子放大1千万倍,也不过 像黄豆那么大。一个水分子的质量约为3 × 10-26Kg,一滴水中大约有1.67 × 1021 个水分子,如果10亿人来数一滴水里的 水分子,每人每分钟数一百个,日夜不 停,要3万多年才能数完。
3、起点低怕什么,大不了加倍努力。人生就像一场马拉松比赛,拼的不是起点,而是坚持的耐力和成长的速度。只要努力不止,进步也会不止。 45、我们从自然手上收到的最大礼物就是生命。 14、给自己一份坚强,擦干眼泪;给自己一份自信,不卑不亢;给自己一份洒脱,悠然前行。轻轻品,静静藏。为了看阳光,我来到这世上;为了与阳光同行,我笑对忧伤。 15、懒惰不会让你一下子跌倒,但会在不知不觉中减少你的收获;勤奋也不会让你一夜成功,但会在不知不觉中积累你的成果。人生需要挑战,更需要坚持和勤奋! 7、每个人的心里,都藏着一个了不起的自己,只要你不颓废,不消极,一直悄悄酝酿着乐观,培养着豁达,坚持着善良,只要在路上,就没有到达不了的远方!
九年级化学上册空气、物质的构成 . 构成物质的微粒Ⅱ—原子和离子原子

归纳 [
(guīnà)
总结]
关于分子和原子的区别,特别要注意在没有前提条件下以下几种说
法都是错误(cuòwù)的:①分子大,原子小;②分子重,原子轻;③分子 能直接构成物质,而原子不能;④分子能保持物质的化学性质,而
原子不能。当物质由分子直接构成时,分子保持该物质的化学性质,
此时构成分子的原子不能保持物质的化学性质;当物质由原子直接
第六页,共二十六页。
2.3 构成(gòuchéng)物质的微粒(Ⅰ)——分子
3.结论
(1)原子(yuánzǐ)是构成物质的另一种微粒,原子(yuánzǐ)构分成子________, 原子也可直接构成某些物质。 (2)在化学变化中,分子本身_______发__生_变__化,而原子本身 ____没_有__根__本_变__化__,只是_____重_新__组_合_成新分子,构成新物质。原 子是_____化__学_变化中的最小微粒。 (3)分子与原子的本质区别是______在__化_学__变_化__(h_uà_xu_é _bi_àn_hu_à)_中_,__分子 __可_再__分_,__而_原__子_不__可_再__分___________。
2.有关原子的说法不正确的是( D)
A.原子可以构成分子
B.化学变化中原子重新组合
C.原子可以直接构成物质 D.原子是最小的微粒
第二十三页,共二十六页。
2.3 构成物质(wùzhì)的微粒(Ⅰ)——分子
知识点2 分子和原子(yuánzǐ)的区别与联系
3.关于分子、原子的叙述错误的是( ) C A.分子可以分成原子 B.分子和原子都可以构成(gòuchéng)物质 C.分子是化学变化中的最小微粒 D.有些物质的化学性质由原子保持
[课堂速记]
九年级化学上册第二章空气、物质的构成2.2构成物质的微粒(Ⅰ)——分子教案(新版)粤教版

5. 题目:设计一个实验来验证分子间存在引力和斥力。
课后作业
1. 题目:解释分子的概念,并给出两个例子说明分子在生活中的应用。
答案:分子是物质的最小粒子,具有保持物质化学性质的作用。例如,水分子(H2O)在生活中的应用包括:水的溶解性、湿润作用、水的电解生成氢气和氧气等。
2. 题目:描述分子间的作用力,并解释其对物质性质的影响。
答案:分子间的作用力包括引力力和斥力力,它们决定了物质的熔点、沸点、溶解度等性质。例如,氢键是一种特殊的分子间作用力,它影响物质的沸点和溶解度,如水分子间的氢键使得水的沸点较高。
1. 知识掌握:学生能够准确地理解分子的概念,掌握分子的基本性质和分子间的作用力。他们能够区分分子、原子和离子,并理解它们在物质构成中的作用。
2. 实验技能:学生通过参与实验观察和实践活动,能够熟练操作实验仪器,观察并分析实验现象。他们能够运用实验结果来验证分子理论,提高实验操作和观察能力。
3. 科学思维:学生能够运用分子的知识来解释和理解一些日常生活中的现象,如溶解、气体扩散等。他们能够运用模型和概念对物质构成进行解释和推理,发展逻辑思维和批判性思维。
鼓励学生分享学习分子的心得和体会,增进师生之间的情感交流。
(六)课堂小结(预计用时:2分钟)
简要回顾本节课学习的分子知识,强调重点和难点。
肯定学生的表现,鼓励他们继续努ቤተ መጻሕፍቲ ባይዱ。
布置作业:
根据本节课学习的分子内容,布置适量的课后作业,巩固学习效果。
九年级化学上册第二章空气物质的构成2.2构成物质的微粒Ⅰ_分子学案无答案粤教版

第二章空气、物质的构成案例一导学设计案例探究点一分子是构成物质的一种微粒[情景展示][问题探究] 分子是构成物质的唯一微粒吗?[思考交流] _______________________________________________________________________________________________________________________________________[归纳提升] 分子是构成物质的一种微粒,如氧气是由氧分子构成的,水是由水分子构成的,二氧化碳是由二氧化碳分子构成的。
但有的物质是由原子、离子构成的。
[课堂速记] _______________________________________________________________________________________________________________________________________探究点二分子的性质[情景展示 1 1][问题探究] 一个水分子有多大呢?[思考交流] _______________________________________________________________________________________________________________________________________[归纳提升] 在 4 ℃时,20 滴水的体积约为 1 mL,质量为 1 g,一滴水中约含有 1.67×10 21个水分子,说明分子很小,质量很小,体积很小。
[课堂速记] _______________________________________________________________________________________________________________________________________[情景展示 2 2] (视频情景详见光盘内容)[问题探究] 氨水能使无色酚酞溶液变红,用大烧杯罩住的烧杯 A 中的酚酞溶液与烧杯 B 中的浓氨水没有混合,为什么浓氨水也会变红呢?[思考交流] _______________________________________________________________________________________________________________________________________[归纳提升] 氨水能使无色酚酞溶液变红,烧杯 A 中的无色酚酞溶液变红,是由于烧杯B 中的浓氨水扩散出了肉眼看不见的微粒(氨分子)进入到烧杯 A 中,使烧杯A 中的无色酚酞溶液变红了,该实验说明分子总是在不断地运动着。
九年级化学上册第二章 空气、物质的构成中考必备知识点(1)
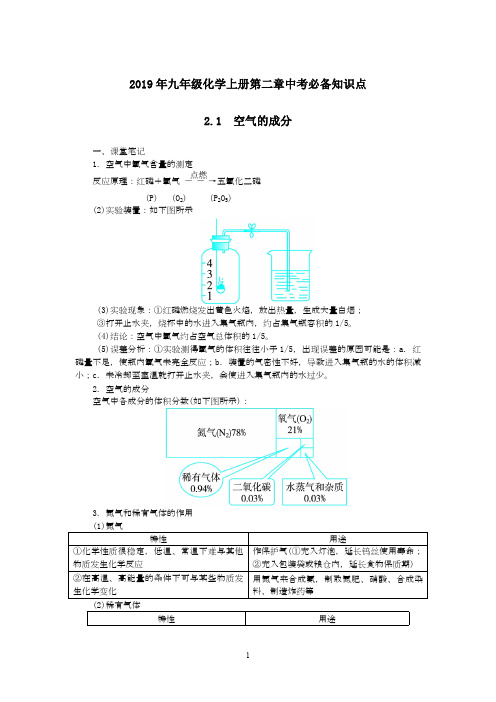
2019年九年级化学上册第二章中考必备知识点2.1 空气的成分一、课堂笔记1.空气中氧气含量的测定反应原理:红磷+氧气――→点燃五氧化二磷 (P) (O 2) (P 2O 5) (2)实验装置:如下图所示(3)实验现象:①红磷燃烧发出黄色火焰,放出热量,生成大量白烟; ③打开止水夹,烧杯中的水进入集气瓶内,约占集气瓶容积的1/5。
(4)结论:空气中氧气约占空气总体积的1/5。
(5)误差分析:①实验测得氧气的体积往往小于1/5,出现误差的原因可能是:a .红磷量不足,使瓶内氧气未完全反应;b .装置的气密性不好,导致进入集气瓶的水的体积减小;c .未冷却至室温就打开止水夹,会使进入集气瓶内的水过少。
2.空气的成分空气中各成分的体积分数(如下图所示):3.氮气和稀有气体的作用 (1)氮气特性用途①化学性质很稳定,低温、常温下难与其他物质发生化学反应作保护气(①充入灯泡,延长钨丝使用寿命;②充入包装袋或粮仓内,延长食物保质期) ②在高温、高能量的条件下可与某些物质发生化学变化用氮气来合成氨,制取氮肥、硝酸、合成染料、制造炸药等(2)稀有气体特性用途①很稳定,一般不跟其他物质反应。
作保护气。
①填充灯泡;②焊接保护气。
②充有稀有气体的放电管,通电时能发出不同颜色的光。
氦气→粉红色光氖气→红光氩气→紫蓝色光氙气→特强白光广泛用于电光源。
①用于制作霓虹灯;②用于激光技术。
③氦气密度很小,很稳定。
填充探空气球。
4.混合物和纯净物(1)概念①混合物:由两种或两种以上的物质组成。
②纯净物:只由一种物质组成5.只有一种元素组成的物质可能是纯净物也可能是混合物。
2.2 构成物质的微粒——分子一、分子的定义:1.(1)分子是构成物质的一种微粒。
例如:氮气是由氮分子构成,氢气是由氢原子构成,二氧化碳是由二氧化碳分子构成。
水是由水分子构成。
(2)由分子构成的物质化学性质由分子去保持。
例如:保持氮气化学性质的最小微粒是氮气分子,保持氢气的化学性质的微粒是氢气分子。
九年级化学上册 第二章 空气、物质的构成 2.2《构成物质的微粒(Ⅰ)—分子》课件

第十四页,共十六页。
我会总结(zǒngjié)
分子 1.分子的定义
分子是保持物质化学性质的一种微粒。
2.分子是构成物质的一种微粒。 n gé); (3)分子的质量和体积都很小。
第十五页,共十六页。
第十六页,共十六页。
第二页,共十六页。
第三页,共十六页。
实验2-3 把香水洒在手帕(shǒupà)上,都开毛巾,绕教室一周。
第四页,共十六页。
?
为什么我们的鼻孔(bíkǒng)与手帕相隔
一段距离,就能闻到香味呢?
香水是由酒精分子和香精分子混合在一起构成的。所以 ,当香水中的这些分子通过运动(yùndòng)扩散到空气中后,我 们就能闻到酒精和香精的气味。
第八页,共十六页。
一、分子(fēnzǐ)
1.分子(fēnzǐ)的定义 分子是保持(bǎochí)物质化学性质的一种微粒。
例如:氨气的化学性质由氨分子保持;
氯化氢的化学性质由氯化氢分子保持。
第九页,共十六页。
2.分子是构成物质的一种微粒(wēilì)。不同的分子,构成不同的物质。
第十页,共十六页。
3.分子(fēnzǐ)的特性
实验2-5 往无色氨水中滴入几滴无色酚酞溶液,震
荡。你观察(guānchá)到了什么现象?
实验现象:试管中溶液(róngyè)由无色变为红色 。
第十一页,共十六页。
实验2-6
A、B两个小烧杯,A杯装蒸馏水,并滴数滴酚酞,B杯装浓氨 大烧杯将A、B两小烧杯罩住一段时间。你观察到什么(shén me)现象?
第五页,共十六页。
实验(shíyàn)2-4
第六页,共十六页。
思考(sīkǎo):为什么就是由酒精分子和香精分子混合在一起构成的。所以,当香水中的这些分 子通过运动扩散到空气中后,我们就能闻到酒精和香精的气味。
初三化学笔记 第二章 空气、物质的构成

第二章 空气、物质的构成第一节 空气的成分1.空气中氧气含量的测定(1)原理:利用红磷燃烧消耗掉密闭容器内空气中的氧气,使密闭容器内压强减小,在大气压的作用下,进入密闭容器内水的体积即为氧气的体积。
①连接装置②检查装置气密性(2)实验步骤 ③在集气瓶内加入适量水,并做标记 ④用弹簧夹夹住胶管⑤点燃过量红磷,快速伸入集气瓶内,并立即塞紧瓶塞 ⑥燃烧结束并冷却到室温后,打开弹簧夹(3)现象:红磷燃烧产生黄色火焰,产生大量白烟(P 2O 5固体小颗粒)。
冷却后打开弹簧夹,水经导管流入集气瓶,流入水的体积约占集气瓶内空气体积的51。
(4)实验分析及结论:红磷燃烧消耗掉了集气瓶内的氧气,生成P 2O 5固体极易溶于水,体积忽略不计,冷却后,集气瓶内压强减小,大气压把水压进集气瓶,压进水的体积为集气瓶内消耗掉的氧气体积。
由此可证明空气中氧气的体积约占空气体积的51。
(5)误差分析:(6)选择此实验的燃烧物必须具备两个条件 a.该物质在空气中就能燃烧,且只跟O 2反应;b.燃烧后的生成物不能是气体。
(7)测量空气中氧气含量的方法总结 ① 测量进入容器中水的体积①装置漏气 ②红磷量不足③未冷却到室温就打开止水夹导致瓶内剩余气体体积偏大引起测量结果偏低①红磷燃烧伸入集气瓶后,没有立即塞紧瓶塞②止水夹没有夹紧引起测量结果偏高使集气瓶内气体逸出②利用刻度测量密闭容器内气体减少的体积③常见装置2.空气的组成成分注意:空气成分一般保持不变,含量相对稳定;不同地区有所不同;同一地区不同时间有所不同。
3.氮气和稀有气体氮气难溶于水,氮气化学性质稳定,可以作灯泡填充气、食品保护气等。
不同稀有气体通电时能发出不同颜色的光,可以制造霓虹灯;氦气密度比空气小,可用于填充探空气球或飞艇;稀有气体化学性质很稳定,可作焊接金属的保护气。
4.混合物与纯净物混合物纯净物混合分离注意:(1)由同种元素组成的物质不一定是纯净物,如O2、O3组成的物质。
