沸石的结构
沸石

沸石沸石(zeolite)是一种矿石,最早发现于1756年。
瑞典的矿物学家克朗斯提(Cronstedt)发现有一类天然硅铝酸盐矿石在灼烧时会产生沸腾现象,因此命名为“沸石”(瑞典文zeolit)。
在希腊文中意为“沸腾”(zeo)的“石头”(lithos)。
此后,人们对沸石的研究不断深入。
沸石因成分不同分为:方沸石Na[AlSi2O6]·H2O、钙沸石Ca[Al2Si3O10]·3H2O。
其含水量与外界温度及水蒸气的压力有关,加热时水分可慢慢逸出,但并不破坏其结晶构造。
一般呈浅色,玻璃光泽,硬度3-3.5,比重2.0-2.4。
沸石族矿物见于喷出岩,特别是玄武岩的孔隙中,也见于沉积岩、变质岩及热液矿床和某些近代温泉沉积中。
简介(历史)1932年,McBain提出了“分子筛”的概念。
表示可以在分子水平上筛分物质的多孔材料。
虽然沸石只是分子筛的一种,但是沸石在其中最具代表性,因此“沸石”和“分子筛”这两个词经常被混用。
人造沸石是:磺酸化聚苯乙烯;天然沸石:铝硅酸钠。
沸石族矿物常见于喷出岩,特别是玄武岩的孔隙中,也见于沉积岩、变质岩及热液矿床和某些近代温泉沉积中。
浙江省缙云县为我国境内沸石储量最高的地区。
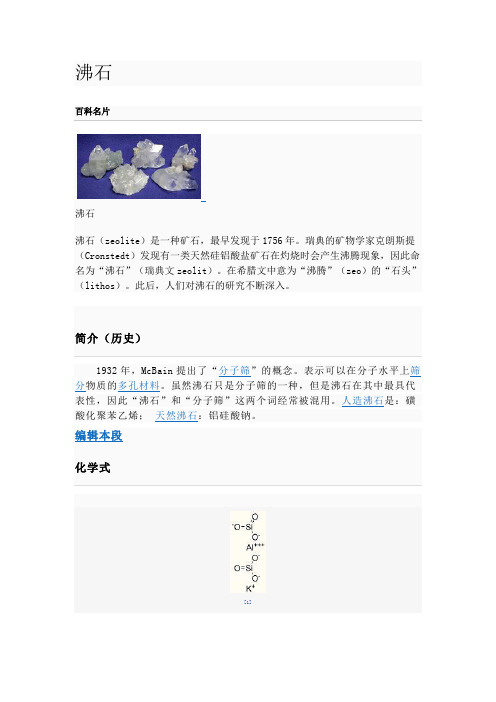
化学式[1]沸石的一般化学式为:AmBpO2p·nH2O,结构式为A(x/q) [ (AlO2)x (SiO2)y ] n(H2O) 其中:A为Ca、Na、K、Ba、Sr等阳离子,B为Al和Si,p为阳离子化合价,m为阳离子数,n为水分子数,x为Al原子数,y为Si原子数,(y/x)通常在1~5之间,(x+y)是单位晶胞中四面体的个数。
分子量:218.247238自然界已发现的沸石有30多种,较常见的有方沸石、菱沸石、钙沸石、片沸石、钠沸石、丝光沸石、辉沸石等,都以含钙、钠为主。
它们含水量的多少随外界温度和湿度的变化而变化。
晶体所属晶系随矿物种的不同而异,以单斜晶系和正交晶系(斜方晶系)的占多数。
沸石的合成

沸石的合成
沸石又称为硅酸钠,是一种无机化合物,化学式为Na2SiO3。
它是游离的单质,也可以用水溶液形式出现,沸石具有一定的覆盖性,能够有效地吸收和储存其他物质。
沸石分为正沸石和负沸石,其中正沸石主要由硅(Si)、氧(O)和钠(Na)元素组成,它们之间通过氧-硝键相互联系,形成一个三维网状结构;而负沸石则是由一维水分子链结构组成,能够很好地保存水分,表面拥有大量的水孔,其中含有的水气体能够有效地吸收空气中的微小颗粒物质。
沸石可以以不同的方式进行合成,其中常见的合成方法有沸石熔融法、燃烧法、湿法合成和气相法合成等。
沸石熔融法:在沸石熔融法中,首先将硅酸盐和氢氧化钠熔融,然后将添加剂添加,使之呈色,最后冷却即可获得沸石。
燃烧法:在燃烧法中,将硅酸盐和氢氧化钠混合,将其放入燃烧炉中,加热燃烧以合成沸石,这种方法可以很好地改变沸石的晶体结构。
湿法合成:这种方法使用硫酸铝、硝酸钠和硝酸钙来合成沸石,将上述物质混合,加入水并搅拌均匀,再放入热水中浸泡,最后冷却或加热,即可得到沸石。
气相法合成:这种方法是将硅气体通过纯净水凝固后形成沸石,由于该方法制备的沸石,具有很高的结构稳定性和抗氧化性,因而得到了广泛应用。
另外,还有一些新型的合成技术,如声波辐射合成沸石,在该方法中,可以利用高频声波辐射实现沸石的高效合成。
同时,也有磁场法合成沸石的方法,在该方法中,磁场可以改变沸石的晶体结构,改变其孔隙结构并增加其表面空间,具有很好的应用前景。
沸石族

沸石族沸石族Zeolite group 为含水的架状铝硅酸盐矿物,化学通式A m X p O 2p ·nH 2O ,其中A=Na 、Ca 、K 和少量的Ba 、Sr 、Mg 等;X=Si 、Al ,四面体位置上的Al ∶Si ≤1(约为1∶5到1∶1)。
沸石族矿物的化学组成可以在相当大范围内变化,使得许多沸石只能给出近似的化学式。
沸石的晶体结构与其它架状硅酸盐差别很大,沸石结构中具有宽阔的空洞和较宽的通道,并被Na 、Ca 、K 等离子和水分子——沸石水所占据。
在沸石结构中具有次级结构单位SBU(secondary building units),系由原始结构单位[SiO 4]、[AlO 4]四面体演化而来。
不考虑结构中四面体的形状,只将每个四面体中Si 或Al 的位置互相连接起来,便构成次级结构单位,形成各种简单的环或双环或更为复杂的结构单位。
这些次级结构单位在晶体结构中组成一定形状的多面体空间,构成所谓的笼。
相邻的笼可以通过次级结构彼此联结,形成各种不同形式的通道。
这种通道体系有3类:(1) 一维信道 各方向的信道彼此不相通。
如方沸石的信道,平行{111}。
(2) 二维信道 如丝光沸石中的信道体系,由平行c 轴、b 轴的两种信道互相联通而成。
(3) 三维通道 三个方向互相联通的通道。
分为等径的与不等径的两种。
如菱沸石中的信道为三维等径通道体系,钙十字沸石中为三维不等径通道体系。
各种沸石形态、物性相差不大,都为纤维状、束状、柱状、板状、也有一部分为粒状;多为无色或白色,因含杂质而染成其它颜色,或因阳离子交换后,有色素离子的进入而染色。
有的沸石有发旋旋光性。
与无水架状硅酸盐相比,具有相对密度轻(一般在1.9~2.3)、硬度低(一般为3.5~5.5)、折射率低及易分解的特点。
一般都有一组完全解理。
天然沸石最早是在玄武岩中发现的。
现已知主要产于未受变质的沉积岩层中,尤其是火山碎屑的沉积岩层中。
沸石的吸附原理

沸石的吸附原理
沸石是一种具有多孔结构的矿石,能够通过吸附分子物质来实现分离、净化和储存等功能。
其吸附原理主要基于以下两个方面:
1. 离子交换作用:沸石的晶格中含有大量的正离子和可交换的正离子空位。
当分子物质接触到沸石表面时,会发生离子交换反应,其中沸石的可交换正离子与分子物质中的正离子发生置换反应,将分子物质吸附在沸石表面。
2. 孔道吸附作用:沸石的晶格中还存在着一些微孔和介孔,这些孔道可以让分子物质分子进入并在其中扩散。
由于沸石具有特定孔径和孔道结构的选择性,可以选择性地吸附和分离分子物质。
具体来说,沸石的吸附原理可以通过以下几个步骤来描述:
1. 外围吸附:分子物质首先与沸石的外围表面发生相互作用,主要是通过范德华力等相互作用力吸附在表面上。
2. 孔道扩散:分子物质进入沸石的孔道结构中,通过与沸石孔道之间的相互作用力,使分子在孔道中扩散和迁移。
孔道的大小和结构决定了能够进入孔道的分子物质的大小。
3. 离子交换:当分子物质与沸石的内部离子发生相互作用时,发生离子交换反应,其中沸石的可交换离子与分子物质中的离子进行置换反应,使之吸附在沸石表面。
通过这些吸附机制,沸石可以有效地吸附不同类型的分子物质,达到分离、净化和储存的目的。
沸石
沸石沸石沸石(zeolite)是一种矿石,最早发现于1756年。
瑞典的矿物学家克朗斯提(Cronstedt)发现有一类天然硅铝酸盐矿石在灼烧时会产生沸腾现象,因此命名为“沸石”(瑞典文zeolit)。
在希腊文中意为“沸腾”(zeo)的“石头”(lithos)。
此后,人们对沸石的研究不断深入。
简介(历史)[1]沸石沸石有很多种,已经发现的就有36种。
它们的共同特点就是具有架状结构,就是说在它们的晶体内,分子像搭架子似地连在一起,中间形成很多空腔。
因为在这些空腔里还存在很多水分子,因此它们是含水矿物。
这些水分在遇到高温时会排出来,比如用火焰去烧时,大多数沸石便会膨胀发泡,像是沸腾一般。
沸石的名字就是因此而来。
不同的沸石具有不同的形态,如方沸石和菱沸石一般为轴状晶体,片沸石和辉沸石则呈板状,丝光沸石又成了针状或纤维状等等。
各种沸石如果内部纯净的话,它们应该是无色或白色,但是如果内部混入了其他杂质,便会显出各种浅浅的颜色来。
沸石还具有玻璃样的光泽。
我们知道沸石中的水分可以跑出来,但这并不会破坏沸石内部的晶体结构。
因此,它还可以再重新吸收水或其他液体。
于是,这也成了人们利用沸石的一个特点。
我们可以用沸石来分离炼油时产生的一些物质,可以让它使空气变得干燥,可以让它吸附某些污染物,净化和干燥酒精等等。
沸石矿物有很广的分布。
特别多见于由火山碎屑形成的沉积岩石中。
在土壤中也有发现。
编辑本段特性沸石沸石是沸石族矿物的总称,是一种含水的碱金属或碱土金属的铝硅酸矿物。
按沸石矿物特征分为架状、片状、纤维状及未分类四种,按孔道体系特征分吸附剂和干燥剂催化剂洗涤剂其他用途(污水处理、土壤改良剂、饲料添加剂)天然沸石是一种新兴材料,被广泛应用于工业、农业、国防等部门,并且它的用途还在不断地开拓。
沸石被用作离子交换剂、吸附分离剂、干燥剂、催化剂、水泥混合材料。
在石油、化学工业中,用作石油炼制的催化裂化、氢化裂化和石油的化学异构化、重整、烷基化、歧化;气、液净化、分离和储存剂;硬水软化、海水淡化剂;特殊干燥剂(干燥空气、氮、烃类等)。
沸石结构的表征

沸石晶体内还存在着三种羟基缺陷
• (1)末端硅羟基,存在于沸石晶体的外表面。
• (2)硅羟基对,由沸石中的 Si-O-Si键水解后断裂生 成。 • (3)羟基空穴,脱铝过程中沸石结构中脱除一个T原 子如铝原子,形成羟基空穴 (hydroxyl nest)。
• 这些硅羟基可以用红外光谱及核磁共振谱鉴别。红外 光谱中的3710cm-1处的谱带吸收值与沸石的羟基空穴 浓度成正比,利用3710cm-1处的吸收值能够定量测定 沸石结构中的羟基空穴含量。上述三类硅羟基也可以 用29Si CP-MAS NMR测定,由它们和三甲基氯硅烷作 用后所得到的不同产物而能够分别检测其浓度。
• 苯吸附后 在谱中的 101等峰处 引起变化, 峰的形状 随着吸附 量的增加 而改变 (图4-15) 但是通常 的XRD技 术不能探 测到。
• C2Cl4和 C2HCl3在沸 石上的吸附 也会改变所 得中子衍射 谱图,例如 图4-16就给 出C2Cl4吸附 在硅沸石-1 的孔道结合 部或直孔道 时,其中子 衍射谱随着 吸附量的变 化。
• 图中上部 曲线中的 点是数据 测试点, 而曲线是 用最小方 差法计算 所得到的. 中部的竖 线标记着 2角度; 底下的曲 线是实际 测定线和 理论计算 的差谱线.
中子衍射技术研究实例
•
实验中发现 C2HCl3、C2Cl4和 苯在硅沸石-1上的 等温吸附线分别呈 现0、1和2个“台 阶”(见左图 C2HCl3(298 K) 、C2Cl4(298 K )和苯 (283 K) 在硅沸石-1上的等 温吸附线)。 为 了探讨其出现的原 因,使用中子衍射 谱进行研究。
4A沸石的SEM照片
AlPO4-5的SEM谱
沿001方向用400kV拍摄的L沸石HRTEM谱, 由于转角原因在 (A)10o、(B)4 o、(C)32.2 o和(D)30 o处重叠而形 成波纹。
生物沸石

生物沸石利用天然非金属矿产来进行水处理由于成本较低,无二次污染,逐渐成为当前环保研究的热点之一。
沸石是一种含水的碱金属或碱土金属的硅铝酸矿物,分子式一般可表示为M2/nO·Al2O3·XSiO2·YH2O,其中n为阳离子的化合价。
沸石骨架最基本单元结构是以Si为中心,形成4个顶点有氧配置的SiO4四面体以及Al取代Si并置换成AlO4四面体的结合体。
硅(铝)氧四面体通过桥氧连接,在平面上显示为多种封闭的环状结构,在三维空间上可形成多种形状的规则多面体,并构成沸石相互连接的多维孔穴群或孔道体系。
正因为沸石具备网架状的特殊空间结构和相互连接的孔穴和孔道,使得其比表面积极大(400~800m2/g)。
另外,由于沸石构架上的碱和碱土金属离子极易与水溶液中的阳离子发生交换作用,从而使沸石具有良好的吸附、交换性能。
由于沸石具备孔隙度高、比表面积大、表面粗糙以及吸附性能良好等特点,可吸附有极性的分子和细菌,对细菌有富集作用。
沸石的微孔结构适于微生物生长繁殖,对微生物无毒害,因此沸石是一种理想的生物载体。
1994年首次提出了“生物沸石”的概念,即以沸石作为微生物生长的载体,借助沸石内部富有空穴和孔道的结构特点,通过吸附富集极性分子和细菌,创造微生物生长条件,使沸石表面生长一层生物膜,以同时发挥沸石的吸附性能和生物膜的作用,去除水中的污染物质。
研究表明生物沸石可以改进沸石的水处理特性,使生物、沸石共同起作用。
例如用它与混凝沉淀相结合,能高效去除水中氨氮、亚硝酸盐氮、锰、有机物、嗅和味、改善色度等;还能利用沸石表面富集的硝化细菌群,将吸附的多量氨氮转化为硝酸盐氮,从而空出吸附位,达到原位再生的目的。
另有研究表明沸石富集水体中的微生物,在充足的溶解氧条件下,微生物在沸石表面形成生物膜,同时沸石自身表面有机物的分解可使以有机物为养料的微生物生长繁殖,使得沸石在一定程度上得以再生,大大延长了生物沸石的使用周期。
沸石mfi结构

沸石mfi结构全文共四篇示例,供读者参考第一篇示例:沸石是一种广泛存在于自然界的矿石,具有多种用途,其中沸石MFI结构是其重要的应用之一。
沸石MFI结构是指一种特定的沸石晶体结构,其独特的孔道结构和化学性质使其在吸附、催化和分离等领域具有广泛的应用价值。
本文将介绍沸石MFI结构的特点、制备方法、应用领域以及未来的发展趋势。
一、沸石MFI结构的特点沸石MFI结构是一种分子筛结构,其主要由硅氧四面体和铝氧四面体交替组成。
在MFI结构中,硅氧四面体形成了沸石的骨架结构,而铝氧四面体位于硅氧四面体之间,形成了孔道结构。
这种孔道结构具有严格的尺寸和形状选择性,使得沸石MFI结构在吸附和分离中具有重要的作用。
沸石MFI结构的孔道大小约为0.55纳米×0.55纳米,这使得其具有很强的选择性吸附能力。
通过调控沸石MFI结构的孔道大小和化学性质,可以实现对不同分子的选择性吸附和分离,从而在催化和分离领域发挥重要作用。
二、沸石MFI结构的制备方法沸石MFI结构的制备主要是通过硅源和铝源在碱性介质中的水热合成。
通常情况下,硅源为硅酸酯或硅酸盐,铝源为铝盐或氢氧化铝。
在水热合成过程中,通过调节反应物的比例、反应时间和温度等条件,可以控制沸石MFI结构的形貌和孔道结构。
还可以通过模板剂法合成沸石MFI结构,其中模板剂是一种有机物或无机盐,可以在沸石合成过程中引导晶体的形成,从而得到特定的孔道结构和形貌。
三、沸石MFI结构的应用领域沸石MFI结构在吸附、分离和催化领域具有广泛的应用。
在吸附方面,沸石MFI结构可以用于气体和液体的分离和净化,具有良好的选择性和吸附容量,特别适用于小分子的分离和富集。
沸石MFI结构还可以用于生物医药、环境保护和能源开发等领域。
通过调控沸石MFI结构的孔道大小和表面性质,可以实现对有害物质的吸附和分解,从而净化水体、空气和土壤。
四、沸石MFI结构的发展趋势随着科学技术的不断发展,沸石MFI结构在吸附、催化和分离领域的应用将得到进一步拓展。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
沸石的结构
沸石矿床主要是由火山玻璃质在碱性水介质的作用下,经过水化、水解和结晶等反应生成。
沸石矿床的矿石主要是沸石,同时有多种类型沸石伴生,如伊利石、蒙脱石、石英等。
目前被广泛应用的沸石有斜发沸石、丝光沸石、菱沸石、毛沸石、钙沸石和铁沸石等。
从内部微观结构看,沸石是一种含水架状结构的多孔性铝硅酸盐晶体,有自然界天然存在的也有人工合成的。
理想的沸石化学式可表示为M x/y Al x Si Y O2(x+y)P·H2O,式中,M为碱金属(如Na、K、Li)和碱土金属(如Ca、Mg、Ba、Sr)。
沸石的化学成分一般可认为是由Al2O3、SiO2、H2O和金属阳离子四部分构成,其中Al2O3、SiO2两种成分约占沸石矿物总量的80%。
在不同的沸石矿物中,硅和铝的含量比例不同,且其比例大小的不同将引起沸石的某些特性变化,如离子交换性和耐酸性能等。
沸石的骨架结构是指由氧、硅和铝三种原子构成的复杂三维空间结构。
结构基本单元是由一个硅或铝原子为中心、四个氧为顶点而形成的硅(铝)氧四面体。
在这种四面体中,中心是硅(或铝)原子,每个硅(或铝)原子的周围有4个氧原子、各个硅氧化四面体通过处于四面体顶点的氧原子相互连接起来,各四面体连接成环状,形成沸石的次级结构单元;沸石的结构中有时还有其他多面体,可以连接成多元环,他们是沸石结构的三级单元。
作为次级和三级单元的各种环以整体形式相互连接,就形成了沸石的骨架。
沸石骨架结构中存在着空洞和孔道,晶穴的体积约为总体积的40%~50%,独特的晶体结构
使其具有大量均匀的微孔,孔径大多在1nm以下。
其均匀的微孔与一般物质的分子大小相当。
各种沸石都有自己特定形状和大小的空洞和孔道。
一般人工合成的沸石具有形状规整,大小均匀的空洞和孔道,能够吸附和截留特定形状和大小的分子,因此又叫分子筛;而天然沸石的孔道常有扭曲,空洞大小分布也不均匀。
