合成氨工艺
合成氨的工艺流程

合成氨的工艺流程1. 空气分离:首先,空气中的氮气和氧气需要被分离。
这可以通过空气压缩和冷却,然后用分子筛或液化分离技术将氮气和氧气分离出来。
2. 氮气制备:通过空气分离得到的氮气需要被进一步提纯。
这可以通过低温分馏或其他技术将氮气提纯到适当的纯度。
3. 氢气制备:氢气可以通过天然气蒸汽重整反应或者电解水得到。
4. 催化剂制备:制备出合成氨反应所需的催化剂,通常是以铁为主要成分的铁钼镍催化剂。
5. 合成氨反应:将氮气和氢气在高压高温的条件下通过催化剂进行反应,生成合成氨。
6. 分离纯化:将合成氨经过冷却和减压,然后通过吸收剂、冷却和压缩等工艺步骤来分离纯化合成氨。
7. 储存和运输:将合成氨储存于合适的储罐中,并通过管道或其他运输方式将其运输到需要的地点。
以上就是合成氨的工艺流程,通过这个工艺流程可以高效地制备出高纯度的合成氨,供给各种化工生产需要。
合成氨的工艺流程是一个复杂而精细的过程,其中的每一步都需要严格控制,以确保产出的合成氨的纯度和质量能够满足工业需求。
在合成氨的工艺中,采用了一系列先进的化工技术和设备,以下将进一步细说合成氨的工艺流程过程。
8. 催化剂再生:在合成氨反应中使用的催化剂需要不断地被再生。
随着反应进行,催化剂表面会积聚一定量的杂质物质,从而影响催化剂的活性和选择性。
因此,通过热气流或蒸汽来清洁催化剂表面,以恢复催化剂的活性和选择性。
9. 热力学控制:合成氨的反应是放热反应,因此需保持适宜的温度。
以确保反应不至于过热,影响产品的选择性及催化剂的稳定性。
使用适当的冷却系统来维持反应温度,是非常关键的。
10. 蒸汽重整制氢:氢气是合成氨反应的一种重要原料。
而氢气通常是通过天然气蒸汽重整反应得到的。
在这个过程中,通过加热天然气并与水蒸气反应,生成氢气和二氧化碳。
11. 压缩系统:由于合成氨反应需要高压,所以需要使用高效的压缩系统,来将氮气和氢气压缩至合适的反应压力。
一般情况下,合成氨反应的压力约为100至200大气压。
合成氨生产工艺
合成氨生产工艺合成氨生产原理:氨是一种重要的化工原料,特别是生产化肥的原料,它是由氢和氮合成。
合成氨工业是氮肥工业的基础。
为了生产氨,一般均以各种燃料为原料。
首先,制成含H2和CO等组分的煤气,然后,采用各种净化方法,除去气体中的灰尘、H2S、有机硫化物、CO、CO2等有害杂质,以获得符合氨合成要求的洁净的1:3的氮氢混合气,最后,氮氢混合气经过压缩至15Mpa以上,借助催化剂合成氨。
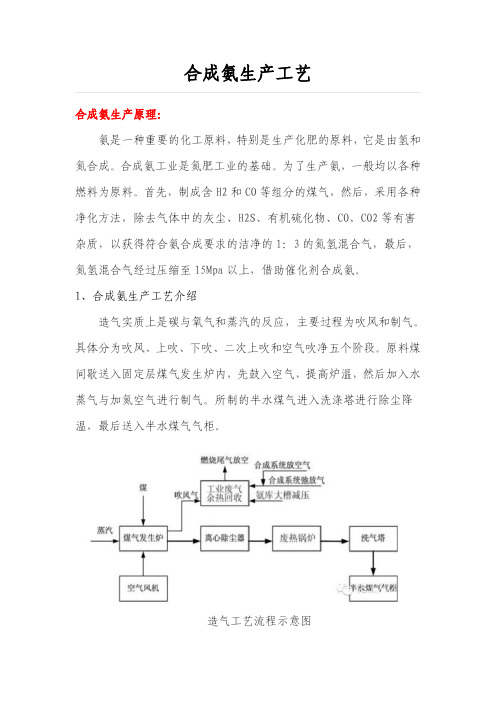
1、合成氨生产工艺介绍造气实质上是碳与氧气和蒸汽的反应,主要过程为吹风和制气。
具体分为吹风、上吹、下吹、二次上吹和空气吹净五个阶段。
原料煤间歇送入固定层煤气发生炉内,先鼓入空气,提高炉温,然后加入水蒸气与加氮空气进行制气。
所制的半水煤气进入洗涤塔进行除尘降温,最后送入半水煤气气柜。
造气工艺流程示意图2、脱硫工段煤中的硫在造气过程中大多以H2S的形式进入气相,它不仅会腐蚀工艺管道和设备,而且会使变换催化剂和合成催化剂中毒,因此脱硫工段的主要目的就是利用DDS脱硫剂脱出气体中的硫。
气柜中的半水煤气经过静电除焦、罗茨风机增压冷却降温后进入半水煤气脱硫塔,脱除硫化氢后经过二次除焦、清洗降温送往压缩机一段入口。
脱硫液再生后循环使用。
脱硫工艺流程图3、变换工段变换工段的主要任务是将半水煤气中的CO在催化剂的作用下与水蒸气发生放热反应,生成CO2和H2。
河南中科化工有限责任公司采用的是中变串低变工艺流程。
经过两段压缩后的半水煤气进入饱和塔升温增湿,并补充蒸汽后,经水分离器、预腐蚀器、热交换器升温后进入中变炉回收热量并降温后,进入低变炉,反应后的工艺气体经回收热量和冷却降温后作为变换气送往压缩机三段入口。
变换工艺流程图4、变换气脱硫与脱碳经变换后,气体中的有机硫转化为H2S,需要进行二次脱硫,使气体中的硫含量在25mg/m3。
脱碳的主要任务是将变换气中的CO2脱除,对气体进行净化,河南中科化工有限责任公司采用变压吸附脱碳工艺。
来自变换工段压力约为1.3MPa左右的变换气,进入水分离器,分离出来的水排到地沟。
合成氨工艺流程简述

合成氨工艺流程简述1、粘结剂制备先将水加入到粘结剂提取罐内,然后向罐内微通蒸汽,加热温度应≤40℃,开动搅拌机在不断搅拌的情况下投入液体烧碱(30%Na0H),待碱液温度达一定时继续搅拌,投入筛好的褐煤(含腐植酸约35%),含量低的褐煤应适当多投,可根据腐植酸含量高低而调整加入量,边投料边通蒸汽,同时不停搅拌,此时由于化学反应而放出热量产生少量气体、液位有所升高,为防止冒槽现象应酌情减少蒸汽加入量,维护反应温度,时间约2小时反应基本完全,可取少量提取液检查,其颜色为黑褐色,有粘结性,用母指和食指捏后拉开有连丝,冷却后粘结性增大,流动性变差,视为提出制液结束。
此时停蒸汽,不停搅拌待用。
2、原料煤的粉碎和粘结剂的加入原料煤先送入一级粉碎机,粉至3毫米以下,后经皮带机送入鼠笼粉碎机粉至1毫米以下,经皮带机送入双轴搅拌机内,此时由操作工视其送入的煤量酌情控制加液阀加入已提取好的粘结剂,在双轴搅拌机内不断的搅拌推进混匀后落入斜皮带机,送至分仓平皮带机,分仓堆沤备用(粘结剂的加入量是根据经验判断掌握调节,一般加液后的煤屑用手抓一把捏得拢,两指能捏散较为合适)。
3、煤棒制备沤化合格的原料煤送煤棒机挤压成型后经皮带机输送到煤棒烘干炉中,利用吹风气回收锅炉的尾气(温度~160℃)将煤棒烘干,再经皮带机输送到造气车间供造气炉制取半水煤气用。
4、半水煤气制取以空气和蒸汽为气化剂,在常压、高温下与煤棒中的炭作用,通过固定床(造气炉)蓄热间歇制气法得到半水煤气,根据氨合成必需的氢、氮气体比例调整空气和蒸汽加入量,保证合成氨系统的循环氢含量,造气过程由微机控制,分为五个阶段:①吹风②上吹制气③下吹制气④二次上吹⑤空气吹净②、③、④、⑤阶段制取的半水煤气经旋风除尘器、蒸汽过热器、显热回收器回收热量,进入洗气塔降温除尘后送入气柜。
以上五个阶段形成一个工作循环,周而复始。
每个工作循环根据原料煤的特性,确定各阶段的工作时间,烘干煤棒的一个工作循环时间120-140秒,为保证半水煤气生产的连续性,采用若干台半水煤气发生炉交替工作。
合成氨的工艺流程

合成氨的工艺流程1. 原料准备:合成氨的原料是氮气和氢气。
氮气通常是从空气中提取,而氢气则是通过蒸汽重整或其他化学反应得到。
这两种气体需要经过净化和压缩处理以确保其纯度和适当的压力。
2. 氮氢混合:氮气和氢气按照一定的比例混合到合成氨反应器中。
通常情况下,氮气和氢气的摩尔比是3:1,经过混合后形成氢气和氮气的混合气体。
3. 合成氨反应:混合气体经过压缩以提高反应速率,并在高温(通常在400-500摄氏度)和高压(通常在100-250大气压)下进入合成氨反应器。
在反应器中,混合气体经过催化剂的作用,发生一系列的化学反应,最终生成合成氨。
4. 分离和提纯:合成氨反应产物中还包含未反应的氮气和氢气,以及少量的副产物。
通过冷凝和减压操作,将未反应的气体和副产物从合成氨中分离出来。
之后,通过蒸馏或其他分离技术提纯合成氨,以得到符合工业标准的合成氨产品。
5. 储存和运输:合成氨产品可以被存储在压力容器中,并通过管道或其他方式进行运输到需要的地方,用于化肥生产或其他工业应用。
以上是合成氨的基本工艺流程,工艺中还有一些细节操作和工艺条件的优化,以确保合成氨的产率和纯度达到要求。
合成氨是一种重要的工业气体,广泛用于农业和工业领域。
它通过哈贝-玻斯过程(Haber-Bosch process)进行生产。
这个过程是由德国化学家弗里茨·哈贝和卡尔·博世于20世纪初发现的,如今,仍然是工业生产合成氨的主要方法。
在合成氨的工艺流程中,反应器是一个关键的组成部分。
工业上通常使用固定床催化剂反应器,其在高压和高温下通过催化剂的作用来促进氮气和氢气之间的反应。
这个过程对反应条件的要求极为严格,既要求高温高压,又要求催化剂的有效性和稳定性。
随着全球工业化的不断发展,对合成氨生产过程的节能减排和工艺的优化也提出了更高的要求。
在现代的合成氨生产过程中,节能减排已经成为了一个重要的发展趋势。
通过改进反应条件和提高生产效率,减少能源消耗,降低碳排放已经成为了工业化生产合成氨的重要目标。
合成氨各工序工艺详细流程

合成氨各工序工艺详细流程合成氨是一种重要的化工原料,广泛用于合成各类农药、肥料、化学品等。
下面将详细介绍合成氨的工序和流程。
合成氨的工艺主要分为三个步骤:气体净化、气体压缩和反应制氨。
1.气体净化:合成氨的原料气体主要有空气和甲烷。
在进入反应装置之前,需要进行气体净化处理。
空气首先经过过滤装置去除微小杂质、灰尘和固体颗粒物。
然后通过制冷装置降低气体温度,使其中的水蒸气凝结成液体,然后被排放。
甲烷通过碳分子筛吸附去除杂质。
这样可以保证反应装置中气体的纯度和稳定性。
2.气体压缩:经过气体净化后的空气和甲烷被分别压缩到一定压力,以满足反应器中的需求。
通常使用压缩机进行压缩,然后将压缩后的气体分别输送到反应器中。
3.反应制氨:反应制氨是整个过程的关键步骤。
通常采用哈柏法(Haber-Bosch)来实现反应制氨。
反应器中,高温高压的空气与甲烷的混合气体通过催化剂床进行催化反应。
常用的催化剂是铁与铁-铝的混合物,也可以加入少量的钾、镁等元素。
反应是一个放热反应,反应温度一般在380-550°C 之间,压力一般在1.7-3.5 MPa之间。
催化剂的存在可以提高反应速率,但也会增加反应的等离子体强度,导致了碳催化剂和蒸汽的选择性降低,产生非氮气杂质。
反应过程中,氮气与氢气进行反应生成氨气。
原料气体经过催化剂床后,反应转化率不高,需要多次通过催化剂床进行反应。
一般采用多级反应器和中间冷却装置,提高氨气的产率和纯度。
经过多级反应后,氨气还需要进行冷却和净化处理,以达到合成氨的纯度要求。
以上是合成氨的工序和流程的详细介绍。
合成氨的过程需要进行气体净化、气体压缩和催化反应制氨。
这个过程需要确保原料气体的纯度和稳定性,通过压缩提高原料气体的压力,催化剂的存在可以提高反应速率和转化率。
经过多级反应,最终得到高纯度的合成氨。
合成氨工艺的不断优化和改进,可以提高合成氨的生产效率和氨气的纯度,降低生产成本。
合成氨工艺原理

合成氨工艺原理合成氨不论采用什么原料和生产方法,大体上包括三个工艺过程:(1)原料气的制造;(2)原料气的净化(包括脱硫、变换脱除CO,碳化、脱碳脱除CO2,精炼脱除微量的CO、CO2、H2S、O2等);(3)氨的合成和为了满足气体净化及合成各工序工艺条件提供能量补偿的压缩工序.生产出氨以后再根据需要加工成碳铵、尿素、硝铵等.其详细原理如下(以煤为原料):一、造气工段合成氨生产所用的半水煤气,要求气体中(CO+H2)与N2的比例为3:1左右.因此生产上采用间歇地送入空气和蒸汽进行气化,将所得的水煤气配入部分吹风气制成半水煤气.即以石灰碳化煤球、无烟块煤为原料,在高温下交替与空气和过热蒸汽进行气化反应(C+O点燃CO2+Q 、2C+O点燃2CO+Q 、2CO+ O点燃2CO2+ Q2H2O(气)+C△CO+2H2-Q制得半水煤气,半水煤气经过除尘,余热回收,水洗降温制得合格的半水煤气,供后工段使用.二、脱硫工段从造气工段的半水煤气中,除氢气和氮气外,还含有27%左右CO、9%左右的CO2以及少量的硫化物,这些硫化物对合成氨生产是有害的.它会腐蚀设备、管道,会引起催化剂中毒,会损坏铜液成份。
因此,必须除去少量硫化物,其原理:用稀氨水(10—15tt)与硫化氢反应(NH3+H2S=NH4HS)将H2S脱除至0。
07g/m3(标)以下,使半水煤气净化,以满足合成氨生产工艺要求。
三、变换工段将脱S后的半水煤气(含CO25%—28%)由压缩工段加压后经增温、加热,在一定的温度和压力下,在变换炉内借助催化剂的催化作用,使半水煤气中CO与H 2O(气)进行化学反应,转变为CO2和H2(CO+H2O(气)催化剂高温CO2+H2+Q),制得合格的变换气,以满足后工段的工艺要求。
其次,系统中设有饱和热水塔、甲交、一水加、二水加、冷却塔等换热设备,以便合理利用反应热和充分回收余热,降低能耗,同时降低变换气温度。
四、碳化与脱碳工段1、碳化将变换气中26%左右的CO2用浓氨水与其反应(CO2+ H2O+ NH3=NH4HCO3)生成碳酸氢铵副产品,同时制得合格的原料气.2、脱碳工段用MEDA脱碳溶液将变换气中26%左右的CO2除去,制成合格的原料气,供后工段使用。
合成氨工艺
合成氨工艺————————————————————————————————作者:————————————————————————————————日期:合成氨工艺流程(1)原料气制备将煤和天然气等原料制成含氢和氮的粗原料气。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;渣油可采用非催化部分氧化的方法获得合成气;对气态烃类和石脑油,工业中利用二段蒸汽转化法制取合成气。
(2)净化对粗原料气进行净化处理,除去氢气和氮气以外的杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程。
①一氧化碳变换过程在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。
合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。
变换反应如下:CO+H2OH→2+CO2 =-41.2kJ/mol 0298HΔ由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。
第一步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO含量降至0.3%左右。
因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
②脱硫脱碳过程各种原料制取的粗原料气,都含有一些硫和碳的氧化物,为了防止合成氨生产过程催化剂的中毒,必须在氨合成工序前加以脱除,以天然气为原料的蒸汽转化法,第一道工序是脱硫,用以保护转化催化剂,以重油和煤为原料的部分氧化法,根据一氧化碳变换是否采用耐硫的催化剂而确定脱硫的位置。
工业脱硫方法种类很多,通常是采用物理或化学吸收的方法,常用的有低温甲醇洗法(Rectisol)、聚乙二醇二甲醚法(Selexol)等。
粗原料气经CO变换以后,变换气中除H2外,还有CO2、CO和CH4等组分,其中以CO2含量最多。
CO2既是氨合成催化剂的毒物,又是制造尿素、碳酸氢铵等氮肥的重要原料。
因此变换气中CO2的脱除必须兼顾这两方面的要求。
一般采用溶液吸收法脱除CO2。
合成氨生产工艺简介
合成氨生产工艺简介
合成氨以煤为原料,采用固定层间歇法制气,制出合格的半水煤气送至气柜。
经静电除尘后的半水煤气进入脱硫塔,经湿法脱硫后去氢氮气压缩机加压后,半水煤气进入饱和塔,传热传质后,进入变换炉,经变换炉将其中的一氧化碳转化为二氧化碳和氢气,进入变脱进一步脱除硫化物,再经过脱碳工段脱除二氧化碳后,进入压缩机加压,经铜洗脱除其中少量的一氧化碳、二氧化碳,进入压缩机七段加压,然后进入合成塔,在高温高压催化剂作用下进行合成反应生成氨,再经氨分离器和冷凝塔分离出液氨,减压、计量后送往液氨仓库备用。
尿素由氨库来液氨经液氨泵加压送往尿素合成塔。
同时由氢氮压缩机三段出口的气体通过脱碳之后,其中二氧化碳气体经二氧化碳压缩机压缩后送入尿素合成塔,由循环系统回收的氨基甲酸铵一氨水溶液;也回到尿素合成塔,在塔内CO2和NH3反应生成尿素熔融物,出塔后多次减压分解,再经过加热蒸浓,液相熔融尿素进入造粒塔后成尿素产品,再经包装制成成品尿素。
未反应的NH3和CO2经回收循环再使用。
甲醇由合成压缩机六段出来的气体,经滤油进入甲醇合成塔,经冷却分离后,进入粗甲醇储槽,经计量后,经商品泵装桶或装槽车销售。
合成氨各工序工艺详细流程
合成氨各工序工艺详细流程
一、蒸汽炒烧式合成氨工艺
1、反应原料预处理及收集:以天然气为反应原料进行洁净预处理,将其中的硫氢离子捕集处理;
2、冷凝:利用空冷凝器将原料液冷凝后进入反应釜;
3、蒸汽炒烧:将原料液放入釜中增温,增温到某个温度时,将蒸汽灌进反应釜并炒烧反应;
4、气-液回收:将反应釜中产生的氰气和氨气经过冷凝式压缩凝结回收;
5、洗涤液回收:将氰气和氨氧化后产生的洗涤液回收处理;
7、回收固体:将反应釜中凝聚的氯化磷等固体物质回收并进行进一步处理;
二、NH3-NH3-N2反应式氨的制备
1、原料准备:准备碘化氨、碳氢气、氮气等原料进行反应;
2、液-液混合:将碳氢气、碳氢气、氮气和碘化氨通过特定设备混合液化;
3、反应:将液态原料放入反应器中,加热反应工艺,由气相催化剂催化反应,化学反应过程中产生的氨收集回收;
4、冷凝:将反应后的气体回收到冷凝器中,通过冷凝介质冷凝凝结;
5、收集:将氨从冷凝罐中收集。
合成氨工艺流程详解
合成氨工艺流程详解
合成氨是一种重要的化工原料,广泛应用于农业、化肥、塑料、医药等领域。
本文将详细介绍合成氨的工艺流程。
合成氨的工艺流程主要包括加气制氢、氨合成反应和氨的分离纯化三个步骤。
第一步是加气制氢。
制氢是合成氨过程中的关键步骤,常用的方法是通过蒸汽重整法或者煤气制氢法进行。
蒸汽重整法是将天然气或液化石油气与水蒸汽进行催化反应,生成含有一氧化碳和氢气的合成气。
而煤气制氢法则是利用煤炭、石油焦等作为原料,通过燃烧生成一氧化碳和氢气的混合气体。
制氢过程中需要注意控制反应温度和催化剂的选择,以提高氢气的产率和纯度。
第二步是氨合成反应。
氨合成反应是将制得的合成气经过催化剂床层,与氮气进行反应生成氨气。
常用的催化剂有铁、铑、镍等金属催化剂,反应温度一般在350-550℃之间。
反应过程中需要控制压力、温度和空速的条件,以提高氨气的产率和选择性。
第三步是氨的分离纯化。
合成氨中常含有一氧化碳、二氧化碳、甲烷等杂质,需要进行分离和纯化。
常用的方法是通过吸附剂吸附和脱附的方式进行。
吸附剂通常选择活性炭或分子筛等材料,通过控制温度和压力来实现氨的吸附和脱附。
吸附脱附过程中需要周期性地对吸附剂进行再生和活化,以保证吸附效果和氨气的纯度。
合成氨的工艺流程包括加气制氢、氨合成反应和氨的分离纯化三个步骤。
通过合理控制各个步骤的条件和催化剂的选择,可以提高氨气的产率和纯度,满足不同领域的需求。
合成氨工艺的优化和改进,对于提高工业生产效率和减少能源消耗具有重要意义。
希望本文对读者了解合成氨的工艺流程有所帮助。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(2)合成氨工业发展简介 1784年,有学者证明氨是由氮和氢组成的。19世纪
末,在热力学、动力学和催化剂等领域取得进展后, 对合成氨反应的研究有了新的进展。1901年法国物理 化学家吕·查得利提出氨合成的条件是高温、高压, 并有适当催化剂存在。
1909年,德国人哈伯以锇为催化剂在17~20MPa地建立了能生产80gh-1氨的试验装置。
合成氨生产的原则流程如图示。
合成氨过程由许多环节构成,氨合成反应过程是整个
工艺过程的核心。
实用文档
2.氨合成理论基础 从化学工艺的角度看其核心是反应过程工艺条件的
确定,而确定反应的最佳工艺条件,需先从事反应热
力学和动力的研究。
(1)氨合成反应的热效应 氢气和氮气合成氨是放热,体积缩小的可逆反应,
反应式如下:
1911年米塔希研究成功以铁为活性组分的合成催 化剂,铁基催化剂活性好、比锇催化剂价廉、易得。
实用文档
(3)合成氨的原料及原则流程 合成氨的原料是氢气和氮气。氮气来源于空气,可以 在制氢过程中直接加入空气,或在低温下将空气液化、 分离而得;氢气来源于水或含有烃的各种燃料。工业 上普遍采用的是以焦炭、煤、天然气、重油等燃料与 水蒸气作用的气化方法。
①动力学过程 氨合成为气固相催化反应,它的宏观 动力学过程包括以下几个步骤。 a.混合气体向催化剂表面扩散(外,内扩散过程); b.氢,氮气在催化剂表面被吸附,吸附的氮和氢发生 反应,生成的氨从催化剂表面解吸(表面反应过程); c. 氨从催化剂表面向气体主流体扩散(内,外扩散过 程氮)、氢气在催化剂表面反应过程的机理,可表示为:
合成氨工艺
编制:一分厂工艺科 2009-9-5
实用文档
1.2合成氨生产
1.概述
(1)合成氨工业的重要性 合成氨工业是基础化学工业的重要组成部分,有
十分广泛的用途。 氨可生产多种氮肥,如尿素、硫酸铵、硝酸铵、碳酸
氢铵等;还可生产多种复合肥,如磷肥等。 氨也是重要的工业原料。基本化学工业中的硝酸、
纯碱及各种含氮无机盐; 有机工业各种中间体,制药 中磺胺药物,高分子中聚纤维、氨基塑料、丁腈橡胶 、冷却剂等。
接近于 1,此时
Kp=Kf。因此Kf可
看作压力很低时
的 Kp。
实用文档
⑶影响平衡氨含量的因素
若总压为p的混合气体中含有N2, H2, NH3的摩尔
分数分别为yN2, yH2和yNH3,其关系为yN2+yH2+yNH3=1.令 原始氢氮比R= yH2/ yN2, 则各组分的平衡分压为
pH2 p(1yN3 Hyi)1 RR pN2 p(1yN3 Hyi)1 1R
N2(g)+Cate —→2N(Cate) H2(g)+Cate —→2H(Cate) N(Cate) + H(Cate) —→NH(Cate)
实用文档
NH(Cate) + H(Cate) —→NH2(Cate) NH2(Cate) + H(Cate) —→NH3(Cate) NH3(Cate)—→NH3(g) + (Cate)
若不考虑R对Kp的影响,解得R=3时,yNH3为最大值;高 压下,气体偏离理想状态,Kp将随R而变,所以具有
最大yNH3时的R略小于3,约在2.68~2.90之间,如图 所示。
实用文档
c.惰性气体的影响 惰性组分的存在,降低了氢、 氮气的有效分压,会使平衡氨含量降低。
实用文档
(4)合成氨反应的动力学
通常 0<a<l,对以铁为主的氨合成催化剂a=0.5,
故
rNH 3 k1pN2
ppN1H.52H 3 k2
pNH 3 p1H.52
反应达到平衡时,r=0,则
整理得
k1pN2
p1H.52 pNH3
k2
的程度,需通过反应的化学平衡研究确定。其平衡常
数为:
实用文档
Kp
pNH 3 pN 0.25p1H.52
1 yNH 3 pyN 0.25y1H.52
式中, p,pi—分别为总压和各组分平衡分压;
yi—平衡组分的摩尔分数。
高压下化学平衡常数Kp值不仅与温度有关,而且与
压力和气体组成有关,用逸度表示:
整理得
yNH 3
1yNH 3 yi
2
Kpp1R 1R .52
此式可分析影响平衡氨含量的诸因素:
a.压力和温度的影响
温度越低,压力越高,平
衡常数Kp越大,平衡氨含量越高。 实用文档
b.氢氮比的影响 当温度、压力及惰性组分含量一
定时,使yNH3为最大的条件为
R(Kp
R1.5 p(R1)2)
0
0.5N2+1.5H2==NH3
ΔH0=46.22 kJ·mol-1
其反应热不仅与温度有关,还与压力和组成有关。
实用文档
下表为纯3H2-N2混合气生成φNH3为17.6%系统反应的 热效应。
(2)化学平衡及平衡常数
应用化学平衡移动原理可知,低温、高压操作有利于
氨的生成。但是温度和压力对合成氨的平衡产生影响
当内扩散控制时,动力学方程为
rNH3=kP
式中rNH3为反应速率,k为扩散系数,p为反应物的总 压。当化学动力学控制时,在接近平衡时:
rNH 3 k1pN2ppN 2H 32H 3k2ppN 2H 32H 31a
式中 rNH3——氨合成反应的净速率: k1,k2——正、逆反应速率常数;
pN2, pH2, pNH3——N2, H2, NH3的分压. a为常数,与催化剂性质及反应条件有关 ,由实验测定。 实用文档
K f fN 0 f2 .N 5fH 3 1 H .2 5N 0.2 N 51 H 3.H 5 2 yN 0 y.2 5 N y1 H 3H .5 2 K K p
Kp Kf /K
式中: f,γ分别为各实平用文衡档 组分的逸度和逸度系数.
研究者
把不同温度、压
力下Kγ值算出并
绘制成图。当压
力很低时,Kγ值
实验结果证明,N2活性吸附是最慢的一步,即为表面 反应过程的控制步骤。
对整个气固相催化反应过程,是表面反应控制还 是扩散控制,取决于实际操作条件。低温时可能是动 力学控制,高温时可能是内扩散控制;
大颗粒的催化剂内扩散路径长,小颗粒的路径短, 所以在同样温度下大颗粒可能是内扩散控制,小颗粒 可能是化学动力学控制。实用文档
