常见有机物结构式
有机物的结构(表示与空间构型)

O CH3 C
OH
CH3 CHO
CH3 COOH
醛基、羧基的结构简式特有的写法
下列有机物分子的结构简式书写正确吗?
1、乙烷:H3C-CH3 2、乙醇:CH2CH3OH 3、丙酸:COOHCH2CH3 4、丁炔:CHCCH2CH3
键线式: 省略:1.将碳、氢元素符号;2. C-H键 表示:点:未指明的起点、拐点或终点均表示一个碳原子; 线:只用线表示分子中碳碳或碳氧等形成的共价键。 H个数的确定:每个交点、端点代表一个碳原子,每一条线段代表 一个共价键,每个碳原子形成4个键,用四减去线段数既是氢原子 个数。
说法不正确的是
A.与环戊烯互为同分异构体
B.二氯代物超过两种(不考虑空间异构)
C.所有碳原子均处同一平面
D.由该物质生成生成1 mol C H 需要2 mol H
小结1:结构中出现饱和碳原子,则整个分子不再共面。
(2)平面结构 a.碳碳双键两端的碳原子与其所连四个原子在同一平 面上; b.苯环结构中的12个原子构成平面六边形; (3)直线结构
碳碳叁键两端的碳原子与直接相连2个原子在同一直线 上;
例1:CH3CH=CH2其结构式可写成如图所示:
⑦
H
H
①
H
⑥
有机物结构的表示方法
一.结构的表示方法
常见有机物的结构表示
有机物 分子式 实验式
甲烷
CH4 CH4
乙烯
C2H4 CH2
乙炔
C2H2 CH
结构式
结构 简式
电子式
CH4
H—C≡C—H
CH2=CH2
CH≡CH
苯
C6H6 CH
注意:碳碳双键、碳碳三键不能省略
有机化学知识的基本概念第一节有机化合物的组成和结构
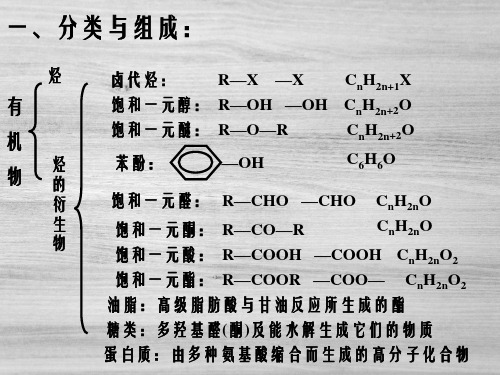
强极性键:如C—O、O—H、C—X等键,一般性质活泼, 较易断裂而发生化学反应。
三、结构与性质的关系:
1、结构与物理性质: (1)熔、沸点:分子量越大;分子中支链越少;分子极
性越大的熔沸点越高。 (2)、溶—解C性H:O只等有官分能子团中的含低有级—化O合H物、可—溶N于H2水、。—其CO余O的H
反应基团:C=C、C=O、C≡C、苯环上的键等
C=O + H—H → H—C—O—H (加氢)
C=C + H—CN → H—C—C—CN (加氢氰酸)
C=C + H—X → H—C—C—X (加卤化氢) C=C + H—OH → H—C—C—OH (加水)
加成反应的规律
. 1mol双键需1molH2 ; 1mol叁键需2molH2 .加成反应发生后,碳链结构不变,一般碳原子数目不 变,但加氢氰酸(HCN)后,碳原子数增加一个。
单体分子中一般应含有至少两个可以发
缩
生缩合反应的官能团
聚 特 反应通常发生在官能团上
反 点 高分子链中一般要通过氧、氮等原子相
·能发生银镜反应的物质有:醛、甲酸、甲酸酯、甲酸盐
有机物燃烧的规律: ⑴ N→有N机2、物X燃→烧H时X,各元素的最终产物:C→CO2、H→H2O、 ⑵烃和烃的含氧衍生物完全燃烧后,产物均为CO2和H2O ⑶烃的含氧衍生物燃烧的耗氧量可转化为烃燃烧的耗氧量
⑷1molC消耗1molO2,4molH消耗1molO2 ⑸ Cn符H2合nO通z的式有C机nH物2nO完z全的燃有烧机,物其完产全物燃C烧O规2和律H:2O(符g)合的通体式积相等。 ⑹100℃以上,有机物完全燃烧前后气体体积不变化的规律。
有机化学基础知识点整理官能团的常见命名与结构式表示

有机化学基础知识点整理官能团的常见命名与结构式表示有机化学基础知识点整理官能团的常见命名与结构式表示在有机化学中,官能团是指分子中具有特定化学性质的“功能部分”。
正确命名和准确表示官能团对于理解和学习有机化学至关重要。
本文将对一些常见的官能团及其命名与结构式表示进行整理和介绍。
I. 烃类官能团烃类是由碳和氢组成的化合物,没有官能团。
常见的烃类有烷烃、烯烃和炔烃。
它们的命名和结构式表示如下:1. 烷烃:以"-ane"为后缀命名,结构式使用线段表示,每个碳原子用顶点表示。
- 甲烷:methane (CH4)- 乙烷:ethane (C2H6)- 丙烷:propane (C3H8)2. 烯烃:以"-ene"为后缀命名,结构式使用线段及双键表示。
- 乙烯:ethylene (C2H4)- 丙烯:propene (C3H6)- 戊烯:butene (C4H8)3. 炔烃:以"-yne"为后缀命名,结构式使用线段及三键表示。
- 乙炔:ethyne (C2H2)- 丙炔:propyne (C3H4)- 戊炔:butyne (C4H6)II. 卤代烃官能团卤代烃是烃类分子中的氢被卤素(氟、氯、溴、碘)取代而成的化合物。
常见的卤代烃有氯代烷、溴代烷和碘代烷。
它们的命名和结构式表示如下:1. 氯代烷:以"-chloride"为后缀命名或使用"chloro-"作为前缀,结构式在相应的碳原子上用Cl表示。
- 氯甲烷:chloromethane(CH3Cl)- 1,2-二氯乙烷:1,2-dichloroethane(CH2Cl-CH2Cl)2. 溴代烷:以"-bromide"为后缀命名或使用"bromo-"作为前缀,结构式在相应的碳原子上用Br表示。
- 溴乙烷:bromoethane(CH3CH2Br)- 2,3,4-三溴戊烷:2,3,4-tribromopentane(CH3CHBr-CHBr-CH3)3. 碘代烷:以"-iodide"为后缀命名或使用"iodo-"作为前缀,结构式在相应的碳原子上用I表示。
有机化学 含氮有机化合物
第十三章含氮有机化合物
⑵芳环上的亲核取代反应
(i)芳环的特征反应是亲电取代反应
邻位或对位被硝基取代的芳香卤代物,由于强吸电子基硝基的影响,使苯环上的电子云密度降低,不利于亲电试剂的进攻,容易发生亲核取代反应。
Cl
NO 2
O 2N
NO 2
2NH 3
NH 2
O 2N
NO 2
NO 2
NH 4Cl
氮原子与脂肪烃基相连的是脂肪胺(R-NH 2),与芳香环直接相连的为芳香胺(Ar-NH 2)
按照分子中所含氨基的数目,有一元、二元或多元胺
注意“氨”、“胺”、“铵”字的用法,在表示基时,如氨基、亚氨基,用“氨”;表示NH 3的烃基衍生物时,用“胺”;而季铵类化合物则用“铵”。
-NH 2(氨基)、-NH-(亚氨基)
(CH3CH2)2NH CH3CH2NH CH3
N CH3N
CH3
CH3
①气相:(CH 3)3N
(CH 3)2NH CH 3NH 2NH 3
>>>(CH 3)3N (CH 3)2NH CH 3NH 2NH 3
>>>②水溶液相:
3°2°
1°3°
2°1°原因:CH 3的+I 效应使N 上电子云密度增加,与H +
的结合力增加,碱性增强。
K b ×10
5
59.542.5 6.73 1.8
(教材错误)。
常见有机物结构式

常见有机物结构式有机物是由碳原子构成的化合物,通常还含有氢、氧、氮、硫等元素。
在有机化学中,结构式是用来表示有机物分子结构的一种标记方法。
常见的有机物结构式包括线性结构、环状结构、分枝结构和立体结构等。
下面是一些常见的有机物结构式:1.甲烷(CH4):甲烷是最简单的有机化合物,由一个碳原子和四个氢原子组成。
HH-C-HH2.乙烷(C2H6):乙烷由两个碳原子和六个氢原子组成。
HHH-C-C-HHH3.乙醇(C2H5OH):乙醇是一种醇类化合物,由两个碳原子、六个氢原子和一个氧原子组成。
HHH-C-C-O-HHH4.甲酸(HCOOH):甲酸是一种羧酸化合物,由一个碳原子、一个氧原子和两个氢原子组成。
OH-C-O-HH5.乙酸(CH3COOH):乙酸也是一种羧酸化合物,由两个碳原子、两个氧原子和四个氢原子组成。
OHH-C-C-O-HHH6.乙醛(CH3CHO):乙醛是一种醛类化合物,由两个碳原子、两个氧原子和四个氢原子组成。
OHH-C-C-HHH7.苯(C6H6):苯是一种芳香烃,由六个碳原子和六个氢原子组成。
HHH-C=C-C=C-HHH8.己烷(C6H14):己烷是一种烷烃化合物,由六个碳原子和十四个氢原子组成。
HHHH-C-C-C-C-C-HHHH这些都是一些常见的有机物结构式,但实际上存在的有机物种类非常多。
有机化学研究的范围非常广泛,涉及到各种有机化合物的合成、结构解析、反应机理等。
有机物结构式是研究和描述有机化合物的重要工具,它可以帮助人们了解有机物的化学性质和结构特征,从而进一步研究和应用有机化学。
生活中的有机物

△
H C H +4Ag(NH3)2OH CO2↑+ 4Ag↓+ 8NH3 + 3H2O
三乙酸
醋的来历?
传说古代山西省有个酿酒高手叫杜康。他儿 子黑塔跟父亲也学会了酿酒技术。后来,从山西 迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把 酒糟浸泡在水缸里。到了第二十一日的酉时,一 开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝 了一口,酸酸的,味道很美。烧菜时放了一些, 味道特别鲜美,便贮藏着作为“调味酱”。故醋 在古代又叫“苦酒”
B.溴水
C.碳酸钠溶液
D.紫色石蕊试液
4.除去乙酸乙酯中含有的乙酸,最好的处理和操作是
(C )
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
5. 关于乙酸的下列说法中不正确的是
( D ).
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激 性气味的液体
2、氧化反应
(1)乙醛在点燃条件下可被空气中的氧气所氧化 2 CH3CHO + 5 O2 点燃 4CO2 + 4H2O
(2)乙醛的催化氧化
催化剂
2CH3CHO + O2 △ 2CH3COOH
(3)乙醛与弱氧化剂银氨溶液反应,显示还原性
△
CH3CHO + 2Ag(NH3)2OH
CH3COONH4 + 2Ag↓+ 3NH3+ H2O 注意事项
与 (2).该反应可用金属铜作催化剂,分步写出反应 思考 的方程式。
有机物的分类
一.有机物的分类1.按碳链的骨架分类2.按官能团分类只含碳链醚键二.有机物中C-C的成键特点键长:键角:*键能:*键能和物质能量跟物质稳定性的关系:能量越低越稳定,键能越高越稳定。
三.同分异构体定义:同分异构的分类1碳链异构2光能团位置异构3官能团类型异构乙醚跟乙醇环丙烷跟丙烯4顺反异构四.结构式,结构简式和键线式1结构式把所有的键都用短横线表示出来2结构简式把所有的键都省略,除了碳碳双键这一特殊例子。
3键线式4.分子式五.有机物的命名1烷烃(1)牢记“长、多、近、小”;①主链要长:最长碳链作主链,主链碳数称某烷。
②支链数目要多:两链等长时,则选择连接支链数目多者为主链。
③起点碳离支链要近:支链近端为起点,依次编号定支链。
④支链位置序号之和要小:主链上有多个取代基时,按取代基所在位置序号之和较小给取代基定位。
(2)牢记五个“必须”;①注明取代基的位置时,必须用阿拉伯数字2、3、4…表示。
②相同取代基合并后的总数,必须用汉字二、三、四…表示。
③名称中的阿拉伯数字2、3、4相邻时,必须用逗号“,”隔开。
④名称中凡阿拉伯数字与汉字相邻时,都必须用短线“—”隔开。
⑤如果有不同的取代基,不管取代基的位次大小如何,都必须把简单的写在前面,复杂的写在后面。
(3)写法:取代基位置→取代基数目→取代基名称→烃名称。
以2,3—二甲基己烷为例,对一般有机物的命名可分析如下图:其它烃或烃的衍生物命名时,需考虑官能团,选主链时应是含官能团在内的最长碳链为主链,编号时应是离官能团最近的一端编号,命名时应标出官能团的2烯烃3炔烃2008-11-19正四面体介于单双键之间C C=C。
高二化学有机化合物的结构与性质
碳碳叁键键能小 于单键键能的3倍、 小于单键和双键的键 能之和。
单键不容易断裂,饱和碳原子性质稳定,烷烃 不能发生加成反应。不饱和碳原子性质较活泼, 烯烃、炔烃容易发生加成反应。
追根寻源
• 甲烷分子的空间构型为什么是正四面体?
• 碳碳双分子中碳碳键为何特殊?
σ键、π键 和大π键
第2节 有机化合物 的结构与性质
联想质疑
燃烧、取代反应 甲烷 燃烧、与高锰酸钾 溶液反应、加成反 应 燃烧、取代反应、 加成反应
乙烯
苯
结构
性质
知识支持 共价键的分类及定义
• 单键:两个原子之间共用一对电子 的共价键。 • 双键:两个原子之间共用两对电子 的共价键。 • 叁键:两个原子之间共用三对电子 的共价键。
位
B、两甲基在不同一个碳原子上
4、主链少三个碳原子
C ∣ C -C - C - C - C - C - C ∣ ∣ C C
4、主链少三个碳原子
C C ∣ ∣ C -C - C - C ∣ ∣ C C
【观察】分子式为C6H14的烷烃在结构式中含有3个 甲基的同分异构体有( )个 ( A ) 2 个 ( B) 3 个 (C)4 个 (D) 5 个
“头碰头”重叠——σ键 “肩并肩”重叠——π 键 苯分子中的大π键
轨道杂化理论: 成键过程中,由于原子间的相互影响, 同一原子中几个能量相近的不同类型的原 子轨道,可以线性组合,重新分配能量和 确定空间,组成数目相等的新的原子轨道
sp杂化 sp2杂化
杂化
杂化
乙烯、乙炔分子中轨道杂化和重叠方式示意图
请你根据上表所提供的数据,从键能和键长的 角度结合乙烷、乙烯和乙炔的性质考虑下列问题, 并与同组同学进行交流和讨论。 1、乙烯为什么容易发生加成反应?
有机物的结构简式
有机物的结构简式编名称分子式结构,简,式号烷烃1甲烷ch42乙烷ch26ch—ch、chch、3333ch—ch—ch、chchch、3233233丙烷ch38、4正丁烷chch—ch—ch—ch、chchchch、41032233223 2—甲基丙烷5ch410,异丁烷,、ch,ch,、33ch—ch—ch—ch—ch、chchchchch、32223322236,正,戊烷ch512ch,ch,ch、32332—甲基丁烷7ch,异戊烷,5122,2—二甲基丙烷8ch512,新戊烷,、c,ch,34ch—ch—ch—ch—ch—ch、3222239正己烷ch614chchchchchch、ch,ch,ch、32222332432—甲基戊烷10ch614,异己烷,113—甲基戊烷ch6142,3—二甲基丁12ch614烷2,2—二甲基丁13ch614烷ch—ch—ch—ch—ch—ch—ch、322222314,正,庚烷ch716chchchchchchch、ch,ch,ch322222332532—甲基己烷15ch716,异庚烷,163—甲基己烷ch7162,2—二甲基戊17ch716烷3,3—二甲基戊18ch716烷2,3—二甲基戊19ch716烷2,4—二甲基戊20ch716烷2,2,3—三甲21ch716基丁烷3—乙基戊烷22ch7162,2,4,4—四甲23ch920基戊烷2,3—二甲基—24ch9203—乙基戊烷3,3,4—三甲基25ch920己烷2,2,4—三甲基26ch818戊烷2,3,3—三甲基27ch818戊烷2,2,3—三甲基28ch818戊烷2,3,4—三甲基29ch818戊烷环烷烃30环丙烷ch36、31环戊烷ch510 、32环己烷ch612、、33甲基环己烷ch714、34乙基环己烷ch816顺对二甲基环35ch816己烷反对二甲基环36ch816己烷烯烃37乙烯ch24ch,ch、2233丙烯chch—ch,ch、chch,ch363232341—丁烯chch,ch—ch—ch、48223352—丁烯chch—ch,ch—ch、chch,chch48333336甲基丙烯ch48ch,ch—ch—ch—ch、2223371—戊烯ch510ch,chchchch、ch,ch,ch,ch22232223ch—ch,ch—ch—ch、323382—戊烯ch510chch,chchch3232—甲基—1—39ch510丁烯3—甲基—1—40ch510丁烯2—甲基—2—41ch510丁烯421,3—丁二烯chch,ch—ch,ch、ch,chch,ch4622222—甲基—1,3—丁二烯43ch58,异戊二烯,2,2,5,5—四甲44ch1020基—3—己烯、,ch,h,chc,ch,33332,4,4—三甲基45ch816—1—戊烯2,4,4—三甲基46ch816—2—戊烯3—甲基—1,347ch814—己二烯2—甲基—483,2,2—乙基,—ch9161,3—丁二烯3,4—二甲基—492—乙基—1—ch918戊烯3—乙基—1,350ch712—戊二烯514—甲基环己烯ch712炔烃52乙炔chhc?ch、h—c?c—h22丙炔hc?c—ch、ch?h53ch3334541—丁炔chhc?c—ch—ch、ch?hch、462323552—丁炔chch—c?c—ch、chc?h463333561—戊炔chhc?c—ch—ch—ch、ch?hchch、58223223572—戊炔chch—c?c—ch—ch、chc?hch58323323 3—甲基—1—58ch58丁炔3—甲基己—359ch710—烯炔3—乙基戊—360ch710—烯炔芳香烃61苯ch66、、62甲苯ch78、、ch—ch65363乙苯ch810、、ch—ch652564邻二甲苯ch810间二甲苯65ch81066对二甲苯ch81067间甲乙苯ch912戊苯68ch1116chch、65511692—苯基戊烷ch11162—甲基—1—70ch1116苯基丁烷3—甲基—1—71ch1116苯基丁烷2—甲基—3—72ch1116苯基丁烷2,2—二甲基—73ch11161—苯基丙烷、chchc,ch,65233743—苯基戊烷ch1116、chch,chch,6523275苯乙烯ch88 、、chch,ch65276苯乙炔ch86、chc,ch6577联二苯ch1210、ch —ch、,ch,6565652二苯甲烷78ch1212、ch,ch,265279萘ch10880,—甲萘ch111081,—甲萘ch1110821,6—二甲萘ch1212831,5—二甲萘ch121284,—乙萘ch121285,—乙萘ch121286蒽ch141087菲ch141088并四苯ch181289并五苯ch2214 90ch161091ch2212卤代烃92一氯甲烷chclchcl3393二氯甲烷chclchcl222294三氯甲烷,氯仿,chclchcl3395四氯化碳ll4496三碘甲烷,碘仿,chichi3397四氟化碳cfcf4498四溴化碳cbrcbr4499四碘化碳cici44100氯乙烷chclchcl、chchcl252532101溴乙烷chbrchbr、chchbr252532102氯苯chcl65、chcl65103溴苯chbr65、、chbr65104四氟乙烯cfcf,cf24221,1,2,2—四溴105chbrchbr—chbr22422乙烷1061,2—二溴乙烯chbrbrch,chbr222107氯乙烯chclch,chcl2323,4—二溴—1108chbrch,ch—chbr—chbr46222—丁烯1,4—二溴—2109chbrchbr—ch,ch—chbr46222—丁烯110邻氯甲苯chcl77111间氯甲苯chcl77112对氯甲苯chcl772,4,6—三溴甲113chbr753苯114苄氯,苯甲氯,chcl771154—溴辛烷chbr817、ch,ch,chbr,ch,ch323223 醇116甲醇choch—oh、choh433117乙醇choch—oh、choh、chchoh262525321181—丙醇choch—oh、choh、chchchoh383737322 2—丙醇,异丙119cho38醇,1—丁醇h—oh、choh、ch,ch,ohc120cho4949323410,正丁醇, 2—丁醇121cho410,异丁醇,2—甲基—1—122cho410丙醇2—甲基—2—123cho410丙醇、2,2—二甲基—124cho5121—丙醇2—甲基—2—125cho512丁醇、、126乙二醇cho262、hohhoh、,choh,2222127丙三醇cho383 、ch,oh,3532—丁炔—1,4128cho462二醇129氨基乙醇chno272,2—二甲基—130cho6141—丁醇3—甲基—1—131cho512丁醇2—戊醇132cho512、1333—戊醇cho5121341,2—丁二醇cho411421352—氯乙醇chocl25136苯甲醇,苄醇,cho78137环丙醇cho36138对甲基环己醇cho714139邻甲基环己醇cho714醚140甲醚choch—o—ch、choch263333141甲乙醚choch—o—ch、choch、chochch38325325323h—o—ch、choch、c25252525142乙醚cho410chchochch、,ch,o3223252143甲正丙醚choch—o—ch、choch、chochchch4103373373223144甲异丙醚cho410choch,ch,、332145甲苯醚cho718146异丙醚cho614、,ch,choch,ch,3232环氧烷147环氧乙烷cho24148二氧杂环己烷cho48149甲基环氧乙烷cho36酚150苯酚cho66、1,2,3—苯三酚151cho663,邻苯三酚,1,3,5—苯三酚152cho663,间苯三酚,2,4,6—三溴苯153chobr633酚、154邻甲苯酚cho78155间甲酚cho78156对甲酚cho782,4,6—三硝基157chno6337苯酚醛和酮158甲醛cho2hcho、乙醛159cho24chcho、3160丙醛chochchcho、chcho363225161丁醛chochchchcho、chcho48322371622—甲基丙醛cho48、,ch,chcho321633—丁羟醛cho482164乙二醛cho222、、,cho,2165丙酮cho36、、,ch,co、chcoch3233166丁酮cho48、chcochch323167丙二烯酮co32o,c,c,c,o、邻乙酰基苯乙168醛羧酸169甲酸cho22hcooh、、170乙酸cho242chcooh、3171丙酸cho362chchcooh、chcooh、3225172丁酸chochchchcooh、chcooh48232237173甲基丙酸cho482、,ch,chcooh32174硬脂酸cho18362chcooh、1735175软脂酸cho16322chcooh、1531油酸176chochcooh183421733、、177苯甲酸cho762chcooh、65178苯正丙酸cho9102、chchchcooh6522179乙二酸cho224、、,cooh,、hooc—cooh2180丙二酸cho344、hooc—ch—cooh、ch,cooh,222181丁二酸cho464、hooc,ch,cooh、,chcooh,2222182顺丁烯二酸cho444183反丁烯二酸cho444184邻苯二甲酸cho864185间苯二甲酸cho864186对苯二甲酸cho864187甲,酸,酐cho,hco,o2232188乙酐cho463、,chco,o32乳酸189cho363,,—羟基丙酸,、,—羟基丙酸190cho3632,2—二甲基丙191cho4102酸、,ch,ooh333—甲基戊—4192cho6122—烯酸193邻羟基苯甲酸cho763194对羟基苯甲酸cho763、间羟基苯甲酸195cho763对羟基苯—2—196cho983丙烯酸间羟基羧基苯197cho884甲醇酯198甲酸甲酯chohcooch、2423199甲酸乙酯chohcooch、hcoochch3622523乙酸甲酯200cho362、chcooch33201乙酸乙酯cho、482chcooch、chcoochch325323202甲酸正丙酯chohcooch、hcoochchch48237223203甲酸异丙酯cho482、、hcooch,ch,32甲酸新戊酯、204甲酸,2,2—二甲cho6122基,丙酯、hcoochc,ch,233甲酸—2—甲基205cho6122丁酯206甲酸异戊酯cho6122、hcoo,ch,ch,ch,2232207对乙酸甲苯酯cho9102丙酸甲酯chchcooch、chcooch208cho323253482对羟基苯甲酸209cho883甲酯2,2—二甲基丙210酸甲酯、cho6122新戊酸甲酯、,ch,cooch333211硬脂酸甘油酯cho571106、,chcoo,ch173535212软脂酸甘油酯cho511706、,chcoo,ch153135213油脂酸甘油酯cho571046、,chcoo,ch173335214苯甲酸甲酯cho882、chcooch653215硝酸乙酯chnochono、chchono2532523223—羟基丙酸正216cho6123丙酯、ho,ch,coo,ch,ch22223 2—羟基丙酸正217cho6123丙酯218丙二酸二乙酯cho7124 、chooc—ch—cooch252252—丁酮酸异丁219cho8143酯220乙酸对甲酚酯cho9102221甲酸氯甲,醇,酯chocl232222异戊酸异戊酯cho10202、,ch,chcoo,ch,ch,ch,32232乙二酸乙二,醇,223cho444酯三硝酸甘油酯224chno3539,硝化甘油,硝基化合物225硝基苯chno652、、ch—no652226硝基甲烷chnoch—no、chno323232227硝基乙烷chnoch—no、chno、chchno252252252322 2,4,6—三硝基228chno7536甲苯,tnt,229,—硝基萘chno1072230,—硝基萘chno10721,8—二硝基萘231chno106242321,5—二硝基萘chno10624糖类233葡萄糖cho6126、choh,choh,cho24234果糖chochoh,choh,cochoh6126232235蔗糖chocho122211122211236麦芽糖chocho122211122211237淀粉,cho,,cho,6115n122211n238纤维素,cho,6115n、[cho,oh,]6723n氨基酸甘氨酸239chno252,氨基乙酸,丙氨酸240chno372,—氨基丙酸苯丙氨酸241,—氨基—,—chno8112苯基丙酸谷氨酸242chno594,—氨基戊二酸高分子化合物243聚乙烯,ch,24n244聚丙烯,ch,36n245聚氯乙烯,chcl,23n246聚苯乙烯,ch,88n、有机玻璃,聚甲247,cho,582n基丙烯酸甲酯,、聚丙烯腈248,ch,23n,人造羊毛,聚四氟乙烯249,cf,24n,塑料王,250酚醛塑料,电木,,cho,76n251脲醛塑料,电玉,,chno,42n252环氧树脂,cho,19203n聚对苯二甲酸253乙二醇酯,cho,10103n,涤纶、的确良,聚己内酰胺254,chno,611n,绵纶,聚乙烯醇缩甲255醛,cho,582n,维尼纶,256丁苯橡胶,ch,1214n257顺丁橡胶,ch,46n258氯丁橡胶,chcl,45n259丁腈橡胶,ch,79n260聚硫橡胶,chs,244n261硅橡胶,chsio,26n262丁基橡胶异戊橡胶263,ch,58n,合成天然橡胶,264聚乳酸,cho,332n265聚丙酸甲酯,cho,462n266聚丙酸正丁酯,cho,7122n267聚乙丙丁酯,ch,918n268人造象牙,cho,2n289聚环氧乙烷,cho,24n290聚乙炔,ch,22n291,ch,916n292戊苯橡胶,ch,1316n293,ch,1010n294,ch,1010n295nomex纤维,chno,141022n296,cho,15166n其它297二恶英,chocl,12424n298维生素c,cho,686n299立方烷,ch,88n2,3,4—三羟基苯甲酸—2,3—300,cho,14109n二羟基—5—羧基苯,酚,酯301苯磺酸chso663302对氨基苯磺酸chnso1093303吗啡chno17173304葡萄糖二酸cho6108三硝酸纤维素305,chno,6739n酯丙二酰氯306chocl3222307丙二酰胺chno36223,7—二甲基—308cho10162,6—辛二烯醛三聚甲醛309cho363310氨基树脂chn66621 / 21__来源网络整理,仅作为学习参考。
常见有机化合物缩写及结构式
常见的有机化合物缩写及结构式A/MMA丙烯腈/甲基丙烯酸甲酯共聚物AA丙烯酸AAS丙烯酸酯-丙烯酸酯-苯乙烯共聚物ABFN 偶氮(二)甲酰胺ABN 偶氮(二)异丁腈ABPS 壬基苯氧基丙烷磺酸钠B 英文缩写全称BAA 正丁醛苯胺缩合物BAC 碱式氯化铝BACN 新型阻燃剂BAD 双水杨酸双酚A酯BAL 2,3-巯(基)丙醇BBP 邻苯二甲酸丁苄酯BBS N-叔丁基-乙-苯并噻唑次磺酰胺BC 叶酸BCD β-环糊精BCG 苯顺二醇BCNU 氯化亚硝脲BD 丁二烯BE 丙烯酸乳胶外墙涂料BEE 苯偶姻乙醚BFRM 硼纤维增强塑料BG 丁二醇BGE 反应性稀释剂BHA 特丁基-4羟基茴香醚BHT 二丁基羟基甲苯BL 丁内酯BLE 丙酮-二苯胺高温缩合物BLP 粉末涂料流平剂BMA 甲基丙烯酸丁酯BMC 团状模塑料BMU 氨基树脂皮革鞣剂BN 氮化硼BNE 新型环氧树脂BNS β-萘磺酸甲醛低缩合物BOA 己二酸辛苄酯BOP 邻苯二甲酰丁辛酯BOPP 双轴向聚丙烯BP 苯甲醇BPA 双酚ABPBG 邻苯二甲酸丁(乙醇酸乙酯)酯BPF 双酚FBPMC 2-仲丁基苯基-N-甲基氨基酸酯BPO 过氧化苯甲酰BPP 过氧化特戊酸特丁酯BPPD 过氧化二碳酸二苯氧化酯BPS 4,4’-硫代双(6-特丁基-3-甲基苯酚) BPTP 聚对苯二甲酸丁二醇酯BR 丁二烯橡胶BRN 青红光硫化黑BROC 二溴(代)甲酚环氧丙基醚BS 丁二烯-苯乙烯共聚物BS-1S 新型密封胶BSH 苯磺酰肼BSU N,N’-双(三甲基硅烷)脲BT 聚丁烯-1热塑性塑料BTA 苯并三唑BTX 苯-甲苯-二甲苯混合物BX 渗透剂BXA 己二酸二丁基二甘酯BZ 二正丁基二硫代氨基甲酸锌C 英文缩写全称CA 醋酸纤维素CAB 醋酸-丁酸纤维素CAN 醋酸-硝酸纤维素CAP 醋酸-丙酸纤维素CBA 化学发泡剂CDP 磷酸甲酚二苯酯CF 甲醛-甲酚树脂,碳纤维CFE 氯氟乙烯CFM 碳纤维密封填料CFRP 碳纤维增强塑料CLF 含氯纤维CMC 羧甲基纤维素CMCNa 羧甲基纤维素钠CMD 代尼尔纤维CMS 羧甲基淀粉D 英文缩写全称DABCO 三乙烯二胺DAF 富马酸二烯丙酯DAIP间苯二甲酸二烯丙酯DAM 马来酸二烯丙酯DAP 间苯二甲酸二烯丙酯DA TBP 四溴邻苯二甲酸二烯丙酯DBA 己二酸二丁酯DBEP 邻苯二甲酸二丁氧乙酯DBP 邻苯二甲酸二丁酯DBR 二苯甲酰间苯二酚DBS 癸二酸二癸酯DBU 1,8二氮杂双环十一碳-7-烯DCCA 二氯异氰脲酸DCCK 二氯异氰脲酸钾DCCNa 二氯异氰脲酸钠DCHP 邻苯二甲酸二环乙酯DCPD 过氧化二碳酸二环乙酯DDA 己二酸二癸酯DDP 邻苯二甲酸二癸酯DEAE 二乙胺基乙基纤维素DEP 邻苯二甲酸二乙酯DETA 二乙撑三胺DFA 薄膜胶粘剂DHA 己二酸二己酯DHP 邻苯二甲酸二己酯DHS 癸二酸二己酯DIBA 己二酸二异丁酯DIDA 己二酸二异癸酯DIDG 戊二酸二异癸酯DIDP 邻苯二甲酸二异癸酯DINA 己二酸二异壬酯DINP 邻苯二甲酸二异壬酯DINZ 壬二酸二异壬酯DIOA 己酸二异辛酯< lan>E 英文缩写全称E/EA 乙烯/丙烯酸乙酯共聚物E/P 乙烯/丙烯共聚物E/P/D 乙烯/丙烯/二烯三元共聚物E/TEE 乙烯/四氟乙烯共聚物E/V AC 乙烯/醋酸乙烯酯共聚物E/V AL 乙烯/乙烯醇共聚物EAA 乙烯-丙烯酸共聚物EAK 乙基戊丙酮EBM 挤出吹塑模塑EC 乙基纤维素ECB 乙烯共聚物和沥青的共混物ECD 环氧氯丙烷橡胶ECTEE 聚(乙烯-三氟氯乙烯)ED-3 环氧酯EDC 二氯乙烷EDTA 乙二胺四醋酸EEA 乙烯-醋酸丙烯共聚物EG 乙二醇2-EH :异辛醇EO 环氧乙烷EOT 聚乙烯硫醚EP 环氧树脂EPI 环氧氯丙烷EPM 乙烯-丙烯共聚物EPOR 三元乙丙橡胶EPR 乙丙橡胶EPS 可发性聚苯乙烯EPSAN 乙烯-丙烯-苯乙烯-丙烯腈共聚物EPT 乙烯丙烯三元共聚物EPVC 乳液法聚氯乙烯EU 聚醚型聚氨酯EV A 乙烯-醋酸乙烯共聚物EVE 乙烯基乙基醚EXP 醋酸乙烯-乙烯-丙烯酸酯三元共聚乳液F 英文缩写全称F/V AL 乙烯/乙烯醇共聚物F-23 四氟乙烯-偏氯乙烯共聚物F-30 三氟氯乙烯-乙烯共聚物F-40 四氟氯乙烯-乙烯共聚物FDY 丙纶全牵伸丝FEP 全氟(乙烯-丙烯)共聚物FNG 耐水硅胶FPM 氟橡胶FRA 纤维增强丙烯酸酯FRC 阻燃粘胶纤维FRP 纤维增强塑料FRPA-101 玻璃纤维增强聚癸二酸癸胺(玻璃纤维增强尼龙1010树脂) FRPA-610 玻璃纤维增强聚癸二酰乙二胺(玻璃纤维增强尼龙610树脂) FWA 荧光增白剂G 英文缩写全称GF 玻璃纤维GFRP 玻璃纤维增强塑料GFRTP 玻璃纤维增强热塑性塑料促进剂GOF 石英光纤GPS 通用聚苯乙烯GR-1 异丁橡胶GR-N 丁腈橡胶GR-S 丁苯橡胶GRTP 玻璃纤维增强热塑性塑料GUV 紫外光固化硅橡胶涂料GX 邻二甲苯GY 厌氧胶H 英文缩写全称H 乌洛托品HDI 六甲撑二异氰酸酯HDPE 低压聚乙烯(高密度)HEDP 1-羟基乙叉-1,1-二膦酸HFP 六氟丙烯HIPS 高抗冲聚苯乙烯HLA 天然聚合物透明质胶HLD 树脂性氯丁胶HM 高甲氧基果胶HMC 高强度模塑料HMF 非干性密封胶HOPP 均聚聚丙烯HPC 羟丙基纤维素HPMC 羟丙基甲基纤维素HPMCP 羟丙基甲基纤维素邻苯二甲酸酯HPT 六甲基磷酸三酰胺HS 六苯乙烯HTPS 高冲击聚苯乙烯I 英文缩写全称IEN 互贯网络弹性体IHPN 互贯网络均聚物IIR 异丁烯-异戊二烯橡胶IO 离子聚合物IPA 异丙醇IPN 互贯网络聚合物IR 异戊二烯橡胶IVE 异丁基乙烯基醚J 英文缩写全称JSF 聚乙烯醇缩醛胶JZ 塑胶粘合剂K 英文缩写全称KSG 空分硅胶L 英文缩写全称LAS 十二烷基苯磺酸钠LCM 液态固化剂LDJ 低毒胶粘剂LDN 氯丁胶粘剂LDPE 高压聚乙烯(低密度)LDR 氯丁橡胶LF 脲LGP 液化石油气LHPC 低替代度羟丙基纤维素LIM 液体侵渍模塑LIPN 乳胶互贯网络聚合物LJ 接体型氯丁橡胶LLDPE 线性低密度聚乙烯LM 低甲氧基果胶LMG 液态甲烷气LMWPE 低分子量聚乙稀LN 液态氮LRM 液态反应模塑LRMR 增强液体反应模塑LSR 羧基氯丁乳胶M 英文缩写全称MA 丙烯酸甲酯MAA 甲基丙烯酸MABS 甲基丙烯酸甲酯-丙烯腈-丁二烯-苯乙烯共聚物MAL 甲基丙烯醛MBS 甲基丙烯酸甲酯-丁二烯-苯乙烯共聚物MBTE 甲基叔丁基醚MC 甲基纤维素MCA 三聚氰胺氰脲酸盐MCPA-6 改性聚己内酰胺(铸型尼龙6)MCR 改性氯丁冷粘鞋用胶MDI 3,3’-二甲基-4,4’-二氨基二苯甲烷MDI 二苯甲烷二异氰酸酯(甲撑二苯基二异氰酸酯) MDPE 中压聚乙烯(高密度)MEK 丁酮(甲乙酮)MEKP 过氧化甲乙酮MES 脂肪酸甲酯磺酸盐MF 三聚氰胺-甲醛树脂M-HIPS 改性高冲聚苯乙烯MIBK 甲基异丁基酮MMA 甲基丙烯酸甲酯MMF 甲基甲酰胺MNA 甲基丙烯腈MPEG 乙醇酸乙酯MPF 三聚氨胺-酚醛树脂MPK 甲基丙基甲酮M-PP 改性聚丙烯MPPO 改性聚苯醚MPS 改性聚苯乙烯MS 苯乙烯-甲基丙烯酸甲酯树脂MSO 石油醚MTBE 甲基叔丁基醚MTT 氯丁胶新型交联剂MWR 旋转模塑MXD-10/6 醇溶三元共聚尼龙MXDP 间苯二甲基二胺N 英文缩写全称NBR 丁腈橡胶NDI 二异氰酸萘酯NDOP 邻苯二甲酸正癸辛酯NHDP 邻苯二甲酸己正癸酯NHTM 偏苯三酸正己酯NINS 癸二酸二异辛酯NLS 正硬脂酸铅NMP N-甲基吡咯烷酮NODA 己二酸正辛正癸酯NODP 邻苯二甲酸正辛正癸酯NPE 壬基酚聚氧乙烯醚NR 天然橡胶O 英文缩写全称OBP 邻苯二甲酸辛苄酯ODA 己二酸异辛癸酯ODPP 磷酸辛二苯酯OIDD 邻苯二甲酸正辛异癸酯OPP 定向聚丙烯(薄膜)OPS 定向聚苯乙烯(薄膜)OPVC 正向聚氯乙烯OT 气熔胶P 英文缩写全称PA 聚酰胺(尼龙)PA-1010 聚癸二酸癸二胺(尼龙1010) PA-11 聚十一酰胺(尼龙11)PA-12 聚十二酰胺(尼龙12)PA-6 聚己内酰胺(尼龙6)PA-610 聚癸二酰乙二胺(尼龙610)PA-612 聚十二烷二酰乙二胺(尼龙612) PA-66 聚己二酸己二胺(尼龙66)PA-8 聚辛酰胺(尼龙8)PA-9 聚9-氨基壬酸(尼龙9)PAA 聚丙烯酸PAAS 水质稳定剂PABM 聚氨基双马来酰亚胺PAC 聚氯化铝PAEK 聚芳基醚酮PAI 聚酰胺-酰亚胺PAM 聚丙烯酰胺PAMBA 抗血纤溶芳酸PAMS 聚α-甲基苯乙烯PAN 聚丙烯腈PAP 对氨基苯酚PAPA 聚壬二酐PAPI 多亚甲基多苯基异氰酸酯PAR 聚芳酰胺PAR 聚芳酯(双酚A型)PAS 聚芳砜(聚芳基硫醚)PB 聚丁二烯-[1,3]PBAN 聚(丁二烯-丙烯腈)PBI 聚苯并咪唑PBMA 聚甲基丙烯酸正丁酯PBN 聚萘二酸丁醇酯PBR 丙烯-丁二烯橡胶PBS 聚(丁二烯-苯乙烯)PBS 聚(丁二烯-苯乙烯)PBT 聚对苯二甲酸丁二酯PC 聚碳酸酯PC/ABS 聚碳酸酯/ABS树脂共混合金PC/PBT 聚碳酸酯/聚对苯二甲酸丁二醇酯弹性体共混合金PCD 聚羰二酰亚胺PCDT 聚(1,4-环己烯二亚甲基对苯二甲酸酯)PCE 四氯乙烯PCMX 对氯间二甲酚PCT 聚对苯二甲酸环己烷对二甲醇酯PCT 聚己内酰胺PCTEE 聚三氟氯乙烯PD 二羟基聚醚PDAIP 聚间苯二甲酸二烯丙酯PDAP 聚对苯二甲酸二烯丙酯PDMS 聚二甲基硅氧烷R 英文缩写全称RE 橡胶粘合剂RF 间苯二酚-甲醛树脂RFL 间苯二酚-甲醛乳胶RP 增强塑料RP/C 增强复合材料RX 橡胶软化剂S 英文缩写全称S/MS 苯乙烯-α-甲基苯乙烯共聚物SAN 苯乙烯-丙烯腈共聚物SAS 仲烷基磺酸钠SB 苯乙烯-丁二烯共聚物SBR 丁苯橡胶SBS 苯乙烯-丁二烯-苯乙烯嵌段共聚物SC 硅橡胶气调织物膜SDDC N,N-二甲基硫代氨基甲酸钠SE 磺乙基纤维素SGA 丙烯酸酯胶SI 聚硅氧烷SIS 苯乙烯-异戊二烯-苯乙烯嵌段共聚物SIS/SEBS 苯乙烯-乙烯-丁二烯-苯乙烯共聚物SM 苯乙烯SMA 苯乙烯-顺丁烯二酸酐共聚物SPP :间规聚苯乙烯SPVC 悬浮法聚氯乙烯SR 合成橡胶ST 矿物纤维T 英文缩写全称TAC 三聚氰酸三烯丙酯TAME 甲基叔戊基醚TAP 磷酸三烯丙酯TBE 四溴乙烷TBP 磷酸三丁酯THF 四氢呋喃TCA 三醋酸纤维素TCCA 三氯异氰脲酸TCEF 磷酸三氯乙酯TCF 磷酸三甲酚酯TCPP 磷酸三氯丙酯TDI 甲苯二异氰酸酯TEA 三乙胺TEAE 三乙氨基乙基纤维素TEDA 三乙二胺TEFC 三氟氯乙烯TEP 磷酸三乙酯TFE 四氟乙烯THF 四氢呋喃TLCP 热散液晶聚酯TMP 三羟甲基丙烷TMPD 三甲基戊二醇TMTD 二硫化四甲基秋兰姆(硫化促进剂TT) TNP 三壬基苯基亚磷酸酯TPA 对苯二甲酸TPE 磷酸三苯酯TPS 韧性聚苯乙烯TPU 热塑性聚氨酯树脂TR 聚硫橡胶TRPP 纤维增强聚丙烯TR-RFT 纤维增强聚对苯二甲酸丁二醇酯TRTP 纤维增强热塑性塑料TTP 磷酸二甲苯酯U 英文缩写全称U 脲UF 脲甲醛树脂UHMWPE 超高分子量聚乙烯UP 不饱和聚酯V 英文缩写全称V AC 醋酸乙烯酯V AE 乙烯-醋酸乙烯共聚物V AM 醋酸乙烯V AMA 醋酸乙烯-顺丁烯二酐共聚物VC 氯乙烯VC/CDC 氯乙烯/偏二氯乙烯共聚物VC/E 氯乙烯/乙烯共聚物VC/E/MA 氯乙烯/乙烯/丙烯酸甲酯共聚物VC/E/V AC 氯乙烯/乙烯/醋酸乙烯酯共聚物VC/MA 氯乙烯/丙烯酸甲酯共聚物VC/MMA 氯乙烯/甲基丙烯酸甲酯共聚物VC/OA 氯乙烯/丙烯酸辛酯共聚物VC/V AC 氯乙烯/醋酸乙烯酯共聚物VCM 氯乙烯(单体)VCP 氯乙烯-丙烯共聚物VCS 丙烯腈-氯化聚乙烯-苯乙烯共聚物VDC 偏二氯乙烯VPC 硫化聚乙烯VTPS 特种橡胶偶联剂W 英文缩写全称WF 新型橡塑填料WP 织物涂层胶WRS 聚苯乙烯球形细粒X 英文缩写全称XF 二甲苯-甲醛树脂XMC 复合材料Y 英文缩写全称YH 改性氯丁胶YM 聚丙烯酸酯压敏胶乳YWG 液相色谱无定型微粒硅胶Z 英文缩写全称ZE 玉米纤维ZH 溶剂型氯化天然橡胶胶粘剂ZN 粉状脲醛树脂胶此外,有关化学试剂按杂质含量的多少分:实验试剂:缩写为LR,又称四级试剂。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机结构、常见有机物结构式 .............................................................................. 1 1烷 ........................................................................................... 1 2 .环烷 ........................................................................................ 2 3•烯 .......................................................................................... 2 4. 炔 ......................................................................................... 2 5. 二烯 ....................................................................................... 2 6 .芳香物 ...................................................................................... 2 7.醇 .......................................................................................... 3 8•酚 .......................................................................................... 3 9•醛 .......................................................................................... 3 10.酮 ......................................................................................... 3 11 •羧酸 ....................................................................................... 4 12. 酯 ......................................................................................... 4 13. 糖 ......................................................................................... 4 14 .氨基酸 .................................................................................... 4 15 .其它 ...................................................................................... 4 、聚合反应 ...................................................................................... 4 1. 单烯加聚 2. 二烯加聚、常见有机物结构式CH 3 CH 3 CH 3CH 3CHCH 3CH 3—CH —CH —C_CH 2—CH 3CH 3 CH 3 I IH H -CH- -C-H-C-CICI —C —CIIIICl HH IH —C —HI HH — CIH-H — CIH-HHHIH_C_HH H HI I IH _C _C _C _H H H HH H H HIlliH _C _C _C _C_HH H H H2.环烷 CH 2CH 2—CH 2 CH 2—CH 2 I I CH2YH 23.烯 H— c- H — c -HHcHc H3HH )/:ccHCHC= C 『 、CH4•炔 180 _H —C±C*H5.二烯 CH 2=CH —C=CH 2 C H 3 6•芳香物 HH H1209C H eC h e」 LH 或CH 3 i CH3 厂CH 3 XX -CH 3CH 3 H CH 3CH=CH 2C=CHCH=CH 2C 三CHCH 37•醇 CH2YH 2 HOCH 2HOCH 2 OTOJOH 2 CH 2OH CHOHCHQHHOCH 2 HOCH HOCH 2CH2— O —NO20H — O —NO 2 CH 2—O —NO 28•酚 CH 3 OH OH j^pCH2OHO OH 5 OC H 3 ONaONaBrNO 2CH OHOHH9.醛 IIR_C_H 9CHH- 9CO 11 —c_IICH3—C —HH O H_bbH 1 HO O ll llH —C —C —HCHO CHO10.酮 O c9COCH 3—C —CH 311 •羧酸CH3—C 0:O(乙酸酐)CH3—c沁OO11c —OH12.酯13•糖14. 氨基酸15•其它二、聚合反应1.单烯加聚nCH 2= CH 2 -fCH^CH 2]n CH 3C H 3n CH = CH 2 -"[ CH —CH 2】nHI N--HI N CO(NH 2)2: HO11—c —0—H O 11H —C —OHO H —C —ONaOCH 3—C —OHHO —C —C —OH COOHO O II ,II,RCORR —C —O —RO - ohcCOOC 2H 5 ICOOC 2H 5CH 3COOCH 2 CH 3C00CH 2卡出- 0-NO 2yH —O — NO 2 CH 2—0—NO 2C 17H 35COOCH 2C 17H 35COOCHC 17H 35COOCH 2R 1COOCH 2R 2COOCHR 3COOCH 2三硝酸甘油酯o 00亠二ONOHN 20 <O<O<O - --HIC199H - -- H H HCH2-CH-CH-CH-CH —CH0 OH OH OH OH OH弹_ 甘―酋―CH _ C_ CH 2OH OH OH OH 0 OHR —yHCOOHNH 2HOOCCH 2CH 2yHCOONaNH 2CH 2COOH NH 2—CH 2—CH 2—CH 3—CH 一CH 2—COOH「A y w(毎超觀蛊)uz匚J-L J ll<世 OHOHU+-u T o T oO Z H(L——U CXI)+H0F0—0——0ZH0ZH001-H—HOZHOZHOOHU+ HO —O —O —OHU88 t:T oH - O£(L ——U)十HOF10—0+H ——H08H0COH0U-) -OCHOc oT o £0—4HHO —ZHO4 Z H OA -—H O H ZH OU半£0—工H工0—£0十1ZH O H I0II 0 叽HouMm_-^x o l x o l £o l £o ^ I ^10110c +£0氏Houe 5-£5 p -c p q =pq b up q —010—^—^— L O —O —5—O-十f v H px u +V H只uL-一一- 」-:->-」d、E 0 r opqH Q Hoz T o oo o -——(e H O O —ZHowH Q T o oo oHO O-I Z H O+TO £O £OO O O -«T O OI£O CNO— T o l £o —-0-l£0— I o —0 I£O I T O —N o NO4HO —£O十f hoh£ou-0 -0华£。
— 工2—。
