6晶体结构详解
常见的晶体结构

常见的晶体结构晶体结构是材料科学中的基础概念之一,也是研究材料性质和应用的重要手段。
通过研究晶体结构,可以了解材料的晶格结构、晶体缺陷、晶体生长以及物理性质等信息。
在本文中,我们将主要介绍几种常见的晶体结构。
1.立方晶系。
立方晶系是最简单、最对称的晶体结构之一,其中所有三个晶轴都是等长且互相垂直。
立方晶系包括体心立方晶体(bcc)和面心立方晶体(fcc)。
在体心立方晶体中,每个原子位于一个正八面体的中心和另外八个顶点之一,而在面心立方晶体中,每个原子位于一个正方形面的中心和其四个相邻原子分别组成的正方形的四个角上。
2.六方晶系。
六方晶系包括一个长度为a和两个垂直于晶轴的长度为c的晶轴,其正交晶面呈六边形。
六方晶系中最常见的是六方密堆积结构,其中每个原子最近的邻居原子共有12个,六个在同一水平面上,另外六个分别位于上下两个平面上。
3.正交晶系。
正交晶系包括三个长度分别为a、b和c的互相垂直的晶轴,其六个面分别为长方形。
正交晶系中最常见的结构是析出相结构,例如钛钶合金中的钛纤维基板。
4.单斜晶系。
单斜晶系包括两个长度不等、互相成锐角的晶轴,以及垂直于这两个轴的垂轴。
单斜晶系中最常见的结构是某些金属、半导体和陶瓷材料中的基体结构。
5.斜方晶系。
斜方晶系包括两个长度不等但互相垂直的晶轴以及一个垂直于晶面的垂轴。
斜方晶系的晶体结构非常多样,但最常见的是钙钛矿结构,这是一种广泛存在于氧化物中的晶体结构。
总结。
以上介绍的几种晶体结构是最常见的晶体结构之一,它们共同构成了材料科学中的基础知识。
了解晶体结构对于研究材料性质和开发新型功能材料非常重要。
另外,随着实验技术和计算方法的不断优化,我们对于各种晶体结构的了解将会越来越深入。
晶体材料基础---第六、七讲 晶体结构及对称性(5) 单形和聚形

复三方双锥:12
中级晶族各晶系的单形
①柱类:三方柱、复三方柱、四方 柱、复四方柱、六方柱、复六方柱
注意:晶面和交棱都平行于高次轴。
中级晶族各晶系的单形
②单锥类:三方单锥、复三方单锥、 四方单锥、复四方单锥、六方单锥、复 六方单锥
注意:出现在没有对称中心和其它水平对称要素 的对称型中。所有晶面交高次轴于一点。
实例⑴
正交晶系以L22P(mm2)为例:
将L2为Z轴,对称面的法线分别为X、Y轴,进行极射 赤平投影。
在1/4的扇形区域内,原始晶面与对称要素之间的相 对位置关系有7种: 3个角顶(1、2、3号晶面) 3条边上(4、5、6号晶面) 中部(7号晶面)
六 单形的推导
Z Y Y X X
位置1:单面{001} 位置2:平行双面{100} 位置3:平行双面{010} 位置4:双面{h0l} 位置5:双面{0kl} 位置 6:斜方柱{hk0} 位置 7:斜方单锥{hkl}
称型逐一进行推导,能导出146种不同的单
形,称为结晶单形。
实际晶体单形的对称型判断
实际晶体的单形都是结晶单形.可根据晶 面花纹、蚀像、物性等特点判断。 如黄铁矿立方体晶面 上常发育有相互垂直的不是3L44L36L29PC
四 47种几何单形的形态特点
五角十二面体的三个变形
有关单形的几个概念:
⒋左形(left-hand form)和右 形(right-hand form) :形状完全 相同而在空间的取向正好彼此相反 的两个形体,若相互间不能借助于 旋转、但可借助于反映而使两者的 取向达到一致,此二同形反向体即 构成左形和右形。
三方偏方面体 的左形和右形
六四面体:
高中化学新教材同步选择性必修第二册第3章微专题6:晶体结构的分析与计算
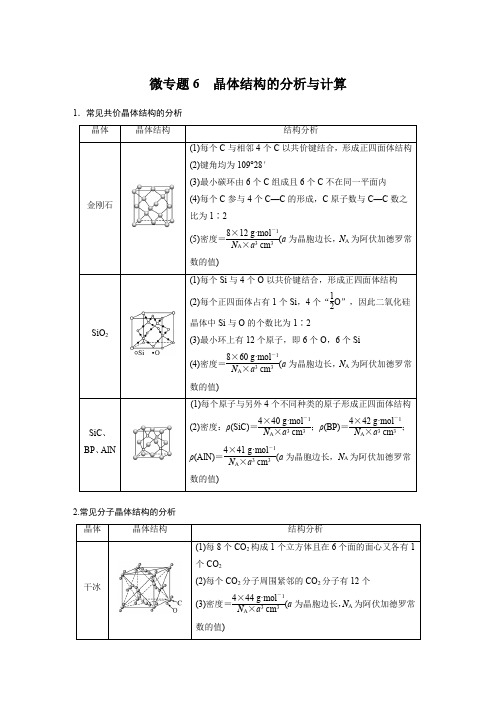
微专题6晶体结构的分析与计算1.常见共价晶体结构的分析晶体晶体结构结构分析金刚石(1)每个C与相邻4个C以共价键结合,形成正四面体结构(2)键角均为109°28′(3)最小碳环由6个C组成且6个C不在同一平面内(4)每个C参与4个C—C的形成,C原子数与C—C数之比为1∶2(5)密度=8×12 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)SiO2(1)每个Si与4个O以共价键结合,形成正四面体结构(2)每个正四面体占有1个Si,4个“12O”,因此二氧化硅晶体中Si与O的个数比为1∶2(3)最小环上有12个原子,即6个O,6个Si(4)密度=8×60 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)SiC、BP、AlN (1)每个原子与另外4个不同种类的原子形成正四面体结构(2)密度:ρ(SiC)=4×40 g·mol-1N A×a3 cm3;ρ(BP)=4×42 g·mol-1N A×a3 cm3;ρ(AlN)=4×41 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)2.常见分子晶体结构的分析晶体晶体结构结构分析干冰(1)每8个CO2构成1个立方体且在6个面的面心又各有1个CO2(2)每个CO2分子周围紧邻的CO2分子有12个(3)密度=4×44 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)白磷密度=4×124 g·mol-1N A×a 3 cm 3(a为晶胞边长,N A为阿伏加德罗常数的值)3.常见离子晶体结构的分析NaCl型CsCl型ZnS型CaF2型晶胞配位数684F-:8;Ca2+:4密度的计算(a为晶胞边长,N A为阿伏加德罗常数的值)4×58.5 g·mol-1N A×a3 cm3168.5 g·mol-1N A×a3 cm34×97 g·mol-1N A×a3 cm34×78 g·mol-1N A×a3 cm31.AB型化合物形成的晶体结构多种多样。
6-晶体结构详解

等价原子有完全相同的化学环境。
平移对称性
在某给定方向上,相距最近的两个等价原子之间的距离为a, 则将晶体沿该方向平行移动距离na(n为整数)晶体就复原, 这种性质就是晶体的平移对称性。 连接晶体中任意两个等价原子得一矢量a,将晶体沿着该矢量 平移a或a的整数倍na,晶体复原。
NaCl 晶胞: 面心立方 复晶胞(4)
c
b a
石墨 晶胞:平行六面体 素晶胞
原子坐标
将晶胞的晶轴a, b, c的方向取作三个坐标轴x, y, z的方向(按右手 定则) ,从晶胞的坐标原点指向原子的位置矢量 r 可以表示为: r = x a + yb + zc (x, y, z)称为该原子的坐标。
(1). 金属Na (2). 金属铜
a c b b
a
b
c
平移对称性:晶体沿a方向平移na复原,沿b方向平移mb复原, 沿c方向平移lc复原。 平移矢量: na + mb + lc
(3). NaCl
(4). 金刚石
c
b c a a
b
(5). 石墨
c
b
a
2. 点阵和结构单元
重复单位: 晶体内部原子、离子或分子, 在三维空间作周期性重 复排列。每个重复单位的化学组成相同,空间结构相同,若 忽略晶体的表面效应,重复单位周围的环境也相同。 重复单位: 单个原子或分子,离子团或多个分子。
点阵点位于立方体的顶点
Na
点阵点:黑点 ,位于立方体的顶点与体心
结构单元= 1个Na = 1个平行六面体 = ½立方体
Cu
点阵点:黑点,位于立方体的顶点与面心
结构单元 = 1个Cu = 斜平行六面体
单质晶体结构-6

第VII族元素,每个原子周围共价单键个数为8-7=1, 因此,其晶体结构是两个原子先以单键共价结合成双原子 分子,双原子分子之间再通过范德华力结合形成分子晶体, 如图1-1-2 。
81 6 1 4 82
体心立方结构
常见体心立方的金属有-Fe、V、Mo等, 晶格中原子坐标为[0,0,0],[1/2,1/2,1/2]。 晶胞中原子数为:
81 1 2 8
密排六方结构
Zn、Mg、Li等是常见的密排六方结构的金属,原 子分布除了简单六方点阵的每个阵点[0,0,0]上有原子 外,在六方棱柱体内还有3个原子。如用平行六面体坐 标表示,其坐标为[1/3,2/3,1/2]或[2/3,1/3,1/2]。在 六方柱晶胞中,顶点的每个原子为6个晶胞所共有,上 下底面中心的原子为2个晶胞所共有,所以六方柱晶胞 所包含的原子数为:
二、非金属元素单质的晶体结构
1.惰性气体元素的晶体 惰性气体在低温下形成的晶体为A1(面心立
方)型或A3(六方密堆)型结构。由于惰性气体 原子外层为满电子构型,它们之间并不形成化学 键,低温时形成的晶体是靠微弱的没有方向性的 范德华力直接凝聚成最紧密堆积的A1型或A3型分 子晶体。
2.其它非金属元素单质的晶体结构 —休谟-偌瑟瑞(Hume-Rothery)规则
图1-1-2 非金属元素单质晶体的结构基元(a)第VII族元素
第VI族元素,单键个数为8-6=2,故其结构是 共价结合的无限链状分子或有限环状分子,链或环之 间由通过范德华力结合形成晶体,如图1-1-3 。
图1-1-3 非金属元素单质晶体的结构基元(b)第VI族元素
七大晶体结构

七大晶体结构七大晶体结构是晶体学中最基本的晶体结构类型,它们分别是立方晶系、四方晶系、正交晶系、单斜晶系、菱形晶系、三斜晶系和六方晶系。
每个晶体结构都具有独特的空间排列方式和晶胞参数。
下面将对七大晶体结构进行详细介绍。
一、立方晶系立方晶系是指晶胞的三个边长相等,三个角度都为90度的晶体结构。
立方晶系包括立方晶体、体心立方晶体和面心立方晶体三种类型。
立方晶体的晶胞中原子或离子分布均匀,具有高度的对称性。
体心立方晶体在立方晶体的每个晶胞中心还有一个原子或离子,而面心立方晶体在立方晶体的每个面中心还有一个原子或离子。
二、四方晶系四方晶系是指晶胞的三个边长相等,其中两个角度为90度,另一个角度为120度的晶体结构。
四方晶系中最典型的晶体是正长石,它具有独特的双锥体晶胞。
三、正交晶系正交晶系是指晶胞的三个边长相等,三个角度都为90度的晶体结构。
正交晶系中的晶体结构较为复杂,包括石英、长石等多种类型。
四、单斜晶系单斜晶系是指晶胞的三个边长不相等,其中两个角度为90度,另一个角度不为90度的晶体结构。
单斜晶系中的晶体结构具有较低的对称性,例如单斜硫。
五、菱形晶系菱形晶系是指晶胞的三个边长相等,三个角度都不为90度的晶体结构。
菱形晶系中的晶体结构具有较低的对称性,例如菱英石。
六、三斜晶系三斜晶系是指晶胞的三个边长不相等,三个角度都不为90度的晶体结构。
三斜晶系中的晶体结构最为复杂,具有最低的对称性,例如石膏。
七、六方晶系六方晶系是指晶胞的三个边长相等,其中两个角度为90度,另一个角度为120度的晶体结构。
六方晶系中的晶体结构具有较高的对称性,例如石墨和冰。
七大晶体结构是晶体学中的基本分类,它们分别具有不同的对称性和晶胞参数,对于研究晶体的物理性质和化学性质具有重要意义。
ca6晶体结构

ca6晶体结构
CA6晶体结构属于六方晶系。
CA6,即六铝酸钙(CaAl12O19或CaO·6Al2O3),是一种具有优异高温性能的材料,广泛应用于钢铁冶金等高温领域。
其晶体结构特点是:
-镜面层与尖晶石基块:CA6的结构由镜面层和尖晶石基块沿着c-轴堆叠而成。
每个晶胞通常包含两个镜面层和两个尖晶石基块。
-六方晶系:由于镜面层中的Ca2+半径大于O2-半径,Ca2+无法进入O2-构成的间隙中,因此CA6的晶体结构是六方晶系而非立方晶系。
此外,在制备过程中,CA6晶体的片状生长特性可能会影响其致密化,从而影响材料的性能。
研究人员正在探索通过结构改性方法来提高CA6的致密度。
综上所述,CA6的晶体结构对其性能有着重要影响,尤其是在高温应用中的稳定性和耐用性。
通过材料科学的研究和工艺改进,可以进一步优化CA6的性能,以满足工业应用的需求。
常见晶胞结构最强整理

常见晶胞结构最强整理常见晶体结构及其详解晶体晶体结构晶体详解原⼦晶体⾦刚⽯(1)每个碳采取杂化⽅式与4个碳以共价键结合,形成结构,键⾓均为 (2)最⼩碳环由个C 组成且六原⼦不在同⼀平⾯内,平均每个碳原⼦被个六元环共⽤,每根C -C 键被个六元环共⽤。
(3)每个C 参与4条C -C 键的形成, C 原⼦个数与C -C 键数之⽐为 ,1mol ⾦刚⽯中,碳碳键为 molSiO 2(1)每⼀个硅原⼦紧邻个氧原⼦,每⼀个氧原⼦紧邻个硅原⼦,形成了由Si-O 键(极性或⾮极性)键构成的元环的最⼩环状结构。
⼀个环上有个硅原⼦,个氧原⼦(2)1mol SiO 2中,硅氧键为 molSiC每个C 原⼦最近的Si 原⼦有个,每个C 原⼦最近的C 原⼦有个分⼦晶体⼲冰(1)⼀个⼆氧化碳晶胞中含有个⼆氧化碳分⼦(2)8个CO 2分⼦构成⽴⽅体且在6个⾯⼼⼜各占据1个CO 2分⼦ (3)每个CO 2分⼦周围等距且紧邻的CO 2分⼦有个冰⼀个⽔分⼦形成个氢键,平均1mol 冰中含有 mol 氢键C 60(1)⾜球烯的分⼦是由60个碳原⼦构成的,空间构型有12个正五边形,20个正六边形(2)⼀个C 60分⼦中含有根单键,根双键 (3)C 60晶胞中与⼀个C 60最近的C 60分⼦有个(与⼲冰的晶胞相似)离⼦晶体NaCl (型)(1)每个Na +周围等距且紧邻的Cl -有个,每个Cl -周围等距且紧邻的Na +有个。
每个Na +周围等距且紧邻的Na +有个,同理Cl -也然。
(2)每个晶胞中含个Na +和4个Cl -。
CsCl (型)(1)每个Cs +周围等距且紧邻的Cl -有个,每个Cl -周围等距且紧邻的Cs +有个。
(2)左图为个晶胞;右图为⼀个晶胞,每个晶胞中含个Cs +,个Cl -。
CaF 21、1个晶胞中含有个Ca 2+,个F -,Ca 2+的配位数为个,F -配位数为个2、Ca 2+周围等距离最近的Ca 2+ 个,F —周围等距离最近的F — 个⾦属晶体简单⽴⽅堆积典型代表空间利⽤率配位数为体⼼⽴⽅堆积典型代表空间利⽤率配位数为⾯⼼⽴⽅堆积典型代表空间利⽤率配位数为六⽅最密堆积典型代表空间利⽤率配位数为混合晶体⽯墨1、碳原⼦的杂化⽅式为,键⾓为2、⽯墨晶体的⽚层结构中,每个六元碳环含有个碳原⼦数,每个六元碳环所含有的共价健数是个3、⽯墨同层C 原⼦间以连接,熔化需要破坏碳碳之间作⽤⼒,故熔沸点较⾼;层与层之间的作⽤⼒为,作⽤⼒⽐较弱,故⽯墨的硬度较低。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1. 晶体的结构特征
晶体是原子、离子或分子在空间按照一定的规律周期性地重复
排列所构成的固体物质。
晶体的基本特性:周期性
周期性:是指在任意方向上,晶体中的原子每隔一定的距
离就重复出现的性质。(忽略晶体的表面效应)
周期性是晶体结构最基本的特征。
周期:某方向上原子重复出现的最小距离。
Se
点阵点
将每个结构单元用一个点来表示,这样的点称为点阵点。
点阵
将表示结构单元的点阵点放置在空间等价的位置,如一组等价 原子的位置,则得到一个点的空间序列,称为点阵。
点阵的基本特性
平移对称性或平移不变性:连结任意两个点阵点得一矢量,按 此矢量平移, 点阵能够复原。
(1) 所有点阵点都是等价的 (2) 每个点阵点都具有完全相同的周围环境
c b a
2. 点阵和结构单元
重复单位: 晶体内部原子、离子或分子, 在三维空间作周期性重 复排列。每个重复单位的化学组成相同,空间结构相同,若 忽略晶体的表面效应,重复单位周围的环境也相同。
重复单位: 单个原子或分子,离子团或多个分子。
结构单元 = 重复单位
结构单元是晶体中所有不等价原子构成的最小集合体。
2. 晶体结构的对称性,晶族晶系与空间点阵型式, 晶体的点 群和群符号
本节讲授晶体中所可能拥有的各种对称元素与对称操作,包括 点操作及其与平移操作的组合。进一步,根据晶体的对称性 将自然界中的所有晶体进行分类描述,包括7大晶系,32个 晶体学点群,然后根据对称性对各大晶系选取合适的标准 晶胞以形成国际通用标准;同一晶系中点阵点在空间的分布 方式也可以不同,从而将晶体划分为14种空间点阵形式。
晶体有确定的熔点 ,有均匀性,各向异性,能自发地形成凸 多面体外形,有特定的对称性,能使X射线、电子流与中 子流产生衍射。
晶体中的原子、分子都按一定的规律周期性地重复排列。
人工宝石
另一类是非晶态或叫玻璃体或叫无定形态。如玻璃、明胶、 碳粉、塑料制品等。
晶体拥有的特性非晶体都没有,如没有确定的熔点,没有对 称性,不能产生衍射等。
3.点阵与平面间距离 介绍点阵点、直线点阵与平面点阵的数学表示方法,用晶面
指标计算晶面间距的公式。 4.空间群及晶体结构的表达* 5.晶体的结构和晶体的性质* 6.晶体的X射线衍射原理 介绍晶体X射线衍射的基本原理,主要是确定衍射方向的布
拉格方程与劳埃方程。
教学要求
理解晶体结构的周期性特征,掌握点阵与晶体结构的关系以 及点阵的平移对称性,掌握晶胞的概念与晶胞内原子的分 数坐标,了解晶体结构的对称性,掌握根据晶体对称性划 分的七大晶系、六种正当晶胞与十四种空间点阵型式,了 解晶面指标与晶面间距。了解晶体衍射方向的两个基本方 程布拉格方程与劳埃方程。
Se
点阵点 = 结构单元
如果在晶体的点阵中的各个点阵点上,按照同一种方式安置 结构单元,则得到整个晶体结构。
晶体结构 = 点阵 + 结ቤተ መጻሕፍቲ ባይዱ单元
例7. 一维直线点阵
(a). Cu: 点阵点=结构单元= 1个铜原子
a
(b). 石墨: 点阵点 = 结构单元 = 两个C原子
a
(c). Se: 点阵点 结构单元 = 3个Se原子
连接晶体中任意两个等价原子得一矢量a,将晶体沿着该矢量 平移a或a的整数倍na,晶体复原。
例4. 一维 平移对称性
(1). 石墨 (2). Se
平移对称性:晶体平移na而复原。
例5. 二维 平移对称性
(1). 石墨烯
(2). NaCl 的一个晶面
T
T
b
b a a
平移对称性:晶体沿a方向平移na复原,沿b方向平移mb复原
平移矢量: na + mb
T = 2a + b
例6. 三维 平移对称性
(1). 金属Na (2). 金属铜
c ba
b
a c
b
平移对称性:晶体沿a方向平移na复原,沿b方向平移mb复原, 沿c方向平移lc复原。
平移矢量: na + mb + lc
(3). NaCl
(4). 金刚石
c b
b
c
a
a
(5). 石墨
例1. 一维周期性
(1). 伸展的聚乙烯(CH2CH2)n
a (2). NaCl晶体的一条晶棱
a 周期为a
例2. 二维周期性
(1). 金属铜 (2). B(OH)3
a a
周期为 2asin(/3) =
31/2a
a
b
两个方向的周期分别为a, b
例3. 三维周期性
(1). 金属Po (2). CsCl
b a
(2). NaCl 结构单元= 虚线的正方形= 1Na+ + 1Cl-
(3). Cu(黑点代表点阵点) 结构单元 = 虚线的平行四边 形 = 1个Cu原子
重点难点
• 1.重点:晶体的周期性结构,点阵和晶胞,晶胞内原子 的分数坐标,晶体的对称性,七大晶系、六种正当晶胞与 十四种空间点阵型式。
• 2.难点:晶体结构的对称性和晶面指标,确定衍射方向 的两个方程。
晶体周期性, 点阵与晶胞
固态物质分为二类
一类是晶体。自然界存在大量的晶体物质,如高山岩石、地 下矿藏、海边砂粒、两极冰川,金属、合金,水泥制品,食 盐和糖等。
a
(d). NaCl: 点阵点 结构单元 = 1Na+ + 1Cl-
a
(e).伸展的聚乙烯(CH2CH2)n: 点阵点结构单元 = CH2CH2
a
例8. 二维平面点阵
(1). 石墨片层
点阵点: 黑点, 放在某一类等价原子, 或者其他等价位置 结构单元 = 两个不等价碳原子 = 虚线的平行四边形
晶体结构
教学内容
1. 晶体结构的周期性,点阵与晶胞
讲授晶体微观结构的周期性或平移不变性或平移对称性;根据 周期性如何从晶体结构中抽象出点阵,什么是结构单元, 如何提取结构单元;进一步如何从点阵划分晶体的晶胞,如 何给出原子分数坐标。本节内容主要就是如何根据晶体对 称性抽象出简单的几何体---晶胞来描述晶体的结构。
a
a
边长方向的周期为a, 面对角线方向的周期为21/2a, 体对角线方向的周期为31/3a。
周期性 平移对称性,或平移不变性
等价原子: 晶体中每隔相等的距离就重复出现的原子。
等价原子有完全相同的化学环境。
平移对称性
在某给定方向上,相距最近的两个等价原子之间的距离为a, 则将晶体沿该方向平行移动距离na(n为整数)晶体就复原, 这种性质就是晶体的平移对称性。
