化学元素核外电子排布表
化学元素核外电子排布表

元素核外电子排布表1 / 378 铂Pt [Xe]6s1 4f14 5d9 2.8.18.32.17.1 d8->d9,注①79 金Au [Xe]6s1 4f14 5d10 2.8.18.32.18.1 d9->d10,注①全满80 汞Hg [Xe]6s2 4f14 5d10 2.8.18.32.18.281 铊Tl [Xe]6s2 4f14 5d10 6p1 2.8.18.32.18.382 铅Pb [Xe]6s2 4f14 5d10 6p2 2.8.18.32.18.483 铋Bi [Xe]6s2 4f14 5d10 6p3 2.8.18.32.18.584 钋Po [Xe]6s2 4f14 5d10 6p4 2.8.18.32.18.6 红色为放射性元素85 砹At [Xe]6s2 4f14 5d10 6p5 2.8.18.32.18.786 氡Rn [Xe]6s2 4f14 5d10 6p6 2.8.18.32.18.8 [Rn]87 钫Fr [Rn]7s1 2.8.18.32.18.8.188 镭Ra [Rn]7s2 2.8.18.32.18.8.289 锕Ac [Rn]7s2 5f0 6d1 2.8.18.32.18.9.2 f1->f0,注②全空90 钍Th [Rn]7s2 5f0 6d2 2.8.18.32.18.10.2 f2->f0,注②全空91 镤Pa [Rn]7s2 5f2 6d1 2.8.18.32.20.9.2 f3->f2,注②92 铀U[Rn]7s2 5f3 6d1 2.8.18.32.21.9.2 f4->f3,注②93 镎Np [Rn]7s2 5f4 6d1 2.8.18.32.22.9.2 f5->f4,注②94 钚Pu [Rn]7s2 5f6 2.8.18.32.24.8.295 镅Am [Rn]7s2 5f7 2.8.18.32.25.8.2 加粗为人造元素96 锔Cm [Rn]7s2 5f7 6d1 2.8.18.32.25.9.2 f8->f7,注②半满97 锫Bk [Rn]7s2 5f9 2.8.18.32.27.8.298 锎Cf [Rn]7s2 5f10 2.8.18.32.28.8.299 锿Es [Rn]7s2 5f11 2.8.18.32.29.8.2100 镄Fm [Rn]7s2 5f12 2.8.18.32.30.8.2101 钔Md [Rn]7s2 5f13 2.8.18.32.31.8.2 兰色为估计排布式102 锘No [Rn]7s2 5f14 2.8.18.32.32.8.2103 铹Lr [Rn]7s2 5f14 6d1 2.8.18.32.32.9.2104 Rf [Rn]7s2 5f14 6d2 2.8.18.32.32.10.2105 Ha [Rn]7s2 5f14 6d3 2.8.18.32.32.11.2106 [Rn]7s2 5f14 6d4 2.8.18.32.32.12.2107 [Rn]7s2 5f14 6d5 2.8.18.32.32.13.2108 [Rn]7s2 5f14 6d6 2.8.18.32.32.14.2109 [Rn]7s2 5f14 6d7 2.8.18.32.32.15.2110 [Rn]7s1 5f14 6d9 2.8.18.32.32.17.1 d8->d9,注①111 [Rn]7s1 5f14 6d10 2.8.18.32.32.18.1 d9->d10,注①全满112 [Rn]7s2 5f14 6d10 2.8.18.32.32.18.2113 [Rn]7s2 5f14 6d10 7p1 2.8.18.32.32.18.3114 [Rn]7s2 5f14 6d10 7p2 2.8.18.32.32.18.4115 [Rn]7s2 5f14 6d10 7p3 2.8.18.32.32.18.5116 [Rn]7s2 5f14 6d10 7p4 2.8.18.32.32.18.6117 [Rn]7s2 5f14 6d10 7p5 2.8.18.32.32.18.7 灰色为未发现元素118 [Rn]7s2 5f14 6d10 7p6 2.8.18.32.32.18.8注:①d亚层在s亚层外,常多填d亚层(使之趋于全满/半满),少填s亚层②d亚层在f亚层外,常多填d亚层,少填f亚层(使之趋于全空/半满)2 / 33 / 3。
知识点 原子核外电子排布与元素周期律

原子核外电子排布与元素周期律一、原子结构(Z 个)原子核注意:(N 个) 质量数(A)=质子数(Z)+中子数(N)1.X 原子序数= = =核外电子(Z 个)2.原子核外电子的排布规律:①电子总是尽先排布在能量 的电子层里;②各电子层最多容纳的电子数是 ;③最外层电子数不超过 个(K 层为最外层不超过 个),次外层不超过 个,倒数第三层电子数不超过 个。
电子层: 一(能量最低) 二 三 四 五 六 七 对应表示符号: 3.元素、核素、同位素元素: 。
核素: 。
同位素: 。
(对于原子来说) 二、元素周期表 1.编排原则:①按 递增的顺序从左到右排列 ②将 相同..的各元素从左到右排成一横行..。
(周期序数=原子的电子层数) ③把 相同..的元素按电子层数递增的顺序从上到下排成一纵行..。
=原子最外层电子数 2.结构特点:核外电子层数 元素种类第一周期 种元素短周期 第二周期 种元素周期 第三周期 种元素元 (7个横行) 第四周期 种元素 素 (7个周期) 第五周期 种元素 周 长周期 第六周期 种元素 期 第七周期 未填满(已有 种元素) 表 主族:ⅠA ~ⅦA 共7个主族族 副族:ⅢB ~ⅦB 、ⅠB ~ⅡB ,共7个副族 (18个纵行) 第Ⅷ族: 纵行,位于 之间 (16个族) 零族: ① 主族(A ):由 和 元素共同组成的族(除第18纵列)列序与主族序数的关系② 副族(B ):完全由 元素组成的族(第8、9、10纵列除外)③ Ⅷ族:包括 三个纵列。
④ 0族:第 纵列,该族元素又称为 元素。
三、元素周期律1.元素周期律: 。
元素性质的周期性变化实质是... 。
族碱金属元素: ( 是金属性最强的元素,位于周期表 ) 第ⅦA 族卤族元素: ( 是非金属性最强的元素,位于周期表 ) ★判断元素金属性和非金属性强弱的方法:(1)金属性强(弱)——① ;② ;③ 。
(2)非金属性强(弱)——① ;② ;③ 。
化学前36号元素电子排布式和简式

化学前36号元素电子排布式和简式化学前36号元素电子排布式和简式是一种通过绘制电子排布式图或简式来表示元素在原子中的电子排布情况的方法。
排布式图可以准确地描述原子内电子在不同能量等级上的排布情况,而简式可以提供一个有限的、容易理解的定性描述。
化学前36号元素电子排布式及简式如下:氢(H):排布式:1s1,简式:1氦(He):排布式:1s2,简式:2锂(Li):排布式:1s22s1,简式:2.1硼(B):排布式:1s22s22p1,简式:2.3碳(C):排布式:1s22s22p2,简式:2.4氮(N):排布式:1s22s22p3,简式:2.5氧(O):排布式:1s22s22p4,简式:2.6氟(F):排布式:1s22s22p5,简式:2.7氖(Ne):排布式:1s22s22p6,简式:2.8钠(Na):排布式:1s22s22p63s1,简式:2.8.1镁(Mg):排布式:1s22s22p63s2,简式:2.8.2铝(Al):排布式:1s22s22p63s23p1,简式:2.8.3磷(P):排布式:1s22s22p63s23p3,简式:2.8.5硫(S):排布式:1s22s22p63s23p4,简式:2.8.6氯(Cl):排布式:1s22s22p63s23p5,简式:2.8.7 氩(Ar):排布式:1s22s22p63s23p6,简式:2.8.8 钾(K):排布式:1s22s22p63s23p64s1,简式:2.8.8.1钙(Ca):排布式:1s22s22p63s23p64s2,简式:2.8.8.2钡(Ba):排布式:1s22s22p63s23p64s23d1,简式:2.8.8.2.1铁(Fe):排布式:1s22s22p63s23p64s23d6,简式:2.8.8.2.6锌(Zn):排布式:1s22s22p63s23p64s23d10,简式:2.8.8.2.10铜(Cu):排布式:1s22s22p63s23p64s13d10,简式:2.8.8.3.10氯(Br):排布式:1s22s22p63s23p65s1,简式:2.8.8.4氪(Kr):排布式:1s22s22p63s23p65s24d5,简式:2.8.8.4.52.8.9.2钯(Pd):排布式:1s22s22p63s23p64d10,简式:2.8.10铑(Rh):排布式:1s22s22p63s23p64d86s1,简式:2.8.10.1铱(Ir):排布式:1s22s22p63s23p64d106s2,简式:2.8.10.2铂(Pt):排布式:1s22s22p63s23p64d106s26f1,简式:2.8.10.2.6金(Au):排布式:1s22s22p63s23p64d105f14,简式:2.8.10.2.5锡(Sn):排布式:1s22s22p63s23p64d105f46s2,简式:2.8.10.2.5.6锑(Sb):排布式:1s22s22p63s23p64d105f26d1,简式:2.8.10.2.5.2碲(Te):排布式:1s22s22p63s23p64d105f26d2,简式:2.8.10.2.5.2碘(I):排布式:1s22s22p63s23p64d105f46d17s1,简式:2.8.10.2.5.6.7砹(At):排布式:1s22s22p63s23p64d105f76d17s2,简式:2.8.10.2.5.7.7氙(Xe):排布式:1s22s22p63s23p64d105f76d17s2,简式:2.8.10.2.5.7.7 氖(Rn):排布式:1s22s22p63s23p64d105f86d18s2,简式:2.8.10.2.5.8.8 钍(Tl):排布式:1s22s22p63s23p64d105f146d2,简式:2.8.10.2.5.14.2铯(Cs):排布式:1s22s22p63s23p65s24d105f146d17s1,简式:2.8.10.3.14.6.7铵(Fr):排布式:1s22s22p63s23p64f145d106s27p1,简式:2.8.11.1.5.6.7 钇(Y):排布式:1s22s22p63s23p64d104f14,简式:2.8.12铒(Er):排布式:1s22s22p63s23p64d104f145d1,简式:2.8.12.1铥(Dy):排布式:1s22s22p63s23p64d104f145d16s2,简式:2.8.12.1.5.6 镤(Pu):排布式:1s22s22p63s23p64d104f145d106s4,简式:2.8.12.1.5.10.4以上就是化学前36号元素的电子排布式和简式。
原子核外电子的排布 课件

54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
原子核外电子的排布规律 (1)各电子层最多能容纳___2_n_2__个电子(n为电子层 数)。 (2)最外层电子数不超过___8__个(当K层为最外层时 不超过___2 _个)。 (3)次外层电子数不超过__1_8__个。 (4) 电子总是尽量先排布在能量____最_低__的电子层里, 然后由里向外,依次排布在能量逐步______升_的高电 子层。
第一章 《物质结构 元素周期律》
第二节 《元素周期律》
核外电子排布规律
① 分层排布:一分、别原用子n 核= 1外、电2、子3、的4、排5布、6、7来表示从
内到外的电子层,并分别用符号K、L、M、N、O、P、Q来表 示); ② 在离核较近的区域运动的电子能量较低,在离核较远的 区域运动的电子能量较高,原子核外的电子总是尽可能地
小结: (1)比较微粒半径大小: 三看
一看电子层数
二看核电荷数
三看核外电子数或 最外层电子数
(2)对于同种元素:①阳离子半径<原子半径
②阴离子半径 > 原子半径 (3)对于电子层结构相同的离子:
核电荷数越大,则离子半径越小。 如 O2- > F-> Na+ > Mg2+>Al3+; S2- > Cl- > K+ >Ca2+
0.186 0.160 0.143 0.117 0.110 0.102 0.099 ----
原子序数
原子半径的变化
3~9
逐渐减小
11~17
逐渐减小
结论:随着原子序数的递增,元素原 子半径呈现 周期性 变化。
如何比较简单微粒 半径大小?
1-36号元素轨道图
dz2
价键法(VB法)价键理论一: 1、要点: ⑴、共价键的形成条件:①、先决条件: 原子具有未成对电子;②、配对电子参与 成键的原子轨道要满足对称匹配、能量相 近以及最大重叠的原则;③、两原子具有 成单的自旋相反的电子配对,服从保里不 相容原理。 ⑵、共价键的本质:是由于原子相互接近 时轨道重叠,原子间通过共用自旋相反的 电子使能量降低而成键。 ⑶、共价键的特征:①、饱和性,一个原 子有几个未成对电子(包括激发后形成的 未成对电子),便和几个自旋相反的电子 配对成键;而未成对电子数是有限的,故 形成化学键的数目是有限的。②、根据原 子轨道最大重叠原理,原子轨道沿其角度 分布最大值方向重叠,即共价键具有一定 的方向性。 ⑷、共价键的类型:单键、双键和叁键。
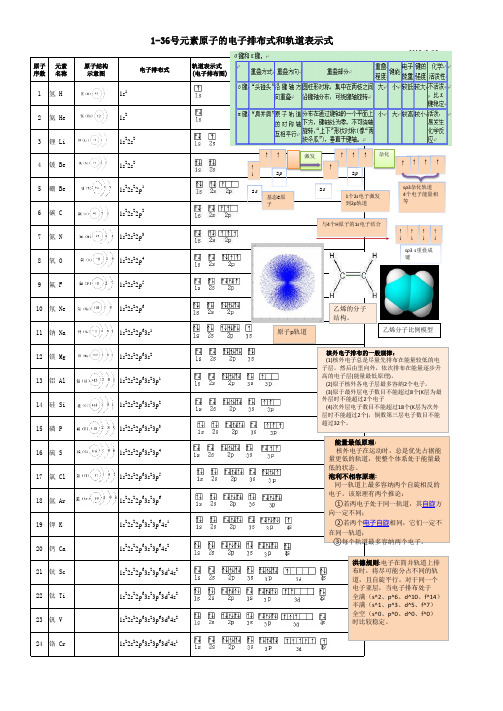
1-36号元素原子的电子排布式和轨道表示式
原子 元素 序数 名称
1 氢H
原子结构 示意图
电子排布式
1s1
轨道表示式 (电子排布图)
2013/9/12
2 氦 He
1s2
3 锂 Li 4 铍 Be 5 硼 Be 6 碳C 7 氮N 8 氧O
1s22s2 1s22s2 1s22s22p1 1s22s22p2 1s22s22p3 1s22s22p4
电离能:气态电中性基态原子失 去一个电子,转化为气态基态正离
子所需要的最低能量叫第一电离能。 符号:“I1”,单位:Kj/mol^-1。 “气态”、“电中性”、“基态” 是保证最低能量的条件。
[规律] 1.总体上金属元素第一电离能较 小非金属元素第一电离能较大. 2.同周期元素第一电离能从左到 右有增大的趋势 3.同主族元素第一电离能从上到 下逐渐减小
35 溴 Br
1s22s22p63s23p63d104s24p5
21到30号元素核外电子排布式

21到30号元素核外电子排布式核外电子排布式是指核外电子排布式的特征,它是指元素原子以外的电子的排布情况。
由于每种元素的核外电子排布式,原子的各种物理和化学特性也有很大的不同。
下面我们将讨论21号到30号元素的核外电子排布式。
21号元素是锰,它有4个核外电子,2个在2s轨道,2个在2p轨道。
22号元素是钛,有5个核外电子,3个在2s轨道,2个在2p轨道。
23号元素是钒,有6个核外电子,4个在2s轨道,2个在2p轨道。
24号元素是铬,有6个核外电子,4个在3s轨道,2个在3p轨道。
25号元素是锰,有7个核外电子,4个在3s轨道,3个在3p轨道。
26号元素是钛,有8个核外电子,4个在3s轨道,4个在3d轨道。
27号元素是铝,它有10个核外电子,4个在3s轨道,6个在3p轨道。
28号元素是锶,它有9个核外电子,5个在4s轨道,4个在3d轨道。
29号元素是镁,它有12个核外电子,6个在3s轨道,6个在3p轨道。
30号元素是锂,它有7个核外电子,4个在2s轨道,3个在2p轨道。
上述仅仅是21号到30号元素原子核外电子排布式的简单说明,让我们意识到它们的重要性,并希望理解核外电子排布式的元素的不同特性,有助于帮助我们更好地提高我们化学知识的水平。
核外电子排布式决定原子不同的性能,这些性能会影响我们元素之间的相互作用。
由于每种元素的核外电子排布式不同,它们可以与他们周围的元素结合在一起,形成更大的分子,形成多种化合物。
核外电子的态必须与原子的核进行协调,以保持其安稳性,并确保原子之间可以相互作用。
核外电子排布式也作用于蛋白质、糖和脂质,这些有机分子具有结构复杂,极具活性的特点。
它们有电子密度分布和电荷密度分布,这就定义了分子内部电荷分布和形状,并可能影响分子间作用,以及外部电场对物质是否被吸收或被特定化合物吸附的方式。
1-36号元素电子排布式
1-36号元素电子排布式化学元素是组成物质的基本单位。
元素的属性不仅受到原子核中质子和中子的影响,电子的排布方式也在很大程度上决定了元素的性质。
为了更好的理解元素的性质以及化学反应过程,学习元素的电子排布式是非常必要的。
本篇文章将介绍1-36号元素的电子排布式。
1. 氢元素(H,原子序数1)氢元素只含有一个电子,因此其电子排布式为1。
2. 氦元素(He,原子序数2)氦元素包含2个电子,因此其电子排布式为1s2。
3. 锂元素(Li,原子序数3)锂元素包含3个电子,其电子排布式为1s2 2s1。
4. 铍元素(Be,原子序数4)铍元素包含4个电子,其电子排布式为1s2 2s2。
5. 碳元素(C,原子序数6)碳元素包含6个电子,其电子排布式为1s2 2s2 2p2。
6. 氮元素(N,原子序数7)氮元素包含7个电子,其电子排布式为1s2 2s2 2p3。
7. 氧元素(O,原子序数8)氧元素包含8个电子,其电子排布式为1s2 2s2 2p4。
8. 氟元素(F,原子序数9)氟元素包含9个电子,其电子排布式为1s2 2s2 2p5。
9. 氖元素(Ne,原子序数10)氖元素包含10个电子,其电子排布式为1s2 2s2 2p6。
10. 钠元素(Na,原子序数11)钠元素包含11个电子,其电子排布式为1s2 2s2 2p6 3s1。
11. 镁元素(Mg,原子序数12)镁元素包含12个电子,其电子排布式为1s2 2s2 2p6 3s2。
12. 铝元素(Al,原子序数13)铝元素包含13个电子,其电子排布式为1s2 2s2 2p6 3s2 3p1。
13. 硅元素(Si,原子序数14)硅元素包含14个电子,其电子排布式为1s2 2s2 2p6 3s2 3p2。
14. 磷元素(P,原子序数15)磷元素包含15个电子,其电子排布式为1s2 2s2 2p6 3s2 3p3。
15. 硫元素(S,原子序数16)硫元素包含16个电子,其电子排布式为1s2 2s2 2p6 3s2 3p4。
1到36号元素核外电子排布式
1到36号元素核外电子排布式:1、H氢:1s12、He氦:1s23、Li锂:1s2 2s14、Be铍:1s2 2s25、B硼:1s2 2s2 2p17、N氮:1s2 2s2 2p38、O氧:1s2 2s2 2p49、F氟:1s2 2s2 2p510、Ne氖:1s2 2s2 2p611、Na钠:1s2 2s2 2p6 3s112、Mg镁:1s2 2s2 2p6 3s213、Al铝:1s2 2s2 2p6 3s2 3p114、Si硅:1s2 2s2 2p6 3s2 3p215、P磷:1s2 2s2 2p6 3s2 3p316、S硫:1s2 2s2 2p6 3s2 3p417、Cl氯:1s2 2s2 2p6 3s2 3p518、Ar氩:1s2 2s2 2p6 3s2 3p619、K钾:1s2 2s2 2p6 3s2 3p6 4s120、Ca钙:1s2 2s2 2p6 3s2 3p6 4s221、Sc钪:1s2 2s2 2p6 3s2 3p6 3d1 4s222、Ti钛:1s2 2s2 2p6 3s2 3p6 3d2 4s223、V 钒:1s2 2s2 2p6 3s2 3p6 3d3 4s224、Cr铬:1s2 2s2 2p6 3s2 3p6 3d5 4s125、Mn锰:1s2 2s2 2p6 3s2 3p6 3d5 4s226、Fe铁:1s2 2s2 2p6 3s2 3p6 3d6 4s227、Co钴:1s2 2s2 2p6 3s2 3p6 3d7 4s228、Ni镍:1s2 2s2 2p6 3s2 3p6 3d8 4s229、Cu铜:1s2 2s2 2p6 3s2 3p6 3d10 4s130、Zn锌:1s2 2s2 2p6 3s2 3p6 3d10 4s231、Ga镓:1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p132、Ge锗:1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p233、As砷:1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p334、Se硒:1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p425、Br溴:1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p536、Kr氪:1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6电子排布的规则1、构筑原理整个体系的能量越低越好。
化学元素核外电子排布表
41
铌Nb
[Kr]5s1 4d4
2.8.18.12.1
d3->d4,注①
42
钼Mo
[Kr]5s1 4d5
2.8.18.13.1
d4->d5,注①半满
43
锝Tc
[Kr]5s2 4d5
2.8.18.13.2
44
钌Ru
[Kr]5s1 4d7
2.8.18.15.1
d6->d7,注①
45
2.8.18.32.11.2
74
钨W
[Xe]6s2 4f14 5d4
2.8.18.32.12.2
75
铼Re
[Xe]6s2 4f14 5d5
2.8.18.32.13.2
76
锇Os
[Xe]6s2 4f14 5d6
2.8.18.32.14.2
77
铱Ir
[Xe]6s2 4f14 5d7
2.8.18.32.15.2
69
铥Tm
[Xe]6s2 4f13
2.8.18.31.8.2
70
镱Yb
[Xe]6s2 4f14
2.8.18.32.8.2
71
镥Lu
[Xe]6s2 4f14 5d1
2.8.18.32.9.2
72
铪Hf
[Xe]6s2 4f14 5d2
2.8.18.32.10.2
73
钽Ta
[Xe]6s2 4f14 5d3
2.8.18.32.32.18.7
灰色为未发现元素
118
[Rn]7s2 5f14 6d10 7p6
2.8.18.32.32.18.8
注:①d亚层在s亚层外,常多填d亚层(使之趋于全满/半满),少填s亚层
化学元素核外电子排布表
d7->d8,注①
46
钯Pd
[Kr]5s0 4d10
2.8.18.18.0
d8->d10,注①全满
47
银Ag
[Kr]5s1 4d10
2.8.18.18.1
d9->d10,注①全满
48
镉Cd
[Kr]5s2 4d10
2.8.18.18.2
49
铟In
[Kr]5s2 4d10 5p1
2.8.18.18.3
41
铌Nb
[Kr]5s1 4d4
2.8.18.12.1
d3->d4,注①
42
钼Mo
[Kr]5s1 4d5
2.8.18.13.1
d4->d5,注①半满
43
锝Tc
[Kr]5s2 4d5
2.8.18.13.2
44
钌Ru
[Kr]5s1 4d7
2.8.18.15.1
d6->d7,注①
45
铑Rh
[Kr]5s1 4d8
35
溴Br
[Ar]4s2 3d10 4p5
2.8.18.7
36
氪Kr
[Ar]4s2 3d10 4p6
2.8.18.8
[Kr]
37
铷Rb
[Kr]5s1
2.8.18.8.1
38
锶Sr
[Kr]5s2
2.8.18.8.2
39
钇Y
[Kr]5s2 4d1
2.8.18.9.2
40
锆Zr
[Kr]5s2 4d2
2.8.18.10.2
24
铬Cr
[Ar]4s1 3d5
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
元素核外电子排布表
79 金Au [Xe]6s1 4f14 5d10 2.8.18.32.18.1 d9->d10,注①全满
80 汞Hg [Xe]6s2 4f14 5d10 2.8.18.32.18.2
81 铊Tl [Xe]6s2 4f14 5d10 6p1 2.8.18.32.18.3
82 铅Pb [Xe]6s2 4f14 5d10 6p2 2.8.18.32.18.4
83 铋Bi [Xe]6s2 4f14 5d10 6p3 2.8.18.32.18.5
84 钋Po [Xe]6s2 4f14 5d10 6p4 2.8.18.32.18.6 红色为放射性元素
85 砹At [Xe]6s2 4f14 5d10 6p5 2.8.18.32.18.7
86 氡Rn [Xe]6s2 4f14 5d10 6p6 2.8.18.32.18.8 [Rn]
87 钫Fr [Rn]7s1 2.8.18.32.18.8.1
88 镭Ra [Rn]7s2 2.8.18.32.18.8.2
89 锕Ac [Rn]7s2 5f0 6d1 2.8.18.32.18.9.2 f1->f0,注②全空
90 钍Th [Rn]7s2 5f0 6d2 2.8.18.32.18.10.2 f2->f0,注②全空
91 镤Pa [Rn]7s2 5f2 6d1 2.8.18.32.20.9.2 f3->f2,注②
92 铀U[Rn]7s2 5f3 6d1 2.8.18.32.21.9.2 f4->f3,注②
93 镎Np [Rn]7s2 5f4 6d1 2.8.18.32.22.9.2 f5->f4,注②
94 钚Pu [Rn]7s2 5f6 2.8.18.32.24.8.2
95 镅Am [Rn]7s2 5f7 2.8.18.32.25.8.2 加粗为人造元素
96 锔Cm [Rn]7s2 5f7 6d1 2.8.18.32.25.9.2 f8->f7,注②半满
97 锫Bk [Rn]7s2 5f9 2.8.18.32.27.8.2
98 锎Cf [Rn]7s2 5f10 2.8.18.32.28.8.2
99 锿Es [Rn]7s2 5f11 2.8.18.32.29.8.2
100 镄Fm [Rn]7s2 5f12 2.8.18.32.30.8.2
101 钔Md [Rn]7s2 5f13 2.8.18.32.31.8.2 兰色为估计排布式102 锘No [Rn]7s2 5f14 2.8.18.32.32.8.2
103 铹Lr [Rn]7s2 5f14 6d1 2.8.18.32.32.9.2
104 Rf [Rn]7s2 5f14 6d2 2.8.18.32.32.10.2
105 Ha [Rn]7s2 5f14 6d3 2.8.18.32.32.11.2
106 [Rn]7s2 5f14 6d4 2.8.18.32.32.12.2
107 [Rn]7s2 5f14 6d5 2.8.18.32.32.13.2
108 [Rn]7s2 5f14 6d6 2.8.18.32.32.14.2
109 [Rn]7s2 5f14 6d7 2.8.18.32.32.15.2
110 [Rn]7s1 5f14 6d9 2.8.18.32.32.17.1 d8->d9,注①
111 [Rn]7s1 5f14 6d10 2.8.18.32.32.18.1 d9->d10,注①全满112 [Rn]7s2 5f14 6d10 2.8.18.32.32.18.2
113 [Rn]7s2 5f14 6d10 7p1 2.8.18.32.32.18.3
114 [Rn]7s2 5f14 6d10 7p2 2.8.18.32.32.18.4
115 [Rn]7s2 5f14 6d10 7p3 2.8.18.32.32.18.5
116 [Rn]7s2 5f14 6d10 7p4 2.8.18.32.32.18.6
117 [Rn]7s2 5f14 6d10 7p5 2.8.18.32.32.18.7 灰色为未发现元素118 [Rn]7s2 5f14 6d10 7p6 2.8.18.32.32.18.8 注:①d亚层在s亚层外,常多填d亚层(使之趋于全满/半满),少填s亚层
②d亚层在f亚层外,常多填d亚层,少填f亚层(使之趋于全空/半满)。
